Kohlenwasserstoffe M Kresken 1 Alkane Verbindungen die nur

Kohlenwasserstoffe M. Kresken 1
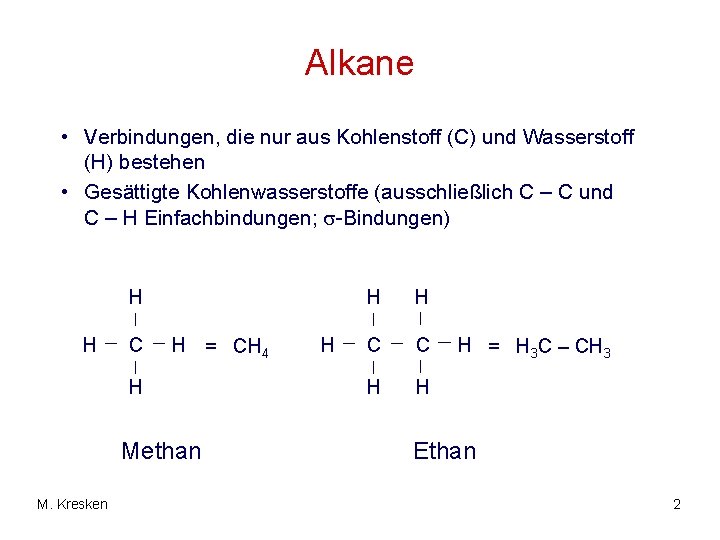
Alkane • Verbindungen, die nur aus Kohlenstoff (C) und Wasserstoff (H) bestehen • Gesättigte Kohlenwasserstoffe (ausschließlich C – C und C – H Einfachbindungen; -Bindungen) H H C H = CH 4 H Methan M. Kresken H H H C C H H H = H 3 C – CH 3 Ethan 2
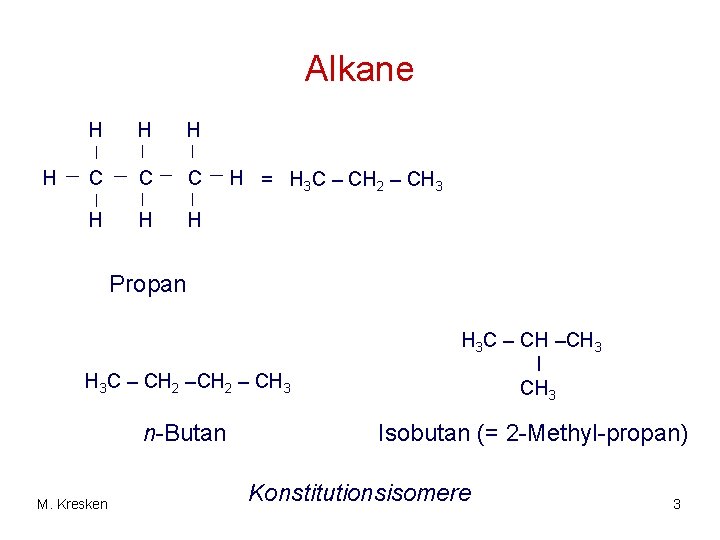
Alkane H H C C C H H = H 3 C – CH 2 – CH 3 Propan H 3 C – CH 2 – CH 3 H 3 C – CH –CH 3 I CH 3 n-Butan Isobutan (= 2 -Methyl-propan) M. Kresken Konstitutionsisomere 3
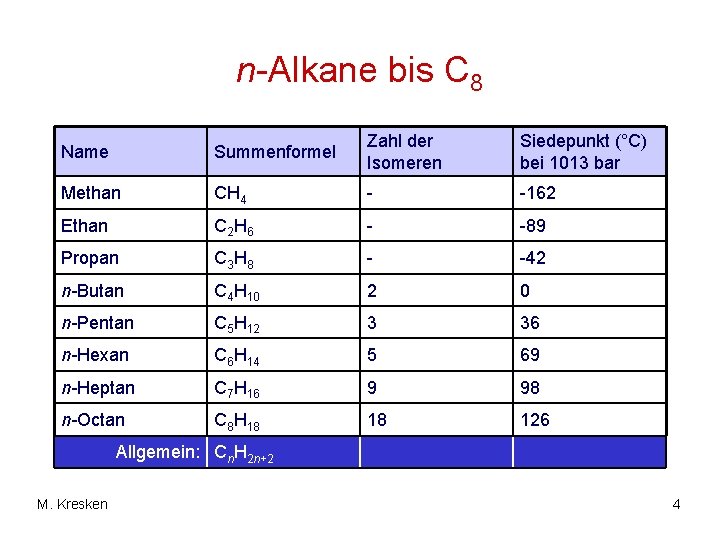
n-Alkane bis C 8 Name Summenformel Zahl der Isomeren Siedepunkt (°C) bei 1013 bar Methan CH 4 - -162 Ethan C 2 H 6 - -89 Propan C 3 H 8 - -42 n-Butan C 4 H 10 2 0 n-Pentan C 5 H 12 3 36 n-Hexan C 6 H 14 5 69 n-Heptan C 7 H 16 9 98 n-Octan C 8 H 18 18 126 Allgemein: Cn. H 2 n+2 M. Kresken 4

Nomenklatur von Alkanen • Bei verzweigten Alkanen gibt der Kohlenwasserstoff, der die längste unverzweigte Kette bildet, der Verbindung den Stammnamen. • Dieser wird durch die Benennung des Substituenten, also der Reste, die statt eines H-Atoms an der Kette stehen, ergänzt. • Kohlenwasserstoffreste heißen Alkylsubstituenten. Ihr Name leitet sich vom zugrunde liegenden Kohlenwasserstoff ab, indem die Endung „ -an“ durch „-yl“ ersetzt wird. • Aus Methan (CH 4) wird Methyl (-CH 3), aus Ethan (C 2 H 6) Ethyl - (-C 2 H 5), usw. – CH 2 – CH 3 n-Propyl CH 3 – CH CH 3 Isopropyl M. Kresken CH 3 I – CH 3 I CH 3 tert-Butyl 5
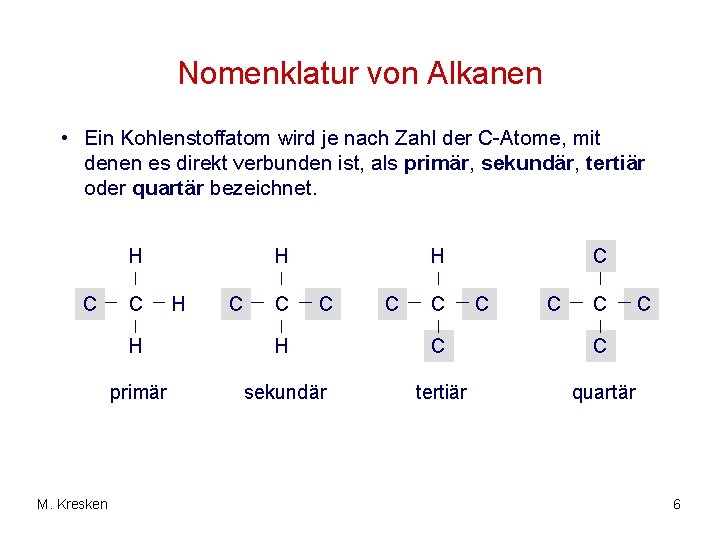
Nomenklatur von Alkanen • Ein Kohlenstoffatom wird je nach Zahl der C-Atome, mit denen es direkt verbunden ist, als primär, sekundär, tertiär oder quartär bezeichnet. H C M. Kresken C H H C C C C C H H C C primär sekundär tertiär quartär C 6
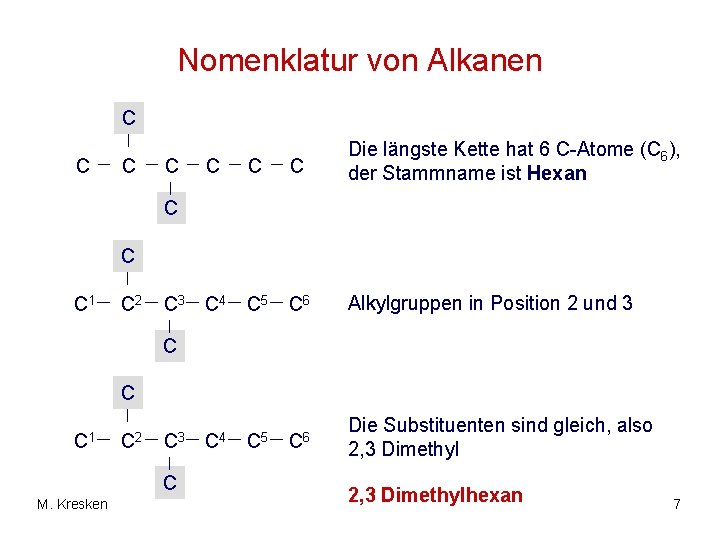
Nomenklatur von Alkanen C C C C Die längste Kette hat 6 C-Atome (C 6), der Stammname ist Hexan C 5 C 6 Alkylgruppen in Position 2 und 3 C 5 C 6 Die Substituenten sind gleich, also 2, 3 Dimethyl C C C 1 C 2 C 3 C 4 C C C 1 C 2 C 3 C M. Kresken C 4 2, 3 Dimethylhexan 7
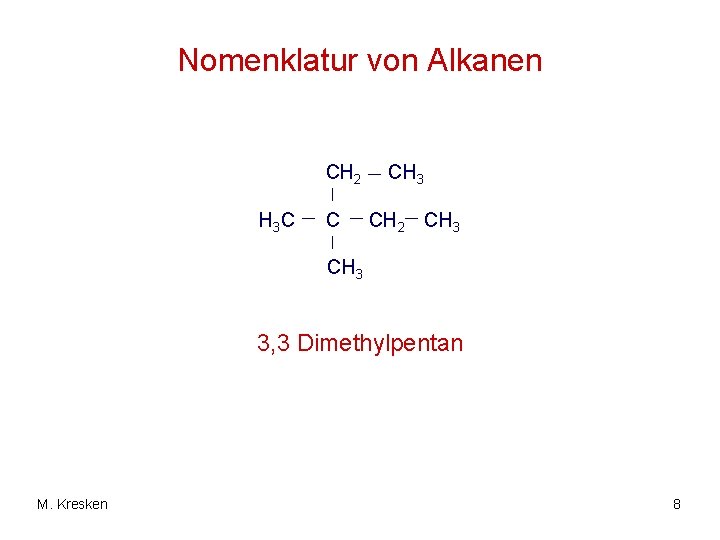
Nomenklatur von Alkanen CH 2 H 3 C C CH 3 CH 2 CH 3 3, 3 Dimethylpentan M. Kresken 8

Alkane • In Kohlenwasserstoffen sind nur unpolare Atombindungen wirksam, dies beeinflusst die Löslichkeit der Stoffe. • Allgemein gilt, dass sich organische Verbindungen in verschiedenen Lösungsmitteln umso besser lösen, je mehr sich die Eigenschaften und Struktur von Substanz und Lösungsmittel (Solvens) gleichen. • Kohlenwasserstoffe lösen sich in Tetrachlorcholenstoff, Dieethylether, Benzol oder Cyclohexan, nicht aber in Wasser. • Man bezeichnet Kohlenwasserstoffe daher als lipophil oder hydrophob. • Umgekehrt werden Stoffe, die sich gut in Wasser lösen als hydrophil oder lipophob bezeichnet. M. Kresken 9

Weitere Kohlenwasserstoffe • Aliphatische Verbindungen - fettartig - Cycloalkane - Alkene (Olefine) - Alkine • Aromaten (Arene) - wohlriechende Substanzen M. Kresken 10
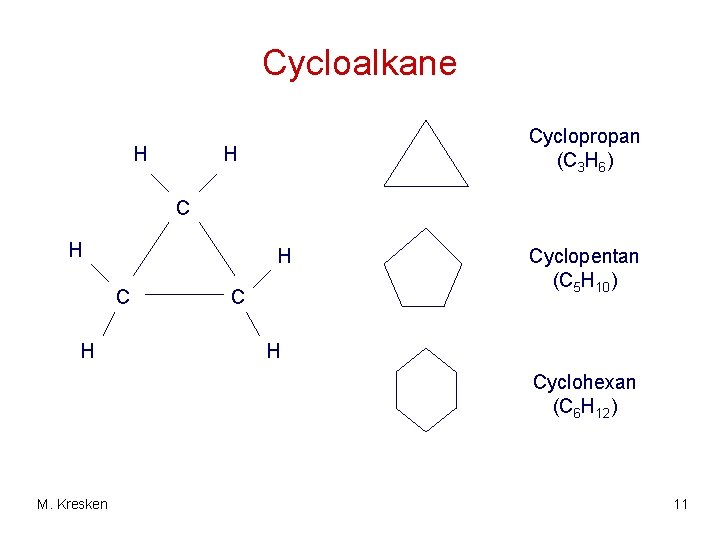
Cycloalkane H Cyclopropan (C 3 H 6) H C H C Cyclopentan (C 5 H 10) H Cyclohexan (C 6 H 12) M. Kresken 11
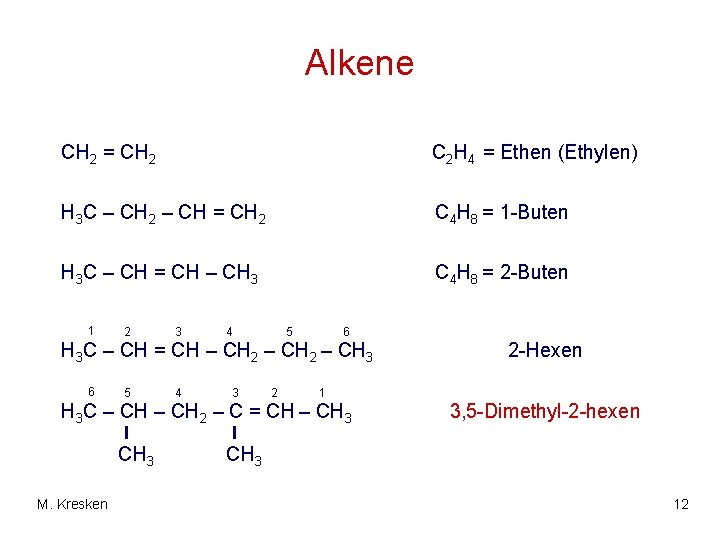
Alkene CH 2 = CH 2 C 2 H 4 = Ethen (Ethylen) H 3 C – CH 2 – CH = CH 2 C 4 H 8 = 1 -Buten H 3 C – CH = CH – CH 3 C 4 H 8 = 2 -Buten 1 2 3 4 5 6 H 3 C – CH = CH – CH 2 – CH 3 6 5 4 3 2 1 H 3 C – CH 2 – C = CH – CH 3 M. Kresken 2 -Hexen 3, 5 -Dimethyl-2 -hexen CH 3 12
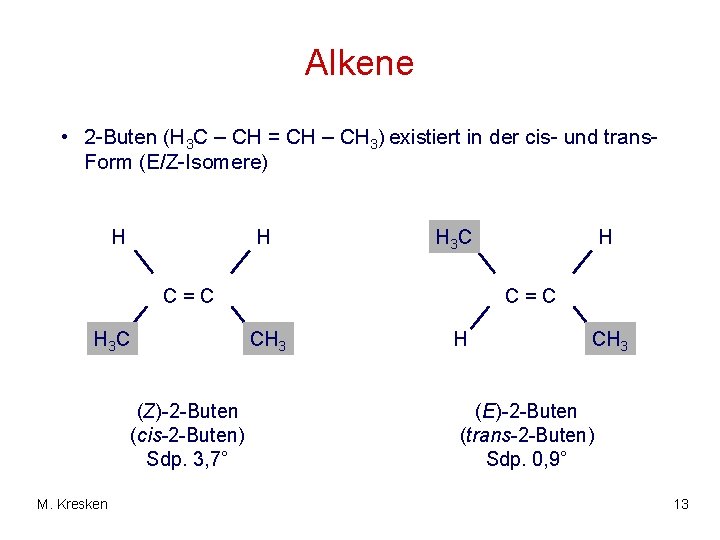
Alkene • 2 -Buten (H 3 C – CH = CH – CH 3) existiert in der cis- und trans. Form (E/Z-Isomere) H H H 3 C C=C H 3 C (Z)-2 -Buten (cis-2 -Buten) Sdp. 3, 7° M. Kresken H C=C CH 3 H CH 3 (E)-2 -Buten (trans-2 -Buten) Sdp. 0, 9° 13

Diene und Polyene • Verbindungen mit zwei Doppelbindungen heißen Alkadiene oder kurz Diene. • Man unterscheidet konjugierte von isolierten Doppelbindungen CH 2 = CH – CH = CH 2 = CH – CH 2 – CH = CH 2 1, 3 -Butadien 1, 4 -Pentadien CH 3 1 4 CH 2 = C – CH = CH 2 2 -Methyl-1, 3 -butadien (Isopren) M. Kresken 14
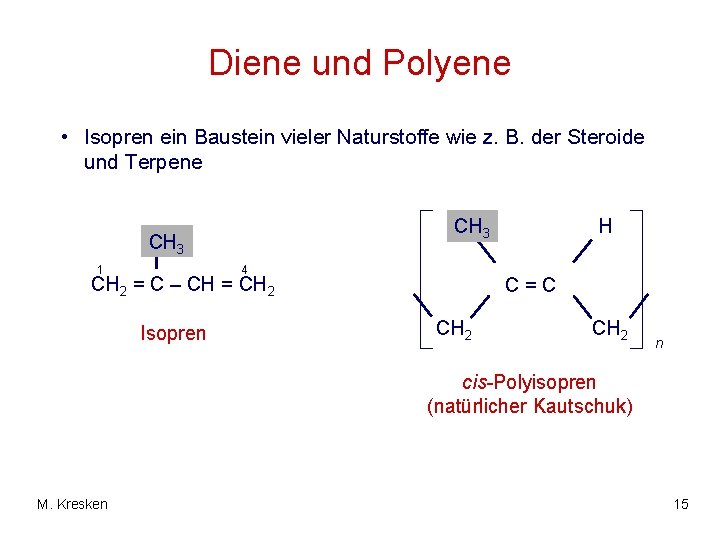
Diene und Polyene • Isopren ein Baustein vieler Naturstoffe wie z. B. der Steroide und Terpene CH 3 1 4 CH 2 = C – CH = CH 2 Isopren H C=C CH 2 n cis-Polyisopren (natürlicher Kautschuk) M. Kresken 15

Alkene • Verbindungen mit olefinischen Doppelbindungen • Bedeutung für den Menschen (Auswahl) - Linolsäure, Linolensäure (essentielle Fettsäuren) - Prostaglandine (Gewebshormone) - Cholesterin (Vorläufer der Steroidhormone) - Vitamin D (Knochenaufbau) - Vitamin A (Retinol) - Sphingolipide (Nervengewebe) M. Kresken 16
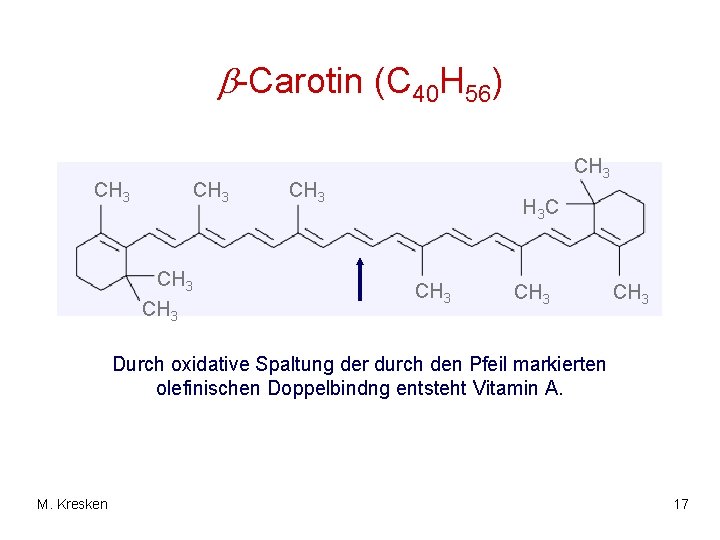
-Carotin (C 40 H 56) CH 3 CH 3 H 3 C CH 3 Durch oxidative Spaltung der durch den Pfeil markierten olefinischen Doppelbindng entsteht Vitamin A. M. Kresken 17
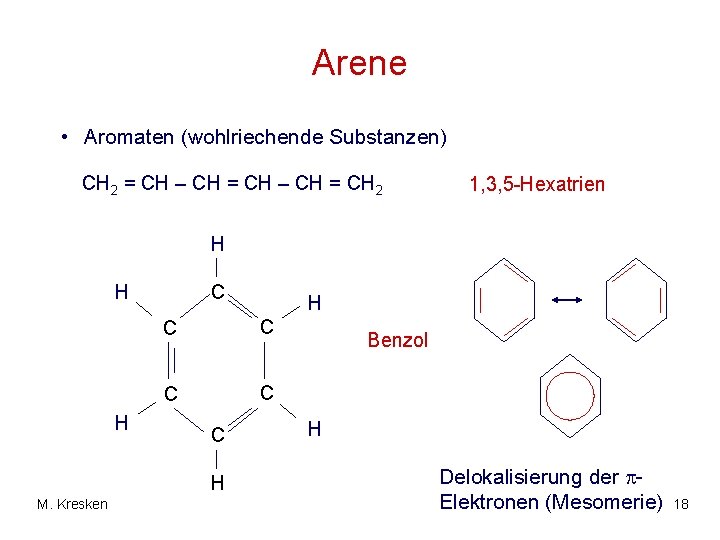
Arene • Aromaten (wohlriechende Substanzen) CH 2 = CH – CH = CH 2 1, 3, 5 -Hexatrien H H H C C C H M. Kresken H Benzol H Delokalisierung der Elektronen (Mesomerie) 18
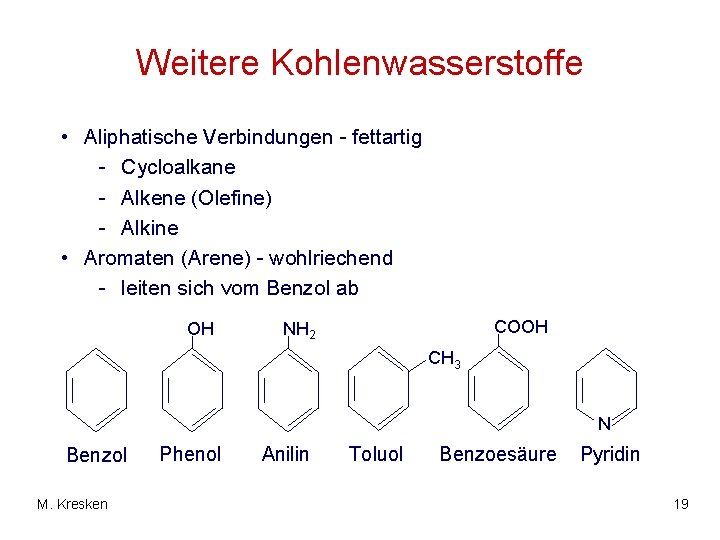
Weitere Kohlenwasserstoffe • Aliphatische Verbindungen - fettartig - Cycloalkane - Alkene (Olefine) - Alkine • Aromaten (Arene) - wohlriechend - leiten sich vom Benzol ab OH COOH NH 2 CH 3 N Benzol M. Kresken Phenol Anilin Toluol Benzoesäure Pyridin 19
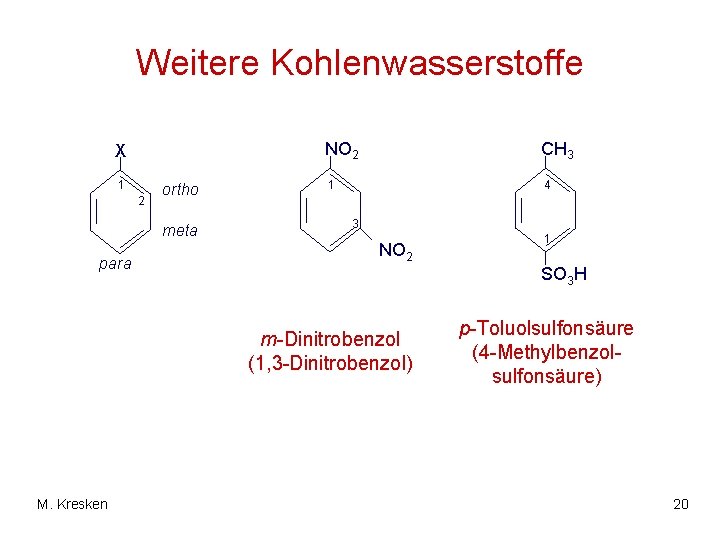
Weitere Kohlenwasserstoffe X 1 2 ortho meta para NO 2 CH 3 1 4 3 NO 2 SO 3 H m-Dinitrobenzol (1, 3 -Dinitrobenzol) M. Kresken 1 p-Toluolsulfonsäure (4 -Methylbenzolsulfonsäure) 20

Aromatische Verbindungen • Bedeutung für den Menschen (Auswahl) - Estrogene (Sexualhormone) - Thyroxin (Hormon der Schilddrüse) - Serotonin, Dopamin (Neurotransmitter) - Tocopherol, Folsäure (Vitamine) - Sulfonamide, Acetylsalicylsäure (Arzneimittel) M. Kresken 21
- Slides: 21