KML DE GNCEL TEDAV Ali Zahit Bolaman Adnan

KML DE GÜNCEL TEDAVİ Ali Zahit Bolaman Adnan Menderes Üniversitesi Tıp Fakültesi zahitb@yahoo. com
KML Tedavisinin Hedefleri Hematolojik yanıt Sitogenetik yanıt (Tam sitogenetik yanıt) Moleküler yanıt (Bcr-abl nin kaybolması) Lösemiz sağkalım=Şifa?

BCR-ABL transkript düzeyleri rezidüel lösemik hücrelerin sayısını yansıtır Tanı sırasında saptanan ortalama değer 1011 1010 109 100% Tam hematolojik yanıt 10% 1% Tam sitogenetik yanıt 0, 1% Majör moleküler yanıt 108 0, 01% 107 0, 001% 106 0, 0001 Tam moleküler yanıt (negatif RT PCR) % BCR-ABL% (Uluslararası “skala”ya göre) Lösemik hücre sayısı 1012
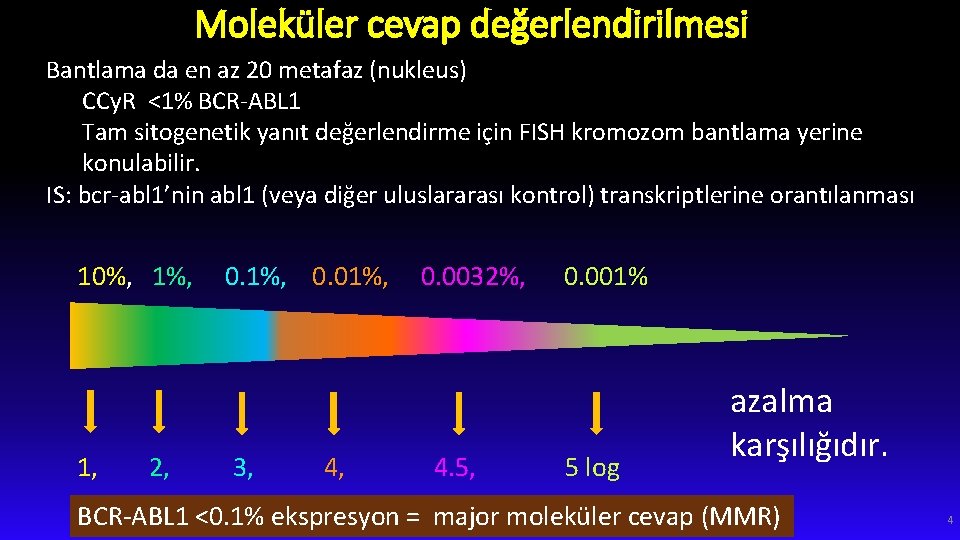
Moleküler cevap değerlendirilmesi Bantlama da en az 20 metafaz (nukleus) CCy. R <1% BCR-ABL 1 Tam sitogenetik yanıt değerlendirme için FISH kromozom bantlama yerine konulabilir. IS: bcr-abl 1’nin abl 1 (veya diğer uluslararası kontrol) transkriptlerine orantılanması 10%, 1%, 1, 2, 0. 1%, 0. 01%, 3, 4, 0. 0032%, 4. 5, 0. 001% 5 log azalma karşılığıdır. BCR-ABL 1 <0. 1% ekspresyon = major moleküler cevap (MMR) 4

Moleküler cevap değerlendirilmesi (2) • MMR 4: 0. 01% BCR-ABL 1 IS veya >10. 000 ABL 1 transkript hastalık saptanmaması • • MMR 4. 5: 0. 0032% BCR-ABL 1 IS veya >32. 000 ABL 1 transkript de ki hastalık saptanmaması 5

Risk skorları 6
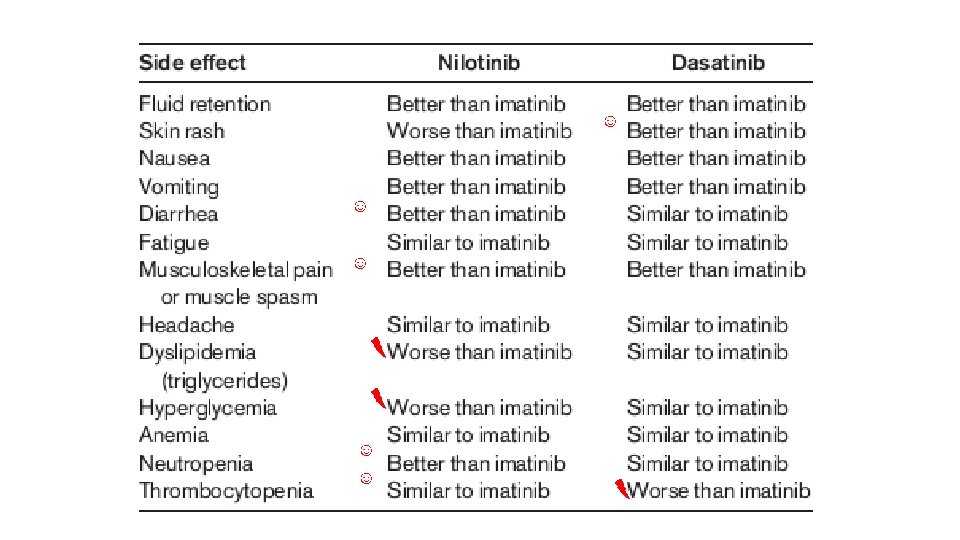
Tedavi Seçenekleri • İmatinib • Nilotinib, Dasatanib • Ponatinib, Bozutanib • Omecataxine • İnterferon • KİT SGK Risk skorları Hekim tercihi Komorbiditeler Hasta tercihi 7
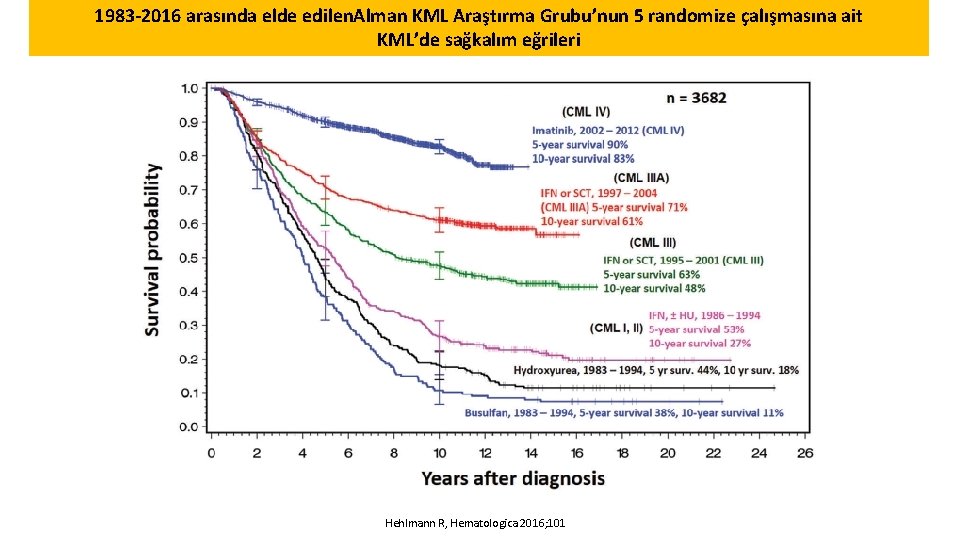
1983 -2016 arasında elde edilen. Alman KML Araştırma Grubu’nun 5 randomize çalışmasına ait KML’de sağkalım eğrileri Hehlmann R, Hematologica 2016; 101
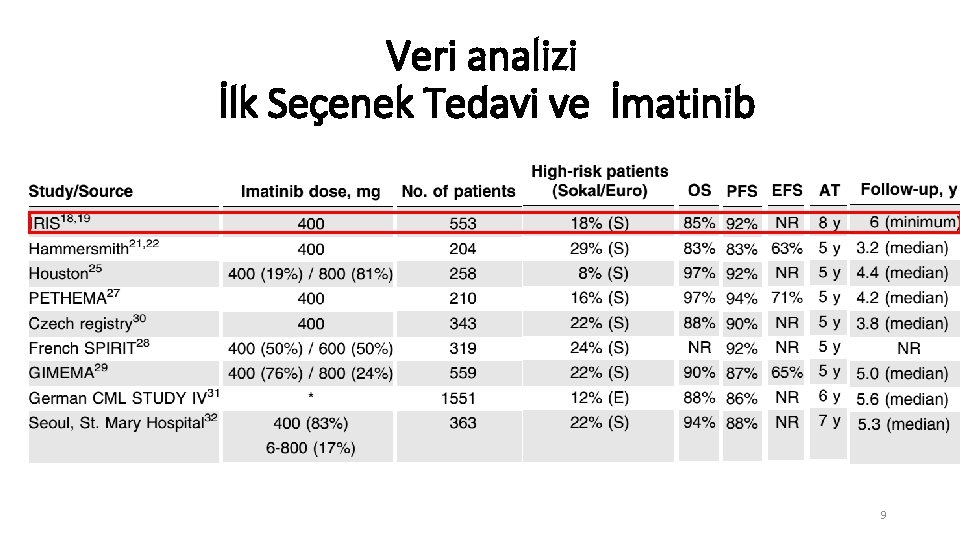
Veri analizi İlk Seçenek Tedavi ve İmatinib 9
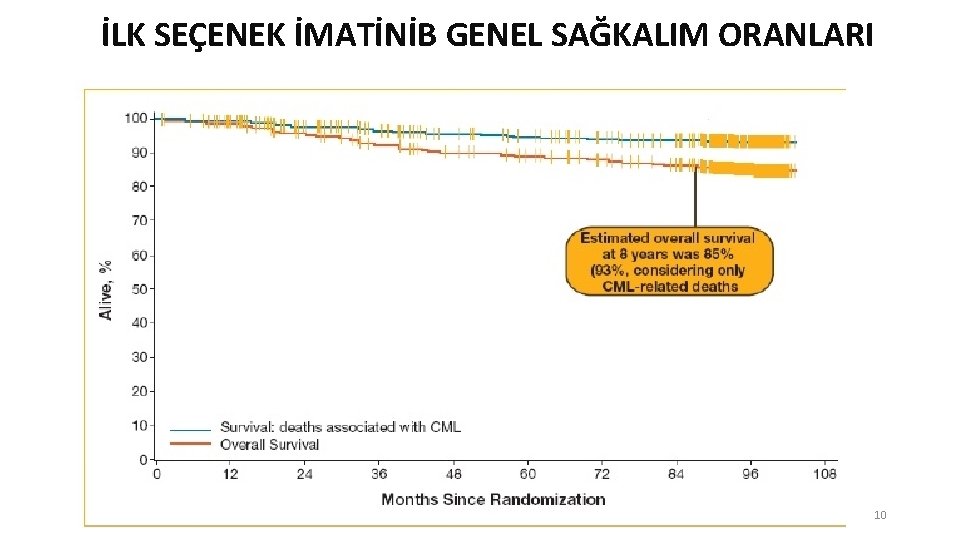
İLK SEÇENEK İMATİNİB GENEL SAĞKALIM ORANLARI 10
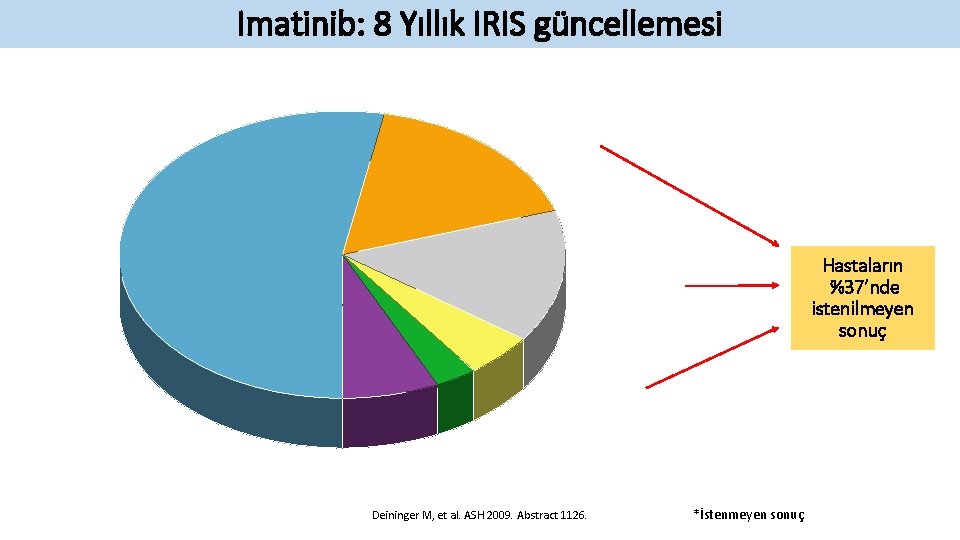
Imatinib: 8 Yıllık IRIS güncellemesi Hastaların %37’nde istenilmeyen sonuç Deininger M, et al. ASH 2009. Abstract 1126. *İstenmeyen sonuç
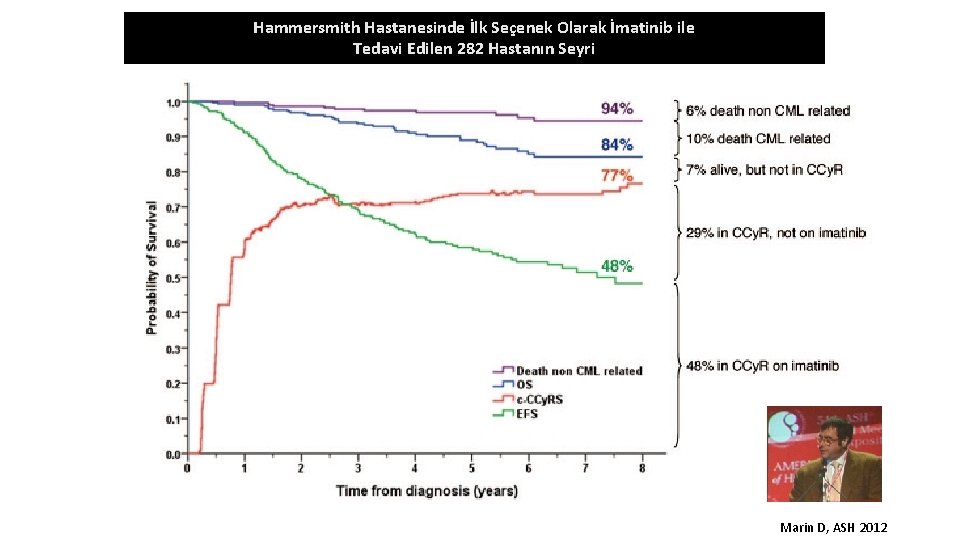
Hammersmith Hastanesinde İlk Seçenek Olarak İmatinib ile Tedavi Edilen 282 Hastanın Seyri Marin D, ASH 2012
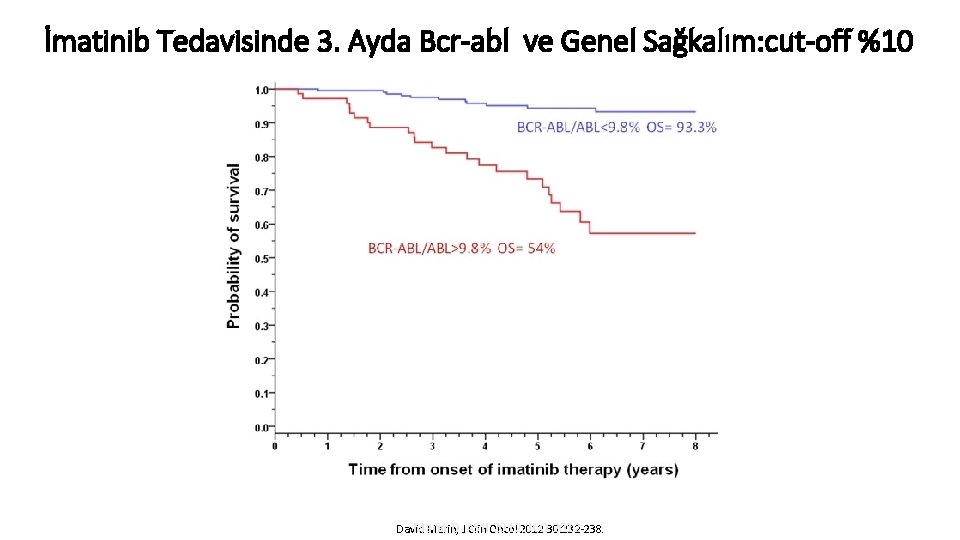
İmatinib Tedavisinde 3. Ayda Bcr-abl ve Genel Sağkalım: cut-off %10 Medyan takip süresi: 69 ay n. 282 hasta Marin D, J ASH 2012, 2012 JCO 30: 232 -238. 2012 David Marin, Clin Oncol

Yüksek doz imatinib • Amaç ? • Kime ? • Hangi dozda ? • Ne sürede 14
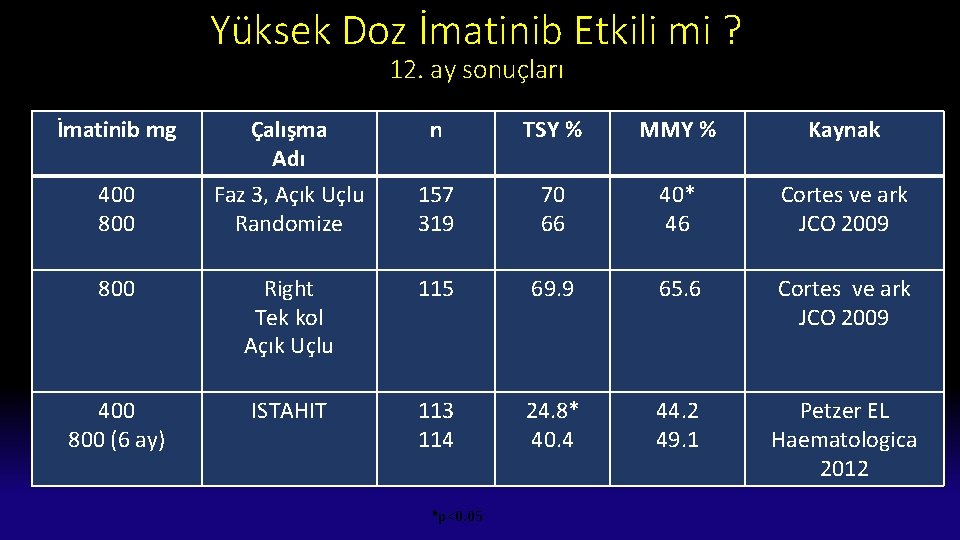
Yüksek Doz İmatinib Etkili mi ? 12. ay sonuçları İmatinib mg 400 800 Çalışma Adı Faz 3, Açık Uçlu Randomize n TSY % MMY % Kaynak 157 319 70 66 40* 46 Cortes ve ark JCO 2009 800 Right Tek kol Açık Uçlu 115 69. 9 65. 6 Cortes ve ark JCO 2009 400 800 (6 ay) ISTAHIT 113 114 24. 8* 40. 4 44. 2 49. 1 Petzer EL Haematologica 2012 *p<0. 05

16
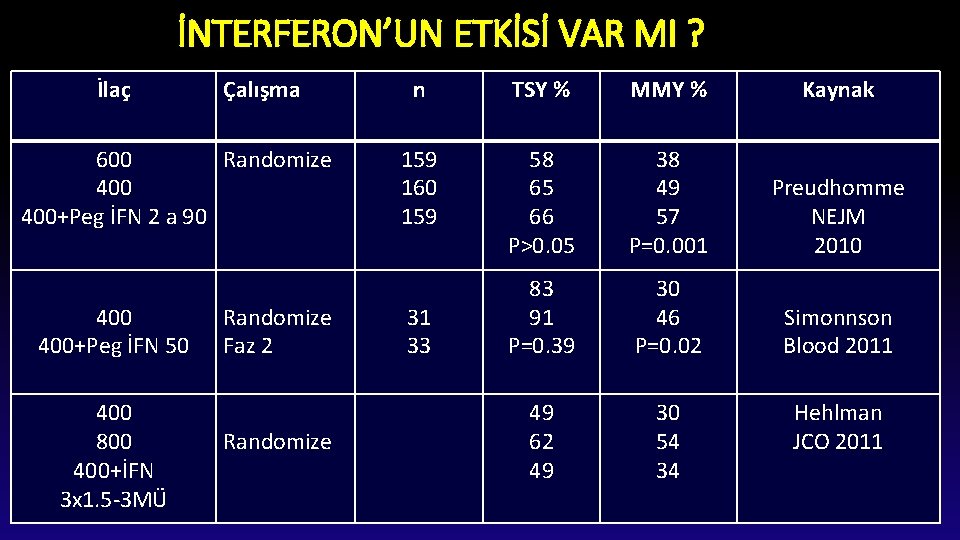
İNTERFERON’UN ETKİSİ VAR MI ? İlaç Çalışma 600 Randomize 400+Peg İFN 2 a 90 400+Peg İFN 50 400 800 400+İFN 3 x 1. 5 -3 MÜ Randomize Faz 2 Randomize n TSY % MMY % Kaynak 159 160 159 58 65 66 P>0. 05 38 49 57 P=0. 001 Preudhomme NEJM 2010 83 91 P=0. 39 30 46 P=0. 02 Simonnson Blood 2011 49 62 49 30 54 34 31 33 Hehlman JCO 2011

İmatinib Direnci 1. Primer direnç 2. Sekonder direnç • Herhangi bir zamanda hematolojik yanıt kaybı • Herhangi bir zamanda sitogenetik yanıt kaybı • Moleküler yanıtta transkript düzeyinin 1 logdan fazla artması

İmatinib tedavisinde TSY’ lı hastada artan bcr-abl transkript düzeyinin önemi Durum MMY kaybı MMY dışı KML Progresyonu Log QPCR n Herhangi 28 0 > 0. 5 -1 >1 <1 >1 12 36 32 8 0 6 1 4 Artış başlangıcından itibaren 4 yılda PFS >1 log artış olmayanlarda % 98 > 1 log artış olanlarda % 72 Kantarjian HM, et al. J Clin Oncol. 2009; 27: 3659 -3663. p <0. 01
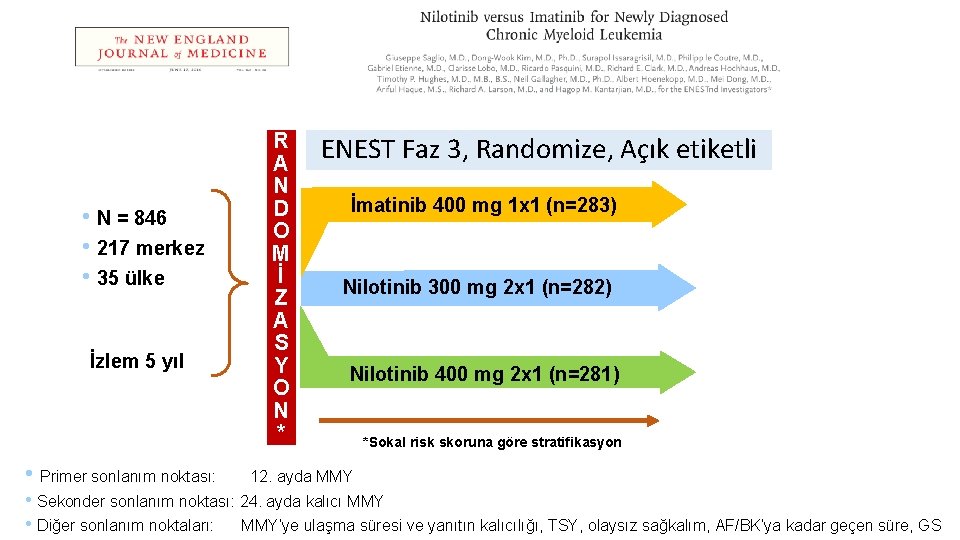
• N = 846 • 217 merkez • 35 ülke İzlem 5 yıl • Primer sonlanım noktası: R A N D O M İ Z A S Y O N * ENEST Faz 3, Randomize, Açık etiketli İmatinib 400 mg 1 x 1 (n=283) Nilotinib 300 mg 2 x 1 (n=282) Nilotinib 400 mg 2 x 1 (n=281) *Sokal risk skoruna göre stratifikasyon 12. ayda MMY • Sekonder sonlanım noktası: 24. ayda kalıcı MMY • Diğer sonlanım noktaları: MMY’ye ulaşma süresi ve yanıtın kalıcılığı, TSY, olaysız sağkalım, AF/BK’ya kadar geçen süre, GS
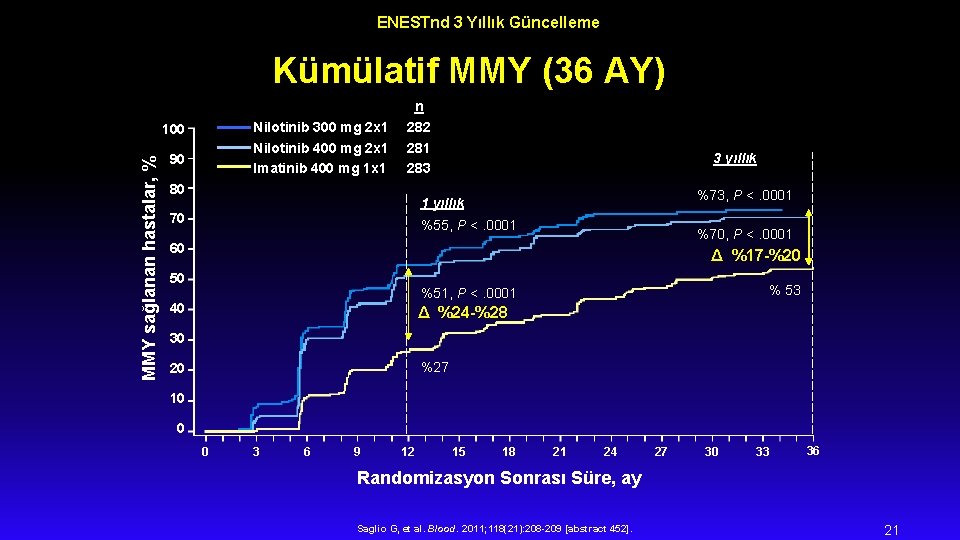
ENESTnd 3 Yıllık Güncelleme Kümülatif MMY (36 AY) n Nilotinib 300 mg 2 x 1 Nilotinib 400 mg 2 x 1 Imatinib 400 mg 1 x 1 MMY sağlanan hastalar, % 100 90 282 281 283 80 3 yıllık %73, P <. 0001 1 yıllık 70 %55, P <. 0001 %70, P <. 0001 60 Δ %17 -%20 50 % 53 %51, P <. 0001 40 Δ %24 -%28 30 %27 20 10 0 0 3 6 9 12 15 18 21 24 27 30 33 36 Randomizasyon Sonrası Süre, ay Saglio G, et al. Blood. 2011; 118(21): 208 -209 [abstract 452]. 21
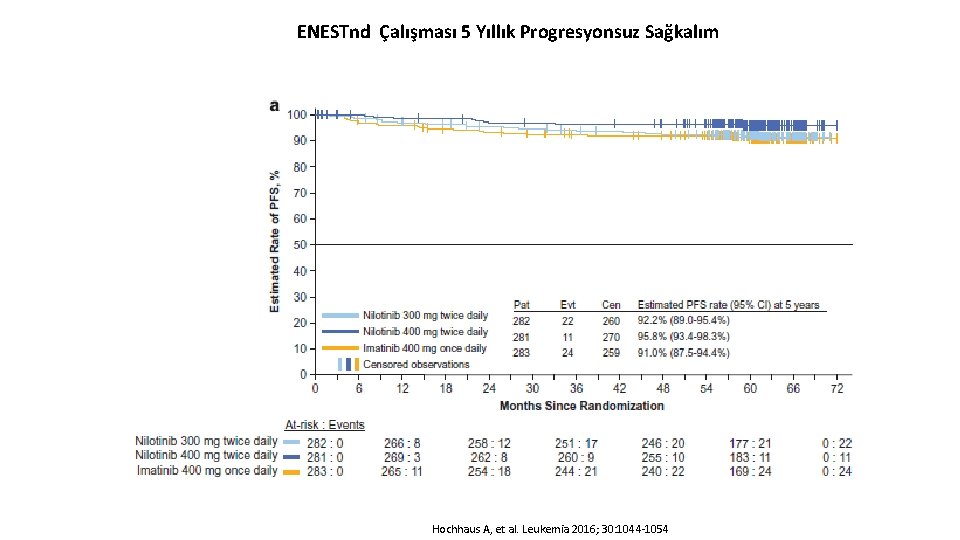
ENESTnd Çalışması 5 Yıllık Progresyonsuz Sağkalım Hochhaus A, et al. Leukemia 2016; 30: 1044 -1054

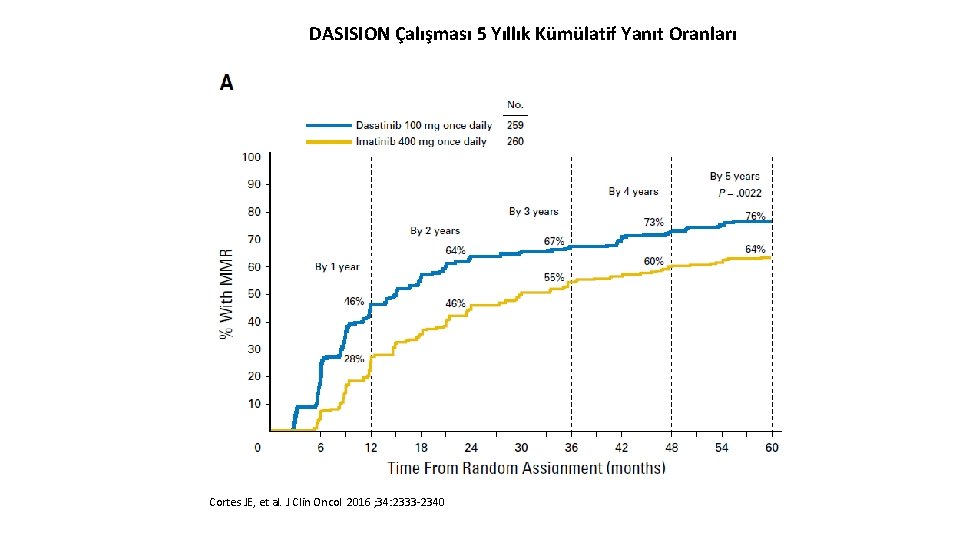
DASISION Çalışması 5 Yıllık Kümülatif Yanıt Oranları Cortes JE, et al. J Clin Oncol 2016 ; 34: 2333 -2340
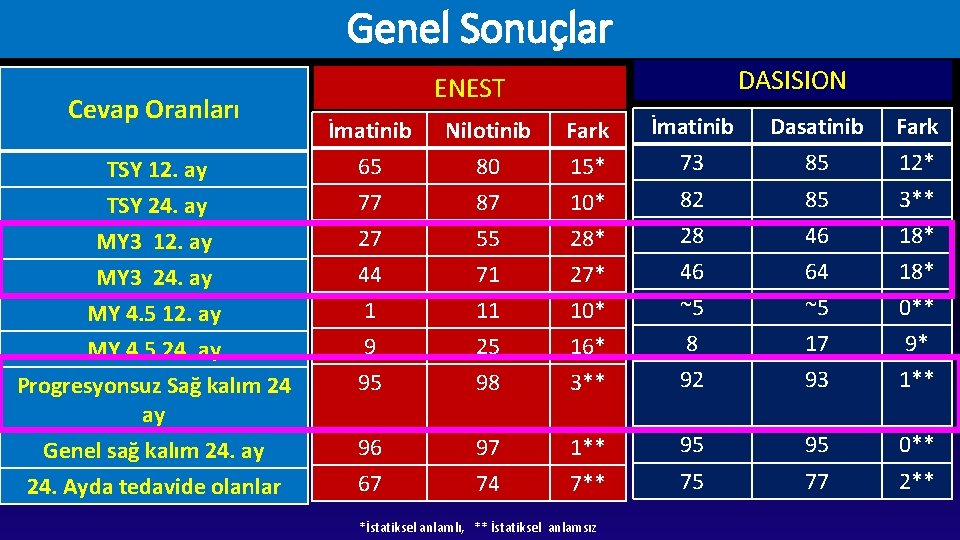
Genel Sonuçlar Cevap Oranları TSY 12. ay TSY 24. ay MY 3 12. ay MY 3 24. ay MY 4. 5 12. ay MY 4. 5 24. ay Progresyonsuz Sağ kalım 24 ay Genel sağ kalım 24. ay 24. Ayda tedavide olanlar DASISION ENEST İmatinib 65 77 27 44 1 9 Nilotinib 80 87 55 71 11 25 Fark 15* 10* 28* 27* 10* 16* İmatinib Dasatinib Fark 73 85 12* 82 85 3** 28 46 18* 46 64 18* ~5 ~5 0** 8 17 9* 95 98 3** 92 93 1** 96 67 97 74 1** 7** 95 95 0** 75 77 2** *İstatiksel anlamlı, ** İstatiksel anlamsız

R A N D O M 1 x 1 İ Z A S Y O N * Bosutinib 500 mg/gün N=250 İmatinünib 400 mg/gün N=250 Tedaviye devam eden hasta: oranı: Bosutinib %63, imatinib %71 Akselere veya blastik faza geçen hasta oranı: Bosutinib %5, imatinib %7 Tedavi sonlandırıldığında mutasyon ortaya çıkmış hasta sayısı: Bosutinib (n=4), imatinib (n=12) Diyare: Bosutinib % 70 imatinib %25 Cortes JE, J Clin Oncol 2012
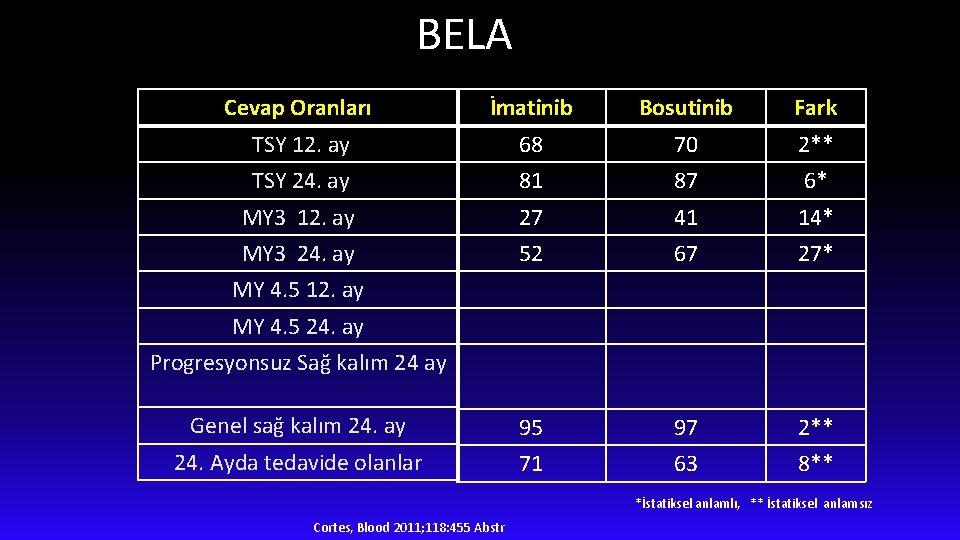
BELA Cevap Oranları İmatinib Bosutinib Fark TSY 12. ay 68 70 2** TSY 24. ay 81 87 6* MY 3 12. ay 27 41 14* MY 3 24. ay 52 67 27* Genel sağ kalım 24. ay 95 97 2** 24. Ayda tedavide olanlar 71 63 8** MY 4. 5 12. ay MY 4. 5 24. ay Progresyonsuz Sağ kalım 24 ay *İstatiksel anlamlı, ** İstatiksel anlamsız Cortes, Blood 2011; 118: 455 Abstr
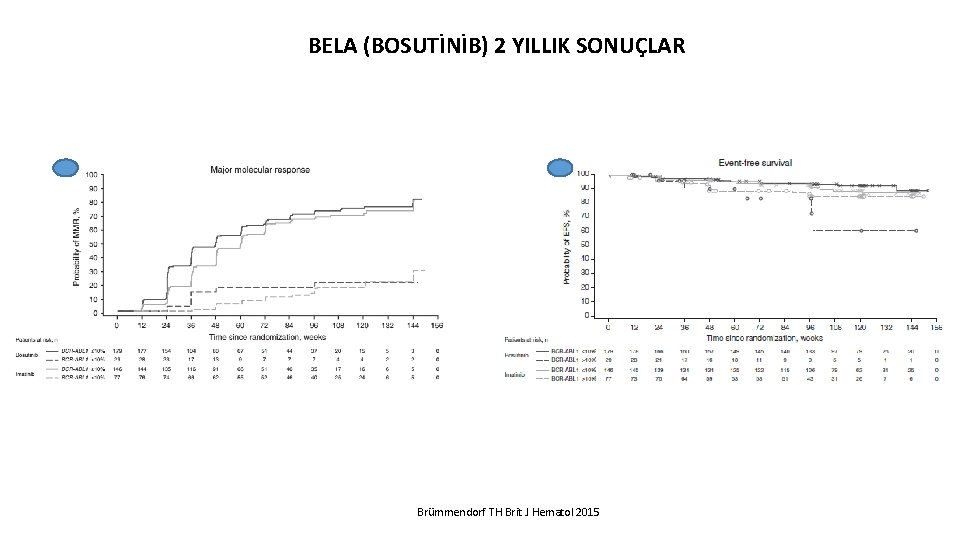
BELA (BOSUTİNİB) 2 YILLIK SONUÇLAR Brümmendorf TH Brit J Hematol 2015

30 EPIC ÇALIŞMASI
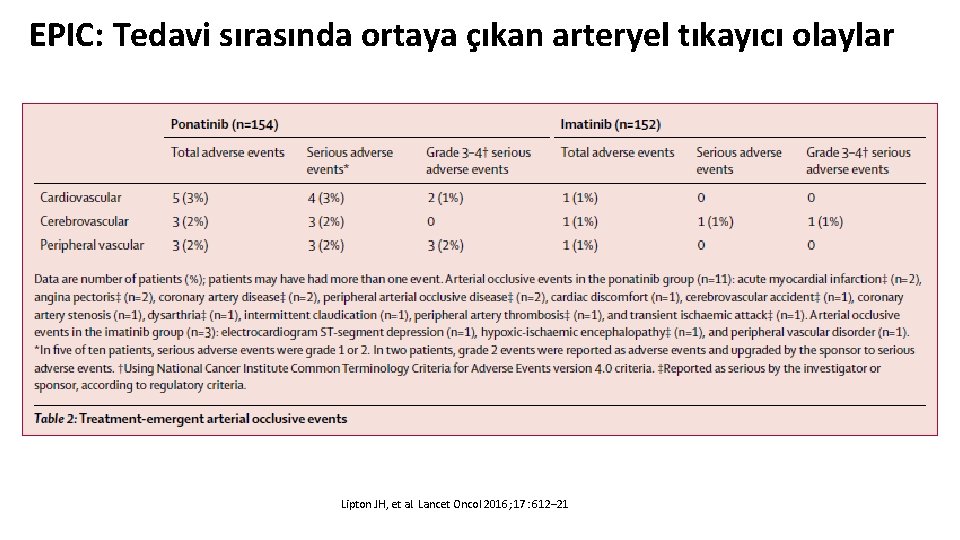
EPIC: Tedavi sırasında ortaya çıkan arteryel tıkayıcı olaylar Lipton JH, et al. Lancet Oncol 2016; 17: 612– 21
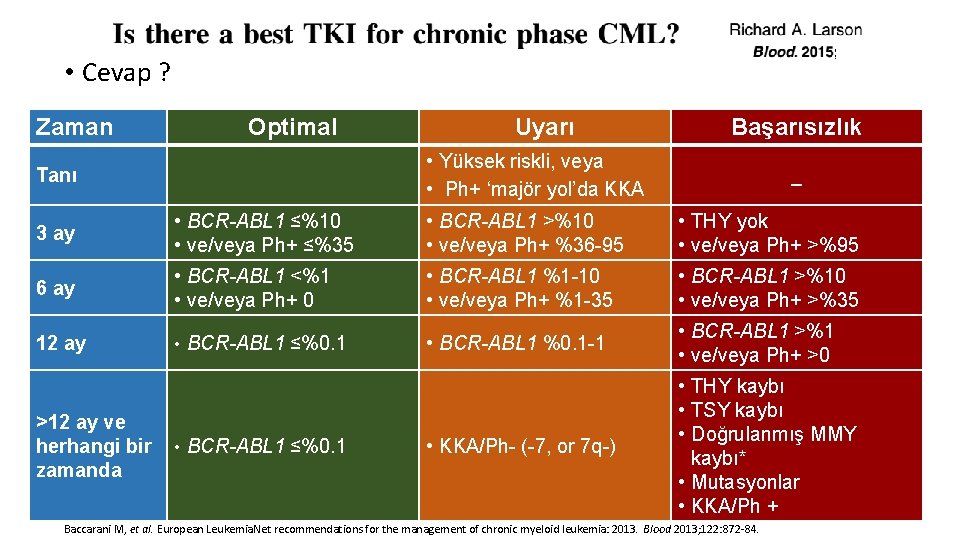
• Cevap ? Zaman Optimal Uyarı Başarısızlık • Yüksek riskli, veya • Ph+ ‘majör yol’da KKA Tanı _ 3 ay • BCR-ABL 1 ≤%10 • ve/veya Ph+ ≤%35 • BCR-ABL 1 >%10 • ve/veya Ph+ %36 -95 • THY yok • ve/veya Ph+ >%95 6 ay • BCR-ABL 1 <%1 • ve/veya Ph+ 0 • BCR-ABL 1 %1 -10 • ve/veya Ph+ %1 -35 • BCR-ABL 1 >%10 • ve/veya Ph+ >%35 12 ay • BCR-ABL 1 ≤%0. 1 • BCR-ABL 1 %0. 1 -1 • BCR-ABL 1 >%1 • ve/veya Ph+ >0 >12 ay ve herhangi bir • BCR-ABL 1 ≤%0. 1 • KKA/Ph- (-7, or 7 q-) zamanda Baccarani M, et al. European Leukemia. Net recommendations for the management of chronic myeloid leukemia: 2013. Blood 2013; 122: 872 -84. • THY kaybı • TSY kaybı • Doğrulanmış MMY kaybı* • Mutasyonlar • KKA/Ph + Baccarani M, et al. European Leukemia. Net recommendations for the management of chronic myeloid leukemia: 2013. Blood 2013; 122: 872 -84. 32

İMATİNİB’E DİRENÇ VARLIĞINDA MUTASYON ANALİZİNE DAYANILARAK YAPILAN TEDAVİ ÖNERİLERİ Mutasyon Önerilen Tedavi T 315 I V 299, T 315 A/I, F 317 L/V/I/C Y 253 H, E 255 K/V, F 359 L/V/I/C , Ponatinib, HKHT veya klinik çalışma Dasatinib yerine nilotinibi düşünülmeli Nilotinibden ziyade dasatinibi düşünülmeli Herhangi bir diğer mutasyon Yüksek doz imatinib, nilotinib, dasatinib Semptomatik lökositoz Hidroksiüre, aferez, imatinib, dasatinib, klinik çalışma Semptomatik trombositoz Hidroksiüre, antiagregan, anagrelid veya aferez Soverini S, et al. Blood 2011; 118: 1208 -15 33

KRONİK FAZ TEDAVİ SEÇİMİ AKSELERE VEYA BLASTİK FAZDA TEDAVİ SEÇİMİ 34
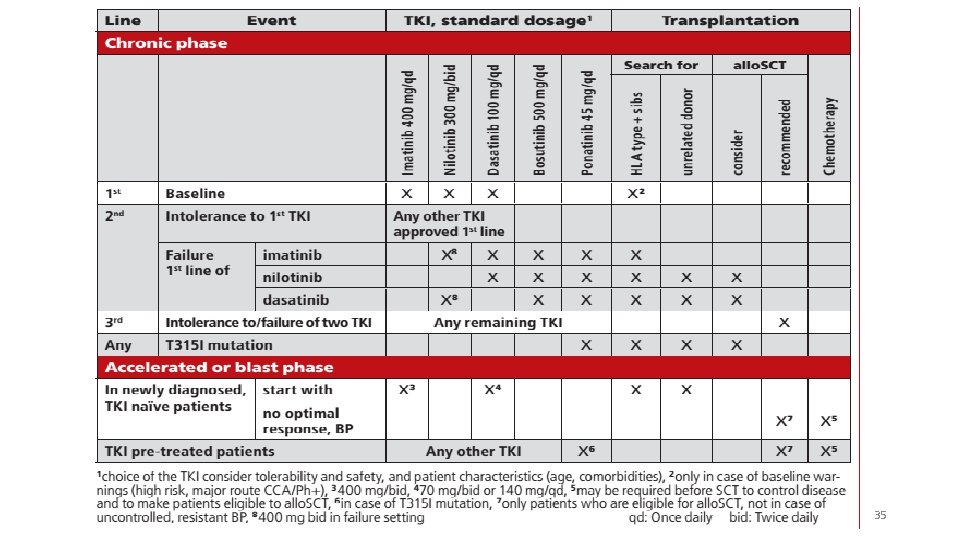
35
Hangi TKİ ? • Tolerans • Komorbidite • Potansiyel geç komplikasyonlar • Risk durumu • Erken moleküler yanıt elde edilebilmesi • Fiyat • SGK

37
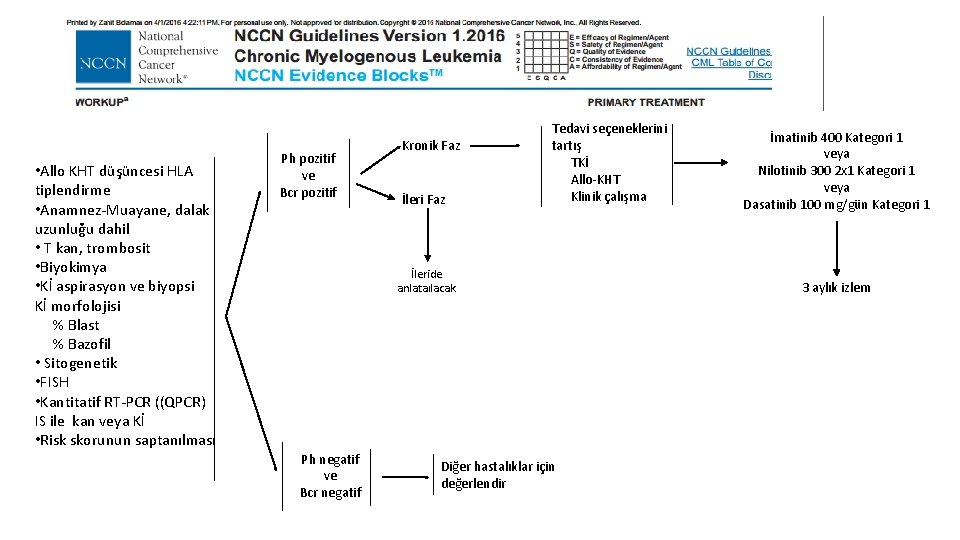
• Allo KHT düşüncesi HLA tiplendirme • Anamnez-Muayane, dalak uzunluğu dahil • T kan, trombosit • Biyokimya • Kİ aspirasyon ve biyopsi Kİ morfolojisi % Blast % Bazofil • Sitogenetik • FISH • Kantitatif RT-PCR ((QPCR) IS ile kan veya Kİ • Risk skorunun saptanılması Ph pozitif ve Bcr pozitif Kronik Faz İleri Faz Tedavi seçeneklerini tartış TKİ Allo-KHT Klinik çalışma İleride anlataılacak Ph negatif ve Bcr negatif Diğer hastalıklar için değerlendir İmatinib 400 Kategori 1 veya Nilotinib 300 2 x 1 Kategori 1 veya Dasatinib 100 mg/gün Kategori 1 3 aylık izlem
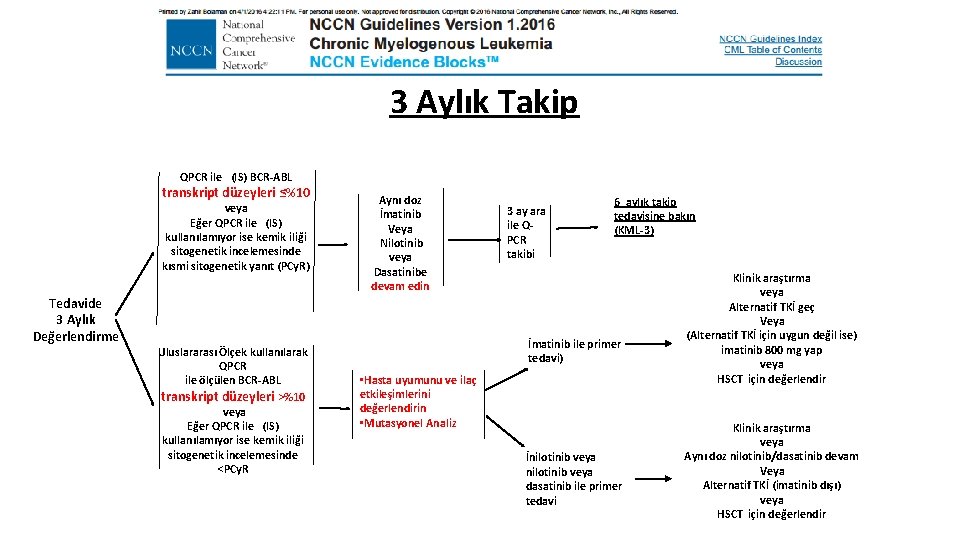
3 Aylık Takip QPCR ile (IS) BCR-ABL transkript düzeyleri ≤%10 veya Eğer QPCR ile (IS) kullanılamıyor ise kemik iliği sitogenetik incelemesinde kısmi sitogenetik yanıt (PCy. R) Tedavide 3 Aylık Değerlendirme Uluslararası Ölçek kullanılarak QPCR ile ölçülen BCR-ABL transkript düzeyleri >%10 veya Eğer QPCR ile (IS) kullanılamıyor ise kemik iliği sitogenetik incelemesinde <PCy. R Aynı doz İmatinib Veya Nilotinib veya Dasatinibe devam edin 3 ay ara ile QPCR takibi 6 aylık takip tedavisine bakın (KML-3) İmatinib ile primer tedavi) • Hasta uyumunu ve ilaç etkileşimlerini değerlendirin • Mutasyonel Analiz İnilotinib veya dasatinib ile primer tedavi Klinik araştırma veya Alternatif TKİ geç Veya (Alternatif TKİ için uygun değil ise) imatinib 800 mg yap veya HSCT için değerlendir Klinik araştırma veya Aynı doz nilotinib/dasatinib devam Veya Alternatif TKİ (imatinib dışı) veya HSCT için değerlendir
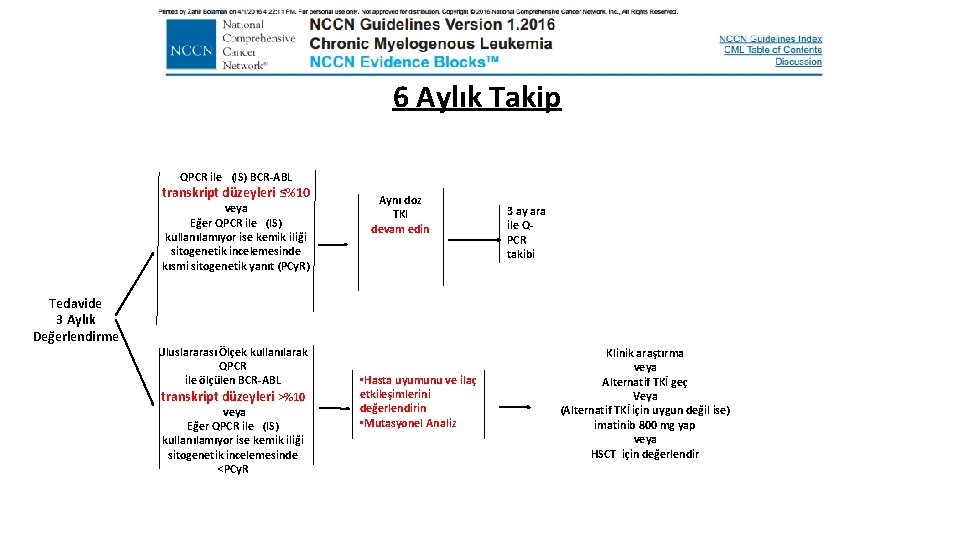
6 Aylık Takip QPCR ile (IS) BCR-ABL transkript düzeyleri ≤%10 veya Eğer QPCR ile (IS) kullanılamıyor ise kemik iliği sitogenetik incelemesinde kısmi sitogenetik yanıt (PCy. R) Tedavide 3 Aylık Değerlendirme Uluslararası Ölçek kullanılarak QPCR ile ölçülen BCR-ABL transkript düzeyleri >%10 veya Eğer QPCR ile (IS) kullanılamıyor ise kemik iliği sitogenetik incelemesinde <PCy. R Aynı doz TKI devam edin • Hasta uyumunu ve ilaç etkileşimlerini değerlendirin • Mutasyonel Analiz 3 ay ara ile QPCR takibi Klinik araştırma veya Alternatif TKİ geç Veya (Alternatif TKİ için uygun değil ise) imatinib 800 mg yap veya HSCT için değerlendir
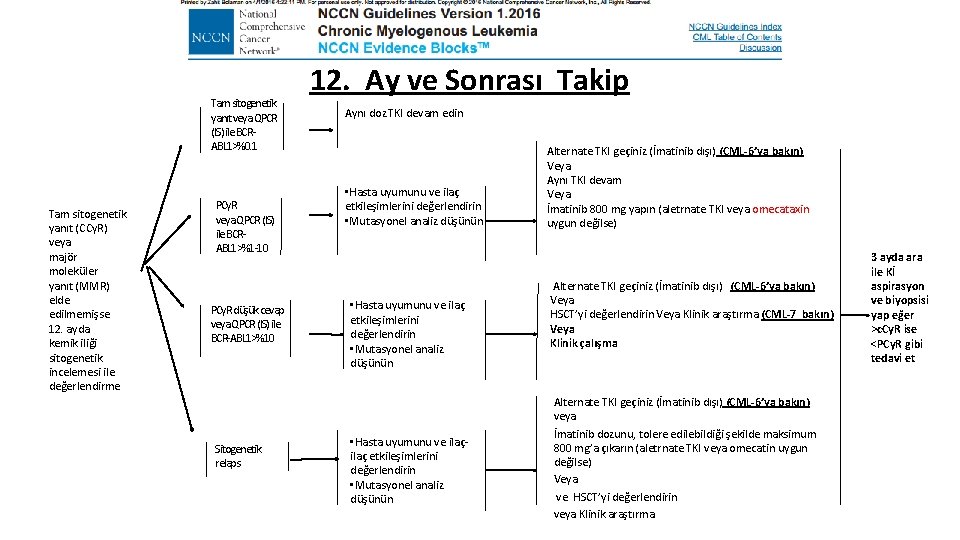
Tam sitogenetik yanıt veya QPCR (IS) ile BCRABL 1>%0. 1 Tam sitogenetik yanıt (CCy. R) veya majör moleküler yanıt (MMR) elde edilmemişse 12. ayda kemik iliği sitogenetik incelemesi ile değerlendirme PCy. R veya QPCR (IS) ile BCRABL 1>%1 -10 PCy. R düşük cevap veya QPCR (IS) ile BCR-ABL 1>%10 Sitogenetik relaps 12. Ay ve Sonrası Takip Aynı doz TKI devam edin • Hasta uyumunu ve ilaç etkileşimlerini değerlendirin • Mutasyonel analiz düşünün Alternate TKI geçiniz (İmatinib dışı) (CML-6’ya bakın) Veya Aynı TKI devam Veya İmatinib 800 mg yapın (aletrnate TKI veya omecataxin uygun değilse) Alternate TKI geçiniz (İmatinib dışı) (CML-6’ya bakın) Veya HSCT’yi değerlendirin Veya Klinik araştırma (CML-7 bakın) Veya Klinik çalışma Alternate TKI geçiniz (İmatinib dışı) (CML-6’ya bakın) veya İmatinib dozunu, tolere edilebildiği şekilde maksimum 800 mg’a çıkarın (aletrnate TKI veya omecatin uygun değilse) Veya ve HSCT’yi değerlendirin veya Klinik araştırma 3 ayda ara ile Kİ aspirasyon ve biyopsisi yap eğer >c. Cy. R ise <PCy. R gibi tedavi et

42

43
44
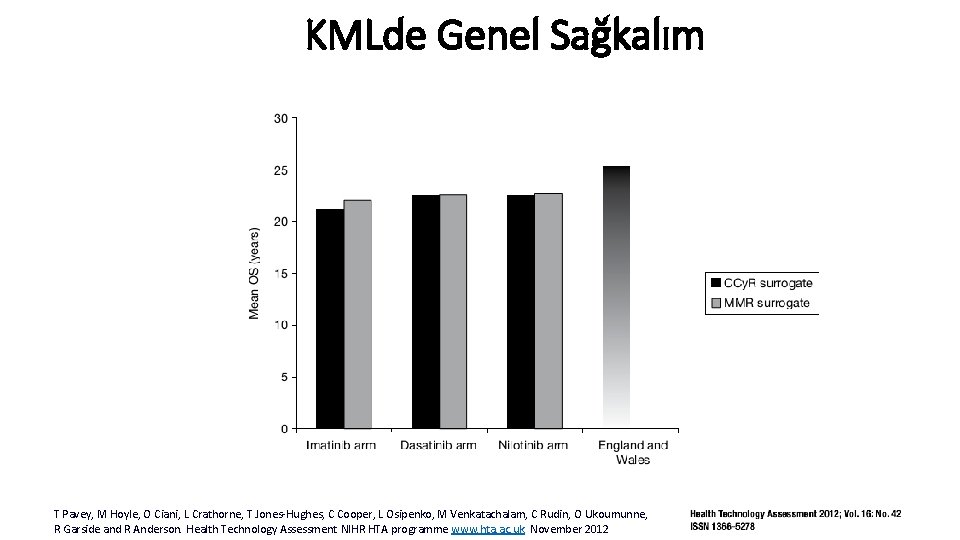
KMLde Genel Sağkalım T Pavey, M Hoyle, O Ciani, L Crathorne, T Jones-Hughes, C Cooper, L Osipenko, M Venkatachalam, C Rudin, O Ukoumunne, R Garside and R Anderson. Health Technology Assessment NIHR HTA programme www. hta. ac. uk November 2012

46
- Slides: 46