Kmiai reakcik sebessge A vltozs nem egyenletes v

Kémiai reakciók sebessége A változás nem egyenletes !!!!!!!!! v= ± dc dt Melyik reagens koncentrációváltozását figyeljük ? ? ? ? ?
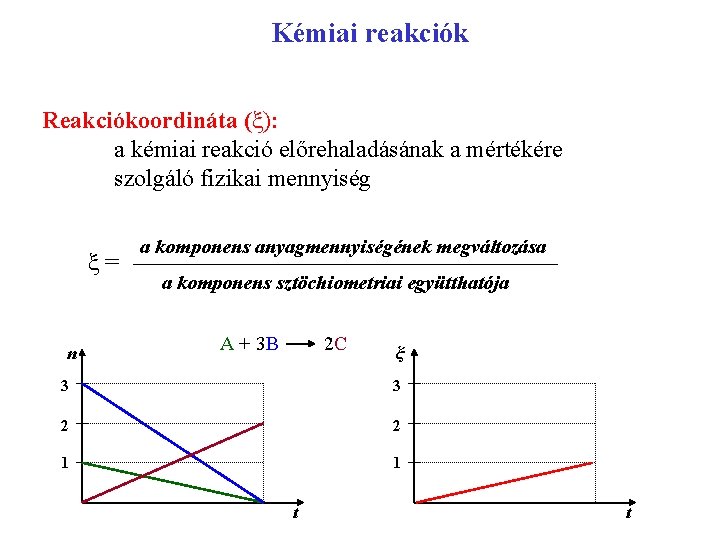
Kémiai reakciók Reakciókoordináta (ξ): a kémiai reakció előrehaladásának a mértékére szolgáló fizikai mennyiség ξ= n a komponens anyagmennyiségének megváltozása a komponens sztöchiometriai együtthatója A + 3 B 2 C ξ 3 3 2 2 1 1 t t

Kémiai reakciók sebessége dc A változás nem egyenletes !!!!!!!!! dt Melyik reagens koncentrációváltozását figyeljük ? ? ? ? ? v= ± Ha a térfogat állandó: Reakciósebesség (vξ) = reakciókoordináta időegységre eső megváltozása vξ= – 1 a d[A] = 1 c dt d[ξ/V] d[C] = dt dt

Reakciósebesség függ: 1. reagáló anyagok kémiai tulajdonsága 2. reagáló anyagok koncentrációja 3. hőmérséklet 4. a reagáló felület nagysága 5. katalizátor Sok reakció sebessége arányos a reagáló anyagok koncentrációinak valamely hatványával.
+ Na+ H 2 CO 3 H 2 O + CO 2

Kémiai reakciók sebessége CH 4 (g) + 2 O 2 (g) CO 2 (g) + 2 H 2 O (g) ∆Hr 0 = ∆Hk 0(CO 2) + 2∙∆Hk 0(H 2 O) – ∆Hk 0(CH 4) – 2∙∆Hk 0(O 2) ∆Hr 0 = 1(-393, 5) + 2(-241, 8) – 1(-74, 81) – 2(0, 0) = -802, 29 k. J 1 mol metán égésekor felszabaduló hő: 802, 29 k. J 4 Fe (sz) + 3 O 2 (g) 2 Fe 2 O 3 (sz) ∆Hr 0 = 2∙∆Hk 0(Fe 2 O 3) – 4∙∆Hk 0(Fe) – 3∙∆Hk 0(O 2) ∆Hr 0 = 2(-831, 1) – 4(0, 0) – 3(0, 0) = -1662, 2 k. J 1 mol Fe „rozsdásodása” során felszabaduló hő: 1662, 2 / 4 = 415, 55 k. J

Kémiai reakciók sebessége pillanatnyi sebesség reakciósebességi állandó Adott hőmérsékleten !!!!!
![[A] az A anyag aktivitása Ideális gázok esetén: Oldatok esetén: a. A a = [A] az A anyag aktivitása Ideális gázok esetén: Oldatok esetén: a. A a =](http://slidetodoc.com/presentation_image_h2/67aa1c35a54411cbbf8733f494aa5a30/image-8.jpg)
[A] az A anyag aktivitása Ideális gázok esetén: Oldatok esetén: a. A a = p/p 0 (p 0= 101, 325 k. Pa) a = γc·c/c 0 (c 0= 1 mol/dm 3) γc → 1, ha c → 0

Reakciósebességi állandó Svante Arrhenius 1889 A = preexponenciális faktor (állandó) Ea= aktiválási energia (állandó)
![Ütközési elmélet Elemi gázfázisú bimolekuláris reakció esetén: ütközési sebesség = konst. [A][B] reakciósebesség = Ütközési elmélet Elemi gázfázisú bimolekuláris reakció esetén: ütközési sebesség = konst. [A][B] reakciósebesség =](http://slidetodoc.com/presentation_image_h2/67aa1c35a54411cbbf8733f494aa5a30/image-10.jpg)
Ütközési elmélet Elemi gázfázisú bimolekuláris reakció esetén: ütközési sebesség = konst. [A][B] reakciósebesség = ƒ ∙ ütközési sebesség ƒ – molekulák hányada, ahol E >Emin Ludwig Boltzmann lnƒ = –Emin RT Molekulák hányada reakciósebesség = ƒ ∙ konst. [A][B] k = ƒ ∙ konst. alacsony hőmérséklet molekulák melyek kinetikus energiája nagyobb, mint Ea magas hőmérséklet Kinetikus energia ln k = ln konst. + ln ƒ
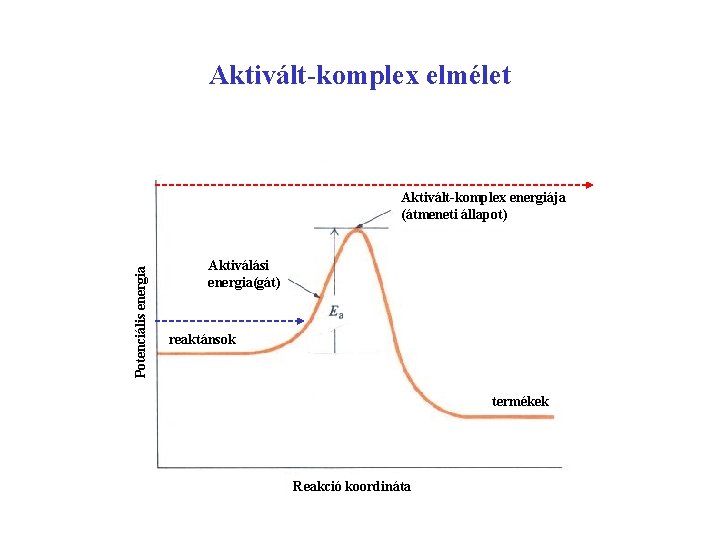
Aktivált-komplex elmélet Potenciális energia Aktivált-komplex energiája (átmeneti állapot) Aktiválási energia(gát) reaktánsok termékek Reakció koordináta
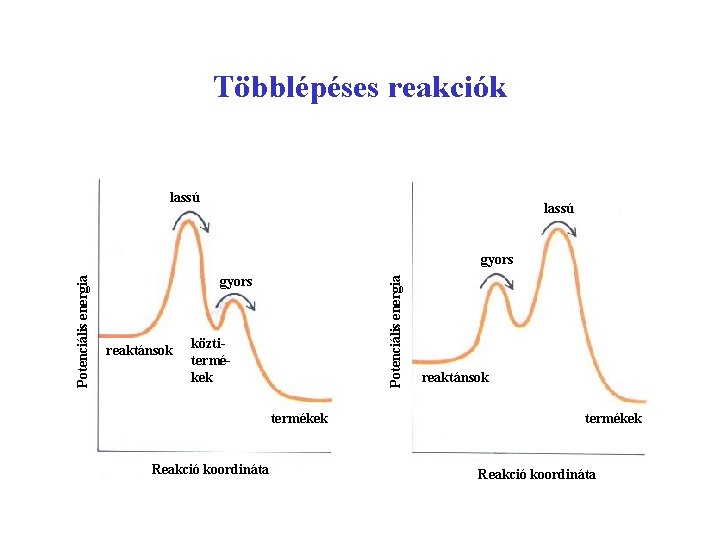
Többlépéses reakciók lassú gyors reaktánsok Potenciális energia gyors köztitermékek Reakció koordináta reaktánsok termékek Reakció koordináta
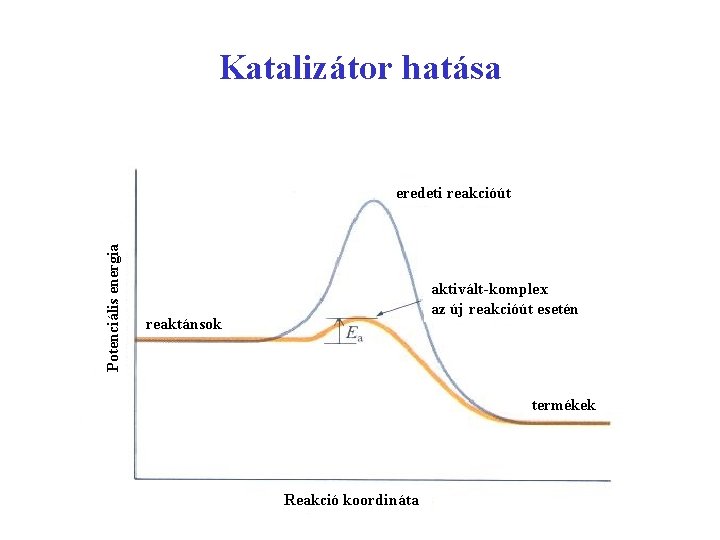
Katalizátor hatása Potenciális energia eredeti reakcióút aktivált-komplex az új reakcióút esetén reaktánsok termékek Reakció koordináta

Potenciális energia Kémiai reakciók lejátszódásának feltétele
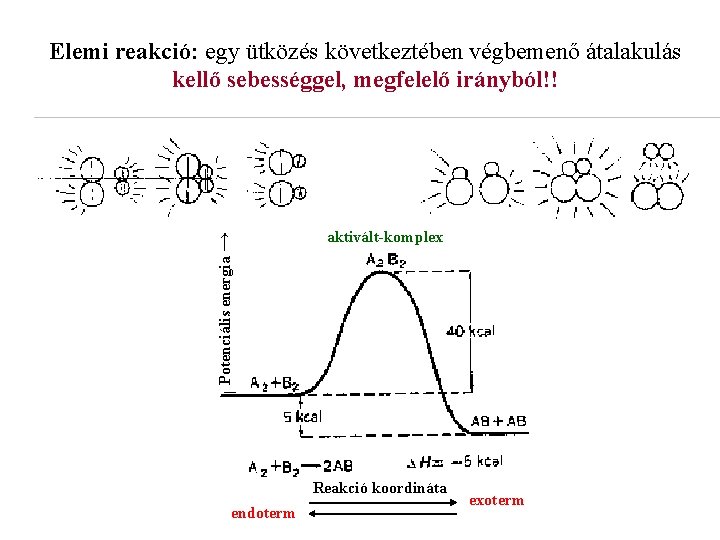
Potenciális energia → Elemi reakció: egy ütközés következtében végbemenő átalakulás kellő sebességgel, megfelelő irányból!! aktivált-komplex Reakció koordináta endoterm exoterm

Kémiai reakciók sebessége Potenciális energia Reakciósebesség (vξ) = reakciókoordináta időegységre eső megváltozása v 1= k[A][B] → ← v 2= k’[C][D] k és k’= reakciósebességi állandók
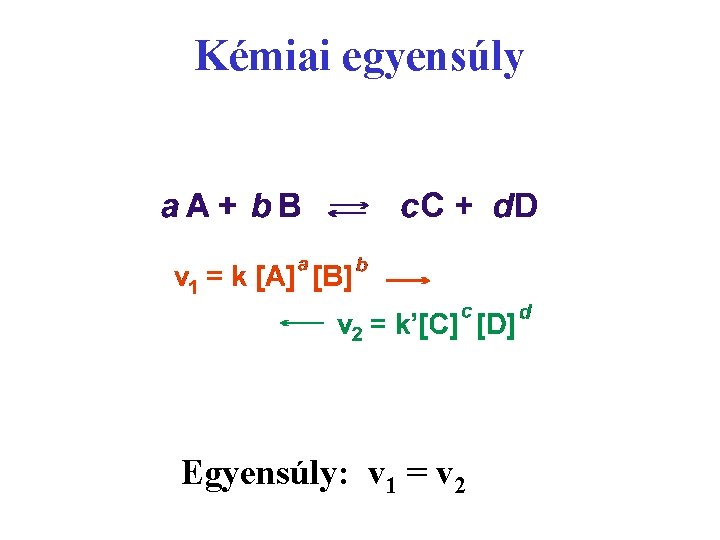
Kémiai egyensúly Egyensúly: v 1 = v 2
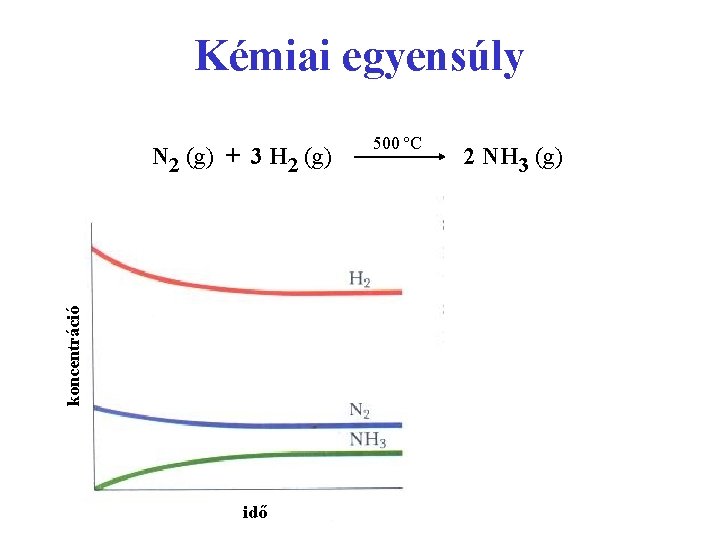
Kémiai egyensúly koncentráció N 2 (g) + 3 H 2 (g) idő 500 ºC 2 NH 3 (g)

Kémiai egyensúly K függ a hőmérséklettől. egyensúlyi koncentrációk

A tömeghatás törvénye: Egy adott hőmérsékleten, egyensúlyban a termékek megfelelő hatványon vett egyensúlyi koncentrációinak szorzata osztva a kiindulási anyagok megfelelő hatványon vett egyensúlyi koncentrációinak szorzatával, állandó.
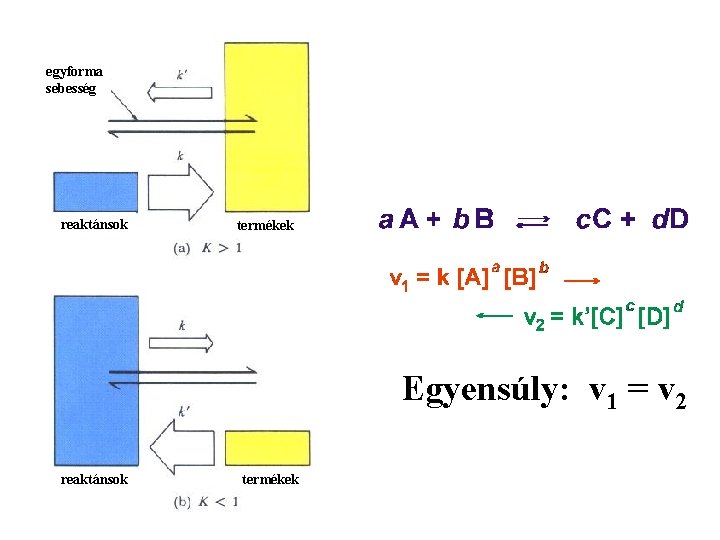
egyforma sebesség reaktánsok termékek Egyensúly: v 1 = v 2 reaktánsok termékek

A körülmények hatása az egyensúlyra Henri Le Chatelier 1884 Le Chatelier elv: egy dinamikus egyensúly külső hatásra úgy viselkedik, hogy a külső hatást tompítani igyekszik. 1. Hőmérséklet 2. Nyomás 3. Hozzáadott reagens
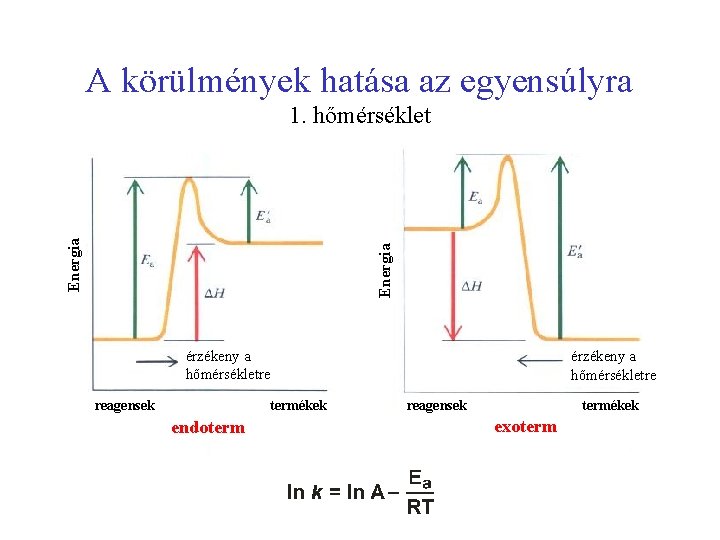
A körülmények hatása az egyensúlyra Energia 1. hőmérséklet érzékeny a hőmérsékletre reagensek termékek endoterm érzékeny a hőmérsékletre reagensek termékek exoterm
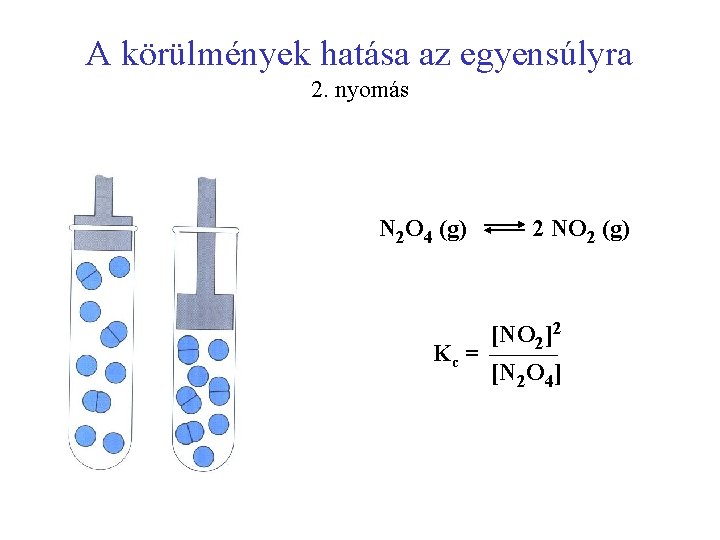
A körülmények hatása az egyensúlyra 2. nyomás N 2 O 4 (g) Kc = 2 NO 2 (g) [NO 2]2 [N 2 O 4]

A körülmények hatása az egyensúlyra 3. hozzáadott reagens megnöveljük

A körülmények hatása az egyensúlyra N 2 (g) + 3 H 2 (g) 500 ºC katalizátor Fe 2 NH 3 (g) exoterm NH 3 keletkezésének kedvez: 1. nyomás növelése 2. hőmérséklet csökkentése reakciósebesség !!!! katalizátor alkalmazása ? ? ? ?

Egyensúlyi állandó Kc= koncentrációkkal kifejezett e. á. (mol/l) Kx= móltörtekkel kifejezett e. á. Kn= mólszámokkal kifejezett e. á. Ka= parciális nyomások és a normál légköri nyomás hányadosával kifejezett e. á. Kp= parciális nyomásokkal kifejezett e. á.

Feladat: Egy kísérlet során 3 mol H 2 -t és 6 mol F 2 -t elegyítünk egy 3 dm 3 térfogatú tartályban. Mennyi a komponensek egyensúlyi koncentrációja a reakció lejátszódása után ? H 2(g) + F 2(g) ↔ 2 HF (g) Kc= 115


Feladat: 2 mol etanol és 3 mol ecetsav reakciója során etil-acetát és víz keletkezett. Számítsa ki a komponensek egyensúlyi móltörtjeit, ha Kx=4, 0.

- Slides: 31