Kmiai anyagszerkezettan Elad Kubinyi Mikls Tel 463 1484

Kémiai anyagszerkezettan Előadó: Kubinyi Miklós Tel: 463 -1484 kubinyi@mail. bme. hu 1

Vegyészmérnök MSc: Fizikai Kémia és Kémiai Anyagszerkezettan (BMEVEFAM 201) Fizikai Kémia előadások: szept. 7. – okt. 21. Szerda 08: 15 -10: 00 (K 255) , Péntek 14: 15 – 16: 00 (K. 1. 34) Statisztikus termodinamika (Dr. Rolik Zoltán, 3 ea. ) Radiokémia (Dr. László Krisztina, 4 ea. ) Felületek, elegyek (Dr. Szilágyi András, 6 ea. ) Dolgozat: 2016. november 4. , pótdolgozat: november 18. Gyógyszermérnök MSc Kémiai Anyagszerkezettan (BMEVEFAM 204) 2

Fizikai Kémia • Fizikai Kémia I. - egyensúlyok (fázisegyensúlyok, kémiai egyensúlyok) • Fizikai Kémia II. - változások (reakciókinetika, transzportfolyamatok) • Fizikai Kémia III. - szerkezet (molekulák szerkezete, anyagok szerkezete) 3


Tananyag az oktatas szerveren: http: //oktatas. ch. bme. hu/oktatas/ konyvek/fizkem/kasz/ előadás: Tananyag 16 jegyzet: Tananyag 05 5

Tananyag I. BEVEZETÉS (Bevez 05) II. A KVANTUMMECHANIKA AXIÓMÁI (Axiom 05) III. A HIDROGÉNATOM SZERKEZETE (H_atom 05) IV. A TÖBBELEKTRONOS ATOMOK ELEKTRONSZERKEZETE (Tobbel 05) V. OPTIKAI SPEKTROSZKÓPIA (Optsp 05) VI. A MOLEKULÁK FORGÓMOZGÁSA (Forgo 05) VII. A MOLEKULÁK REZGŐMOZGÁSA (Rezgo 05) VIII. A MOLEKULÁK ELEKTRONSZERKEZETE (Molel 05) IX. FOTOELEKTRON-SPEKTROSZKÓPIA (UPSXPS 05) X. LÉZEREK, LÉZERSPEKTROSZKÓPIAI MÓDSZEREK (Lezer 05) XI. AZ ATOMMAGOK ENERIGIAÁLLAPOTAI (Magszerk 05) XII. A MÁGNESES MAGREZONANCIA XII. AZ ELEKTRONSPIN-REZONANCIA XIV. TÖMEGSPEKTROSZKÓPIA (Tomegsp 05) XV. A RÖNTGENDIFFRAKCIÓ (Rontg 05) 6

Bevezetés I. Példák kémiai szerkezetvizsgálati feladatokra 7
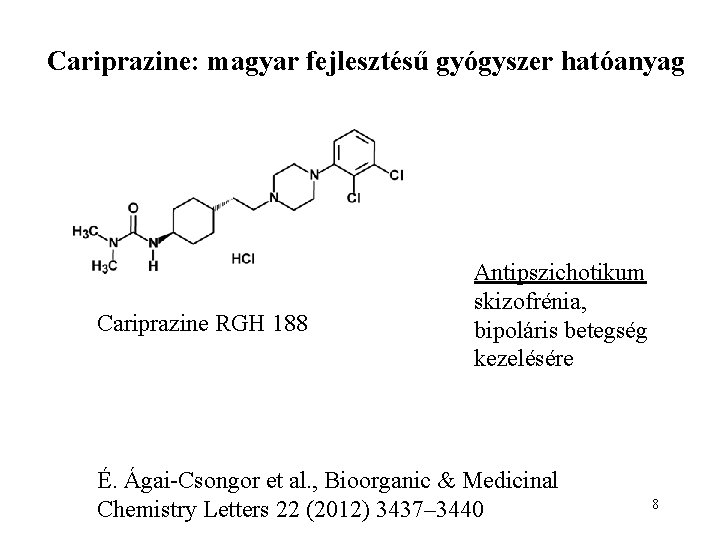
Cariprazine: magyar fejlesztésű gyógyszer hatóanyag Cariprazine RGH 188 Antipszichotikum skizofrénia, bipoláris betegség kezelésére É. Ágai-Csongor et al. , Bioorganic & Medicinal Chemistry Letters 22 (2012) 3437– 3440 8
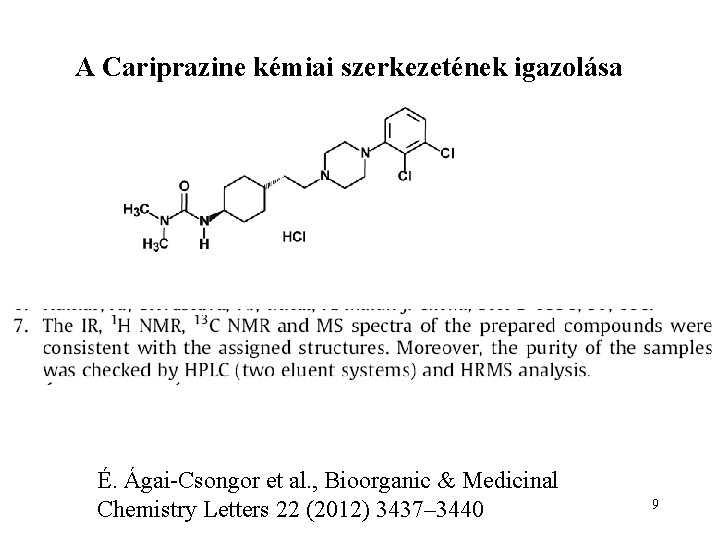
A Cariprazine kémiai szerkezetének igazolása É. Ágai-Csongor et al. , Bioorganic & Medicinal Chemistry Letters 22 (2012) 3437– 3440 9
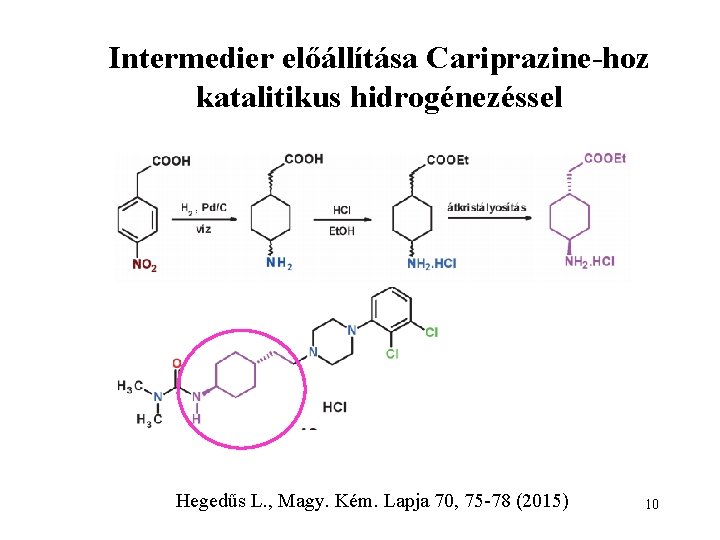
Intermedier előállítása Cariprazine-hoz katalitikus hidrogénezéssel Hegedűs L. , Magy. Kém. Lapja 70, 75 -78 (2015) 10
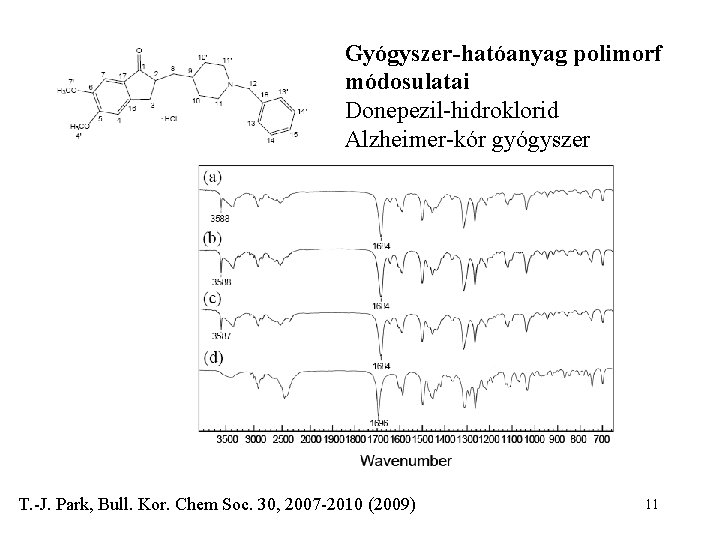
Gyógyszer-hatóanyag polimorf módosulatai Donepezil-hidroklorid Alzheimer-kór gyógyszer T. -J. Park, Bull. Kor. Chem Soc. 30, 2007 -2010 (2009) 11
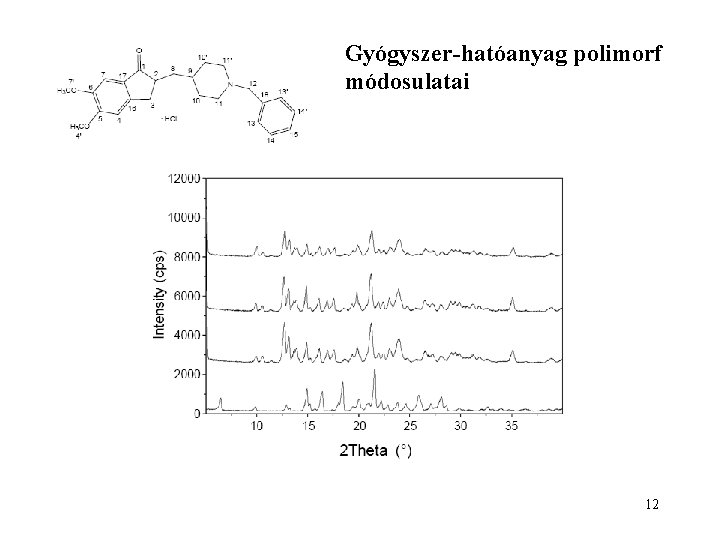
Gyógyszer-hatóanyag polimorf módosulatai 12
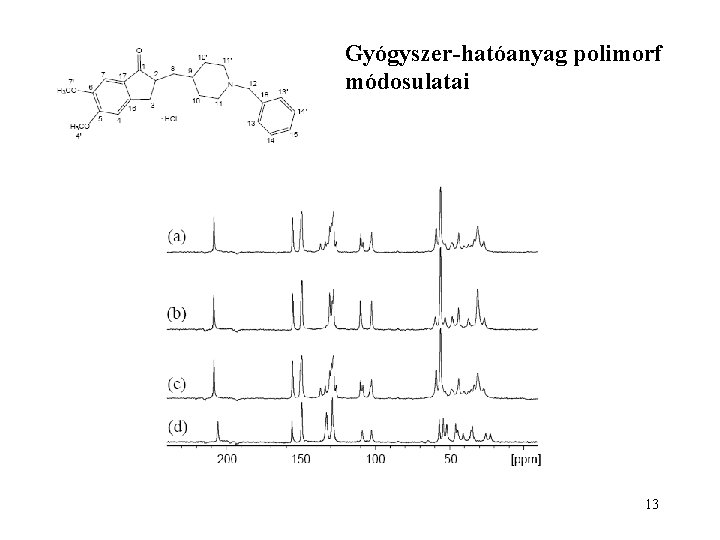
Gyógyszer-hatóanyag polimorf módosulatai 13
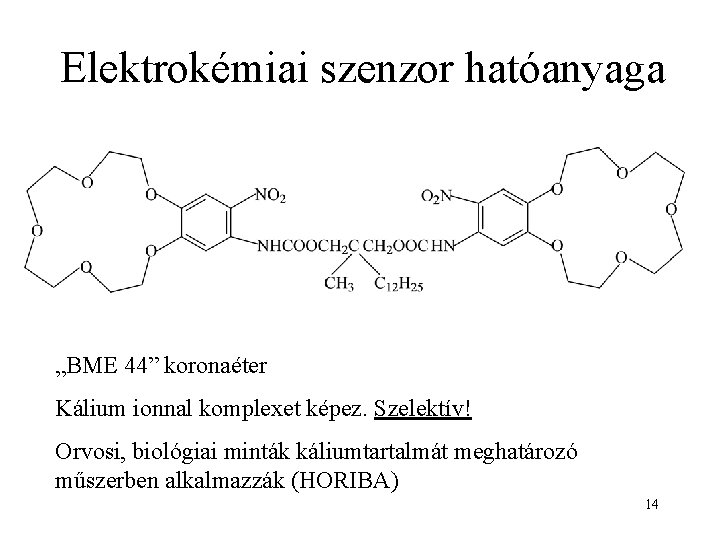
Elektrokémiai szenzor hatóanyaga „BME 44” koronaéter Kálium ionnal komplexet képez. Szelektív! Orvosi, biológiai minták káliumtartalmát meghatározó műszerben alkalmazzák (HORIBA) 14
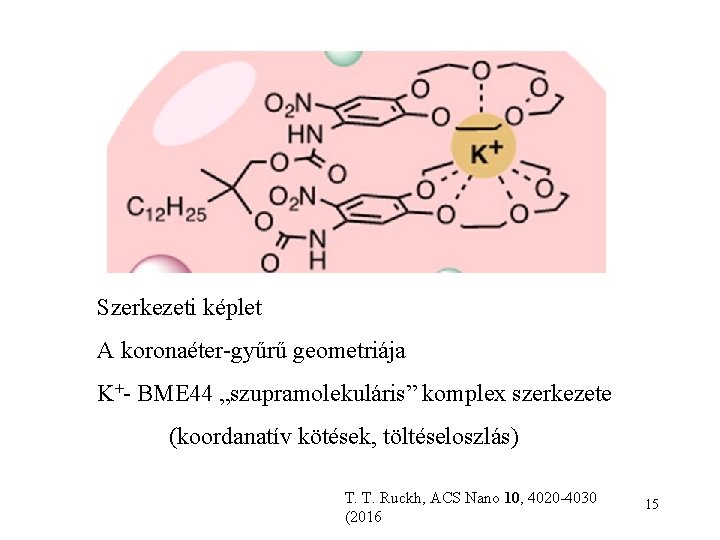
Szerkezeti képlet A koronaéter-gyűrű geometriája K+- BME 44 „szupramolekuláris” komplex szerkezete (koordanatív kötések, töltéseloszlás) T. T. Ruckh, ACS Nano 10, 4020 -4030 (2016 15

1. 1. Bevezetés a spektroszkópiába 16

A molekuláknak és a többi mikrorészecskének szerkezetét a kvantummechanika írja le. A kvantummechanika alapvető törvényeit az 1920 as években ismerték fel. Előzmény: néhány kísérlet, amely a klasszikus fizikának ellentmondó eredményre vezetett. 17

Joseph Fraunhofer kísérlete 1815 A Nap fényét prizmákon felbontotta. A folytonos színképben fekete vonalakat észlelt. 18

19

Magyarázat: a Nap folytonos sugárzást ad a Napot és a Földet körülvevő gázburok molekulái csak bizonyos hullámhosszú/frekvenciájú fotonokat (fénykvantumokat) nyelnek el. Az A molekula a rá jellemző A 1, A 2. . . a B molekula a rá jellemző B 1, B 2. . . Ezért az A molekula energiája EA= h A 1, h A 2… energiakvantumokkal változhat, a B molekuláé EB= h B 1, h B 2… energiakvantumokkal, stb. 20

A mikrorészecskék fizikai sajátságai közül egyesek köztük az energiájuk - csak bizonyos meghatározott kvantált - értékeket vehetnek fel. Erre utal a kvantummechanika elnevezés. 21

EGYSUGARAS UV-LÁTHATÓ ABSZORPCIÓS SPEKTROMÉTER 22
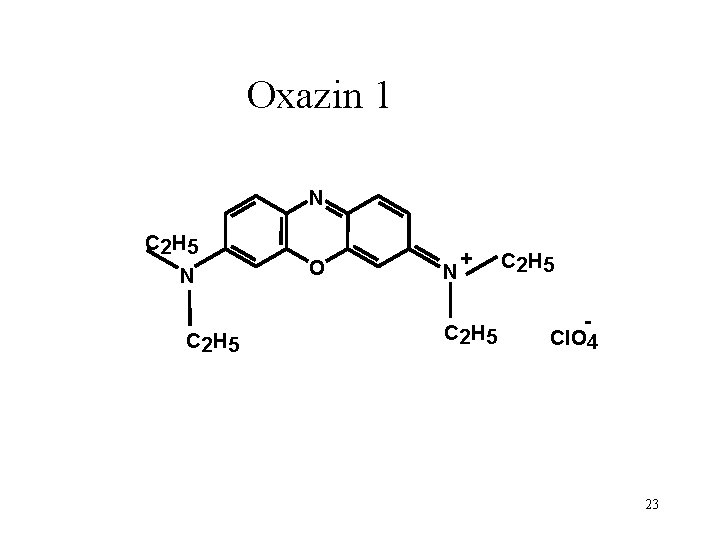
Oxazin 1 N C 2 H 5 O N + C 2 H 5 Cl. O 4 23
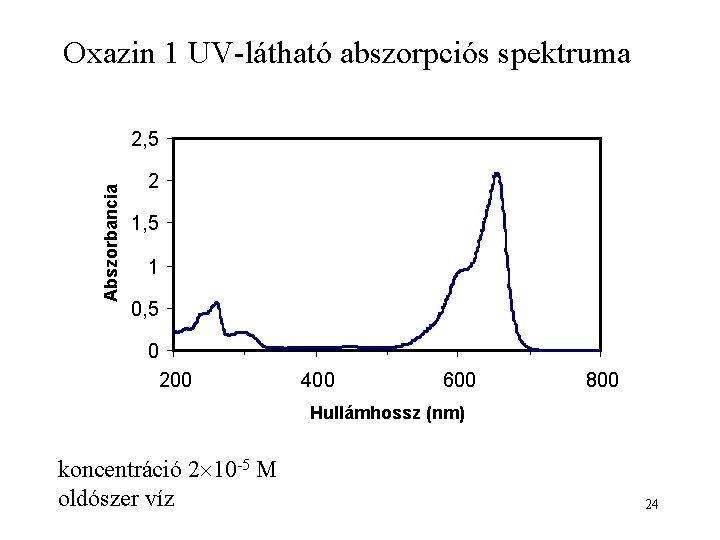
Oxazin 1 UV-látható abszorpciós spektruma Abszorbancia 2, 5 2 1, 5 1 0, 5 0 200 400 600 800 Hullámhossz (nm) koncentráció 2 10 -5 M oldószer víz 24
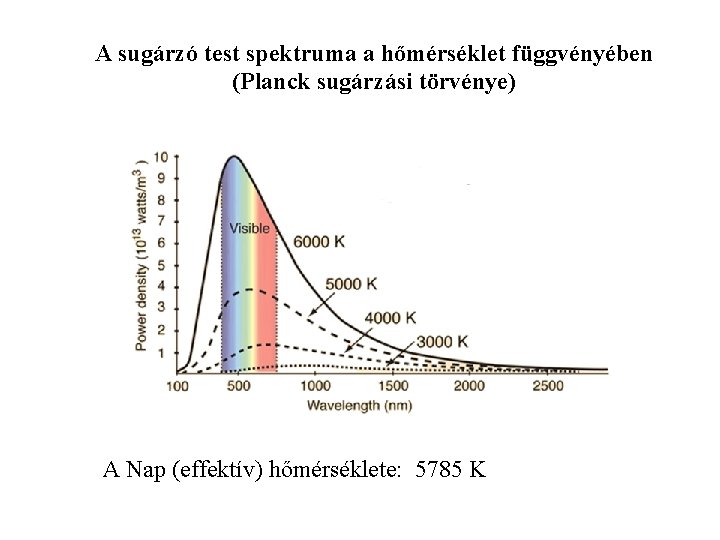
A sugárzó test spektruma a hőmérséklet függvényében (Planck sugárzási törvénye) A Nap (effektív) hőmérséklete: 5785 K
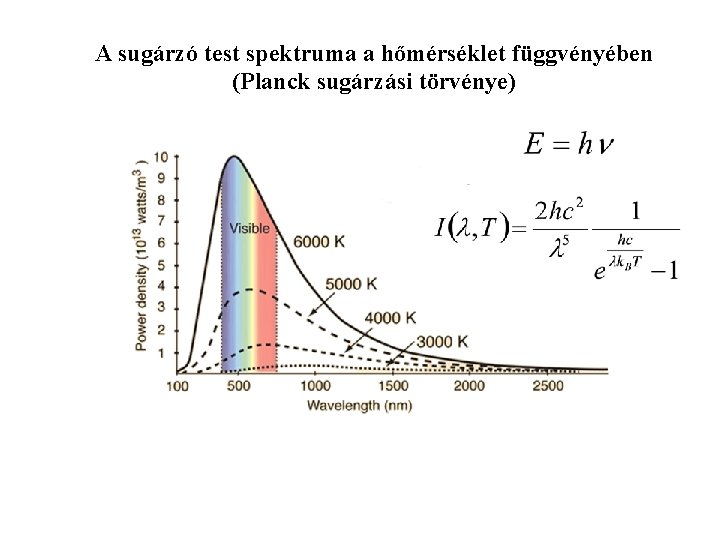
A sugárzó test spektruma a hőmérséklet függvényében (Planck sugárzási törvénye)

1. 2. Bevezetés a kvantummechanikába 27

Erwin Schrödinger: Quantisierung als Eigenwertproblem négy közlemény 1926 -ban, első rész: E. Schrödinger, Ann. Phys. 79, 361 -376 (1926) 28

A Schrödinger-egyenlet A kvantummechanika legfontosabb összefüggése! (Röviden: ) 29

Differenciálegyenlet a molekulát alkotó atommagok és elektronok helykoordinátái szerinti differenciálhányadosokat tartalmaz ezen koordináták közös jelölése: 30

Pl. : H 2 S molekula esetében (magok) (elektronok) 31

Hamilton-operátor Az operátor függvényen végzett műveletet jelöl ki. A Hamilton-operátor több tagból áll, amelyek közül egyesek a magok és az elektronok térkoordinátái szerinti parciális deriválást tartalmaznak. ( ) a molekula állapotfüggvénye E a molekula energiája 32

A differenciálegyenletek megoldásai függvények. A Schrödinger-egyenlet megoldásai a 0( ) állapotfüggvény és a hozzátartozó E 0 energia-sajátérték, a 1( ) állapotfüggvény és a hozzátartozó E 1 energia-sajátérték, 2( ), E 2. . . 33

A kvantummechanikai számítás eredményei A molekula -ik állapotát jellemző ( ) állapotfüggvény megadja, hogy a tér egyes pontjaiban mekkora az elektronok és a különféle atommagok tartózkodási valószínűsége. Ebből leszármaztatható - a magok elhelyezkedését jellemző kötéstávolságok, kötésszögek (molekulageometria) - az atomok parciális töltései (reakciókészséghez fontos) - kémiai kötések erőssége 34

A kvantummechanikai számítás eredményei Elméleti úton számítható a spektrum! 35

Elnyelési (abszorpciós spektrum): a fényelés intenzitása a fény frekvenciájának függvényében. Kibocsátási (emissziós) spektrum: a fénykibocsátás intenzitása a fény frekvenciájának függvényében. 36

A kvantummechanikai számítás eredményei Elméleti úton számítható a spektrum! Az elnyelési frekvenciákat a kiindulási állapot ( ) és a végállapot ( ) energiájának különbsége határozza meg: E - E = h A spektrumvonal intenzitása arányos a két állapot ( és ) közötti sugárzásos átmenet valószínűségével, amely kiszámítható, ha ismerjük a molekula állapotfüggvényét kiindulási állapotban ( ( )) és a végállapotban ( ( )). 37

1. 3. A kémiai szerkezetvizsgálati módszerek áttekintése 38

NMR Laboratórium
![Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1818 1010 1022 [Hz] Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1818 1010 1022 [Hz]](http://slidetodoc.com/presentation_image_h2/be25ea16e2c1fb697ef58eb210a1c5a5/image-40.jpg)
Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1818 1010 1022 [Hz] rádióhullámú mikrohullámú infravörös látható ultraibolya röntgen gamma 40
![Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1818 1010 1022 [Hz] Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1818 1010 1022 [Hz]](http://slidetodoc.com/presentation_image_h2/be25ea16e2c1fb697ef58eb210a1c5a5/image-41.jpg)
Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1818 1010 1022 [Hz] rádióhullámú mikrohullámú infravörös látható ultraibolya röntgen gamma OPTIKAI SPEKTROSZKÓPIA (molekulák gerjesztése) 41
![Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1818 1010 1022 [Hz] Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1818 1010 1022 [Hz]](http://slidetodoc.com/presentation_image_h2/be25ea16e2c1fb697ef58eb210a1c5a5/image-42.jpg)
Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1818 1010 1022 [Hz] rádióhullámú mikrohullámú infravörös látható ultraibolya röntgen gamma OPTIKAI SPEKTROSZKÓPIA (molekulák gerjesztése) NMR SPEKTROSZKÓPIA (magok gerjesztése) 42
![Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1818 1010 1022 [Hz] Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1818 1010 1022 [Hz]](http://slidetodoc.com/presentation_image_h2/be25ea16e2c1fb697ef58eb210a1c5a5/image-43.jpg)
Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1818 1010 1022 [Hz] rádióhullámú mikrohullámú infravörös látható ultraibolya röntgen gamma OPTIKAI SPEKTROSZKÓPIA (molekulák gerjesztése) NMR SPEKTROSZKÓPIA (magok gerjesztése) FOTOELEKTRON SPEKTROSZKÓPIA (molekulák ionizálása) 43
![Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1018 1022 1020 [Hz] Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1018 1022 1020 [Hz]](http://slidetodoc.com/presentation_image_h2/be25ea16e2c1fb697ef58eb210a1c5a5/image-44.jpg)
Az elektromágneses sugárzás tartományai 106 108 1010 1012 1014 1016 1018 1022 1020 [Hz] rádióhullámú mikrohullámú infravörös látható ultraibolya röntgen gamma OPTIKAI SPEKTROSZKÓPIA (molekulák gerjesztése) NMR SPEKTROSZKÓPIA (magok gerjesztése) FOTOELEKTRON SPEKTROSZKÓPIA (molekulák ionizálása) MÖSSBAUER SPEKTROSZKÓPIA (magok gerjesztése) 44

Alapkérdések 1. Írja fel a foton energiájának képletét! 2. Mit nevezünk Fraunhofer-vonalaknak, és mi a magyarázat a megjelenésükre? 3. Írja fel a stacionárius Schrödinger-egyenlet általános alakját! 4. Sorolja fel az elektromágneses hullám tartományait növekvő frekvencia szerint! 5. Milyen fő részekből épül fel az egy-utas UV-látható abszorpciós spektrométer? 6. Milyen összefüggés áll fenn az elektromágneses hullám frekvenciája és hullámhossza között? 45
- Slides: 45