Kmia termktervezknek Kovcs Attila BME Szervetlen s Analitikai

Kémia terméktervezőknek Kovács Attila BME, Szervetlen és Analitikai Kémia Tanszék MTA-BME Anyagszerkezeti és Modellezési Kutatócsoport akovacs@mail. bme. hu http: //amkcs. ch. bme. hu/ka. htm Tel. : 463 -22 -78

Kurzussal kapcsolatos tudnivalók • Vizsgaidőszakban írásbeli vizsga • Opcionális: évközben előadásidőben 3 db zárthelyi megajánlott jegy (Időpont megegyezés szerint, csak az utolsó előadás napja fix) • Előadásanyag (ppt) honlapról előre letölthető http: //amkcs. ch. bme. hu/ka. htm • Előadás: K 140, 17. 15 - ? ?
A kémia helye a természettudományok között

Miért van szüksége a gépész terméktervezőnek kémiai tudásra? • Vegyiparban, kutatóintézetekben, egyéb laborokban • • gépekkel, műszerekkel dolgoznak Gépeket felépítő anyagnak vannak kémiai vonatkozásai • fém, ötvözet, műanyag • megfelelő szilárdság, környezeti hatásokkal szembeni ellenállóság Gépek működésének kémiai vonatkozásai • működésbiztosítás (kenőolaj) • megmunkált anyag tulajdonságai • műszerekkel nyert kémiai információ (gép célja)

Tematika • Általános kémia • Szervetlen kémia • Szerves kémia • • • Atomok, molekulák, kémiai kötések Periódusos rendszer (http: //www. ptable. com/) Anyagi halmazok (gáz, folyadék, szilárd, ötvözetek) Kémiai reakciók (reakcióegyenlet, egyensúlyok, energetika) Elektrokémia (galvánelem, akkumulátor, korrózió)

Tematika • Általános kémia • Szervetlen kémia • Szerves kémia • Elemek • Alkáli-, alkáliföld- és átmeneti fémek vegyületei • Nemfémes elemek vegyületei

Tematika • Általános kémia • Szervetlen kémia • Szerves kémia • • Alifás vegyületek Aromás vegyületek Alkoholok, karbonsavak, aminok Polimerek (Dr. Wagner Ödön)

Az atom az anyag azon legkisebb stabil része, melyre az anyag kémiai úton bontható. A különböző elemek különböző atomokból állnak. Az adott atom határozza meg az adott elem kémiai tulajdonságait. Atomok egymásba való átalakítása csak nagy energiájú magreakciókkal történhet: • Radioaktív bomlás (14 C → 14 N + e-, felezési idő 5700 év) • Maghasadás (235 U + n 0 → kisebb atomok + 2 -3 n) • Magfúzió (2 H + 3 H → 4 He + n 0) Az atomok mérete: 10 -10 m (1 Å) nagyságrendnyi. Az atomok tömege: 10 -27 -10 -25 kg között. Makroszkopikus dimenzió: 1 mól = 6. 022. 1023 db részecske (atom, molekula) Moláris tömeg: 1 mól anyag tömege. Avogadro-féle állandó, NA
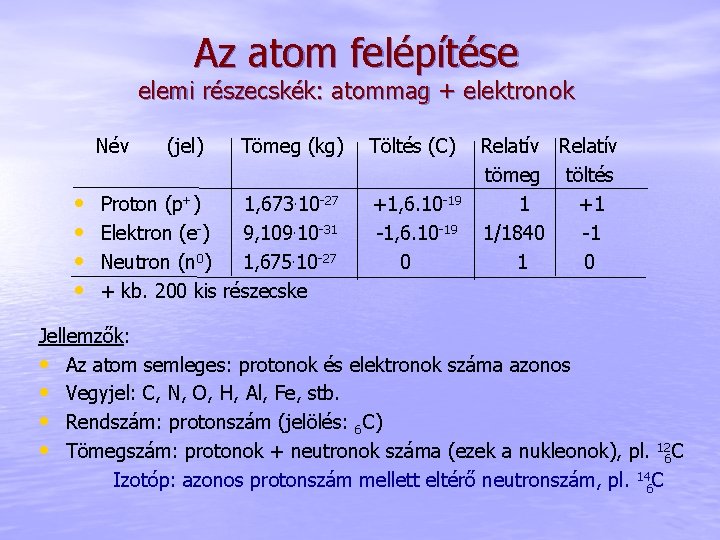
Az atom felépítése elemi részecskék: atommag + elektronok Név • • (jel) Tömeg (kg) Proton (p+) 1, 673. 10 -27 Elektron (e-) 9, 109. 10 -31 Neutron (n 0) 1, 675. 10 -27 + kb. 200 kis részecske Töltés (C) +1, 6. 10 -19 -1, 6. 10 -19 0 Relatív tömeg töltés 1 +1 1/1840 -1 1 0 Jellemzők: • Az atom semleges: protonok és elektronok száma azonos • Vegyjel: C, N, O, H, Al, Fe, stb. • Rendszám: protonszám (jelölés: 6 C) • Tömegszám: protonok + neutronok száma (ezek a nukleonok), pl. 126 C Izotóp: azonos protonszám mellett eltérő neutronszám, pl. 146 C

Elektronok Az elektronok a kb. 10 -15 m átmérőjű atommagok körül mozognak meghatározott energiájú és alakú elektronpályákon. Elektronpálya (atomok esetében atompálya) = ahol az elektron mozgása közben 90%-os valószínűséggel megtalálható. Jellemzők: • • Atommag – elektronok közötti vonzás Elektron – elektron taszítás Elektron mozog (tartózkodási valószínűség) Energiaminimumra való törekvés = alacsonyabb energia kedvezőbb (helyzeti energia analógja) További fogalmak: • Alapállapot: minden elektron a legalacsonyabb energiájú pályán van • Gerjesztett állapot: egy vagy több elektron magasabb E-jú pályán (instabil) • Pályaenergia: felszabadul, ha az elektron az atomon kívülről belép

Elektronszerkezet Az elektronok az atommag körül jól definiált rendszerint mozognak. Az atompályák elektronhéjakba/alhéjakba csoportosíthatók, melyeket kvantumszámokkal jellemzünk. Főkvantumszám (n): elektronhéjat definiálja (K, L, M, N, …) Mellékkvantumszám (l): elektron alhéjat definiálja (s, p, d, f, …) • K (n=1): 1 s 2 Alhéj: egyúttal különböző alakú pályákat jelent: • L (n=2): 2 s 2, 2 p 6 • s (l=0) 2 6 10 • M (n=3): 3 s , 3 p , 3 d • p (l=1) • N (n=4): 4 s 2, 4 p 6, 4 d 10, 4 f 14 • d (l=2) • f (l=3) • …… Mágneses kvantumszám: atompálya térbeli iránya mágneses térben • 1 -féle s pálya (2 db s e-) Értéke: egész szám -l … +l tartományban • 3 -féle p pálya (6 db p e-) Spinkvantumszám: +1/2 és -1/2 • 5 -féle d pálya (10 db d e-) Két elektron lehet minden pályán • 7 -féle f pálya (14 db f e-)
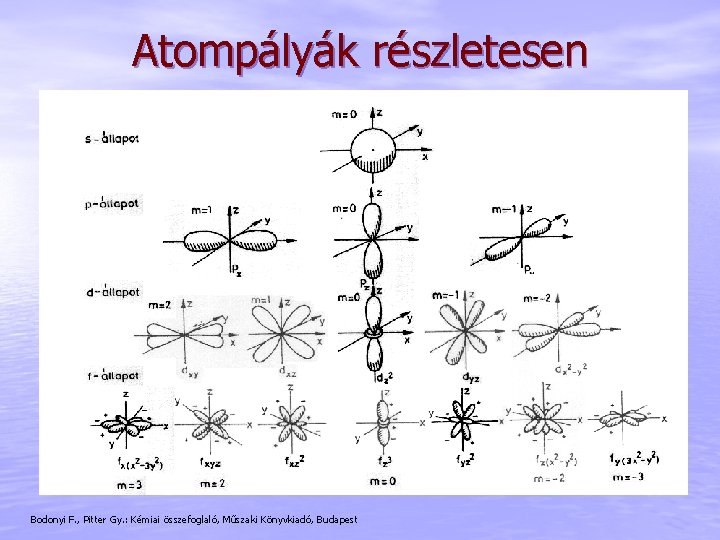
Atompályák részletesen Bodonyi F. , Pitter Gy. : Kémiai összefoglaló, Műszaki Könyvkiadó, Budapest

Elektronszerkezet Pályaenergiák és beépülés: • K (n=1): 1 s 2 • L (n=2): 2 s 2, 2 p 6 • M (n=3): 3 s 2, 3 p 6, 3 d 10 • N (n=4): 4 s 2, 4 p 6, 4 d 10, 4 f 14 • …… Pályaenergiák sorrendje kicsit eltér: 1 s, 2 p, 3 s, 3 p, 4 s, 3 d, 4 p, 5 s, 4 d, … (lásd majd a periódusos rendszert) Pauli elv: egy atomban nem lehet két olyan elektron, melynek mind a négy kvantumszáma megegyezik. Azaz minden cellában maximum két (ellentétes spinű elektron) lehet csak. Bodonyi F. , Pitter Gy. : Kémiai összefoglaló, Műszaki Könyvkiadó, Budapest Hund szabály: egy alhéjon adott számú elektron úgy helyezkedik el, hogy maximális legyen a párosítatlan spinű elektronok száma. Pl. Fe 3 d 6 betöltöttsége:

Elektronszerkezet 28 Ni • • • elektronszerkezet felépülése: 28 elektron 1 s 2, 2 p 6, 3 s 2, 3 p 6, 4 s 2, 3 d 8 Vegyértékelektronok: telítetlen héj(ak)on levő elektronok. Ezek vesznek részt kémiai reakciókban és a másik atomokkal való kölcsönhatásokban. Atomtörzs: atommag + nem vegyértékelektronok (kémiailag inert)

Lángfestés (gerjesztés) A lángban az elektronok a hő hatására magasabb energiájú pályára kerülnek. A gerjesztés után az energiaszinteknek megfelelő energiakülönbség kisugárzása közben visszakerülnek az eredeti energiaszintre. Egyes elemeknél a kibocsátott foton hullámhossza a látható fény tartományába esik. Na: 3 p foton kibocsátás hő 3 s fém lítium (Li) nátrium (Na) kálium (K) kalcium (Ca) bárium (Ba) réz (Cu) szín bíborvörös sárga fakóibolya téglavörös sárgászöld

Tűzijáték rakéta Színek: vörös: stroncium-klorid, stroncium-hidroxid stroncium-nitrát zöld: bárium-klorid, kék: réz-oxid, réz-klorid bíbor: réz-klorid + stroncium-klorid lila: stroncium-klorid, lítium-klorid halvány ibolya: kálium-klorid • Begyújtás a bal oldalon levő gyújtózsinórral. • A motortérben levő feketelőpor égése gázt termel, mely hajtja a • rakétát. Ha a feketelőpor elfogy, begyullad a robbanófej: csillagok, stb.

Fluoreszcencia (UV fénnyel besugározva) Kalcit (Ca. Co 3) Gipsz (Ca. SO 4) Fluorit (Ca. F 2) http: //www. mineraltivadar. hu/About. The. Minerals. htm

Fluoreszcencia (foszforeszcencia) (G. G. Stokes, 1852, fluorit) Néhány anyag UV fénnyel megvilágítva elnyeli az UV sugárzást és helyette látható fényt bocsát ki. Fluoreszcencia: 10 -9 s Foszforeszcencia: 10 -3 – 103 s Magyarázat: 1. UV foton hatására egy vegyértékelektron magasabb energiájú pályára gerjesztődik: EUVfoton=DEelektron + egyéb gerjesztés. 2. A rendszer az egyéb gerjesztett állapotból relaxálódik. 3. Az elektron visszaugrik az alapállapotba DEelektron-nak megfelelő látható tartományba eső foton kisugárzása közben.
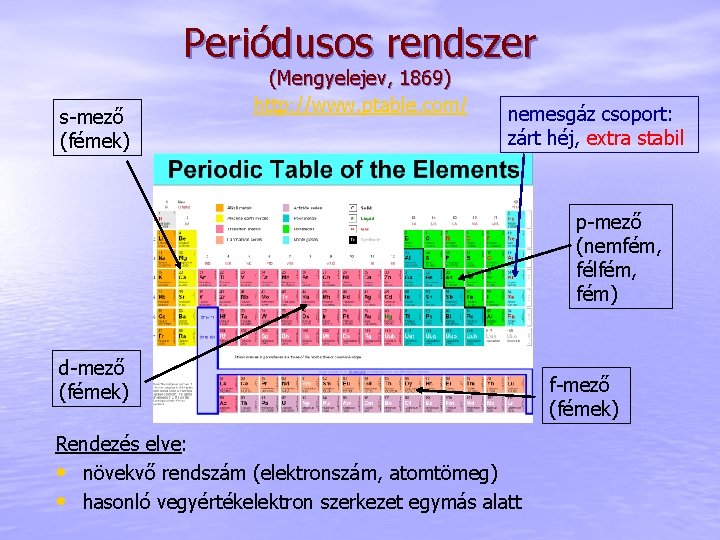
Periódusos rendszer s-mező (fémek) (Mengyelejev, 1869) http: //www. ptable. com/ nemesgáz csoport: zárt héj, extra stabil p-mező (nemfém, félfém, fém) d-mező (fémek) Rendezés elve: • növekvő rendszám (elektronszám, atomtömeg) • hasonló vegyértékelektron szerkezet egymás alatt f-mező (fémek)

Kémiai kötések Az atomok kémiai kötésekkel kapcsolódnak egymáshoz molekulákat vagy nagyobb rendszereket alkotva: • Elsőrendű kötések (általában atomok között) • Ionos kötés • Kovalens kötés (koordinatív kötés) • Fémes kötés • Másodrendű kötések (általában molekulák között) • Hidrogénkötés • Dipólus-dipólus kölcsönhatás • Diszperziós kölcsönhatás Elektronegativitás: az atom elektronvonzó képessége. Két atom kölcsönhatásakor a nagyobb elektronegativitású képes bizonyos fokig elszívni a másik egyes vegyértékelektronjait. • Kis elektronegativitás: s-, d-, f-mező fémei (ENCs=0. 7) • Nagy elektronegativitás: p-mező nemfémes elemei (ENF=4) • Változás: csoportban felfelé, sorban jobbra nő. Nemesgáz elektronszerkezetre való törekvés = stabilitás!

Ionos kötés Egy negatív és egy pozitív töltésű ion közötti elektrosztatikus (Coulombféle) vonzóerő. Anion: semleges atomból elektron felvétellel (nemfémes elemek: F-, Cl-, O 2 -) Kation: semleges atomból elektron leadással (fémek: Na+, Ca 2+, Al 3+, stb. ) Összetett ionok: NH+4 , SO 42 -, CO 32 -, stb. Vegyületképzés: Al 2 O 3 semleges! (Első) Ionizációs energia (Ei): energia, mely ahhoz szükséges, hogy semleges atomból egyszeres pozitív töltésű kation képződjék. Elektronaffinitás (Ea): energia, mely felszabadul (vagy szükséges ahhoz), hogy semleges atomból egyszeres negatív töltésű anion képződjék. K+ F- Kötéstávolság: elektrosztatikus vonzás és taszító (mag-mag, e--e-) erők egyensúlya határozza meg
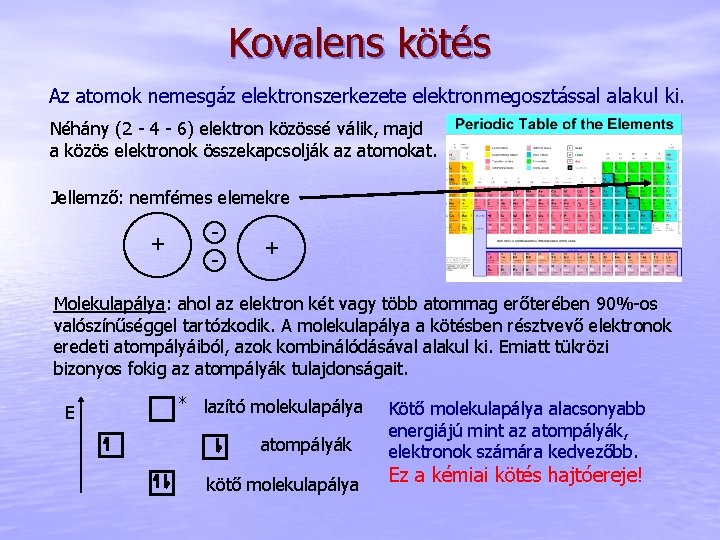
Kovalens kötés Az atomok nemesgáz elektronszerkezete elektronmegosztással alakul ki. Néhány (2 - 4 - 6) elektron közössé válik, majd a közös elektronok összekapcsolják az atomokat. Jellemző: nemfémes elemekre + - + Molekulapálya: ahol az elektron két vagy több atommag erőterében 90%-os valószínűséggel tartózkodik. A molekulapálya a kötésben résztvevő elektronok eredeti atompályáiból, azok kombinálódásával alakul ki. Emiatt tükrözi bizonyos fokig az atompályák tulajdonságait. E * lazító molekulapálya atompályák kötő molekulapálya Kötő molekulapálya alacsonyabb energiájú mint az atompályák, elektronok számára kedvezőbb. Ez a kémiai kötés hajtóereje!

Kovalens kötés s (egyszeres) kötés Kialakulhat: • s – s elektronok között • s – p elektronok között • px – px elektronok között Jellemző: az elektronsűrűség maximuma a két atomot összekötő egyenes (kötéstengely) mentén van. Egyszeres kötés = egyvegyértékű atom az egyik partner: F • hidrogén vegyületei (HBr, H 2 O, NH 3, CH 4) E • halogének vegyületei (F 2, Cl 2, SCl 2, PF 3, CCl 4) http: //dl. clackamas. edu/ch 106 -02/sigma. htm F 2 F

Kovalens kötés p kötés Kialakulhat: • py – py elektronok között • pz – pz elektronok között Jellemző: a két atomot összekötő egyenes (kötéstengely) mentén nincs elektron, az elektronsűrűség az egyenes alatt és felett épül ki (két érintkezési pont, de csak egy kötés!). A gyengébb p-p átlapolás miatt a p kötések gyengébbek mint a s kötés. Ezért a többszörös kötésekben az egyik általában s kötés, csak a második illetve harmadik p. p kötés = két- vagy háromvegyértékű atomok között • kettős kötés (O 2, CO 2, SO 3, H 2 C=CH 2) N • hármas kötés (N 2, HCCH, HCN) p atompályák a második p merőleges az első síkjára http: //dl. clackamas. edu/ch 106 -02/sigma. htm p pályák s pálya N 2 N E

Kovalens kötés egyéb fontosabb jellemzői: • Nemkötő elektronpár: kötésben részt nem vevő vegyértékelektronok pl: N 2 N N a N vegyértékhéja: 2 s 2 2 p 3 • Kötéshossz: a kötést létesítő atomok magjai közti távolság • Kötésszög: a kapcsolódó atomok magjai által bezárt szög • Kötési energia: kötés felszakításához szükséges energia • Kötésrend = (kötőelektronok – lazító pályán levő elektronok)/2 Pl. H 2 : 1 H 2: 0. 5 + H 2: 0. 5 E lazító E E atompályák kötő Miért nincs kovalens kötésű He 2 molekula? (2 e- kötő, 2 e- lazító pályán lenne)

Kovalens kötés Koordinatív (datív) kötés: A kötő elektronpárt az egyik atom adja (volt nemkötő elektronpárja) Pl. C O C (2 s 2 2 p 2) p atompályák O (2 s 2 2 p 4) Molekulák között is: H 3 B + NH 3 H 3 B NH 3 p pályák s pálya Vegyérték: egy adott molekulában az adott atomhoz tartozó kötő elektronpárok száma. HCl (1; 1), H 2 O (1; 2), NH 3 (3; 1), CH 4 (4; 1), H 2 S (1; 2), SO 2 (4; 2), SO 3 (6, 2) (a) (b) S vegyértékhéja: 3 s 2 3 p 4 3 d 0 kis energia befektetéssel átalakulhat: (a) 3 s 2 3 p 3 3 d 1 illetve (b) 3 s 1 3 p 3 3 d 2 -vé
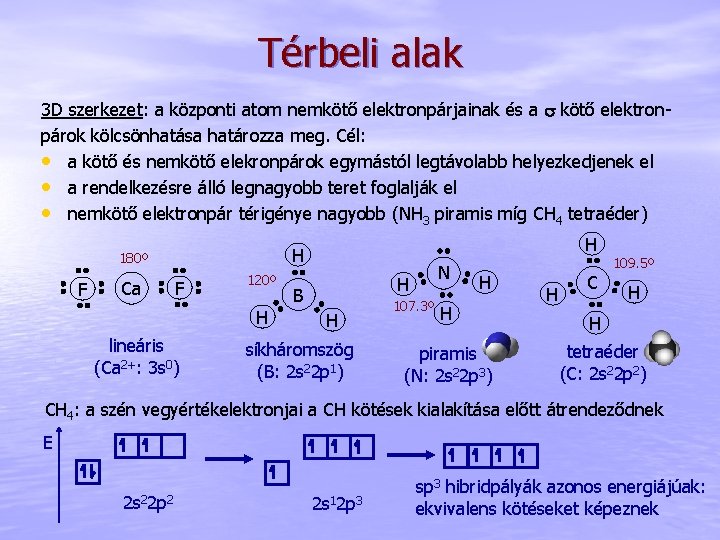
Térbeli alak 3 D szerkezet: a központi atom nemkötő elektronpárjainak és a s kötő elektronpárok kölcsönhatása határozza meg. Cél: • a kötő és nemkötő elekronpárok egymástól legtávolabb helyezkedjenek el • a rendelkezésre álló legnagyobb teret foglalják el • nemkötő elektronpár térigénye nagyobb (NH 3 piramis míg CH 4 tetraéder) F Ca H H 180º F 120º H lineáris (Ca 2+: 3 s 0) N H B H síkháromszög (B: 2 s 22 p 1) 107. 3º H H piramis (N: 2 s 22 p 3) H C 109. 5º H H tetraéder (C: 2 s 22 p 2) CH 4: a szén vegyértékelektronjai a CH kötések kialakítása előtt átrendeződnek E 2 s 22 p 2 2 s 12 p 3 sp 3 hibridpályák azonos energiájúak: ekvivalens kötéseket képeznek

Polaritás Kötések polaritása: Az eltérő elektronegativitású atomok poláris kötéseket létesítenek. A nagyobb elektronegativitású atom jobban vonzza maga felé a kötő elektronpárt: a kötés elektronfelhője torzul. Megbomlik a töltésegyensúly, a nagyobb elektronegativitású atom parciálisan negatív, míg a másik parciálisan pozitív töltésű lesz. Pl. HCl, CO, H 2 O. Apoláris kötés van azonos atomok kapcsolódása esetén. Pl. H 2, O 2, N 2, F 2. Molekulák polaritása: Apoláris kötés esetén a molekula is apoláris. Poláros kötéssel kapcsolódó kétatomos molekulák polárisak. Poláris kötéssel kapcsolódó többatomos molekulák polaritása függ a szimmetriától: d+ ddd. O C O O d+ H 105º H d+ szén-dioxid: apoláris víz: erős dipólus pozitív és negatív súlypont egybeesik

Fémes kötés A fémek kis elektronegativitásuk miatt könnyen leadják vegyérték elektronjaikat. Szilárd és olvadt halmazállapotban pozitív töltésű fématomtörzsek és delokalizált (helyhez nem kötött) elektronrendszer jön létre. A szilárd halmazállapotban kialakuló szerkezet a fémrács: + + + + + Alapja a fémes tulajdonságok: • elektromos vezetés • jó hővezetés • megmunkálhatóság (ugyanolyan környezet mint megmunkálás előtt) + + + + +

Másodrendű kötések (általában molekulák között) Elsőrendű kötések kötési energiája: 80 -850 k. J/mol Másodrendű kötések (általában molekulák között) • Hidrogénkötés • Dipólus-dipólus kölcsönhatás • Diszperziós kölcsönhatás 8 -40 k. J/mol 0. 8 -12 k. J/mol 1. 0 Å Hidrogénkötés: O-H/N-H/Halogén-H kötések nagy polaritása miatt nagyon kicsi a H körüli elektronsűrűség. Emiatt közelben levő másik elektronegatív atom vonzza a H-t. Vegyes ionos - kovalens jellegű a kölcsönhatás. Annál erősebb, minél elektronegatívabbak a nem-H atomok. O d+ H d+ 1. 9 Å O d+ H d+ Dipólus-dipólus kölcsönhatás: aszimmetrikus elektronsűrűség (töltés) eloszlással rendelkező molekulák között. Pl. CO d+ d. Diszperziós kölcsönhatás: apoláris molekulák térközelbe kerülve tudják egymást polarizálni, kistöltésű indukált dipólusok jönnek létre. Pl. dihalogének (F 2, Cl 2, Br 2) Nagyobb méret → erősebb polarizáció. d d + -

Halmazállapotok Gáz Avogadro törvénye: azonos nyomású és hőmérsékletű gázok egyenlő térfogatában – az anyagi minőségtől, molekula méretétől függetlenül – azonos számú molekula van. Állapot Jellemzők Moláris térfogat (dm 3/mol) Standard 25ºC, 0, 1 MPa 24, 5 Szobahőmérséklet 20ºC, 0, 1 MPa 24, 0 Normál 0ºC, 0, 1 MPa 22, 41 Általános gáztörvény: p. V=n. RT (R=8, 314 m 3 Pa/mol. K, moláris gázállandó) mértékegységek R dimenziója alapján Példa: 0. 5 mol Cl 2 gáz térfogata 20 ºC-on 101300 Pa • V = 0. 5 mol • 8, 314 • (273 + 20) K V = 0. 012 m 3

Halmazállapotok Folyadékkristályok: • Részlegesen rendezett állapotban levő folyadékok (átmenet a folyadék és kristályos anyagok között. • Hosszúkás molekulák, melyek hosszú távú rend kialakítására képesek. • Sok fizikai tulajdonságuk a kristályokéhoz hasonlóan anizotróp, azaz irányfüggő. • Elektromos vagy mágneses mező hatására a csoportok rendeződnek. Felhasználás: órák, számológépek, műszerekben kijelzők, LCD monitorok, TV különböző típusú (molekulától függő) elrendeződések

Halmazállapotok Oldatok Jellemzők: • Ionos (és poláris) vegyületek poláris oldószerekben oldódnak jól (H 2 O, alkohol). A szilárd ionrács ionokra esik szét. • Nemfémes elemek (pl. I) és apoláris szerves anyagok apoláris szerves oldószerekben oldódnak (benzol, kloroform, éter) • Oldhatóság: pl. 100 g oldószer által feloldható anyag tömege • Telítetlen – telített – túltelített (instabil) oldat • Gázok oldhatóságát nyomással lehet növelni. • Hőmérséklet szerepe: • Melegítés segít: KNO 3, NH 4 Cl (itt oldódás endoterm) • Hűtés segít: NH 3, SO 2, H 2 SO 4 (itt oldódás exoterm) • Oldáshő: mekkora hő szabadul fel, vagy mennyi hőt vesz fel a rendszer 1 mol • anyag feloldásakor. Qoldás=DErács + DEszolv 1 mol anyag szolvatációját (hidratációját) kísérő energiaváltozás a szolvatációs (hidratációs) energia. Értéke negatív (energiafelszabadulás).

Halmazállapotok Oldatok: koncentrációszámítás Fontosabb koncentrációk: • moláris koncentráció (c): mol oldott anyag/1 dm 3 oldatban (mol/dm 3) • tömegszázalék: gramm oldott anyag/100 gramm oldatban (m/m%) • tömegkoncentráció: kg oldott anyag/1 m 3 oldatban (kg/m 3) Számítási példa: Számítsuk ki annak az oldatnak a moláris koncentrációját, melyet 100 g Na. Cl 0. 4 dm 3 vízben történt feloldásával kaptunk. Az atomtömegek: MNa=23, MCl= 35. 5 Az Na. Cl moltömege: 23+35. 5=58. 5 g/mol 100 g Na. Cl = 100/58. 5 = 1. 71 mol ha 0. 4 dm 3 vizben van oldva 1. 71 mol Na. Cl akkor 1 dm 3 vizben van oldva 4. 275 mol Na. Cl. Tehát az oldat koncentrációja 4. 275 mol/dm 3

Halmazállapotok Kristályos anyagok, atomrács Szilárd anyagok: kémiai kötések az atomok/ionok/molekulák között • Amorf: a részecskék elhelyezkedése rendezetlen, vagy csak kis körzetekben rendezett. Nincs határozott olvadáspontjuk = op (lágyulás → folyadék) • Kristályos anyagok: a részecskék a tér minden irányában szabályos rendben helyezkednek el. Jól definiált (anyag azonosítására is használt) olvadáspontjuk van. • Atomrács: rácspontokban atomok, melyek irányított egyszeres (s) kovalens kötéssel kapcsolódnak egymáshoz: gyémánt, Si, Ge, B, Si. O 2, Zn. S, Si. C Kemények, hőt és elektromosságot nem vezetik, op magas, sem vízben, sem szerves oldószerekben nem oldódnak. Gyémánt (Si, Ge, Zn. S, Si. C) Minden C atom körül tetraéderes elrendeződésben van a többi azonos távol-ságra, azonos kötésszöggel. 109. 5º

Halmazállapotok Fémrács aranyrög ++ +++++++ Jellemzők: • Rácspontokban pozitív töltésű fém atomtörzsek, amiket hozzájuk közösen tartozó delokalizált elektronok kötnek össze → vezetőképesség • Erős kötés: kemény, magas op (Cr, W) • Szürke szín (kivétel Cu, Au): minden típusú fotont elnyel (e--k gerjesztődnek) • Oldhatóság: egymás olvadékaiban → ötvözet, ill. kémiai átalakulással savakban Leggyakoribb rácstípusok: térben középpontos kockarács (Na, K, Fe, Cr) mindenféle lapon középpontos kockarács (Au, Ag, Al, Cu) puha, megmunkálható hatszöges rács (Mg, Ni, Zn) kemény, rideg

Halmazállapotok Fémrács: ötvözetek Az ötvözet fémes anyag, mely legalább két kémiai elemből áll, s legalább az egyik fém. Legismertebbek: acél, sárgaréz (réz + cink), bronz (ón + réz) Fizikai tulajdonságok, mint a sűrűség, reakciókészség, rugalmassági modulus, elektromos- és hővezető képesség általában nem mutatnak nagy eltérést az alkotóelemekéhez képest, de a mechanikai tulajdonságok, mint a szakító- és nyírószilárdság lényegesen különbözhetnek. Oka az atomok különböző mérete: a nagyobb atomok nyomóerőt fejtenek ki a szomszédos atomokra, míg a kisméretű atomok húzóerővel hatnak a szomszédjaikra, ami fokozza az ötvözet deformációval szembeni ellenálló képességét. Előállítás: elsősorban fémek megolvasztásával és összekeverésével. A tiszta fémekkel ellentétben a legtöbb ötvözetnek nem jól definiált olvadáspontja van, hanem olvadási tartománya: • Szolidusz: az a hőmérsékletet, amelyen az olvadás megkezdődik • Likvidusz: az a hőmérsékletet, amelyen az olvadás befejeződik • Eutektikus ötvözet: alkotóknak egy olyan aránya, amikor egyetlen (vagy ritkán kettő) olvadáspont létezik

Halmazállapotok Ötvözetek: szilárd oldat Olyan szilárd halmazállapotú homogén keverék, melyben a kisebb mennyiségű ”oldott anyag” nem változtatja meg az oldószer kristályszerkezetét. A szerepek fel is cserélődhetnek. • hasonló atomsugarak (<15% eltérés) • azonos kristályszerkezet • hasonló elektronegativitás • hasonló vegyérték Fázisdiagram (K) A és B keverékének olvadása (hal-görbe): • T 2 alatt csak szilárd anyag van • T 1 felett csak olvadék van • a görbe belsejében olvadék+szilárd keverék • T 1 – T 2 között a szilárd illetve folyadék komponens összetétel a nyilak alapján folyadék T 1 likvidusz görbe folyadék+szilárd szolidusz görbe szilárd oldat xszilárd 100%A 70%A, 30%B T 2 xfolyadék 10%A, 90%B 100%B

Halmazállapotok Ötvözetek Kétkomponensű rendszer eutektikus ponttal: • A és B nem képez szilárd oldatot, a szilárd fázis a két anyag kristályainak heterogén keveréke • Az eutektikus összetételű szilárd keverék egyszerre megolvad, a többi összetételnél az olvadás egy hőmérséklet tartományban történik p=állandó T Eutektikus pont, hőmérséklet Folyadék szilárd A + folyadék szilárd B + folyadék szilárd A + B A x% B Csoportosítás kristályrács szerint: • Helyettesítéses (szubsztitúciós): Az alkotó elemek atomjai hasonló méretűek, • • így a kristályrácsban egyszerűen helyettesíthetik egymást (pl. sárgaréz). Intersticiós: az egyik alkotóelem atomja lényegesen kisebb a másiknál, és a kisebb atomok beépülnek a nagyobb atomok közti (rácsközi) helyekre. Kristályrács, ami nem hasonlít egyik összetevő kristályrácsához sem (nagyon bonyolult). Ezek nagyon kemény, rideg fémvegyületek, pl. Fe 3 C (cementit), WC (volfrámkarbid).

Halmazállapotok Ötvözetek Egyéb csoportosítás: • Természetes ötvözetek: geológiai folyamatok által jönnek létre, például az • • • égitestek belsejében. Nincs jól meghatározott összetételük és tulajdonságaik. Vasötvözetek: acélok és öntöttvas; a széntartalom szerint tesznek köztük különbséget. Nemesacélok: krómot és nikkelt tartalmaznak. Nemvas ötvözetek: nem vas alapú ötvözetek. Pl. sárgaréz, bronz, amalgámok. Diffúziós ötvözetek: az ötvöző elem atomjai az alapfémbe diffundálnak. Főleg a periódusos rendszer kis rendszámú elemei (pl. szén), kis atomjaik miatt. Heusler-ötvözetek: ferromágneses ötvözetek, amik nem tartalmaznak vasat, nikkelt vagy kobaltot. Ilyen például a Cu 2 Al. Mn fémvegyület. Emlékező ötvözetek: átformálás után, ha újra felveszik az eredeti hőmérsékletüket, visszanyerik az eredeti alakjukat. Fémporok összekeverése, felhevítése, majd összenyomása: olyan fémekkel, amik folyékony állapotban nem keverednek egymással. Pl. volfrámötvözetek. Leírás: az egyes fémek tömegszázaléka szerint. Például a Cu. Zn 37 ötvözetben 37% a cink, és 63% a réz. Arany tisztasága: • • • 24 karát: 100 % arany 18 karát: 75 % arany 12 karát: 50 % arany

Halmazállapotok Ionrács Jellemzők: • Rácspontokban szoros illeszkedéssel kationok és anionok vannak. Kifelé semleges. • Kemények, ridegek, magas olvadáspontúak, elektromos áramot nem vezetik • Olvadékuk és oldataik vezetők • Többségük vízben oldódik, ionjaira disszociál Leggyakoribb rácstípusok: Cs. I, térben középpontos kockarács Na. Cl, lapon középpontos kockarács

Halmazállapotok Molekularács Jellemzők: • Rácspontokban molekulák vannak, melyek másodlagos kötőerőkkel kapcsolódnak egymáshoz. • Hidrogénkötés 8 -40 k. J/mol • Dipólus-dipólus kölcsönhatás • Diszperziós kölcsönhatás 0. 8 -12 k. J/mol • Szinte minden szerves molekula, valamint H 2, O 2, N 2, CO 2 (szárazjég), stb. • Keménység kicsi, olvadás- és forráspont alacsony, kis sűrűség, áramot sem • szilárd, sem olvadt állapotban nem vezetik. Apoláris szerves oldószerekben (pl. CCl 4) oldódnak. Jég: 16 különböző szilárd fázisú szerkezetben létezik. Hexagonális kristályrendszer

Grafit gyémánt Három rácstípusból van benne: • Szénatomok egyszeres s kovalens kötéssel kapcsolódnak 3 szomszédjukhoz (atomrács). • A negyedik elektron delokalizáltan van a kovalens kötésű síkokban (fémrács). • A hexagonális szerkezetű síkok között másodlagos kötőerők hatnak (molekularács). Ebből adódnak tulajdonságai: • Magas op. (3700 ºC) • Vezeti az áramot • Jó kenőanyag (síkok egymáson elcsúsznak)

Kémiai reakciók reakcióegyenletek A kémiai reakciókban atomok/molekulák/ionok elektronszerkezete változik (kötések bomlanak fel, új kötések jönnek létre): • bomlás: Ca. CO 3 = Ca. O + CO 2 • egyesülés: NH 3 + HCl = NH 4 Cl • atom/atomcsoport csere: Ca. CO 3 + HCl = Ca. Cl 2 + H 2 CO 3 (→CO 2 + H 2 O) Reakcióegyenlet: reagáló anyagok => termékek • tömegmegmaradás: azonos típusú atomok száma mindkét oldalon azonos • töltésmegmaradás: töltések összege mindkét oldalon azonos (általában 0 ) • kémiai számítások alapja általában az egyenlet Számítási példa: Számítsuk ki hány cm 3 1 mol/dm 3 -es kénsav kell 2 dm 3 normál állapotú HCl gáz készítéséhez a következő kiegészítendő reakcióegyenlet alapján: Ca. Cl 2 + H 2 SO 4 = Ca. SO 4 + HCl

Kémiai reakciók kémiai számítás Számítási példa: Számítsuk ki hány cm 3 1 mol/dm 3 -es kénsav kell 2 dm 3 normál állapotú HCl gáz készítéséhez a következő kiegészítendő reakcióegyenlet alapján: Ca. Cl 2 + H 2 SO 4 = Ca. SO 4 + HCl Egyenlet rendezése anyagmegmaradás elve alapján: Ca. Cl 2 + H 2 SO 4 = Ca. SO 4 + 2 HCl 22, 41 dm 3 a térfogata 1 mol HCl gáznak normál állapotban (0 ºC, 0, 1 MPa) Ez alapján 2 dm 3 HCl megfelel (1/22, 41)*2=0, 089 molnak 2 mol (molekula) HCl fejlesztéséhez kell 1 mol (molekula) H 2 SO 4 0, 089 mol HCl fejlesztéséhez kell (1/2)*0, 089=0, 0445 mol H 2 SO 4 1 mol H 2 SO 4 van 1000 cm 3 (1 dm 3) 1 mol/dm 3 -es oldatban 0, 0445 mol H 2 SO 4 van (1000/1)*0, 0445=44, 5 cm 3 oldatban Tehát 44, 5 cm 3 1 mol/dm 3 -es H 2 SO 4 oldat kell.

Kémiai reakciók kémiai számítás Számítási példa: Számítsuk ki hány g 36 m/m%-os HCl oldat kell 100 g Fe. Cl 3 készítéséhez a következő kiegészítendő reakcióegyenlet alapján: Fe 2 O 3 + HCl = Fe. Cl 3 + H 2 O MFe=55. 8, MO=16, MCl= 35. 5, MH=1 Egyenlet rendezése anyagmegmaradás elve alapján: Fe 2 O 3 + 6 HCl = 2 Fe. Cl 3 + 3 H 2 O Molekulatömegek: MFe. Cl 3=162, 3, MHCl=36. 5 100 g Fe. Cl 3 = (1/162, 3)*100 = 0, 616 mol 2 mol Fe. Cl 3 keletkezése igényel 6 mol HCl-at 0, 616 mol Fe. Cl 3 keletkezése igényel (6/2)*0, 616=1, 848 mol = 1, 848*36, 5=67, 452 g HCl-at 36 g HCl van 100 g 36 m/m%-os HCl oldatban 67, 452 g HCl van (100/36)*67, 452=187, 37 g HCl oldatban Tehát 187, 37 g 36 m/m%-os HCl oldat kell.

Kémiai reakciók reakcióhő Reakcióhő (Qr, k. J): reakcióegyenlet által definiált reakció hőváltozása A kémiai reakciókban kötések bomlanak fel és új kötések alakulnak ki. • Kötésfelbomlás: energia befektetést igényel (+ előjel) • Kötés kialakulás: energia szabadul fel (- előjel) • Ha fázisátalakulás történik, annak is van energiavonzata. Pl. gáz kondenzálása energia felszabadulással jár a szilárd fázisbeli kötések kialakulása miatt. (CO 2 miért gáz szobahőmérsékleten? ) • Exoterm reakció: energia szabadul fel (C + O 2 = CO 2, Qr < 0) • Endoterm reakció: energiát igényel (H 2 O → H 2 + ½O 2, Qr > 0) Képződéshő (Qk, k. J/mol): annak a reakciónak az energiaváltozása, melyben egy vegyület 1 mólja standard körülmények (25 ºC, 0, 1 MPa) között alapállapotú elemeiből keletkezik. Alapállapotú elemek képződéshője standard körülmények között 0 k. J/mol.

Kémiai reakciók reakcióhő Reakcióhő a képződéshőkből: a termékek együtthatókkal szorzott képződéshőinek összegéből levonjuk a kiindulási anyagok együtthatókkal szorzott képződéshőinek összegét. Hess tétel: a reakcióhő független a reakció útjától (általában többféle útvonal van), csak a kezdeti és végállapottól függ. I. Ca. CO 3 + 2 HCl = Ca. Cl 2 + CO 2 + H 2 O Qr = Qk. Ca. Cl 2 + Qk. CO 2 + Qk. H 2 O – Qk. Ca. CO 3 – 2 Qk. HCl II. Ca. CO 3 = Ca. O + CO 2 Ca. O + 2 HCl = Ca. Cl 2 + H 2 O Qr = Qk. Ca. O + Qk. CO 2 + Qk. H 2 O + Qk. Ca. Cl 2 – Qk. Ca. O - Qk. Ca. CO 3 – 2 Qk. HCl A Ca. O csak átmeneti termék, keletkezik és megszűnik, ezért képződéshője a II. összetett reakcióban kiesik. Reakcióentalpia (DH, k. J): ugyanaz mint a reakcióhő, csak ki van kötve a nyomás állandóságának feltétele (zárt edényben gázok reakciójakor lehet különbség ha mólszám változás van)

Kémiai reakciók Szabadentalpia Entrópia (S, k. J/K): egy rendszer rendezetlenségének mértéke. A rendezetlenség kedvezőbb állapot: • kristályos anyag oldódása (oldott anyag oldószerben való eloszlása) • gázok keveredése (kibocsátott CO 2, füst) A természetes folyamatokat az irányítja, hogy: • csökkenjen a rendszer energiája (energia-felszabadulás) • növekedjen a rendezetlenség mértéke G: szabadentalpia, k. J Ezt fejezi ki a szabadentalpia: G = H – TS H: entalpia, k. J Valamely folyamat (kémiai reakció) szabadentalpia változása: DG = DH – TDS T: hőmérséklet, K Spontán folyamat akkor megy végbe, ha szabadentalpia változás negatív (DG<0). Az entrópia tagnak inkább csak magas hőmérséklet esetén (T > 1500 K) van jelentősége, szobahőmérsékleten általában elhanyagolható, azaz DG ≈ DH
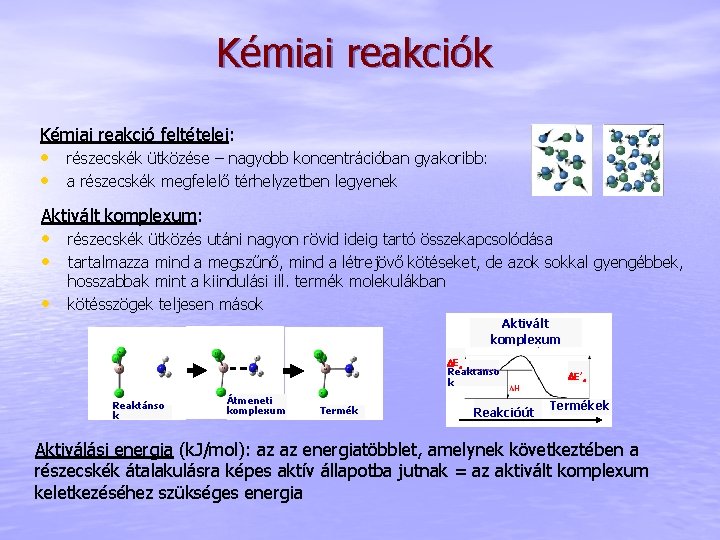
Kémiai reakciók Kémiai reakció feltételei: • részecskék ütközése – nagyobb koncentrációban gyakoribb: • a részecskék megfelelő térhelyzetben legyenek Aktivált komplexum: • részecskék ütközés utáni nagyon rövid ideig tartó összekapcsolódása • tartalmazza mind a megszűnő, mind a létrejövő kötéseket, de azok sokkal gyengébbek, • hosszabbak mint a kiindulási ill. termék molekulákban kötésszögek teljesen mások Aktivált komplexum DEa Reaktánso k Átmeneti komplexum Termék Reakcióút DE’a Termékek Aktiválási energia (k. J/mol): az az energiatöbblet, amelynek következtében a részecskék átalakulásra képes aktív állapotba jutnak = az aktivált komplexum keletkezéséhez szükséges energia

Kémiai reakciók reakciósebesség Reakciósebesség: egységnyi térfogatban egységnyi idő alatt hány mol alakul át a kiindulási anyagok valamelyikéből, vagy hány mol keletkezik a termékek valamelyikéből. Függ: • • 2 H 2 + O 2 = H 2 O a reakciótól (reagáló anyagok minősége) reagáló anyagok koncentrációjától hőmérséklettől katalizátortól v=k c. H 22 c. O 2 mol/(dm 3 s) • • k= reakciósebességi állandó Reakció katalizátor nélkül E Reakció katalizátorral Katalizátor: olyan anyag, mely a kémiai reakciók sebességét nagymértékben megnövelik (alacsonyabb energiájú aktivált komplexumot képeznek. A reakció lejátszódása után újra felszabadulnak (kis mennyiség elég), reakcióhőt nem befolyásolják, csak az aktiválási energiát. Y→X X→Y Reakcióút Inhibítor: kémiai reakciókat lassító vagy gátló anyagok.

Kémiai reakciók katalízis Egyszerű reakciók: az előbb ismertetett módon a katalizátor csökkenti az aktiválási energiát. Pl: Pt 2 H + O 2 H O 2 2 2 Pt felületén megköti a H 2 és O 2 molekulákat, felbontja a H 2 és fellazítja az O 2 kötését, így kisebb energiát kell a reakcióhoz befektetni. Összetett reakciók: az eredeti reakció mellett egy másik, gyorsabban lejátszódó reakcióút nyílik meg. Pl: NH 3 és HCl reakciója víz jelenlétében (katalizátor nélkül a két molekula megfelelő ütközése kellene) NH 3 + H 2 O = NH 4+ + OHNH 4+ + HCl = NH 4 Cl + H+ H+ + OH- = H 2 O A H 2 O átmeneti vegyületet hoz létre NH 3 -al, mely könnyebben reagál a HCl-el. A katalizátor visszaalakul, s újabb reakcióra kész.

Kémiai reakciók katalízis Katalizátorok fajtái: Aszerint, hogy a katalizátor és a reaktánsok azonos vagy különböző fázisban vannak, megkülönböztetünk • homogén katalízis (azonos fázis) – NH 3 és HCl előbbi reakciója (víz = folyadék fázisban) – élő rendszerekben, katalizátorok az enzimek • heterogén katalízis (különböző fázis) – az ipari méretű szintéziseknél, (a reakció után a katalizátor egyszerűen kinyerhető a rendszerből), pl. hidrogénezések = telítetlen szerves vegyületek telítése H 2 -el Pd katalizátor alkalmazásával Katalizátor autókban: Pt (Pd, Rh) környezetre kevésbé ártalmas termékek. kerámia méhsejt szerkezetű mag: • Nitrogén-oxidok redukciója: 2 NOx → x. O 2 + N 2 • CO oxidációja: 2 CO + O 2 → 2 CO 2 • Elégetlen szénhidrogének oxidációja: Cx. H 2 x+2 + 2 x. O 2 → x. CO 2 + 2 x. H 2 O

Kémiai reakciók egyensúlyi reakciók: A B Minden kémiai reakció elvileg oda-vissza mehet, a fő különbség a befektetendő aktiválási energiában van. Aktivált komplexum DEa Reaktánso k Reakcióút DE’a Termékek DEa Reaktánso k DE’a Termékek Reakcióút (Gyakorlatilag) egyirányú reakciók: • nagyon stabilis a termék • a termék más halmazállapota miatt eltávozik a rendszerből: - gáz: H 2 CO 3 → H 2 O + CO 2 - csapadék: Ag. NO 3 + HCl → Ag. Cl + HNO 3

Kémiai reakciók kémiai egyensúly ctermék Idő → egyensúly ckiindulási anyag ctermék Idő → egyensúly Reakcósebesség → ckiindulási anyag Koncentráció → Kémiai egyensúly kifejeződése a koncentrációkban és a reakciósebességekben: v 1 egyensúly v 2 Idő → • Kiindulási anyagok felé tolódott egyensúlyban végig: ckiindulási anyag > ctermék • Termék felé tolódó egyensúlyban egy idő után: ckiindulási anyag < ctermék • Egyensúlyban az oda-vissza alakulás reakciósebessége megegyezik (v 1 = v 2) ! A koncentrációban nincs változás, de az oda-vissza reakció folyamatosan történik! DINAMIKUS EGYENSÚLYI ÁLLAPOT

Kémiai reakciók egyensúlyi állandó Tömeghatás törvénye: egyensúlyban a termékek megfelelő hatványon vett egyensúlyi koncentrációinak szorzata, osztva a kiindulási anyagok megfelelő hatványon vett egyensúlyi koncentrációinak szorzatával, egy adott hőmérsékleten és nyomáson állandó érték. a. A + b. B c. C + d. D reakcióra: (levezetve: v 1=k 1[A]a[B]b, v 2=k 2[C]c[D]d k 1 [C]c[D]d a b c d = egyensúlyban: v 1=v 2, azaz k 1[A] [B] =k 2[C] [D] → k 2 [A]a[B]b Az egyensúlyi állandó (K) csak a külső körülményektől (nyomás, hőmérséklet) függ, független a koncentráció értékektől. • K>1: egyensúlyban a termékek vannak nagyobb mennyiségben • K<1: egyensúlyban a kiindulási anyagok vannak nagyobb mennyiségben

Kémiai reakciók egyensúlyi állandó Le Chatelier-Braun elv (legkisebb kényszer elve): egy dinamikus egyensúlyban levő rendszer megzavarásakor annak a folyamatnak lesz nagyobb a sebessége, amely a zavaró hatást csökkenteni igyekszik. a) koncentrációváltoztatás (K-t nem változtatja, de a reakciósebességeket igen A+B C + D reakcióban megnöveljük B mennyiségét y-al: eredeti egyensúlyban k 1[A][B]=k 2[C][D], változtatva k 1[A][B+y]→k 2[C][D] új egyensúlyban: k 1[A-x][B+y-x]=k 2[C+x][D+x] K= [C+x][D+x] [A-x][B+y-x] K = [C ] [D ] [A ] [B ] b) hőmérsékletváltoztatás: K-t változtatja, s azon keresztül a reakciósebességeket, koncentrációkat. • T növelés: endoterm reakciónál termékképződés exoterm reakciónál visszaalakulás • T csökkentés: exoterm reakciónál termékképződés endoterm reakciónál visszaalakulás

Kémiai reakciók egyensúlyi állandó Le Chatelier-Braun elv: c) nyomásváltoztatás: csak molekulaszám változással járó reakciókban K-t változtatja, s azon keresztül a reakciósebességeket, koncentrációkat. • p növelés: molekulák számának csökkenése felé • p csökkentés: molekulák számának növekedése felé pl: H 2 O + CO 2 H 2 CO 3: megfelelő mennyiségű CO 2 -t nyomással oldanak az ásványvízben d) katalizátor nem változtatja meg az egyensúlyi állandót, csak a reakciósebességeket (mindkét irányét) növeli Ok: az egyensúlyi állandó a kiindulási anyagok és végtermékek relatív energiájától függ, ezt pedig a katalizátor nem befolyásolja.

Kémiai reakciók Protolitikus reakciók Hidrogénion (proton) átadással járó reakciók főként vizes oldatban Brönsted szerint: oxónium ion • savak: protont leadó molekulák és ionok (HCl + H 2 O H 3 O+ + Cl-) • bázisok: protont felvevő molekulák és ionok (NH 3 + H 2 O NH 4+ + OH-) Proton sosincs szabad állapotban az oldatban, ezért ezen (mindig) egyensúlyi reakciókban a sav és bázis együttesen van jelen: HCl + H 2 O H 3 O+ + Clsav bázis Amfoter vegyület: partnertől függően savként illetve bázisként reagál: H 2 O A sav-bázis párok erőssége ellentétes: minél erősebb a sav (pl. HCl), annál gyengébb a bázis párja (Cl-). Arrhenius-féle sav-bázis elmélet (korábbi, közelebb áll a mindennapi élethez) Csak vizes oldatokra érvényes! • savak: vízben H+-ionra és anionra disszociálnak: HCl H+ + Cl • bázisok: vízben OH--ionra és kationra disszociálnak: Na. OH Na+ + OH-

Kémiai reakciók Protolitikus reakciók: egyensúlyi állandók Disszociációs egyensúlyi állandók: sav illetve bázis HNO 3 - + H+ NH 4 OH [NO 3 -][H+] Ks= [HNO 3] NH 4+ + OH- [NH 4+][OH-] Kb = [NH 4 OH] A […] koncentrációk mindig az egyensúlyi koncentrációk, nem pedig kiindulási vagy bruttó koncentrációk, ami példákban sokszor szerepel. Víz disszociációja: H 2 O + H 2 O H 3 O+ + OHAutoprotolízis: egy vegyület molekulái egymással lépnek sav-bázis reakcióba [H 3 O+][OH-] A folyamatra felírva a tömeghatástörtet: K= [H 2 O]2 A H 2 O molekulák koncentrációja gyakorlatilag állandó (55, 5 mol/dm 3), ezért összevonható K-val: Kvíz= [H 3 O+][OH-] = 10 -14 (mol/dm 3)2 vízionszorzat 25 ºC-on

Protolitikus reakciók p. H Vízionszorzat jelentése: H 3 O+ (H+) és OH- ionok mindig vannak jelen az oldatban, és meghatározzák egymás koncentrációját. Kémhatás: • semleges oldat: [H 3 O+]=[OH-] = 10 -7 mol/dm 3 • savas oldat: H 3 O+ ionok vannak többségben (>10 -7 mol/dm 3) • bázikus (lúgos) oldat: OH- ionok vannak többségben (>10 -7 mol/dm 3) A kémhatás számszerű jellemzésére a -lg[H 3 O+] értéket használjuk, neve p. H • savas oldat: p. H < 7 • bázikus (lúgos) oldat: p. H > 7 (Analóg módon p. OH is létezik, de a gyakorlatban nem használatos. ) Számítási példa: Mennyi a 0. 1 mol/dm 3 -es HCl illetve Na. OH oldatok p. H-ja? HCl disszociációja után [H 3 O+]=0. 1 mol/dm 3 → p. H=-lg[H 3 O+] =1 Na. OH oldatban [OH-]=0. 1 mol/dm 3 vízionszorzatból [H 3 O+]=10 -13 mol/dm 3 → p. H=13
![Protolitikus reakciók Gyenge savak disszociációja Hidrogén-cianid (részleges disszociáció): [H O+][CN-] 3 Ks= HCN + Protolitikus reakciók Gyenge savak disszociációja Hidrogén-cianid (részleges disszociáció): [H O+][CN-] 3 Ks= HCN +](http://slidetodoc.com/presentation_image_h2/9ad1c3c9314fd81ba03b2792d5ddd0ff/image-62.jpg)
Protolitikus reakciók Gyenge savak disszociációja Hidrogén-cianid (részleges disszociáció): [H O+][CN-] 3 Ks= HCN + H 2 O H 3 O+ + CN[HCN] = 10 -9 mol/dm 3 Számítási példa: 1. Mennyi az 1 mol/dm 3 -es HCN oldat p. H-ja? A disszociáció során azonos mennyiségű H 3 O+ és CN- keletkezik: [H 3 O+]=[CN-] A maradó HCN koncentrációja: 1 -[H 3 O+] mol/dm 3 behelyettesítve a tömeghatástörtbe: 10 -9= [H 3 O+]2 1 -[H 3 O+] A másodfokú egyenlet megoldása: [H 3 O+]=3. 2. 10 -5 mol/dm 3 → p. H=4. 5 2. Mennyi lesz a CN--koncentráció, ha a fenti oldat p. H-ját erős savval 2 -re állítjuk? A tömeghatástört: 10 -9= [10 -2][CN-] , melyből [CN -]=10 -7 mol/dm 3 1 -[CN-] Gyenge bázisok p. H számítása analóg, csak ott a végén OH--koncentrációt kapunk, amiből a vízionszorzat segítségével kapjuk meg a H 3 O+-koncentrációt.

Protolitikus reakciók Hidrolízis Erős sav és erős bázis sójának (pl. Na. Cl) vizes oldata semleges kémhatású. Ha vagy a sav, vagy a bázis gyenge, a vizes oldat nem lesz semleges. • gyenge sav+erős bázis (Na. CN): lúgos kémhatás • gyenge bázis + erős sav (NH 4 Cl): savas kémhatás A feloldáskor keletkező ionok reagálnak a víz molekulákkal: lúgos CN- + H 2 O HCN + OHsavas NH 4+ + H 2 O NH 4 OH + H+ (H 3 O+) A fenti hidrolízisek is egyensúlyi folyamatok: [HCN][OH-] K h= [CN-] [NH 4 OH][H 3 O+] és Kh= , [H 2 O] beépítve Kh hidrolízisállandóba + [NH 4 ] A Ks(Kb) disszociációs állandók Kvíz K = és a megfelelő hidrolízisállandók h K s között összefüggés van: Kvíz [H 3 O+][OH-][HCN] =Kh = + [CN ][H 3 O ] Ks
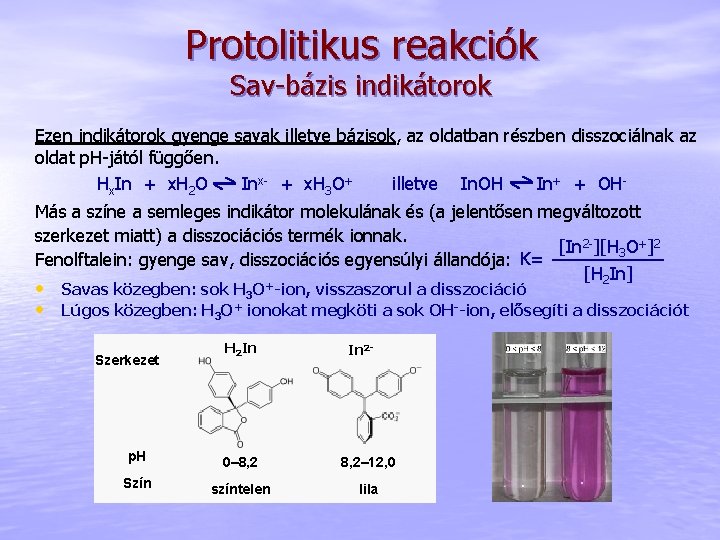
Protolitikus reakciók Sav-bázis indikátorok Ezen indikátorok gyenge savak illetve bázisok, az oldatban részben disszociálnak az oldat p. H-jától függően. Hx. In + x. H 2 O Inx- + x. H 3 O+ illetve In. OH In+ + OHMás a színe a semleges indikátor molekulának és (a jelentősen megváltozott szerkezet miatt) a disszociációs termék ionnak. [In 2 -][H 3 O+]2 Fenolftalein: gyenge sav, disszociációs egyensúlyi állandója: K= [H 2 In] • Savas közegben: sok H 3 O+-ion, visszaszorul a disszociáció • Lúgos közegben: H 3 O+ ionokat megköti a sok OH--ion, elősegíti a disszociációt Szerkezet H 2 In In 2 - p. H 0– 8, 2– 12, 0 Szín színtelen lila

Protolitikus reakciók Univerzális indikátor www. lmpc. edu. au/. . . /indicator. htm encarta. msn. com/. . . /universal_indicator. html Különböző indikátorok (fenolftalein, brómtimolkék, metilvörös, és timolftalein) keveréke, melyek más-más p. H-nál változtatják színüket.

Redoxireakciók Oxidáció: 2 Mg + O 2 = 2 Mg. O Részfolyamatok: 2 Mg - 4 e- = 2 Mg 2+, O 2 + 4 e- = 2 O 2 oxidáció redukció A redoxi folyamatokban: • oxidáció: elektron leadás • redukció: elektron felvétel Nemcsak oxigénnel: 2 Al + 3 Cl 2 = 2 Al. Cl 3 Részfolyamatok: 2 Al - 6 e- = 2 Al 3+ 3 Cl 2 + 6 e- = 6 Cl- (oxidáció) (redukció) 2 Al 3+ + 6 Cl- = 2 Al. Cl 3 2 Mg 2+ + 2 O 2 - = 2 Mg. O

Redoxireakciók Oxidáció: 2 Mg + O 2 = 2 Mg. O Részfolyamatok: 2 Mg - 4 e- = 2 Mg 2+, O 2 + 4 e- = 2 O 2 oxidáció 2 Mg 2+ + 2 O 2 - = 2 Mg. O redukció A redoxi folyamatokban: • oxidáció: elektron leadás • redukció: elektron felvétel • oxidálószer: az ami a másikat elektron leadásra (oxidációra) készteti • redukálószer: az ami a másikat elektron felvételre (redukcióra) készteti Oxidáció és redukció mindig együtt játszódik le, mert az oxidálószer felveszi a másik által leadott elektronokat (redukálódik). Elektron egy reakcióban nem veszhet el (tömegmegmaradás törvénye), s általában nem is marad szabadon. Az oxidációra (redukcióra) való hajlam összefügg az elektronegativitással, azaz az elektronvonzási képességgel: F Cs További redoxireakciók: Zn + Cu 2+ = Cu + Zn 2+ Cl 2 + 2 I- = 2 Cl- + I 2 Zn + 2 H+ = Zn 2+ + H 2

Oxidációs szám Semleges atomhoz képesti oxidációs állapot: az atom névleges vagy valódi töltése egy adott vegyületben. • elemek: 0 • egyatomos ionok: az ion töltése • molekulák: a névleges töltés, ha a kötő elektronpárokat gondolatban a nagyobb elektronegativitású atomhoz rendeljük. Pl: H 2 O-ban O=-2, H=+1 Semleges molekulában az oxidációs számok összege 0, többatomos ion esetében pedig az ion töltése. Jellemző oxidációs számok: • • • (semleges atomból oxidációval) alkálifémek (Na, K, …): +1 alkáliföldfémek (Mg, Ca, …): +2 fluor (F): -1 (semleges atomból redukcióval) oxigén (O): -2 (kivétel peroxidok mint H 2 O 2) hidrogén (H): +1 (kivétel hidridek mint Na. H) elemek többségének több oxidációs száma lehet (de: ≠vegyérték): S=-2, +4, +6 Számítható a fentiek alapján: pl. H 2 SO 4 -ben a kén oxidációs száma 6 0=2*(+1) + S + 4*(-2)

Redoxi egyenletek Redoxireakciókban oxidációsszám-változás történik (korrózió is ide tartozik!) • C + O 2 = CO 2 • Al + 3 HCl = Al. Cl 3 + 1½H 2 Reakció során valamely atom oxidációs száma csak úgy növekedhet, ha egy másiké csökken: az egyenlet adott oldalán az oxidációsszám-változások összege 0 kell legyen. Ionok esetében valós, kovalens kötésű molekulákban pedig formális elektronátmenet történik. Redoxi egyenletek rendezése: tömegmegmaradás + töltésmegmaradás Mn 4+ + Ce 3+ = Mn 2+ + Ce 4+ oxidációs számok összege: 7 6 Mn 4+ + 2 Ce 3+ = Mn 2+ + 2 Ce 4+ oxidációs számok: +5 3*(-2) IO 3↑ 5 IO 3 - -1 + + + 0 3*(-2) I- = I 2 +3 O 2↓ 1 5 I- = I 2 +3 O 25 I- = 3 I 2 +3 O 2 -

Redoxireakciók iránya Rendszer Eº (V) Rendszer Redoxipotenciál: számszerűen fejezi ki az F 2/2 F +2. 87 Sn/Sn 2+ egyes atomok/ionok/molekulák oxidációs Mn. O 4 -/Mn 2+ +1. 49 Fe/Fe 2+ illetve redukciós képességét. Információt Br 2/2 Br+1. 07 Zn/Zn 2+ I 2/2 I+0. 54 2 H 2 O/H 2+2 OHad arra, hogy egy adott redoxireakció Cu/Cu 2+ +0. 34 Al/Al 3+ végbemehet-e. H 2/2 H+ 0. 00 Na/Na+ Fontosabb törvényszerűségek: • pozitívabb redoxipotenciálú rendszer oxidálja a negatívabbat • negatívabb redoxipotenciálú rendszer redukálja a pozitívabbat Eº (V) -0. 14 -0. 44 -0. 76 -0. 83 -1. 66 -2. 71

Redoxireakciók iránya Rendszer Eº (V) Redoxipotenciál: számszerűen fejezi ki az 2+ F 2/2 F +2. 87 Sn/Sn -0. 14 egyes atomok/ionok/molekulák oxidációs 2+ 2+ Mn. O 4 /Mn +1. 49 Fe/Fe -0. 44 2+ illetve redukciós képességét. Információt Br 2/2 Br +1. 07 Zn/Zn -0. 76 I 2/2 I+0. 54 2 H 2 O/H 2+2 OH- -0. 83 ad arra, hogy egy adott redoxireakció Cu/Cu 2+ +0. 34 Al/Al 3+ -1. 66 végbemehet-e. + + H 2/2 H 0. 00 Na/Na -2. 71 Fontosabb törvényszerűségek: • pozitívabb redoxipotenciálú rendszer oxidálja a negatívabbat • negatívabb redoxipotenciálú rendszer redukálja a pozitívabbat • negatív redoxipotenciálú rendszert képező fémek savakban H 2 fejlődése mellett oldódnak • -0. 83 V-nál negatívabb redoxipotenciálú fémek vízben H 2 -fejlődés közben oldódnak (Al kivétel a felületén képződő védő oxidréteg miatt) • Példák: Zn + Cu 2+ → Cu + Zn 2+ (Zn 2+ + Cu ≠ Cu 2+ + Zn) Br 2 + 2 KI → 2 KBr + I 2 (I 2 + 2 KBr ≠ 2 KI + Br 2) Zn + 2 HCl → Zn. Cl 2 + H 2 (Cu + 2 HCl ≠ Cu. Cl 2 + H 2) 2 Na + 2 H 2 O → 2 Na+ + H 2 + 2 OH- (Zn + 2 H 2 O ≠ Zn 2+ + H 2 + 2 OH-)

Korrózió A környezet hatására a fémek felületéről kiinduló kémiai változások. (Latin: corrodo = szétrágni). Lényegében oxidáció, mely a fémek teljes vagy részleges átalakulásához vezet. 1967: Silver Bridge (West Virginia) 1 perc alatt összeomlott, 46 áldozat. USA 1998: 279 milliárd USD kár (3. 1% GDP) Margit-híd

Korrózió Vas korróziója (rozsdásodás): Bruttó reakció: 4 Fe + 3 O 2 + 6 H 2 O = 2 Fe 2 O 3. 6 H 2 O Részfolyamatok: • • vasrozsda: barna, pikkelyes szerkezetű Fe oxidációja: Fe = Fe 2+ + 2 e. O 2 redukciója: O 2 + 2 H 2 O + 4 e- = 4 OHFe(II)-hidroxid képződése: Fe 2+ + 2 OH- = Fe(OH)2 Fe(II)-hidroxidációja: 4 Fe(OH)2 + O 2 + 2 H 2 O = 2 Fe 2 O 3. 6 H 2 O Egyéb jellemzők: • Zn, Mg rúddal összekötve a vas rudat a korrózió lassul a negatívabb redoxipotenciálú rendszer hajlamosabb az oxidációra! • Cu rúddal összekötve a vas rudat a korrózió gyorsul • Mivel a reakcióhoz nedvesség szükséges, a korróziót az elektrokémiai folyamatok körébe soroljuk Rendszer Cu/Cu 2+ Fe/Fe 2+ Zn/Zn 2+ Mg/Mg 2+ Eº (V) +0. 34 -0. 44 -0. 76 -2. 38

Elektrokémia Galvánelem Alapkísérlet: cink lapot teszünk Cu. SO 4 oldatba Rendszer Cu/Cu 2+ Zn/Zn 2+ Eº (V) +0. 34 -0. 76 ox: Zn → Zn 2+ red: Cu 2+ → Cu Bruttó: Zn(s)+ Cu 2+(aq) → Zn 2+(aq) + Cu(s) Térben különválasztva a két folyamatot áram indul meg a két cellarész között: • fent fémes vezető (elektronokat szállítja) • Na 2 SO 4 sóhíd szulfátionok szállítására, így az oldatok semlegesek maradnak (egyszerűbb cellákban porózus diafragma) elektrolitok: Zn. SO 4, Cu. SO 4 oldatok • Celladiagram: - Zn(s)|Zn 2+(aq) || Cu 2+(aq)|Cu(s)+ • Zn anód (-, oxidáció), Cu katód (+, redukció) • Elektromotoros erő: feszültségkülönbség az fázishatár sóhíd fázishatár elektródok között árammentes esetben

Korrózió elleni (passzív) védekezés • korrodálódó fém módosítása (ötvözet), helyettesítése • nedvességtartalom csökkentése a környezetben • különböző bevonatok (fém, festék, műanyag) fémekkel galvánelem alakul ki! § § § elektrokémia: anódként szereplő komponens oxidálódik, azaz oldatba megy (korrodálódik) oxidbevonat: Fe-oxid laza szerkezetű, gyorsan oldja az elektrolit Zn-bevonat: a Zn oldódik, acél nem korrodálódik amíg egy kevés Zn is van rajta Cu-bevonat: addíg jó, míg a Cu meg nem sérül, utána gyorsan korrodálódik festék: addíg jó, míg nem sérül, előkezelés nélkül tapadása nem igazán jó néhány tized mikron vasfoszfát réteg elősegíti a festék tapadását, maga is korróziógátló
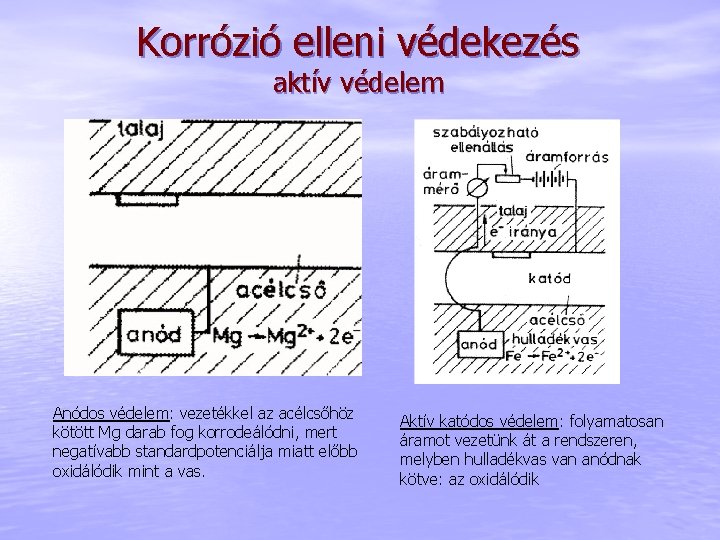
Korrózió elleni védekezés aktív védelem Anódos védelem: vezetékkel az acélcsőhöz kötött Mg darab fog korrodeálódni, mert negatívabb standardpotenciálja miatt előbb oxidálódik mint a vas. Aktív katódos védelem: folyamatosan áramot vezetünk át a rendszeren, melyben hulladékvas van anódnak kötve: az oxidálódik

Más galvánelemek Leclanché „szárazelem” (a hagyományos, legolcsóbb) • • • elektródok: grafit (katód), cink (anód) elektrolit: NH 4 Cl–Mn. O 2–szénpor, nedves pép működés: Mn 4+ Mn 3+, ill. Zn Zn 2+: Bruttó: 2 H+ + Zn + 2 Mn. O 2 Zn 2+ + 2 Mn. O(OH) Alkálikus: (nagyobb teljesítmény, hosszabb élettartam) szigetelő grafit Mn. O 22, , Mn. O grafitpor NH 4 Cl+Zn. Cl 2 elektrolit • elektrolit: KOH • anód: Zn(s) + 2 OH–(aq) Zn. O(s) + H 2 O + 2 e– • katód: 2 Mn. O 2(s) + H 2 O + 2 e– Mn 2 O 3(s) + 2 OH–(aq) Gombelemek: Zn helyett Li (Li-vegyület) Alkálikus „ezüstoxid”: (még nagyobb teljesítmény, még hosszabb élettartam) • • elektrolit: KOH vagy Na. OH oldat anód: Zn(s) + 2 OH–(aq) Zn. O(s) + H 2 O + 2 e– katód: Ag 2 O(s) + 2 e– 2 Ag alkalmazás: gombelemek illetve hadieszközökben mint Mark 37 torpedó Zn

Akkumulátorok Savas akkumulátor (pl. ólomakkumulátor): • • elektrolit: 33. 5 t/t% (~6 mol/dm 3) H 2 SO 4 elektródok: Pb és Pb. O 2 (Pb. SO 4 bevonat működés közben) ha kisütésről töltésre váltunk, a redoxfolyamatok felcserélődnek töltés: 2 H 2 O + Pb. SO 4(s) → Pb. O 2(s) + 2 e- + SO 42 - + 4 H+ (ox) Pb. SO 4(s) + 2 e- → Pb(s) + SO 42 - (red) • kisütés: Pb. O 2(s) + H 2 SO 4(aq) + 2 H+ + 2 e- → Pb. SO 4(s) + 2 H 2 O (red) Pb(s) + SO 42 -(aq) → Pb. SO 4(s) + 2 e- (ox) • töltéskor energiát fektetünk be, kisütéskor energiát kapunk (70 -92%) Alkalikus akkumulátorok (pl. Ni-Cd) • elektrolit: KOH oldat • elektródok: Ni. O(OH) és Cd • kisütés: Ni. O(OH)(s) + 2 H 2 O +2 e- Ni(OH)2 + 2 OH- (red) Cd(s) + 2 OH- → Cd(OH)2 + 2 e- (ox) • töltéskor fordítva • hatásfok: 70 -90%
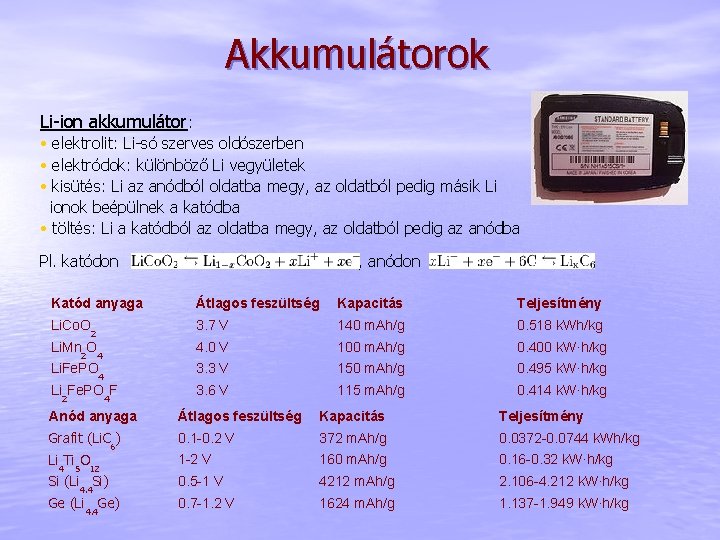
Akkumulátorok Li-ion akkumulátor: • elektrolit: Li-só szerves oldószerben • elektródok: különböző Li vegyületek • kisütés: Li az anódból oldatba megy, az oldatból pedig másik Li ionok beépülnek a katódba • töltés: Li a katódból az oldatba megy, az oldatból pedig az anódba Pl. katódon , anódon Katód anyaga Átlagos feszültség Kapacitás Teljesítmény Li. Co. O 3. 7 V 140 m. Ah/g 0. 518 k. Wh/kg 4. 0 V 100 m. Ah/g 0. 400 k. W·h/kg 3. 3 V 150 m. Ah/g 0. 495 k. W·h/kg 3. 6 V 115 m. Ah/g 0. 414 k. W·h/kg 2 Li. Mn O 2 4 Li. Fe. PO 4 Li Fe. PO F 2 4 Anód anyaga Átlagos feszültség Kapacitás Teljesítmény Grafit (Li. C 6) 0. 1 -0. 2 V 372 m. Ah/g 0. 0372 -0. 0744 k. Wh/kg Li 4 Ti 5 O 12 1 -2 V 160 m. Ah/g 0. 16 -0. 32 k. W·h/kg Si (Li 4. 4 Si) 0. 5 -1 V 4212 m. Ah/g 2. 106 -4. 212 k. W·h/kg Ge (Li 4. 4 Ge) 0. 7 -1. 2 V 1624 m. Ah/g 1. 137 -1. 949 k. W·h/kg

Üzemanyagcellák Üzemanyagcella: kémiai reakcióval elektromos áramot állít elő, mely addig történik, míg tápláljuk bele az üzemanyagot Alkáli üzemanyagcella (jelenleg a legjobban kidolgozott típus) • elektrolit: 30%-os vizes KOH oldat Alkáli üzemanyagcella • elektródok: platina Elektromos áram • működés: Katalizátor (általában platina) segítségével a hidrogénmolekulák és az elektrolitból jövő hidroxid-ionok vízzé alakulnak, miközben elektronok szabadulnak fel. Ezek aztán a katódra áramlanak, ahol (szintén katalizátor segítségével) az oxigén és víz reakciójával OH- ionokat képeznek. Az elektronok katódra való áramlása adja a hasznosítható elektromos áramot. Reakciók: Anódon: 2 H 2 + 4 OH- → 4 H 2 O + 4 e. Katódon: O 2 + 2 H 2 O + 4 e- → 4 OHA teljes reakció: 2 H 2 + O 2 → 2 H 2 O Elektromos hatásfok: 60 -70% Víz és hő Anód KOH oldat Katód

Elektrokémiai fogalmak Elektródpotenciál (e): standard hidogénelektróddal szemben mért cellapotenciál Standard hidrogénelektród (mindig a katód) • platina elektród (H 2 atomizálása) • 0, 1 MPa H 2 gáz • 1 mol/dm 3 H 3 O+-tartalmú savoldat • elektródpotenciálja megállapodás alapján 0. Elektródpotenciál meghatározása: • mérőcella ábra alapján • standard H 2 elektródot katódnak kapcsoljuk • mérjük az elektromotoros erőt: EME = ekatód - eanód • EME lehet pozitív és negatív is • függ az elektrolit ionkoncentrációjától Nernst-egyenlet: e = eº. (RT/z. F)lncion platina Zn anód eº: standardpotenciál (elektródra jellemző anyagi állandó) azonos azon standard redoxipotenciálokkal, melynél egyik forma az elem z: elektrolitban levő ion töltése F: Faraday állandó = 96494 C (1 mól elektron töltése)

Elektrolízis Elektromos energia segítségével kémiai átalakítást csinálunk, azaz redoxireakciót hajtunk végre. Elektrolizáló cella: galváncella, melyben az elektródokat és elektrolitot a célnak megfelelően választjuk meg Katód: negatív elektród, redukció történik Anód: pozitív elektród, oxidáció történik Faraday-törvény: képződött anyag mennyisége arányos az átfolyt töltéssel. It n= z. F átfolyt töltés 1 mol anyag leválasztásához szükséges töltés Vízbontás: katódon: 2 H 2 O + 2 e- = H 2 + 2 OH- (eº=-0, 83 V) anódon: 2 H 2 O = O 2 + 4 H+ + 4 e- (eº=+1, 23 V) Na vizes oldatból elektrolízissel nem állítható elő, mert a Na + + e- = Na folyamat standardpotenciálja (eº=-2, 71 V) nagyobb mint a H+ redukciójáé (eº=-0, 83 V), azaz a kevesebb energiát igénylő H 2 -fejlődés megy végbe. Na előállítása ezért: Na. Cl olvadékból történő elektrolízissel.
- Slides: 82