Klinische Chemie Leereenheid 4 Evelien Zonneveld 15 december

Klinische Chemie Leereenheid 4 Evelien Zonneveld 15 december 2005
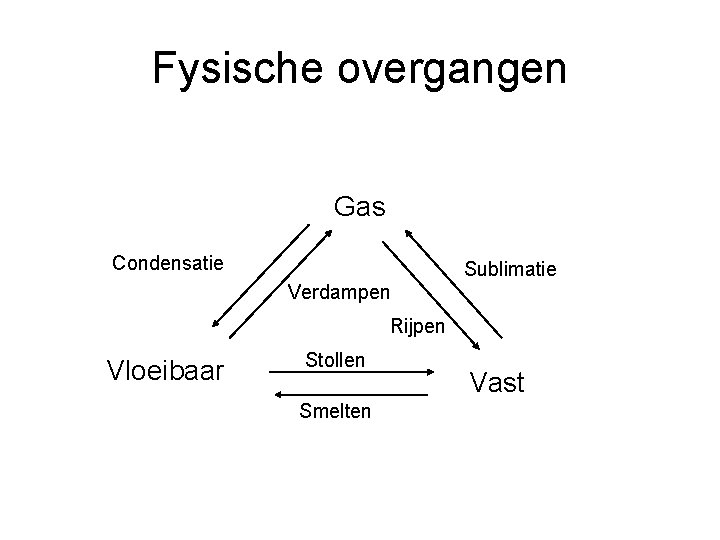
Fysische overgangen Gas Condensatie Sublimatie Verdampen Rijpen Vloeibaar Stollen Smelten Vast
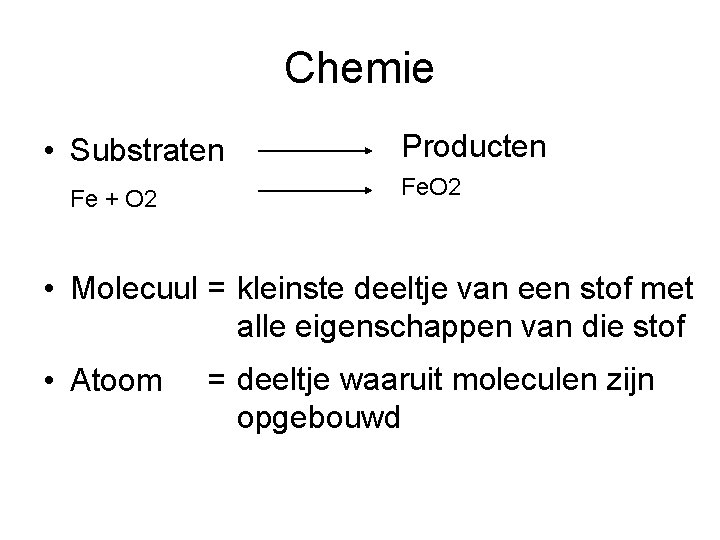
Chemie • Substraten Fe + O 2 Producten Fe. O 2 • Molecuul = kleinste deeltje van een stof met alle eigenschappen van die stof • Atoom = deeltje waaruit moleculen zijn opgebouwd
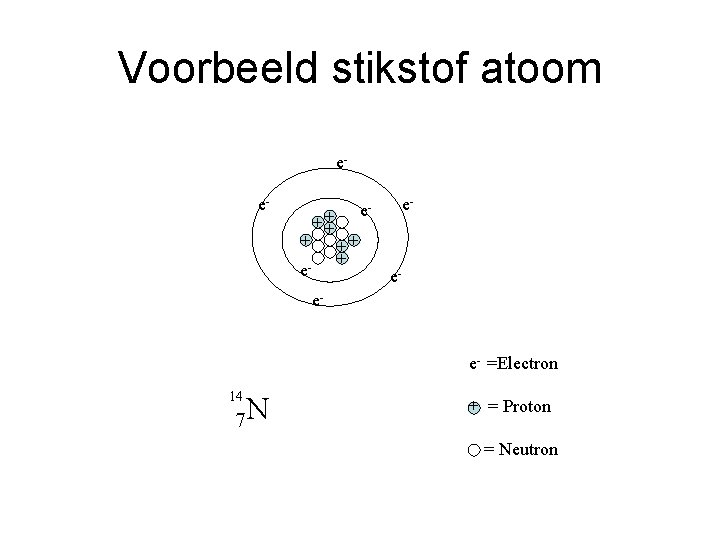
Voorbeeld stikstof atoom ee+ ++ + e- e- e++ + e- ee- =Electron 14 7 N + = Proton - = Neutron
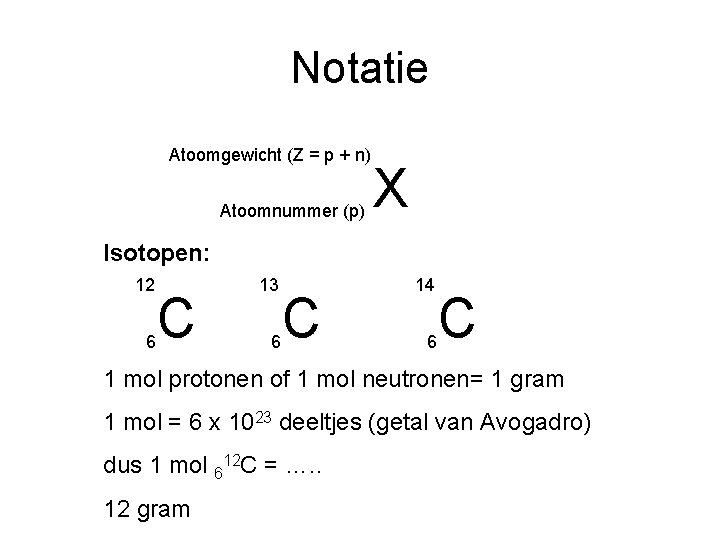
Notatie Atoomgewicht (Z = p + n) Atoomnummer (p) X Isotopen: 12 6 C 13 6 C 14 6 C 1 mol protonen of 1 mol neutronen= 1 gram 1 mol = 6 x 1023 deeltjes (getal van Avogadro) dus 1 mol 612 C = …. . 12 gram
Periodiek systeem der elementen

Edelgasconfiguratie • = 8 elektronen in buitenste schil. Uitzondering He (2 in buitenste schil) • K, l, m, n, etc schil met maximaal 2, 8, 8, 18 elektronen Buitenste schil max 8 e k l m n • Streven alle atomen na, want reageert niet makkelijk

Radio-activiteit • = straling die vrijkomt uit instabiele kern • -straling: teveel massa: 42 He-kern vrij • β-straling: teveel n: n p + β- deeltje • -straling: teveel E: fotonen vrij
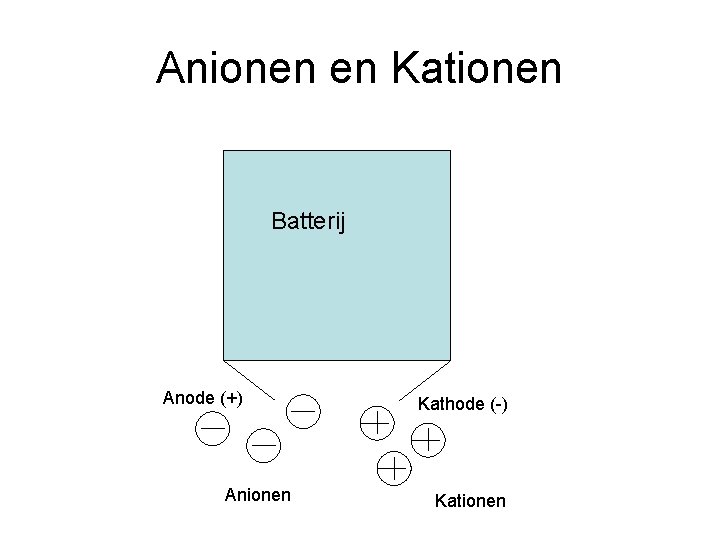
Anionen en Kationen Batterij Anode (+) Anionen Kathode (-) Kationen
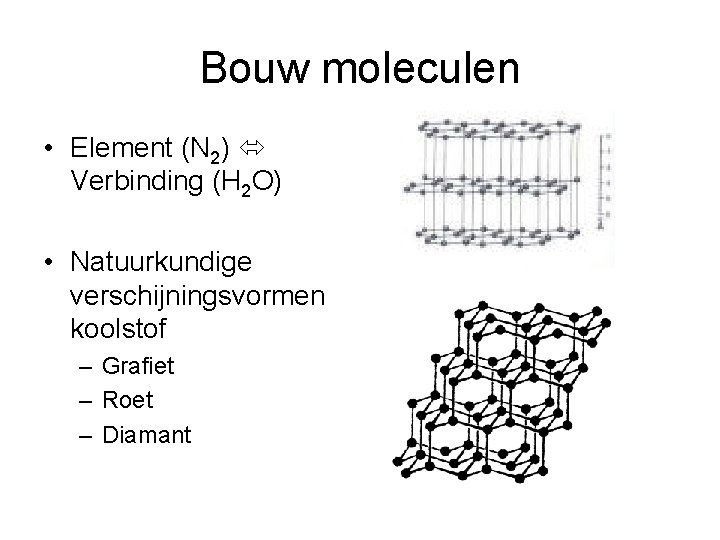
Bouw moleculen • Element (N 2) Verbinding (H 2 O) • Natuurkundige verschijningsvormen koolstof – Grafiet – Roet – Diamant
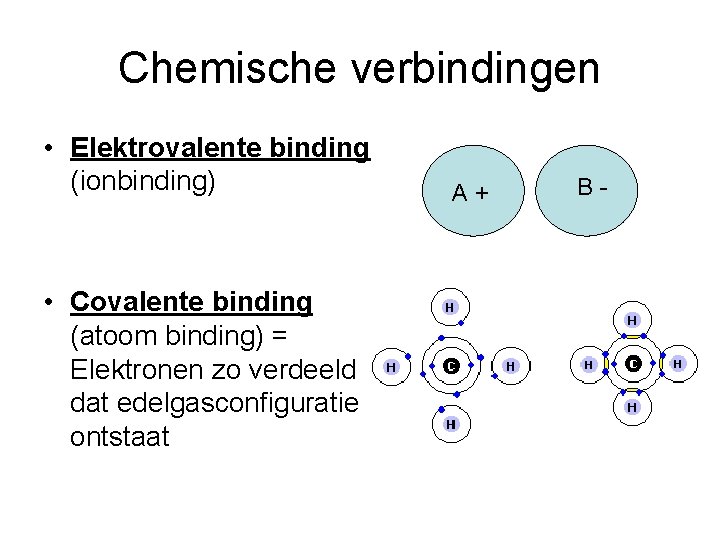
Chemische verbindingen • Elektrovalente binding (ionbinding) • Covalente binding (atoom binding) = Elektronen zo verdeeld dat edelgasconfiguratie ontstaat A+ B-
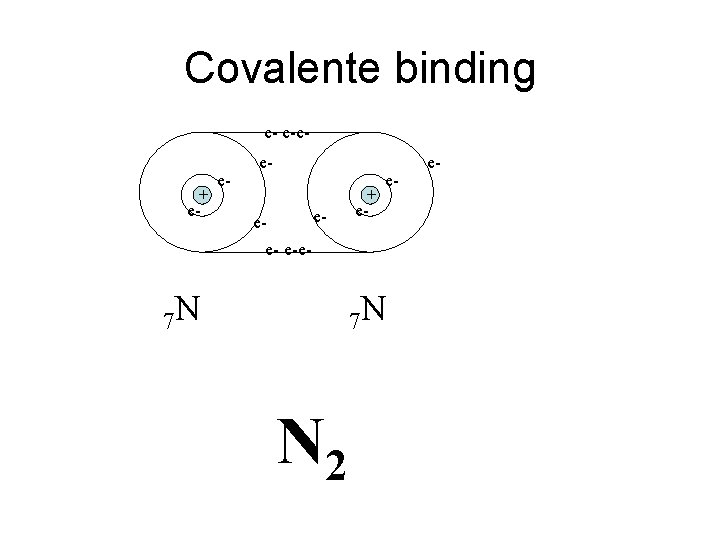
Covalente binding e- e-e+ e- e- eeee- e-e- 7 N + e- e- 7 N N 2 e-
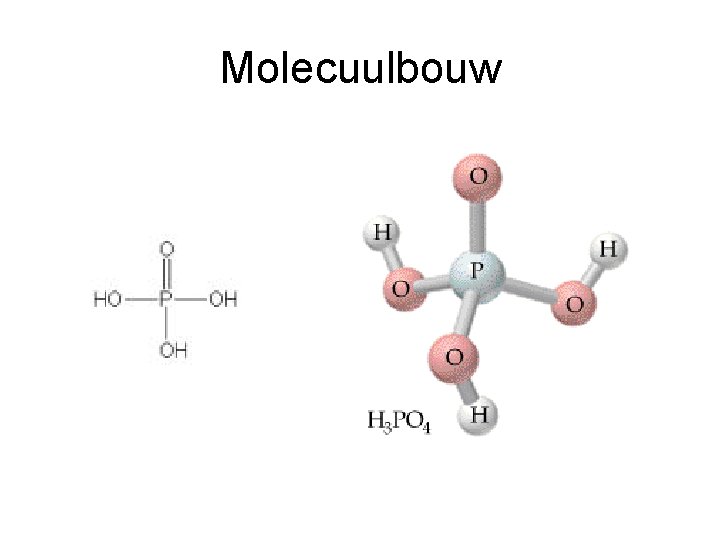
Molecuulbouw
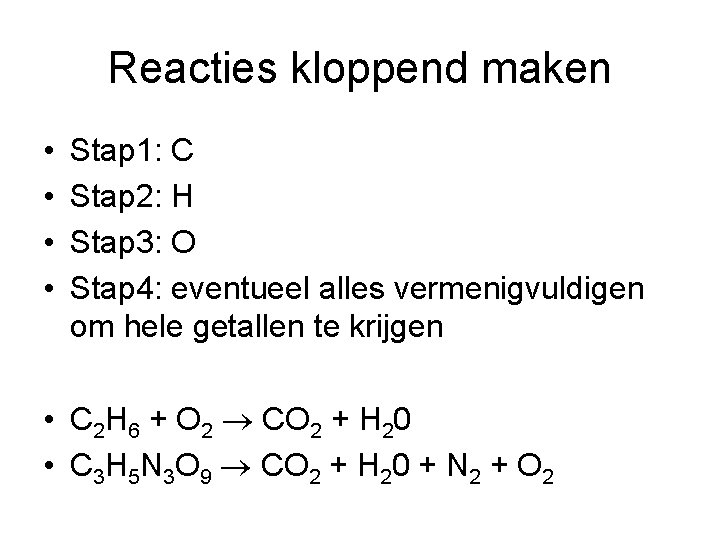
Reacties kloppend maken • • Stap 1: C Stap 2: H Stap 3: O Stap 4: eventueel alles vermenigvuldigen om hele getallen te krijgen • C 2 H 6 + O 2 CO 2 + H 20 • C 3 H 5 N 3 O 9 CO 2 + H 20 + N 2 + O 2

Oplosbaarheid • Polair lost op in polair (H 2 O) – O trekt harder aan e- dan H O wordt ‘negatief’ – Richt zich naar polaire stof – zie reader fig 1 -4 p 57 + • Apolair lost op in apolair (vet) – Geen richting van aantrekkingskracht +

Zuur-base • Zuren: laten H+ los – Sterk= heel makkelijk H+ los, zuurrest is zwakke base – Zwak= moeilijk H+ los, zuurrest is sterke base • Basen: binden H+ – Sterk= makkelijk H+ binden – Zwak= moeilijk H+ binden • p. H = - log [H 30+] – – Bv: [H 3 O+]= 1 x 10 -7 mol/l p. H= -log (1 x 10 -7) = -(-7)= 7 Zure opl p. H < 7 Basische opl p. H > 7
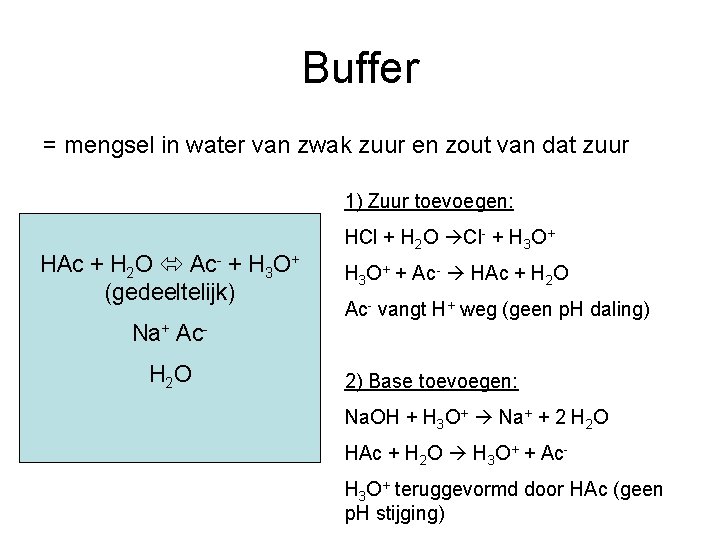
Buffer = mengsel in water van zwak zuur en zout van dat zuur 1) Zuur toevoegen: HAc + H 2 O Ac- + H 3 O+ (gedeeltelijk) Na+ Ac. H 2 O HCl + H 2 O Cl- + H 3 O+ + Ac- HAc + H 2 O Ac- vangt H+ weg (geen p. H daling) 2) Base toevoegen: Na. OH + H 3 O+ Na+ + 2 H 2 O HAc + H 2 O H 3 O+ + Ac. H 3 O+ teruggevormd door HAc (geen p. H stijging)
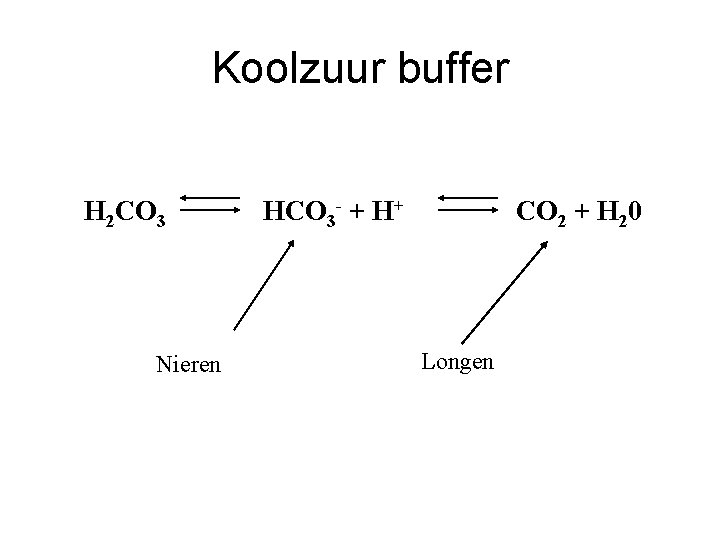
Koolzuur buffer H 2 CO 3 Nieren HCO 3 - + H+ CO 2 + H 20 Longen
- Slides: 18