Klik Sumber Tegangan Sumber tegangan adalah alat yang

Klik Sumber Tegangan Sumber tegangan adalah alat yang dapat membuat beda potensial Berdasarkan arah arus yang ditimbulkan sumber tegangan Klik dibedakan menjadi dua yaitu : 1. Sumber tegangan arus bolak balik ( AC ) Contoh generator, dynamo sepeda, stop kontak PLN 2. Sumber tegangan arus searah (dc ) Contoh elemen volta, baterai, akumulator, sel surya. Berdasarkan dapat diisi kembali atau tidaksumber tegangan Klik dibedakan menjadi dua yaitu : 1. Sumber tegangan Primer ( bila habis tidak dapat diisi lagi ) Contoh elemen volta, elemen daniel , elemen laclanche, baterai 2. Sumber tegangan sekunder ( bila habis dapat diisi lagi ) Contoh baterai Ni Cd, akumulator, sel surya, dynamo
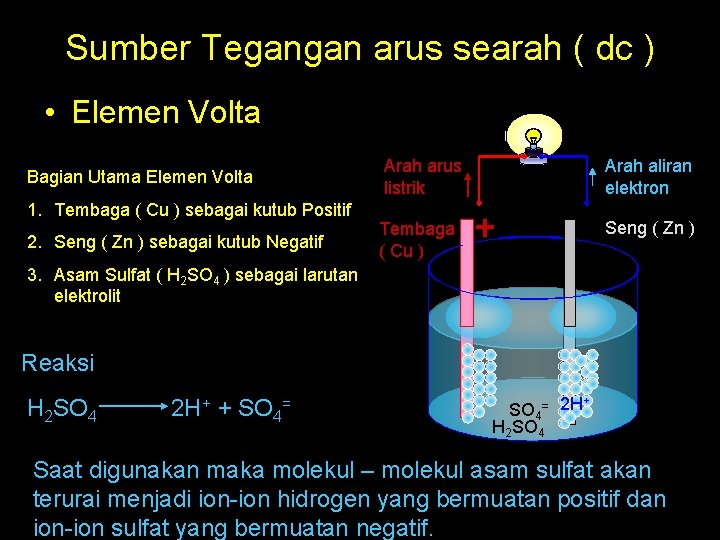
Sumber Tegangan arus searah ( dc ) • Elemen Volta Bagian Utama Elemen Volta 1. Tembaga ( Cu ) sebagai kutub Positif 2. Seng ( Zn ) sebagai kutub Negatif Arah arus listrik Arah aliran elektron Seng ( Zn ) Tembaga ( Cu ) 3. Asam Sulfat ( H 2 SO 4 ) sebagai larutan elektrolit Reaksi H 2 SO 4 2 H+ + SO 4= 2 H H 2 SO 4 Saat digunakan maka molekul – molekul asam sulfat akan terurai menjadi ion-ion hidrogen yang bermuatan positif dan ion-ion sulfat yang bermuatan negatif.
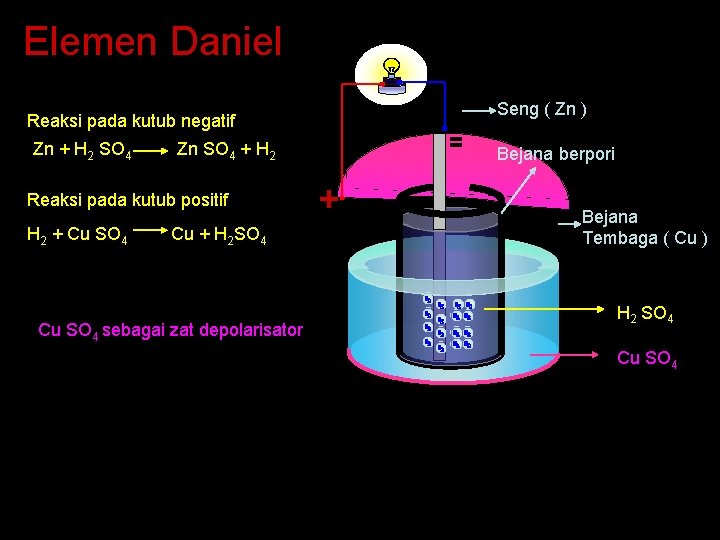
Elemen Daniel Reaksi pada kutub negatif Zn + H 2 SO 4 Zn SO 4 + H 2 Reaksi pada kutub positif H 2 + Cu SO 4 Cu + H 2 SO 4 Cu SO 4 sebagai zat depolarisator Seng ( Zn ) Bejana berpori Bejana Tembaga ( Cu ) H 2 SO 4 Cu SO 4
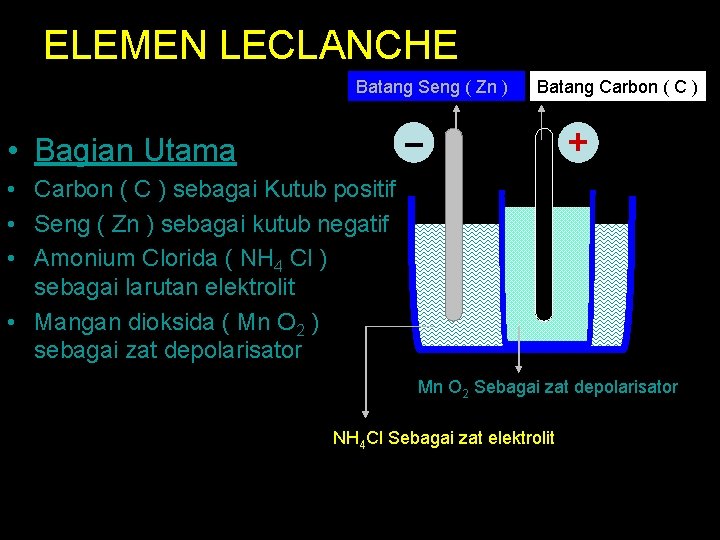
ELEMEN LECLANCHE Batang Seng ( Zn ) Batang Carbon ( C ) • Bagian Utama • Carbon ( C ) sebagai Kutub positif • Seng ( Zn ) sebagai kutub negatif • Amonium Clorida ( NH 4 Cl ) sebagai larutan elektrolit • Mangan dioksida ( Mn O 2 ) sebagai zat depolarisator Mn O 2 Sebagai zat depolarisator NH 4 Cl Sebagai zat elektrolit

ELEMEN KERING • Bagian Utama • Carbon ( C ) sebagai Kutub positif • Seng ( Zn ) sebagai kutub negatif • Amonium Clorida ( NH 4 Cl ) sebagai zat elektrolit yang berbentuk pasta ( kering ) • Mangan dioksida ( Mn O 2 ) sebagai zat depolarisator • Beda potensial carbon dan seng adalah 1, 5 Volt Carbon ( C ) Mangan dioksida ( Mn O 2) Amoniun Clorida ( NH 4 Cℓ) Seng ( Zn )
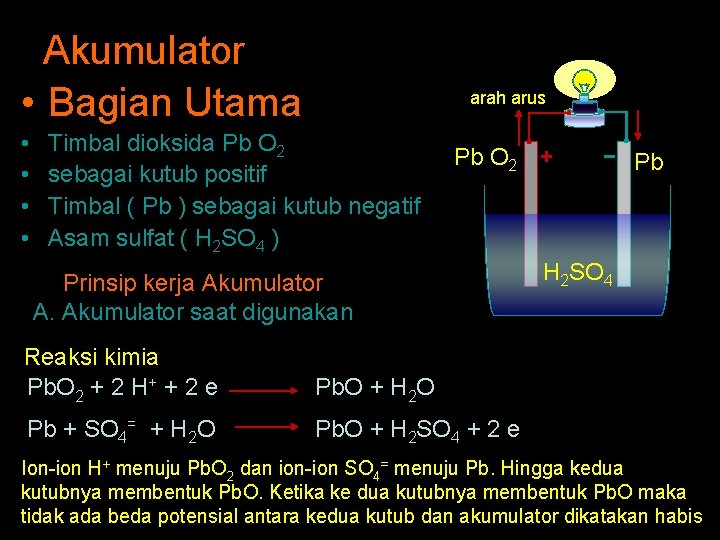
Akumulator • Bagian Utama • • arah arus Timbal dioksida Pb O 2 sebagai kutub positif Timbal ( Pb ) sebagai kutub negatif Asam sulfat ( H 2 SO 4 ) Pb O 2 Prinsip kerja Akumulator A. Akumulator saat digunakan Reaksi kimia Pb. O 2 + 2 H+ + 2 e Pb. O + H 2 O Pb + SO 4= + H 2 O Pb. O + H 2 SO 4 + 2 e Pb H 2 SO 4 Ion-ion H+ menuju Pb. O 2 dan ion-ion SO 4= menuju Pb. Hingga kedua kutubnya membentuk Pb. O. Ketika ke dua kutubnya membentuk Pb. O maka tidak ada beda potensial antara kedua kutub dan akumulator dikatakan habis
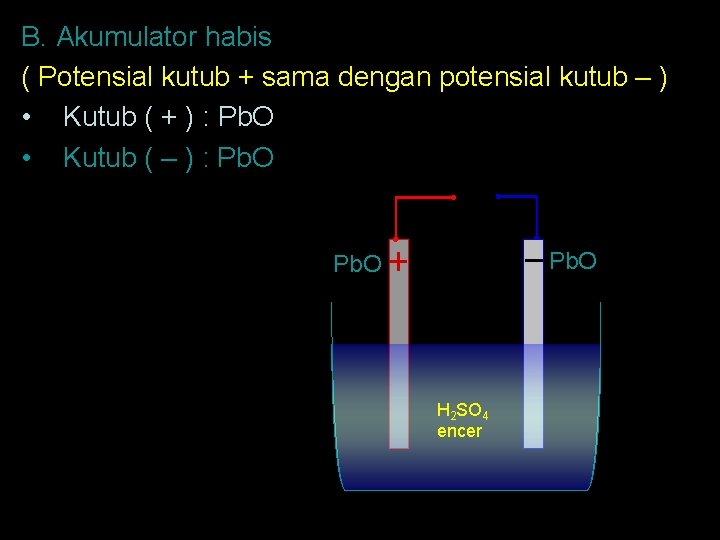
B. Akumulator habis ( Potensial kutub + sama dengan potensial kutub – ) • Kutub ( + ) : Pb. O • Kutub ( – ) : Pb. O H 2 SO 4 encer
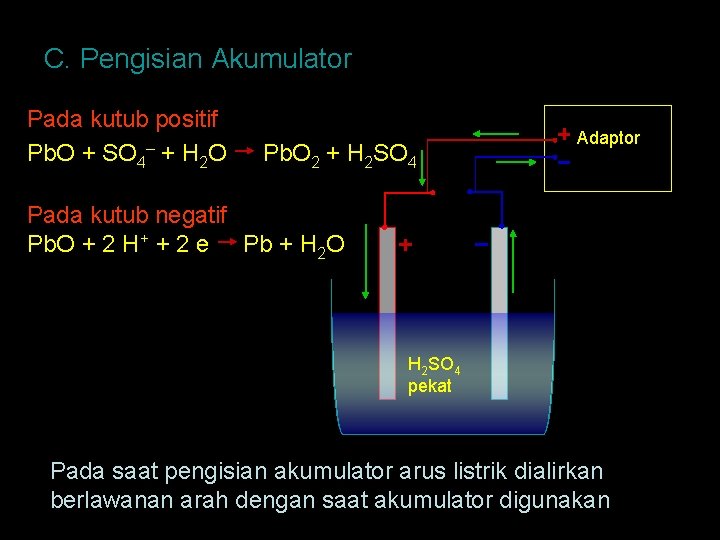
C. Pengisian Akumulator Pada kutub positif Pb. O + SO 4– + H 2 O Pb. O 2 + H 2 SO 4 Adaptor Pada kutub negatif Pb. O + 2 H+ + 2 e Pb + H 2 O H 2 SO 4 pekat Pada saat pengisian akumulator arus listrik dialirkan berlawanan arah dengan saat akumulator digunakan
- Slides: 8