Kk Hanmlar Kk Beyler Sizler hepiniz gelecein bir

Küçük Hanımlar, Küçük Beyler! Sizler hepiniz geleceğin bir gülü, yıldızı, bir mutluluk parıltısısınız! Memleketi asıl aydınlığa boğacak sizsiniz. Kendinizin ne kadar mühim, kıymetli olduğunu düşünerek ona göre ça Sizlerden çok şey bekliyoruz.







![Konsantrasyon 1, 0 [AB] [A 2] 0, 5 [B 2] 0 20 40 60 Konsantrasyon 1, 0 [AB] [A 2] 0, 5 [B 2] 0 20 40 60](http://slidetodoc.com/presentation_image/2603782431b05534c03bb6ca0d274d6c/image-9.jpg)
Konsantrasyon 1, 0 [AB] [A 2] 0, 5 [B 2] 0 20 40 60 80 Zaman 100






![[AB] [A 2] veya [B 2] [AB] [A 2] veya [B 2]](http://slidetodoc.com/presentation_image/2603782431b05534c03bb6ca0d274d6c/image-16.jpg)
[AB] [A 2] veya [B 2]


![[A 2] / mol·L– 1 0, 05 0, 04 0, 03 0, 02 0, [A 2] / mol·L– 1 0, 05 0, 04 0, 03 0, 02 0,](http://slidetodoc.com/presentation_image/2603782431b05534c03bb6ca0d274d6c/image-19.jpg)
[A 2] / mol·L– 1 0, 05 0, 04 0, 03 0, 02 0, 01 0 10 20 30 40 50 Zaman (t) / s







Bu hız ifadesi, tepkime hızının N 2 O 5 derişimi ile doğrudan orantılı olduğunu gösterir. Eğer derişim iki katına çıkarılırsa hız da iki katına çıkar. Eğer derişim üç katına çıkarılırsa hız da üç katına çıkar.


NO 2 derişimi iki katına çıkarılırsa, tepkime hızı da iki katına çıkar. HCl in derişiminin iki katına çıkarılması da tepkime hızını iki katına çıkarır. Eğer tepkimeye giren her iki maddenin derişimi de aynı anda iki katına çıkarılırsa, tepkime hızı dört katına çıkar.







Son örnek, bazı tepkimelerin basit mertebeden olmadıklarını gösterir. Bu tepkimeye ilişkin hız eşitliğinin, ürün (HBr) derişimi için de bir terim içerdiğine dikkat ediniz.
![Başlangıç derişimi Başlangıç hızı [NO] [O 2] NO 2 in oluşum hızı Deney Başlangıç derişimi Başlangıç hızı [NO] [O 2] NO 2 in oluşum hızı Deney](http://slidetodoc.com/presentation_image/2603782431b05534c03bb6ca0d274d6c/image-36.jpg)
Başlangıç derişimi Başlangıç hızı [NO] [O 2] NO 2 in oluşum hızı Deney mol/litre mol/ (litre∙s) A 1 · 10‒ 3 7 · 10‒ 6 B 1 · 10‒ 3 2 · 10‒ 3 14 · 10‒ 6 C 1 · 10‒ 3 3 · 10‒ 3 2 l · 10‒ 6 D 2 · 10‒ 3 3 · 10‒ 3 84 · 10‒ 6 E 3 · 10‒ 3 189 · 10‒ 6


3· 10– 3 mol/L =3 1· 10– 3 mol/L 32 = 9 olduğundan, x üssü 2 olmalı ve buna göre de, NO derişimini gösteren teri min karesi alınmalıdır. 189· 10– 3 mol/L =9 – 3 21· 10 mol/L Buna göre hız eşitliği şeklindedir. NO 2 in oluşum hızı: = k [NO]2[O 2] k nın değeri, deneylerden herhangi birindeki değerler kullanılarak bu lunabilir. Herbir halde aynı değer elde edilmelidir. Örneğin, A deneyindeki de ğerler yardımıyla k değeri aşağıdaki gibi hesabedebilir. NO 2 in oluşum hızı = k [NO]2[O 2] 7 ∙ 10‒ 6 mol/(litre·s) = k ( l ∙ 10‒ 3 mol/litre)2( l∙ 10‒ 3 mol/litre) 7 ∙ 10‒ 6 mol/(litre·s) = k ( l ∙ 10‒ 9 mol/litre 3) k= 7· 10– 6 mol/(litre·s) 1· 10– 9 mol 3/L 3 k = 7∙ 10‒ 6 litre 2/(mol 2·s)



Bu tepkimenin iki basamaklı bir mekanizma izlediğine inanılmaktadır. Mekanizma basamakları toplandığında, net tepkimenin kimyasal eşitliğinin elde edildiğine dikkat ediniz. Birinci basamakta oluşan F atomları, ikinci basamakta kullanıldığından, toplama sırasında birbirini götürürler. F atomları tepkimenin ara ürünleridir. Tepkimeye giren madde veya ürün olmayıp, tepkime sırasında oluşan ve tüketilen maddelere tepkime ara ürünleri denir.




1

Başlangıç Olay Sonuç

1
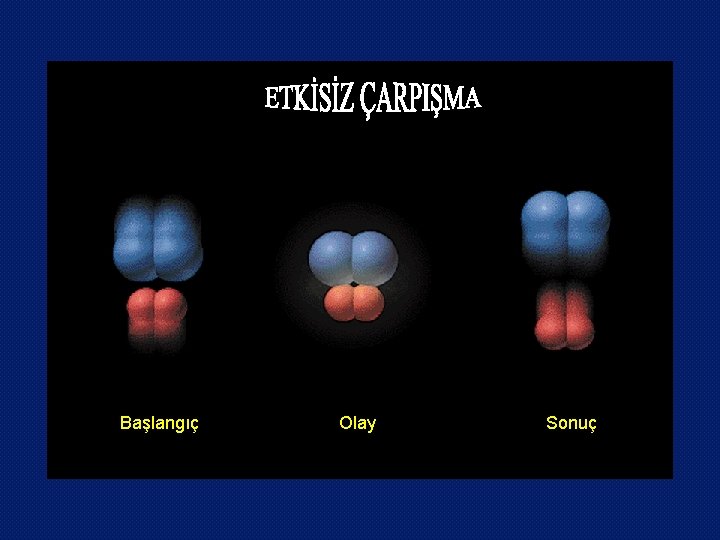
Başlangıç Olay Sonuç

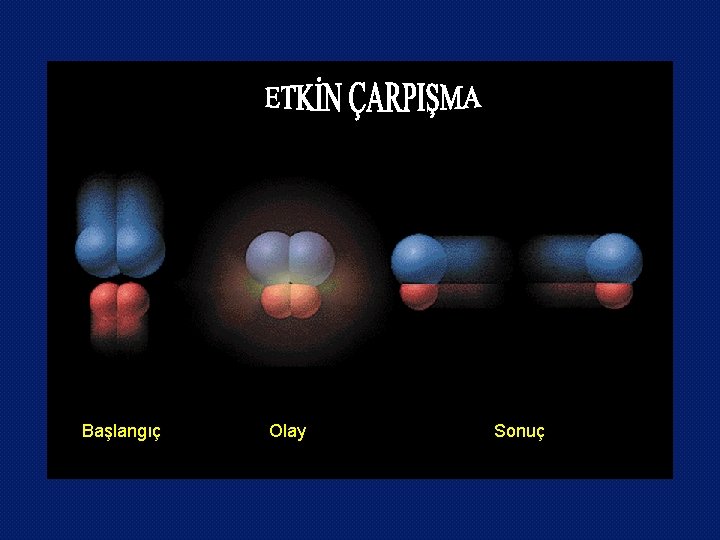
Başlangıç Olay Sonuç

Sıcaklık yükseltildiğinde, hemen bütün kimyasal tepkimelerin hızları artar. Bu etki, endotermik tepkimelerde olduğu gibi ekzotermik tepkimelerde de gözlenir. Oda sıcaklığına yakın sıcaklıklarda, sıcaklıktaki 10°C lık bir artışın, çoğu kez tepkime hızında % 100 den % 300 e kadar değişen bir artış sağladığı gözlenir. Sıcaklıktaki artışın sonucu oluşan daha hızlı moleküler hareket, birim zamanda daha fazla moleküler çarpışma oluşturur. Ancak bu faktör tek başına hızdaki artışın nedenini açıklayamaz. Sıcaklığın 25°C den 35°C a çıkarılması moleküler çarpışmaların toplam sayısında sadece % 2 kadar bir artışa neden olur.
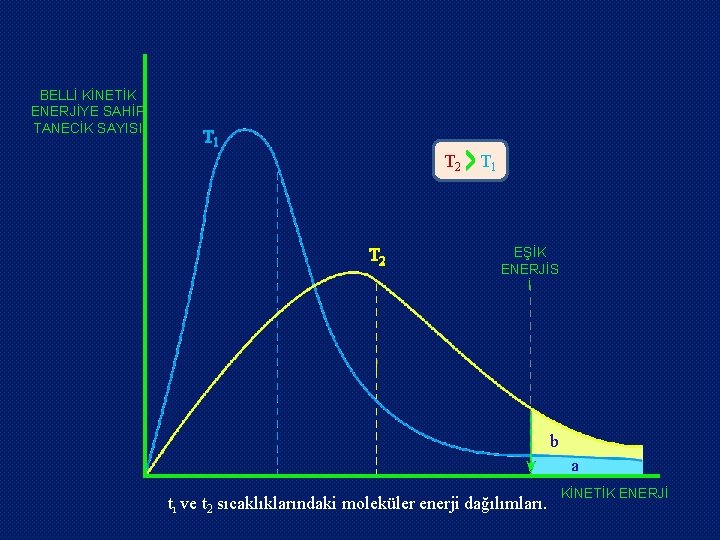
BELLİ KİNETİK ENERJİYE SAHİP TANECİK SAYISI T 1 T 2 T 1 EŞİK ENERJİS İ b a tı ve t 2 sıcaklıklarındaki moleküler enerji dağılımları. KİNETİK ENERJİ







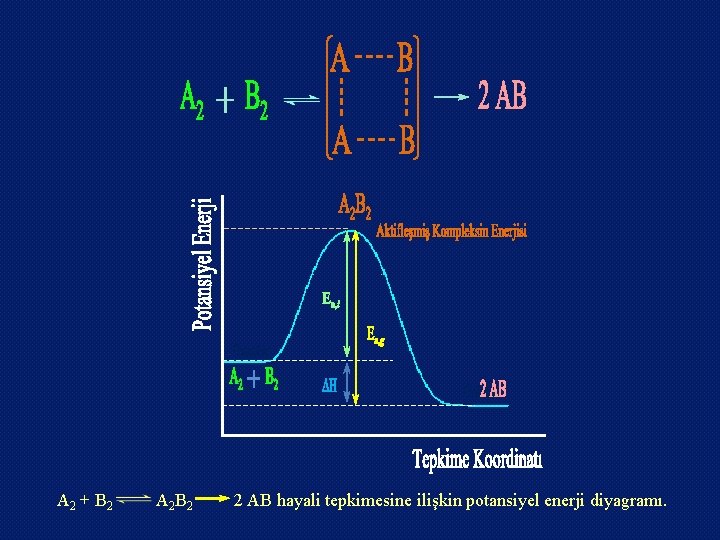
A 2 + B 2 A 2 B 2 2 AB hayali tepkimesine ilişkin potansiyel enerji diyagramı.








Bu yöntem, kimyasal eşitlik, yalnızca tek basamaklı bir tepkime ilgili ise kullanılır.

Genellikle aşağıdaki basamak türleri ile karşıla şılır. Tek moleküllü mertebedendir. bir tepkime birinci Bu tepkime, hız eşitliğinde görüldüğü gibi, A ya göre birinci mertebeden, B ye göre birinci mertebeden ve toplam olarak ikinci mertebedendir. Bu tepkime, hız eşitliğinde görüldüğü gibi, A ya göre ve toplam olarak ikinci mertebedendir.

Aynı anda üç taneciğin bir araya gelmesini gerektiren bu tür çarpışmalar çok seyrek oluşur. Moleküleritesi üçten daha yüksek olan basamaklar hiçbir zaman önerilmez. Herhangi bir düzen içinde oluşacak dörtlü bir çarpışma şansı çok kü çük olduğu için böyle çarpışmalar, hiçbir zaman bir tepkime mekanizmasının parçası olarak kabul edilmez.





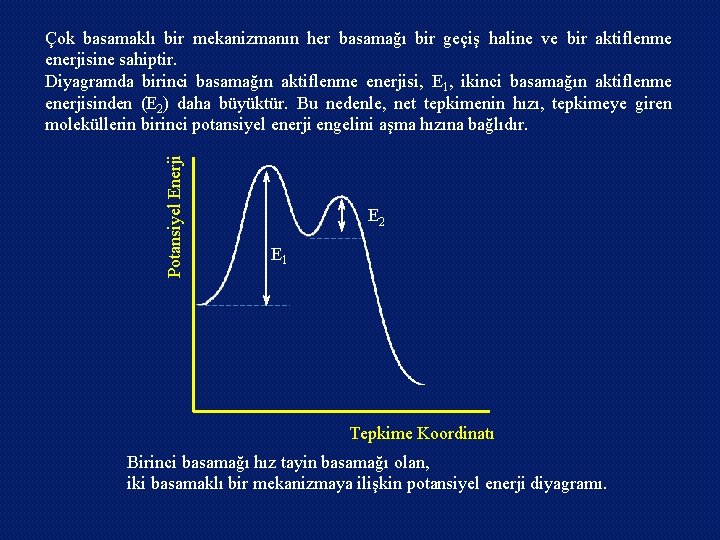
Potansiyel Enerji Çok basamaklı bir mekanizmanın her basamağı bir geçiş haline ve bir aktiflenme enerjisine sahiptir. Diyagramda birinci basamağın aktiflenme enerjisi, E 1, ikinci basamağın aktiflenme enerjisinden (E 2) daha büyüktür. Bu nedenle, net tepkimenin hızı, tepkimeye giren moleküllerin birinci potansiyel enerji engelini aşma hızına bağlıdır. E 2 E 1 Tepkime Koordinatı Birinci basamağı hız tayin basamağı olan, iki basamaklı bir mekanizmaya ilişkin potansiyel enerji diyagramı.


Bu eşitlikte; A incelenen tepkimeye ilişkin bir sabit (Frekans sabiti), e doğal logaritma tabanı (2, 718. . . ), Ea tepkimenin aktiflenme enerjisi (J/mol cinsinden), R molar gaz sabiti (8, 3143 J/mol· K) ve T ise mutlak sıcaklıktır. Bu eşitlik, ilk kez 1889 yılında Svante Arrhenius tarafından önerilmiş olup Arrhenius eşitliği olarak bilinir.


1/T 4, 0· 10‒ 3 3, 0· 10‒ 3 2, 0· 10‒ 3 1, 0· 10‒ 3 log k y x 15 10 5 0 ‒ 5 (1/K)
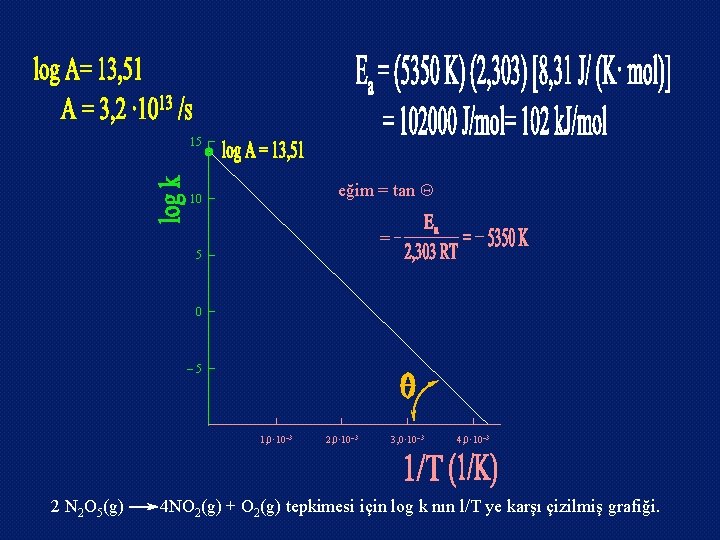
15 eğim = tan 10 = 5 0 ‒ 5 1, 0· 10‒ 3 2, 0· 10‒ 3 3, 0· 10‒ 3 4, 0· 10‒ 3 2 N 2 O 5(g) 4 NO 2(g) + O 2(g) tepkimesi için log k nın l/T ye karşı çizilmiş grafiği.



2 NOCl (g) 2 NO(g) + Cl tepkimesine ilişkin hız eşitliği 2(g) Cl 2 un oluşum hızı = k[NOCI]2 şeklindedir. Tepkimenin 300 K ve 400 K deki hız sabitleri sırasıyla, 2, 6 ∙ 10‒ 6 litre/ (mol ∙ s) ve 4, 9 ∙ 10‒ 4 litre/ (mol ∙ s) dir. Bu bilgilerden yararlanarak tepki menin aktiflenme enerjisini, Ea , bulunuz. ÇÖZÜM T 1 = 300 K T 2 = 400 K k 1 = 2, 6 ∙ 10‒ 6 litre/ (mol ∙ s) k 2 = 4, 9 ∙ 10‒ 4 litre/ (mol ∙ s) olduğundan ve molar gaz sabiti R = 8, 31 J/(K ∙ mol) olarak bilindiğinden tepkimenin aktiflenme enerjisi aşağıdaki gibi hesabedilir. Ea = 2, 303∙R T 1 T 2 − T 1 k 2 log k 1 Ea = 2, 303 [8, 31 J/(K∙mol)] (300 K) (400 K) 400 K − 300 K log 4, 9∙ 10− 4 litre/(mol∙s) 2, 6∙ 10− 8 litre/(mol∙s) = [19, 1 J/(K· mol] (1200 K) log (1, 88· 104) = (22900 J/mol) (4, 28)= 98000 J/mol = 98 k. J/mol

Bir önceki sorudaki bilgilerden yararlanarak 500 K deki k değerini hesaplayınız. ÇÖZÜM T 1 = 400 K T 2 = 500 K k 1 = 4, 9 ∙ 10‒ 4 litre/ (mol ∙ s) Ea = 9, 8 ∙ 104 J/mol k 2 = bilinmiyor olduğundan aşağıdaki eşitliği kullanırız log k 2 k 1 = = Ea 2, 303 R T 2 − T 1 T 2 9, 8∙ 104 J / mol 500 K− 400 K (400 K)(500 K) 2, 303 [8, 31 J/(K∙mol)] = (5, 13· 103 K)(5, 00· 10‒ 4 /K) = 2, 57 bu nedenle, k 2 k 1 = antilog 2, 57 = 3, 7 · 102 k 2 = (3, 7 · 102) kı = (3, 7 · 102) [4, 9 · 10‒ 4 litre/(mol · s)] = 0, 18 litre/(mol · s)





Mn. O 2 yanında, bu tepkime çok daha hızlı olup, KCl. O 3 daha düşük sıcaklıklarda bile yeteri hızla bozunur.





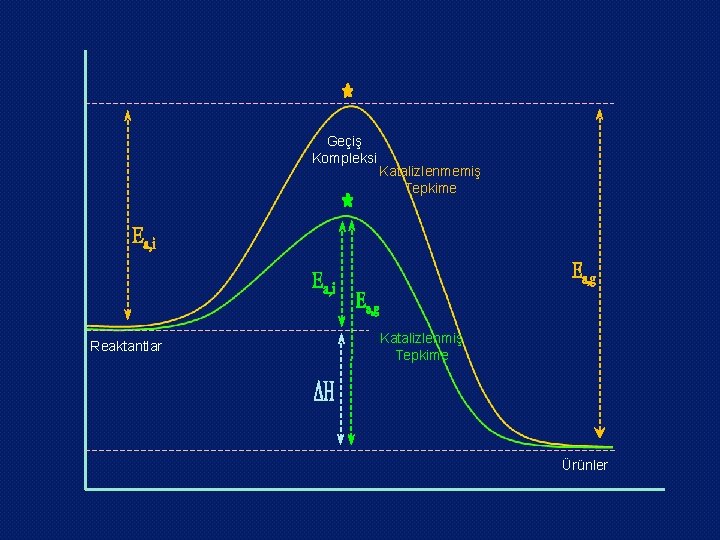
Geçiş Kompleksi Reaktantlar Katalizlenmemiş Tepkime Katalizlenmiş Tepkime Ürünler
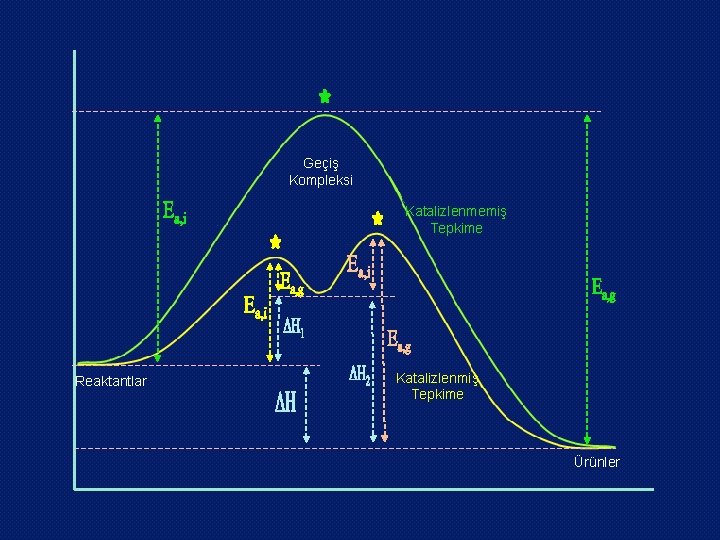
Geçiş Kompleksi Katalizlenmemiş Tepkime Reaktantlar Katalizlenmiş Tepkime Ürünler





Bu tür işlemlerde, tepkimeye giren moleküller katalizör yüzeyinde adsorplanır ve tepkime yüzeyde gerçekleşir. Odun kömürü, zararlı gazlar için gaz maskelerinde adsorban (adsorplayan madde) olarak kullanılır. Heterojen ka taliz, çoğunlukla kimyasal adsorpsiyon (ya da kemisorpsiyon) ile oluşmaktadır. Fiziksel adsorpsiyonda moleküller yüzeyde London kuvvetleri ile tutulurlar. Kimyasal adsorpsiyonda ise, moleküller yüzeyde kimyasal bileşiklerdeki bağlara benzer kuvvetli bağlar ile tutulmaktadır. Yüzey katalizli bir tepkimede, atom veya moleküllerin kimyasal olarak adsorplandıkları tabaka, bir tepkime ara ürünü olarak görev yapar.





Yüzey katalizinin son yıllardaki ilginç ve yararlı uygulamalarından birisi de otomobil eksozlarına katalitik dönüştürücülerin takılmasıdır. Otomobil motorlarında kullanılan yakıtın tam yanmaması nedeniyle çevreye verilen karbonmonoksit ve hidrokarbonlar oldukça ciddi ve tehli keli bir şekilde çevre kirliliğine neden olmaktadır. Otomobil eksozlarına takılan mini dönüştürücüler metal oksit katalizörleri içermekte olup, çıkış gazları ve ilave hava çevreye verilmeden önce bu dönüştürücüden geçirilmek suretiyle CO ve hidrokarbonlar oldukça zararsız olan CO 2 ve H 2 O ya dönüştürülerek atmosfere bırakılırlar. Ancak, katalizör kurşun tarafından zehirlendiği için, katalitik dönüştürücü (konvertör) bulunan otomobillerde kurşunsuz benzin kullanılmalıdır.

Enzimler olarak bilinen doğal katalizörler yaşam için çok daha büyük bir öneme sahiptir. Son derece karmaşık yapılara sahip olan enzimler sindirim, solunum ve hücre sentezi gibi oldukça önemli yaşam proseslerini katalizlerler. Canlı bünyesinde oluşan ve yaşam için gerekli olan çok sayıda karmaşık kimyasal tepkime, enzimlerin etkisiyle oldukça düşük vücut sıcaklığında oluşabilmektedir. Her karmaşık tepkime spesifik (özgün) bir enzim tarafından katalizlenmektedir. Enzimlerin etkileri ve yapıları üzerine yapılan oldukça yoğun araştırmalar, hastalık nedenlerinin ve büyüme mekanizmasının anlaşılabilmesine yardımcı olabilecektir.


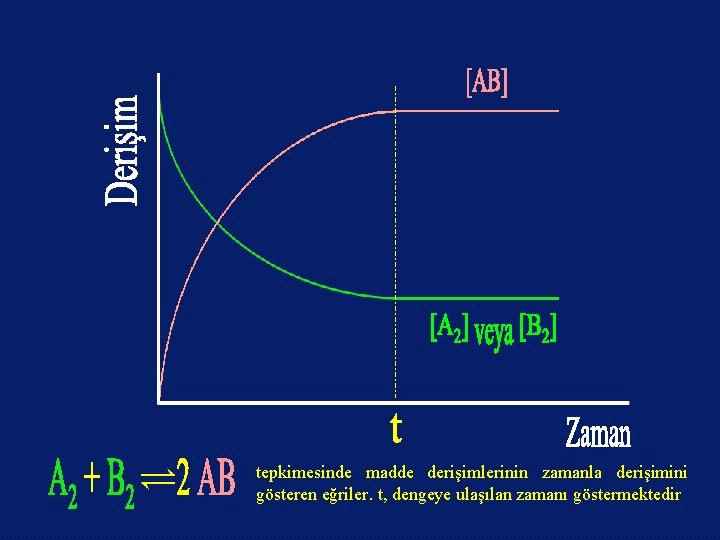
tepkimesinde madde derişimlerinin zamanla derişimini gösteren eğriler. t, dengeye ulaşılan zamanı göstermektedir










Tam doğru olabilmesi için, denge sabitlerine ilişkin eşitlikler, derişimler ya da basınçlar yerine aktiviteler cinsinden yazılmalıdır. Bununla beraber, düşük derişimler de ve birkaç atmosfere kadar düşük basınçlarda, derişimlerin kullanılması önemli bir hataya neden olmaz.




İki ya da daha çok fazlarda bulunan maddeler arasındaki dengeler heterojen dengeler olarak isimlendirilir. Sabit sıcaklık ve basınçta, saf katı ve saf sıvıların derişimleri sabittir. Bu nedenle, herhangi bir heterojen dengede, tepkime sisteminde yer alan saf katı ya da saf sıvıların derişim değerleri K değerine katılır ve bu maddelerin derişim terimleri denge sabiti ifadesinde gözükmez.


K denge sabiti ifadesinde, kimyasal eşitliğin sağ tarafındaki maddelerin (ürünler) derişim terimleri paya, sol tarafındaki maddelerin (tepkimeye giren maddeler) derişim terimleri ise paydaya yazılır. Tepkime sisteminde yer alan maddelerin stoki yometrik katsayıları ise derişim terimlerinin üstü alarak göste rilir. Saf katılar ve saf sıvılar için derişim terimleri yazılmaz. K nın değeri bu terimleri içerir. Herhangi bir dengeye ilişkin K değeri denge sıcaklığı değişmediği sürece sabittir. Farklı sıcaklıklardaki K değerleri farklıdır. Herhangi bir dengeye ilişkin K denge sabitinin büyüklüğü, denge konumunu belirler. Büyük bir K değeri, sağa doğru alan tep kimenin hemen tam olduğunu, küçük bir K değeri ise sola doğru olan tepkimenin hemen tam olduğunu gösterir. Ne çok büyük ne de çok küçük alan bir K değeri ise, bu ikisi arasında alan bir hali gösterir.
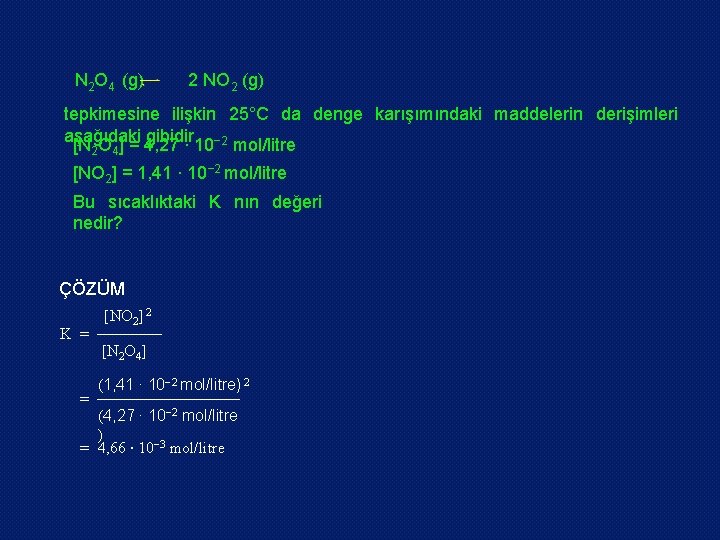
N 2 O 4 (g) 2 NO 2 (g) tepkimesine ilişkin 25°C da denge karışımındaki maddelerin derişimleri aşağıdaki gibidir. [N O ] = 4, 27 ∙ 10− 2 mol/litre 2 4 [NO 2] = 1, 41 ∙ 10− 2 mol/litre Bu sıcaklıktaki K nın değeri nedir? ÇÖZÜM K = = [NO 2] 2 [N 2 O 4] (1, 41 ∙ 10− 2 mol/litre) 2 (4, 27 ∙ 10− 2 mol/litre ) = 4, 66 ∙ 10− 3 mol/litre
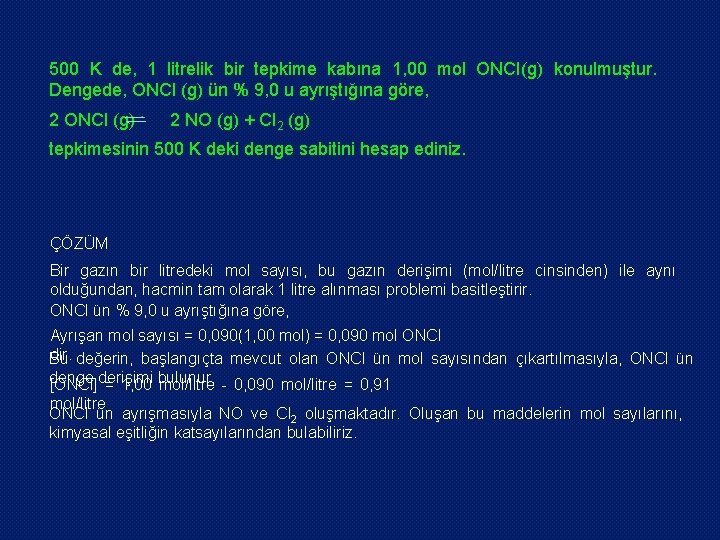
500 K de, 1 litrelik bir tepkime kabına 1, 00 mol ONCI(g) konulmuştur. Dengede, ONCl (g) ün % 9, 0 u ayrıştığına göre, 2 ONCl (g) 2 NO (g) + Cl 2 (g) tepkimesinin 500 K deki denge sabitini hesap ediniz. ÇÖZÜM Bir gazın bir litredeki mol sayısı, bu gazın derişimi (mol/litre cinsinden) ile aynı olduğundan, hacmin tam olarak 1 litre alınması problemi basitleştirir. ONCl ün % 9, 0 u ayrıştığına göre, Ayrışan mol sayısı = 0, 090(1, 00 mol) = 0, 090 mol ONCl dir. değerin, başlangıçta mevcut olan ONCl ün mol sayısından çıkartılmasıyla, ONCl ün Bu denge [ONCl]derişimi = 1, 00 bulunur. mol/litre 0, 090 mol/litre = 0, 91 mol/litre ONCl ün ayrışmasıyla NO ve Cl 2 oluşmaktadır. Oluşan bu maddelerin mol sayılarını, kimyasal eşitliğin katsayılarından bulabiliriz.

2 ONCl (g) 2 NO (g) 0, 090 mol + Cl 2 (g) 0, 045 mol Kimyasal eşitliğe göre, 2 mol ONCl den 2 mol NO ve 1 mol Cl 2 oluşmaktadır. Bu nedenle, 0, 090 mol ONCl den 0, 090 mol NO ve 0, 045 mol Cl 2 oluşacaktır. Buna göre, tepkime sisteminde yer alan maddelerin denge derişimleri [ONCI] = 0, 91 mol/litre [NO] = 0, 090 mol/litre [CI 2] = 0, 045 mol/litre olduğundan, denge sabiti K = = [NO] 2 [Cl 2] [ONCl]2 (0, 09 mol/litre) 2 (0, 045 mol/litre) (0, 91 mol/litre )2 = 4, 4 ∙ 10− 4 mol/litre

H 2 (g) + I 2 (g) 2 HI(g) tepkimesinin 425 o. C deki denge sabiti 54, 8 dir. Bir miktar HI (g) 1 litrelik bir tepkime kabına konularak dengeye gelmesi bekleniyor. HI (g) ün denge derişimi 0, 50 mol/litre olduğuna göre, H 2 (g) ve I 2 (g) un denge derişimleri nedir! ÇÖZÜM HI (g) ün bozunması ile denge stokiyometrisine göre eşit mol sayısında H 2 (g) ve I 2 (g) oluşacağından, bunların derişimleri de eşit olmalıdır. Bu nedenle, [H 2 ] = [I 2 ] = x yazılır. HI(g) nın denge derişimi [HI] = 0, 50 mol/litre olduğundan, : bu değerler denge sabiti ifadesinde yerlerine konur ve x'e göre, çözülür. [HI] 2 K = = 54, 8 [H 2] [I 2] litre/mol [0, 050 mol/litre] 2 = 54, 8 x·x litre/mol 54, 8 · = 0, 025 mol 2/litre 2 x 2 = 0, 00456 mol 2/litre 2 = x = 0, 0068 mol/litre [HI] = 0, 50 mol/litre [H 2] = 0, 068 mol/litre [I 2] = 0, 068 mol/litre

H 2 (g) + CO 2 (g) CO (g) + H 2 O (g) tepkimesinin 750 o. C deki K değeri 0, 771 dir. Eğer 750 o. C de 1 litrelik bir tepkime kabında. 0, 0100 mol H 2 ile 0, 0100 mol CO 2 karıştırılırsa, tepkimede yer alan tüm maddelerin denge derişimleri ne olur? ÇÖZÜM Eğer tepkime ortamındaki maddelerden x mol H 2, x mol CO 2 ile tepkimeye girerse, tepkime stokiyometrisine göre x mol H 2 O ve x mol CO oluşur. Kabın hacmi 1 litre olduğundan, tepkimede yer alan maddelerin denge derişimleri (mol/litre cin sinden} aşağıdaki gibi olmalıdır. H 2 (g) + CO 2 (g) CO (g) + H 2 O (g) [H ] = [CO ] = 0, 0100 x (0, 0100 x) Buna göre, [H 2 O] [CO] K = = 0, 77 [H 2] [CO 2] 1 = x 2 x x = 0, 77 (0, 0100 – x)[CO 12] 2 2 = 0, 0100 – 0, 00468 = 0, 0053 mol/litre = 5, 3· 10‒ 3 mol/litre [H 2 O] = [CO] = x = 0, 00468 mol/litre = 4, 68· 10‒ 3 mol/litre x = 0, 00468






2 SO 3 (g) 2 SO 2 (g) + O 2 (g) tepkimesinin 1100 K deki denge sabiti 0, 0271 mol/litre olduğuna göre, bu sıcaklıktaki Kp sabiti nedir? ÇÖZÜM İki mol SO 3 (g) den toplam 3 mol gaz oluştuğundan, Δn = + 1 Kp = K (RT) +1 = (0, 0271 mol/litre) [(0, 0821 litre atm/K mol) (1100 K)] dir. = 2, 45 atm
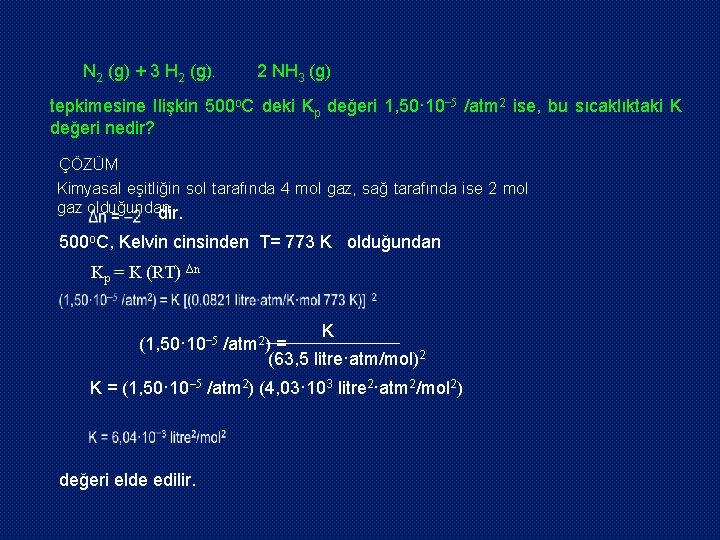
N 2 (g) + 3 H 2 (g) 2 NH 3 (g) tepkimesine Ilişkin 500 o. C deki Kp değeri 1, 50· 10‒ 5 /atm 2 ise, bu sıcaklıktaki K değeri nedir? ÇÖZÜM Kimyasal eşitliğin sol tarafında 4 mol gaz, sağ tarafında ise 2 mol gaz olduğundan dir. 500 o. C, Kelvin cinsinden T= 773 K olduğundan Kp = K (RT) Δn K (1, 50· 10‒ 5 /atm 2) = (63, 5 litre·atm/mol)2 K = (1, 50· 10‒ 5 /atm 2) (4, 03· 103 litre 2·atm 2/mol 2) değeri elde edilir.

C (k) + CO 2 (g) 2 CO (g) tepkimesinin 1000 o. C deki Kp değeri 167, 5 atm dir. CO 2 (g) in dengedeki kısmi basıncı 0, 100 atm olduğuna göre CO (g) in dengedeki kısmi basıncı nedir? ÇÖZÜM Kp = P 2 CO PCO 2 = 167, 5 atm P 2 CO = 167, 5 atm 0, 100 atm P 2 CO = 16, 75 atm 2 PCO = 4, 10 atm

Fe. O (k) + CO (g) Fe (k) + CO 2 (g) dengesi için 1000 o. C deki Kp değeri 0, 403 dir. Eğer bir tepkime kabına 1000 o. C de, 1, 000 atm basınçta CO(g) ve aşırı miktarda Fe. O (k) konulursa, dengeye ulaşıldığında CO(g) ve CO 2 (g) in basınçları ne olur? ÇÖZÜM Dengedeki CO 2 in kısmi basıncına x dersek, Fe. O (k) + CO (g) (1, 00 x) atm Kp = PCO 2 PCO = 0, 403 X atm = 0, 403 (1, 000 x) atm x = PCO 2 = 0, 287 atm 0, 100 x= PCO = 0, 713 atm değerleri elde edilir. Fe (k) + CO 2 (g) x atm

Henry Le Chatelier 1850 1936







Toplam 3 mol gaz Toplam 2 mol gaz

Toplam 2 mol gaz




Ekzotermik Endotermik

Endotermik Ekzotermik



- Slides: 158