Kjemiforkurs 2014 Dag 1 Kjemi grunnstoff binding periodesystemet

Kjemi-forkurs 2014 Dag 1: Kjemi, grunnstoff, binding periodesystemet, reaksjonar

Mål for dagen �Kunne oktettregelen �Kunne balansere reaksjonslikningar �Skjøne oppbygninga til Periodesystemet �Kunne ulike bindingstypar

Kva er kjemi? � «the study of the composition, structure, properties and change of matter» - wikipedia �Kvifor og korleis?

Kvifor skjer kjemiske reaksjonar? �Energigevinst ved elektronoverføringar og –endringar �(Entalpi og entropi på torsdag)

Atomet �Positiv kjerne av proton of nøytron �Elektron i skall rundt (K, L, M. . . ) ◦ Underskall (s, p d, f. . . ) �Grunnstoff kjernen har eit gitt tal proton i

Grunnstoffa og periodesystemet �Grunnstoffa vert arrangert i periodar etter kva for skall dei yttste elektrona er i og i grupper etter kor mange elekron dei har i dei ulike underskalla
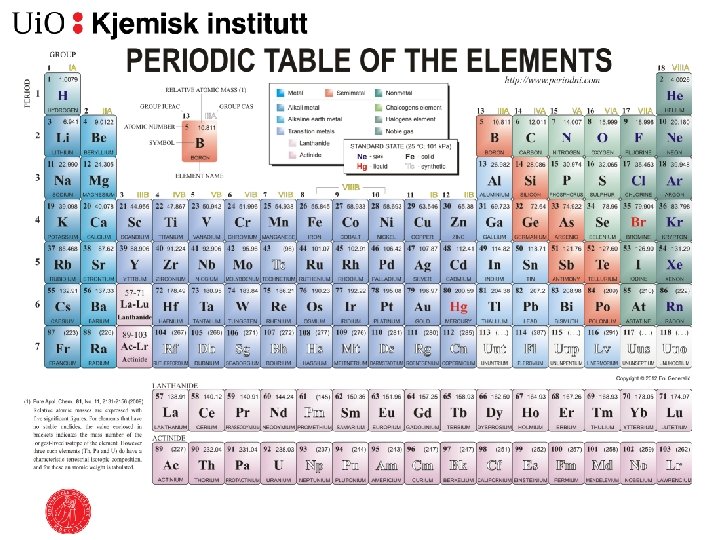
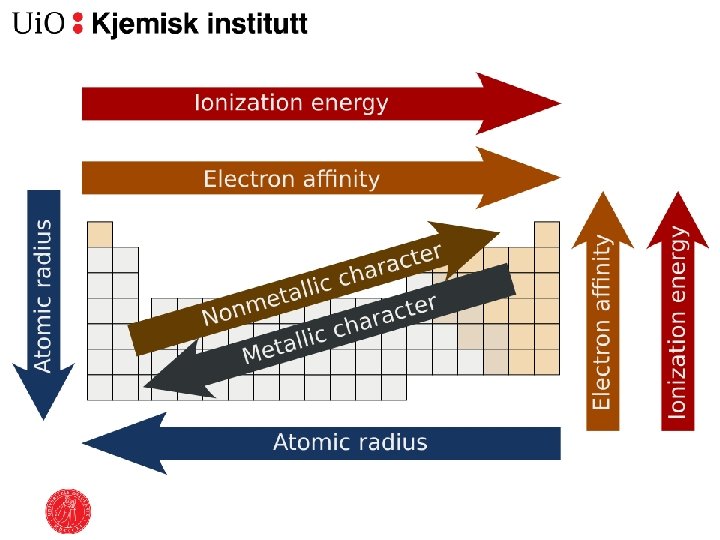

Elektronegativitet �Evnen til eit atom til å tiltrekke seg elektron �Synk høgre til venstre og topp til botn i Periodesystemet

Elektronegativitet

Oktettregelen �Prinsipp: Alle vil vere ein edelgass dvs. 8 elektron i yttste skall �Eksempel: ◦ Oksygen har 6 valenselektron binder seg til to hydrogen har no 8 �HUGS: Kun «permanent» flytting av elektron gir ladning

Binding �Sterke bindingar �Svake bindingar

Sterke bindingar �Ulike typar bindingar: ◦ Ionisk binding – Lokaliserte ioner ◦ Metallbinding – Delokaliserte elektroner ◦ Kovalent binding – Delte elektron, elektronparbinding
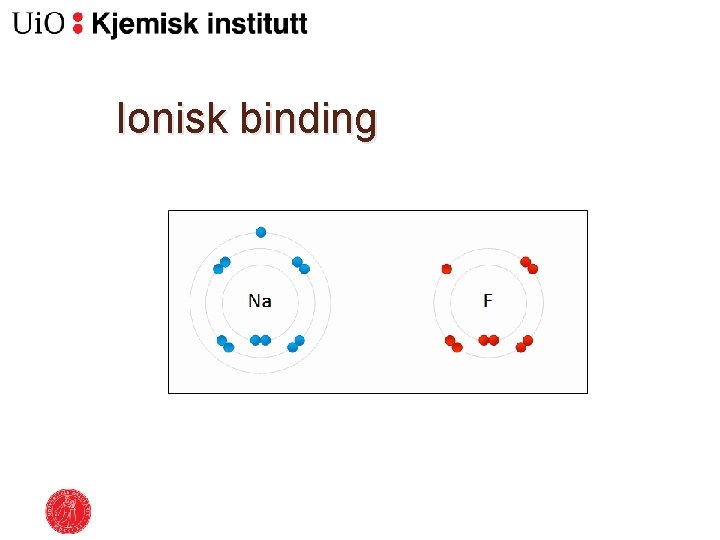
Ionisk binding
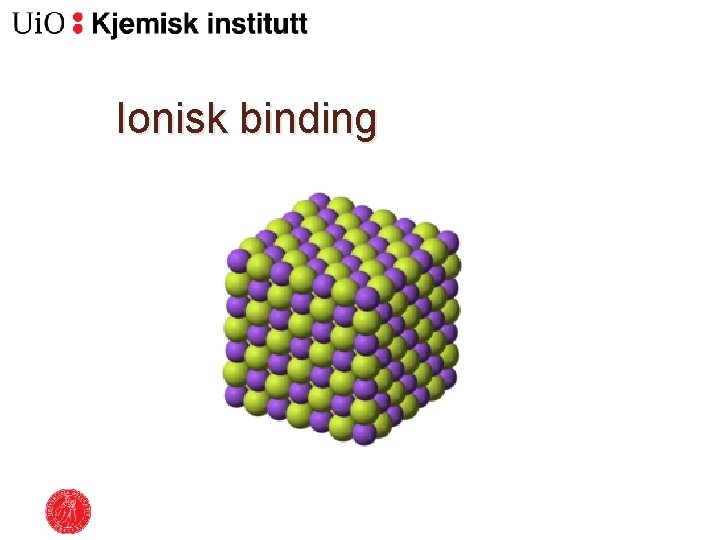
Ionisk binding
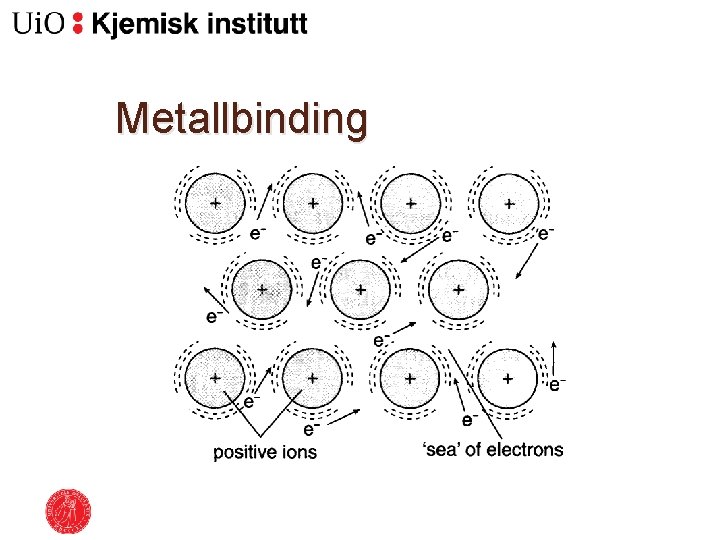
Metallbinding
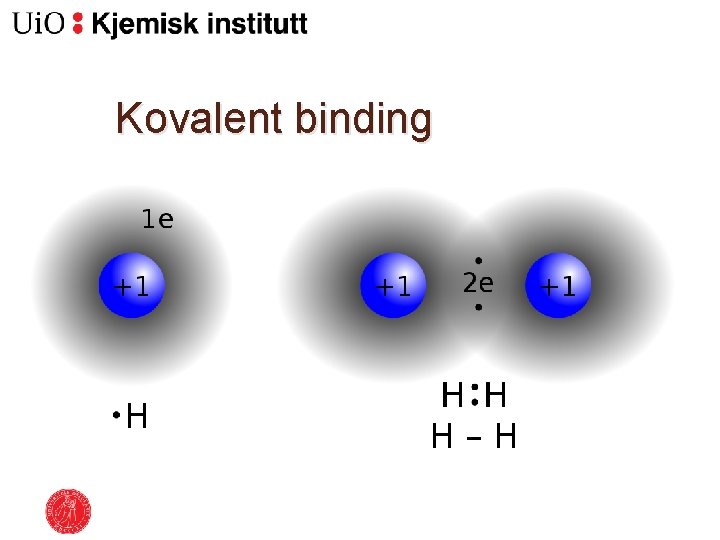
Kovalent binding
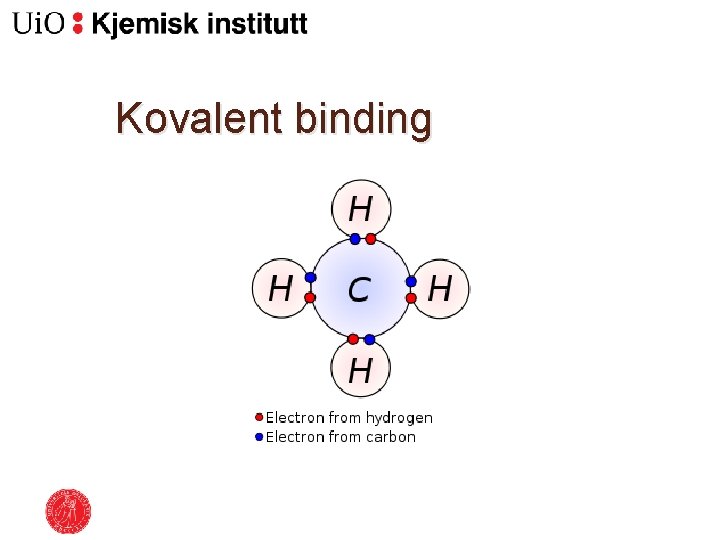
Kovalent binding
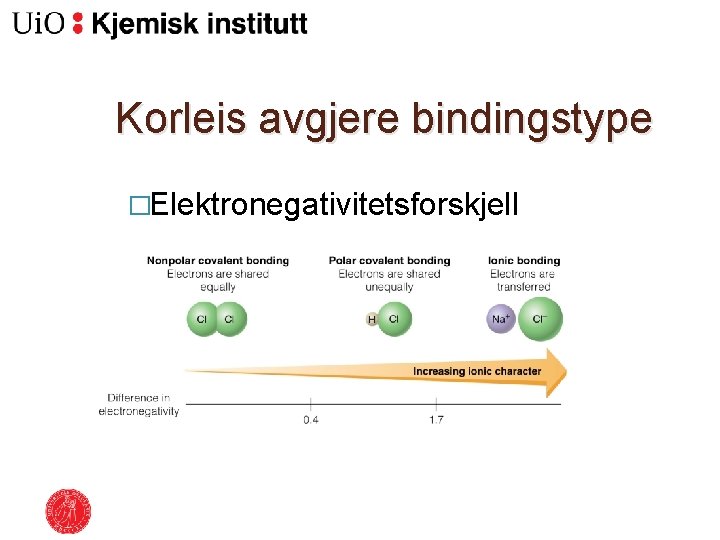
Korleis avgjere bindingstype �Elektronegativitetsforskjell

Svake bindingar �Hydrogenbindingar ◦ Frå F, N, O til H bunden til F, N eller O �Dispersjonskrefter ◦ Dipol-dipol (elektronegativitet)

Klassiske reaksjonstypar �Forbrenning �Syntese: A + B → AB �Dekomposisjon: AB → A + B �Enkel utbytting: A + BC → AB + C �Dobbel utbyttning: AB + CD → AC + BD

Reaksjonstypar �Syre-base: ± «proton» �Red-oks: ± «elektron» �Utfelling

Reaksjonslikningar �

Balansering � 1) � 2) Skriv likninga med alle involverte stoff Sørg for at det atomet som står færrest plassar har same tal atom på båe sider av pila � 3) Korigér for endringar fororsaka av den fyrste balanserninga � 4) Evt. Gjer 2) og 3 igjen med eit anna atom � 5) Skriv balansert likning

Eksempel på balansering �

Appendix 2 - Tilrådd literatur �J. Keeler, P. Wothers: Why chemical reactions happen, 2003, OUP �R. Chang, J. Overby, General Chemistry, kap. 2 -4 �Kjemien stemmer 1, kap.
- Slides: 26