KISELINE I BAZE Pripremio Varga Itvan HEMIJSKOPREHRAMBENA SREDNJA

KISELINE I BAZE Pripremio: Varga Ištvan HEMIJSKO-PREHRAMBENA SREDNJA ŠKOLA ČOKA varga. i@neobee. net

Arenijusova teorija kiselina i baza • Kiseline su supstance koje disocijacijom u vodenim rastvorima daju vodonikove jone, dok baze hidroksidne jone. Opštim jednačinama: HA H + + AMOH M+ + OH-
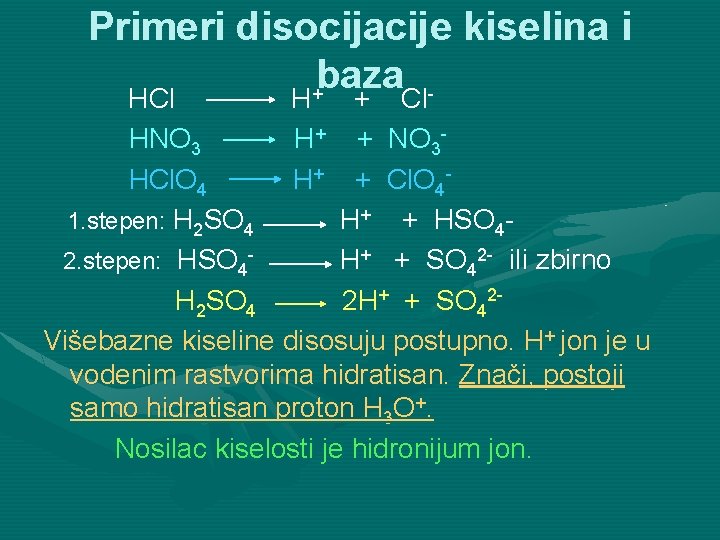
Primeri disocijacije kiselina i baza + HCl H + Cl. HNO 3 H+ + NO 3 HCl. O 4 H+ + Cl. O 41. stepen: H 2 SO 4 H+ + HSO 42. stepen: HSO 4 H+ + SO 42 - ili zbirno H 2 SO 4 2 H+ + SO 42 Višebazne kiseline disosuju postupno. H+ jon je u vodenim rastvorima hidratisan. Znači, postoji samo hidratisan proton H 3 O+. Nosilac kiselosti je hidronijum jon.
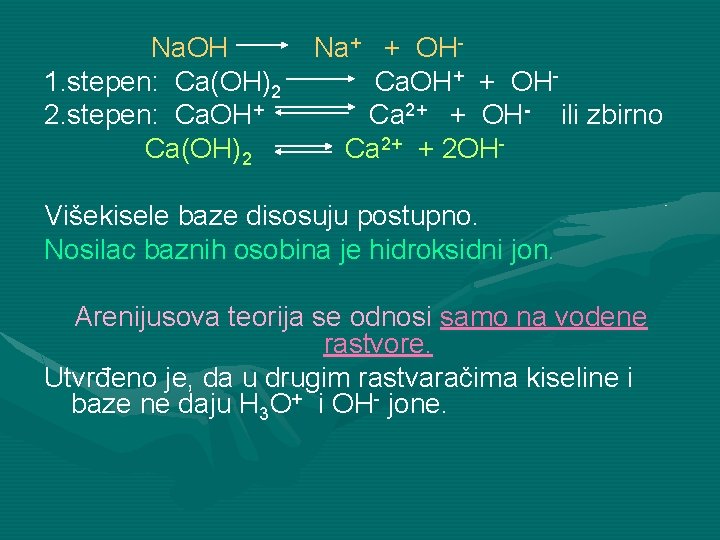
Na. OH 1. stepen: Ca(OH)2 2. stepen: Ca. OH+ Ca(OH)2 Na+ + OHCa. OH+ + OHCa 2+ + OH- ili zbirno Ca 2+ + 2 OH- Višekisele baze disosuju postupno. Nosilac baznih osobina je hidroksidni jon. Arenijusova teorija se odnosi samo na vodene rastvore. Utvrđeno je, da u drugim rastvaračima kiseline i baze ne daju H 3 O+ i OH- jone.

Protolitička teorija kiselina i baza KISELINE su supstance koje mogu da daju proton ( proton donori ), a BAZE su supstance koje mogu da prime protone ( proton akceptori ). Brenšted i Lori 1923. god. KISELINA i obrnuto: BAZA + H+ KISELINA
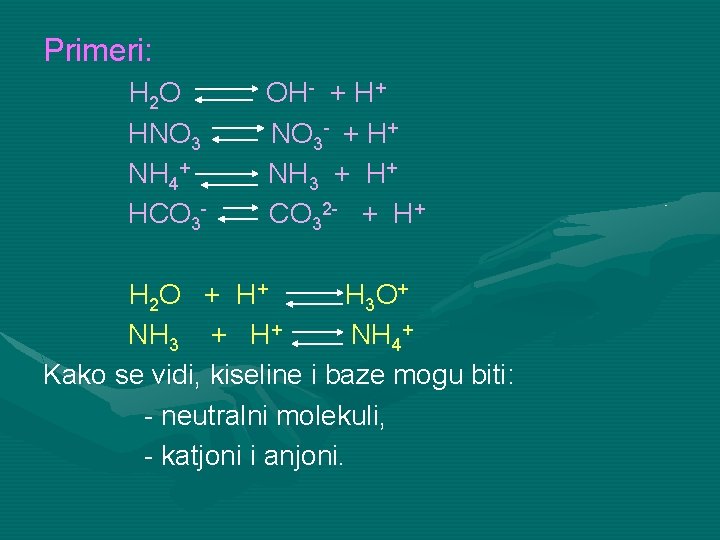
Primeri: H 2 O HNO 3 NH 4+ HCO 3 - OH- + H+ NO 3 - + H+ NH 3 + H+ CO 32 - + H+ H 2 O + H 3 O + NH 3 + H+ NH 4+ Kako se vidi, kiseline i baze mogu biti: - neutralni molekuli, - katjoni i anjoni.
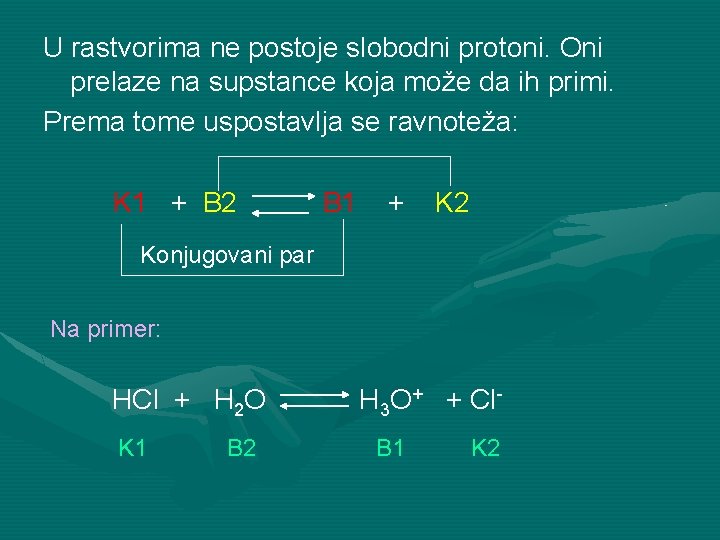
U rastvorima ne postoje slobodni protoni. Oni prelaze na supstance koja može da ih primi. Prema tome uspostavlja se ravnoteža: K 1 + B 2 B 1 + K 2 Konjugovani par Na primer: HCl + H 2 O K 1 B 2 H 3 O+ + Cl. B 1 K 2
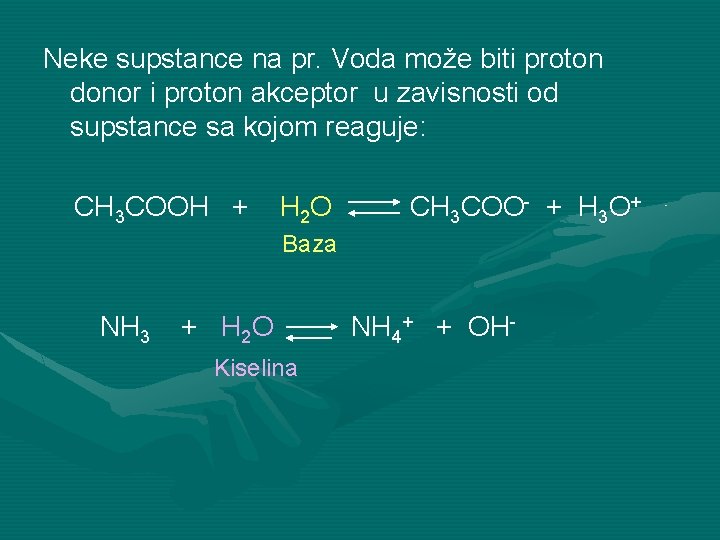
Neke supstance na pr. Voda može biti proton donor i proton akceptor u zavisnosti od supstance sa kojom reaguje: CH 3 COOH + H 2 O CH 3 COO- + H 3 O+ Baza NH 3 + H 2 O Kiselina NH 4+ + OH-

Jačina kiselina i baza • Zavisi od rastvarača U vodenim rastvorima jake kiseline su potpuno disosovane, daju H 3 O+ jone i probližno su iste jačine. Zato je najjača kiselina u vodenom rastvoru H 3 O+ jon. Konjugovane baze jakih kiselina su najslabije baze u vodenim rastvorima. Najjača baza u vodenom rastvoru je OH- jon, jer je voda njegova konjugovana kiselina, najslabija kiselina.

Amfoterni elektroliti ( amfoliti ) Hidroksidi metala slabo rastvorljivi u vodi, pokazuju osobine i kiselina i baza: • U reakciji sa bazama ponašaju se kao kiseline. • U reakciji sa kiselinama ponašaju se kao baze. Na primer: Zn(OH)2(s) + 2 HCl Zn. Cl 2 + 2 H 2 O Baza Zn(OH)2(s) + 2 Na. OH Kiselina Na 2[Zn(OH)4] Natrijum-tetrahidroksocinkat (II)

Amfoterni elektroliti su još i : Pb(OH)2 Sn(OH)2 Al(OH)3 Cr(OH)3 As(OH)3 Sb(OH)3 Sn(OH)4 i drugi.

Slabi elektroliti. Konstanta disocijacije Disocija slabih elektrolita u vodenim rastvorima je povratan proces na koji se može primeniti zakon o dejstvu masa: Slaba kiselina disosuje: HA H + + A- Konstanta disocijacije kiseline
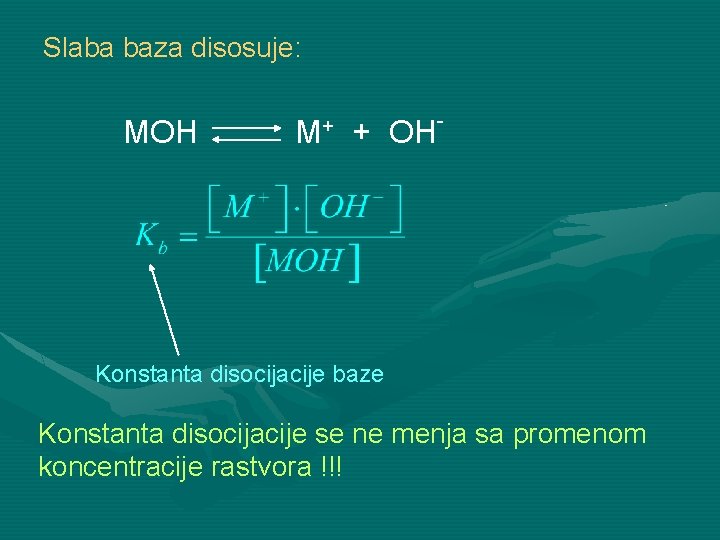
Slaba baza disosuje: MOH M+ + OH- Konstanta disocijacije baze Konstanta disocijacije se ne menja sa promenom koncentracije rastvora !!!

Konstanta disocijacije je merilo jačine slabih elektrolita. Ona zavisi: - od prirode elektrolita; - temperature rastvora. U odnosu na veličinu konstante disocijacije kiseline se dele na: • Vrlo slabe K ≤ 10 -7 mol/dm 3 • Slabe K ≤ 10 -2 mol/dm 3 • Jake K ≤ 1000 mol/dm 3 • Vrlo jake K > 1000 mol/dm 3.

Veza između konstante disocijacije i stepena disocijacije je: analitička koncentracija Gornji izraz je poznat kao OSTVALDOV zakon razblaženja. Kod veoma slabih elektrolita α teži nuli, zato se izraz pojednostavljuje:
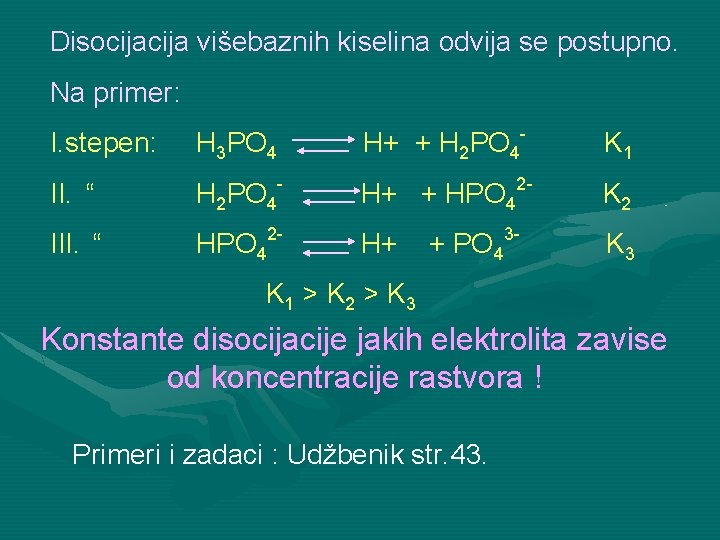
Disocija višebaznih kiselina odvija se postupno. Na primer: - I. stepen: H 3 PO 4 H+ + H 2 PO 4 II. “ H 2 PO 4 - H+ + HPO 42 - III. “ HPO 42 - H+ + PO 43 - K 1 K 2 K 3 K 1 > K 2 > K 3 Konstante disocijacije jakih elektrolita zavise od koncentracije rastvora ! Primeri i zadaci : Udžbenik str. 43.

Izračunavanje koncentracije H+ i OH- jona u rastvorima slabih kiselina i baza 1. Kiselina: 2. Baza:

Suzbijanje disocijacije slabih elektrolita Uticaj zajedničkog jona Ako se rastvoru slabog elektrolita doda jak elektrolit s kojim on ima zajednički jon, doći će do suzbijanja disocijacije slabog elektrolita. Kod kiselina: Rastvoru CH 3 COOH dodajemo so CH 3 COONa U rastvoru su prisutni sledeći joni: CH 3 COOH H+ + CH 3 COO - CH 3 COONa Na+ + CH 3 COO - i

Pošto u rastvoru ima višak CH 3 COO – jona, po Le Šateljeovom principu mora se odvijati ona reakcija kojom se smanjuje koncentracija CH 3 COO – jona. – Prema tome CH 3 COO joni će reagovati sa H+ jonima dajući CH 3 COOH i pri tome dolazi do smanjenja koncentracije H+ jona. Kod baza: Slaboj bazi NH 4 OH dodajemo so NH 4 Cl. Rastvor će sadržati NH 4+ jone u višku jer i baza i + + so disocijacijom daju NH 4 jone. Zato NH 4 joni stupaju u reakciju sa OH – jonima dajući NH 4 OH.

Koncentracija H+ i OH – jona izračunava se prema sledećim izrazima: Primeri iz udžbenika str. 49, 50.
- Slides: 20