Kinetika chemickch reakc VY32 INOVACECHE113 AUTOR Ing Ladislava



















- Slides: 22

Kinetika chemických reakcí VY-32 -INOVACE-CHE-113 AUTOR: Ing. Ladislava Semerádová ANOTACE: Výukový materiál je určen pro studenty 1. ročníku SŠ. Může být použit při výkladu chemické rovnováhy KLÍČOVÁ SLOVA:

Chemická rovnováha

• V chemii dlouho panoval názor, že každá chemická reakce probíhá až do úplné přeměny reaktantů v produkty • Výsledky experimentů prokázaly, že u většiny chemických reakcí jsou v reakční směsi přítomny jak částice reaktantů, tak i produktů • Je takový stav soustavy v němž se nemění její složení, i když v ní neustále probíhají chemické děje

• Z tohoto pohledu dělíme reakce: • Nevratné – probíhají do úplné přeměny reaktantů • zvratné- po skončení děje jsou přítomny reaktanty i produkty • Většina dějů je zvratných !

Zvratné reakce • • U těchto reakcí probíhají současně dvě reakce Přímá – vznikají produkty Zpětná – část produktů se rozkládá Po určité době se za daných podmínek ( teplota a tlak) koncentrace látek dále nemění a nastane tzv. rovnovážný stav • Jedná se o dynamický proces – tzn. Látky stále vnikají a rozkládají se , ale konečné množství je konstantní

Zápis zvratných reakcí • Tyto reakce, při kterých probáhájí jak přímé tak zpětné reakce zapisujeme jedinou reakcí s protisměrnými šipkami V 1 • H 2 + I 2 v 2 HI 2 V 1 = k 1. c (H 2). c(I 2) V 2 = k 2. c (HI) 2 přímá rekce zpětná reakce

• Rychlost přímé rekce je největší na počátku a v průběhu času se snižuje • Rychlost zpětné je naopak na počátku nejmenší a v průběhu reakce se zvětšuje • Po určité době se rychlost přímé i zpětné reakce vyrovnají a nastane dynamická rovnováha, kdy platí: v 1=v 2

Rovnovážná konstanta • Uvažujme obecnou zvratnou reakci • a. A + b. B c. C + d. D • Přímá reakce v 1 = k 1[A]a. [B]b

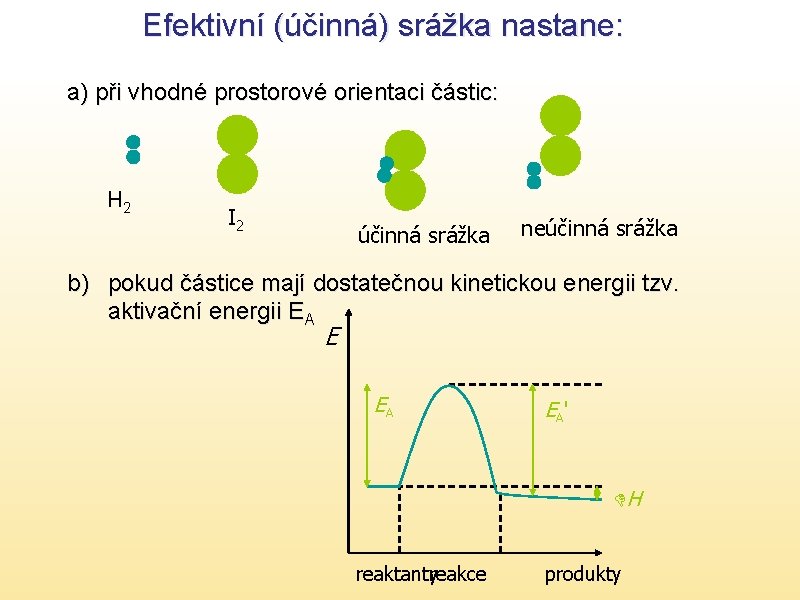
Efektivní (účinná) srážka nastane: a) při vhodné prostorové orientaci částic: H 2 I 2 účinná srážka neúčinná srážka b) pokud částice mají dostatečnou kinetickou energii tzv. aktivační energii EA EA' DH reaktanty reakce produkty

Aktivační energie EA • představuje určitou energetickou bariéru, kterou je třeba překonat, aby došlo k chemické reakci • jde o energii potřebnou k zániku stávajících vazeb a vytvoření vazeb nových • na grafu je vidět počáteční energie výchozí látky, je vidět energetický val, který musí látka překonat

Reakční teplo Qr • Rozdíl mezi energii reaktantů a energii produktů se nazývá reakční teplo Qr • Podle velkosti Qr dělíme reakce na exotermní a endotermní

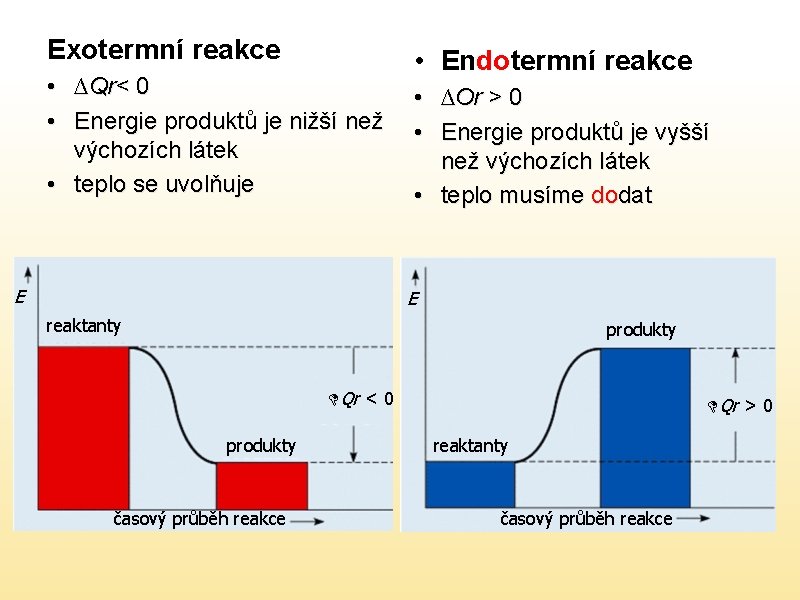
Exotermní reakce • ∆Qr< 0 • Energie produktů je nižší než výchozích látek • teplo se uvolňuje E • Endotermní reakce • ∆Or > 0 • Energie produktů je vyšší než výchozích látek • teplo musíme dodat E reaktanty produkty DQr < 0 produkty časový průběh reakce DQr > 0 reaktanty časový průběh reakce

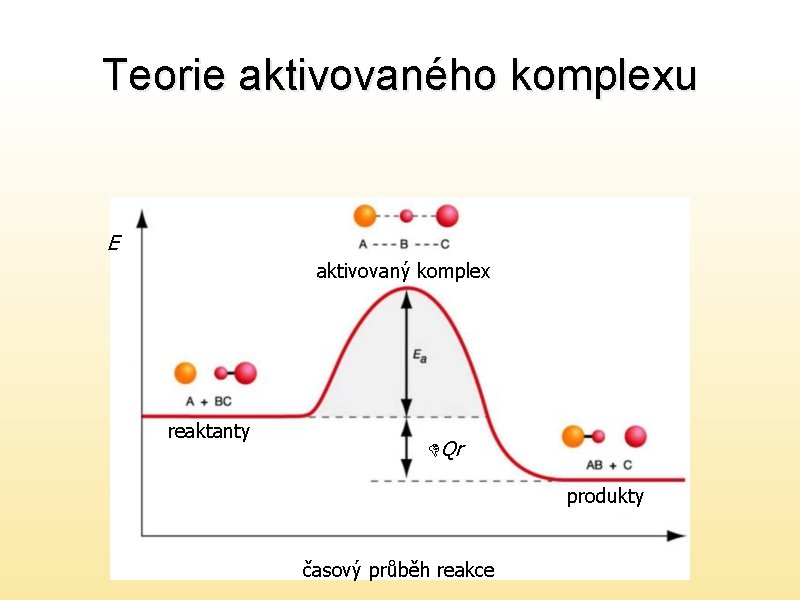
Teorie aktivovaného komplexu E aktivovaný komplex reaktanty DQr produkty časový průběh reakce

Reakční rychlost • definujeme jako přírůstek látkového množství produktu nebo reaktantu za jednotku času • Kinetická rovnice v = k [A]a [B]b • k • a, b • [A], [B] rychlostní konstanta stechiometrické koeficienty koncentrace reaktantů

Faktory ovlivňující reakční rychlost: a) koncentrace b) teplota c) katalyzátory d) velikost styčné plochy

a) vliv koncentrace • čím větší jsou látkové koncentrace reaktantů, tím větší je pravděpodobnost počtu srážek těchto částic, a tím větší je i rychlost reakce v = k [A]a [B]b • rychlost reakce je přímo úměrná součinu reaktantů umocněných na stechiometrické koeficienty

b) vliv teploty • zvýšením teploty vrůstá kinetická energie, vzrůstá rychlost pohybu i pravděpodobnost vzájemných srážek • zvyšováním teploty vždy vrůstá rychlost chemické reakce • Empirické pravidlo: • zvýšením teploty o 10 o. C se rychlost většiny reakcí zvýší 2 x až 4 x

c) vliv katalyzátorů • bez katalyzátoru s katalyzátorem

Katalyzátory látky, které ovlivňují rychlost chemické reakce tím, že : • mění mechanismus reakce – dvoustupňový proces • ovlivňuji velikost aktivační energie • umožňují, aby reakce proběhla

Inhibitory • látky, které jsou opakem katalyzátoru • reakce znesnadňují, zpomalují popřípadě potlačují • např. látky přidávající se do plastických hmot jako retardéry hoření

d) velikost styčné plochy • zvýšením povrchu reaktantů vzrůstá rychlost chemické reakce • např. granulovaný zinek reaguje s kyselinou dusičnou pomaleji než práškový zinek • rychlost také vzrůstá se zvyšujícím se rozptýlením částic reaktantů • rychle probíhají reakce plynných látek, neboť jsou roztýleny až na molekuly nebo atomy ( atomy vzácných plynů)

POUŽITÉ ZDROJE: DUŠEK, Bohuslav a Vratislav FLEMR. Obecná a anorganická chemie pro gymnázia. SPN, 2007. ISBN 80 -7235 -369 -1. Klouda P. Obecná a anorganická chemie. Ostrava: Pavel Klouda, Ostrava, 2004. ISBN 80 -8636910 -2. www. glassschool. cz