Kimyasal reaksiyon Bir veya birden fazla madde nin
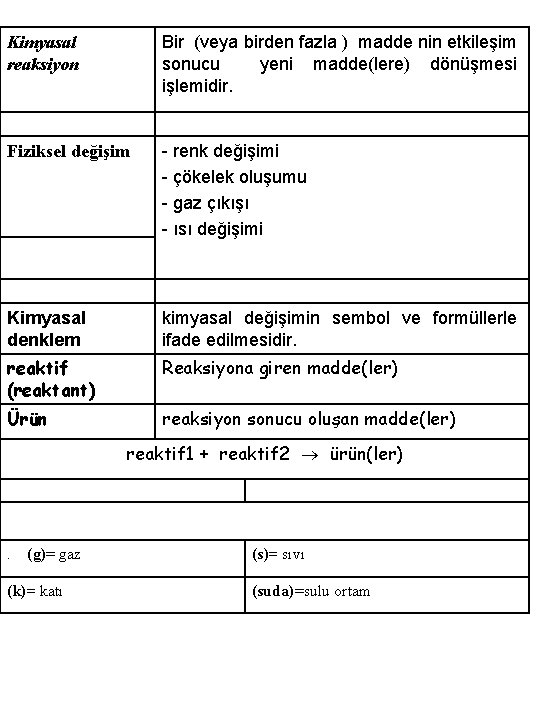
Kimyasal reaksiyon Bir (veya birden fazla ) madde nin etkileşim sonucu yeni madde(lere) dönüşmesi işlemidir. Fiziksel değişim - renk değişimi - çökelek oluşumu - gaz çıkışı - ısı değişimi Kimyasal denklem kimyasal değişimin sembol ve formüllerle ifade edilmesidir. reaktif (reaktant) Reaksiyona giren madde(ler) Ürün reaksiyon sonucu oluşan madde(ler) reaktif 1 + reaktif 2 ürün(ler) . (g)= gaz (s)= sıvı (k)= katı (suda)=sulu ortam

Kimyasal Denklemlerin Denkleştirilmesi Denklem denkleştirme reaktif ve ürünlerin başına uygun katsayılar ekleyerek reaksiyona, giren ve çıkan atomların sayısını eşitlemektir. (eşitliğin her iki tarafındaki atomların sayısı eşit olmalıdır) CH 4 + O 2 Reaktifle r Ürünler 1 C 1 C 4 H 2 H 2 O 3 O CO 2 + H 2 O Denkleştirilmiş reaksiyon CH 4 + 2 O 2 CO 2 + 2 H 2 O.
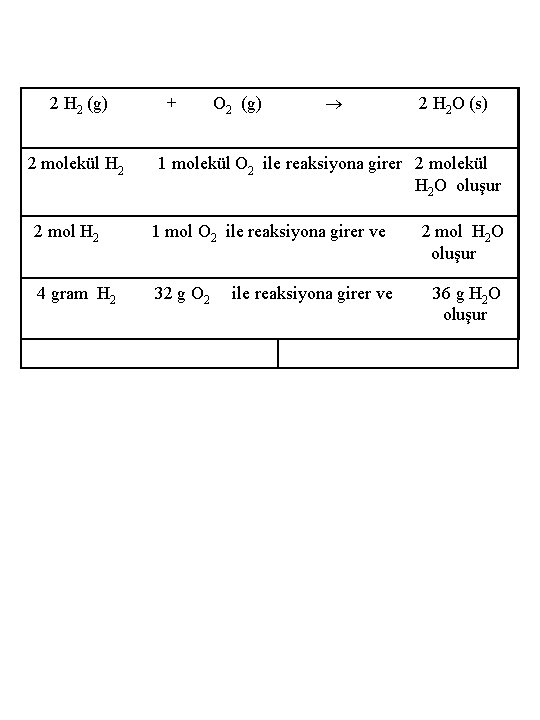
2 H 2 (g) 2 molekül H 2 + O 2 (g) 2 H 2 O (s) 1 molekül O 2 ile reaksiyona girer 2 molekül H 2 O oluşur 2 mol H 2 1 mol O 2 ile reaksiyona girer ve 4 gram H 2 32 g O 2 ile reaksiyona girer ve 2 mol H 2 O oluşur 36 g H 2 O oluşur

soru: 2. 72 mol H 2 a) yeteri kadar O 2 ile b) 1 mol O 2 ile reaksiyona girdiğinde kaç gram H 2 O oluşur?

Aşağıdaki reaksiyonları denkleştiriniz. N 2 H 4 + N 2 O 4 Na. OH + CO 2 Ca. O + P 4 O 10 N 2 + H 2 O Na 2 CO 3 + H 2 O Ca 3(PO 4)2

Sınırlayıcı Reaktif Kimyasal reaksiyonda, reaktifin biri tamamen tükendiğinde reaksiyon tamamlanır. Reaksiyonda tamamen (ilk) tükenen reaktife sınırlayıcı reaktif (bileşen) dir.

Soru. 1. 20 mol Sb ile 2. 40 mol I 2 reaksiyona girdiğinde sınırlayıcı reakti ve oluşan ürün miktarını hesaplayınız. Sb + I 2 Sb. I 3 Sb: 243 I: 127. 0

Soru: 3, 45 gr KBr içeren çözelti ile 7, 28 gr Ag. NO 3 içeren çözelti karıştırıldığında kaç gr Ag. Br oluşur. KBr + Ag. NO 3 Ag. Br + K+ + NO 3 -

Reaksiyon verimi Teorik verim bir reaksiyonda sınırlayıcı reaktif tamamen tükendiğinde oluşması gereken ürün miktarıdır. Gerçek verim: reaksiyon sonunda pratikte elde edilen ürün miktarıdır. Yüzde verim gerçek verimin teorik verime yüzde oranıdır. Yüzde verim = Gerçek verim ----------Teorik verim x %100

Soru Fe + O 2 Fe 2 O 3 : Reaksiyonunda 11. 2 g Fe yeteri kadar oksijenle reaksiyona girdiğinde 10. 0 g Fe 2 O 3 oluşuyor. Reaksiyonun teorik verimi, gerçek verimi ve yüzde verimini hesaplayınız. Fe : 56 O: 16

Soru: Na 3 PO 4 (aq) + Ba(NO 3)2(aq) Ba 3(PO 4)2(k) + Na. NO 3 (aq) Reaksiyonunda 3. 50 Na 3 PO 4 ile 6. 40 gram Ba(NO 3)2 reaksiyona girdiğinde kaç gram Ba 3(PO 4)2 oluşur? Hangi reaktif sınırlayıcı bileşendir?
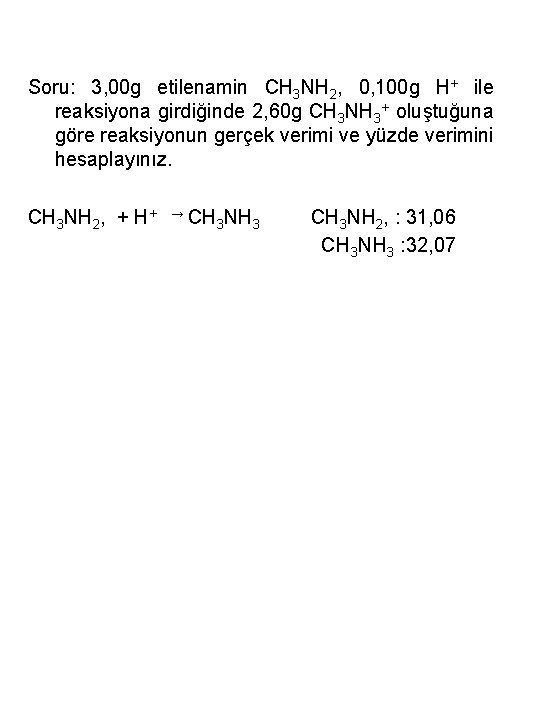
Soru: 3, 00 g etilenamin CH 3 NH 2, 0, 100 g H+ ile reaksiyona girdiğinde 2, 60 g CH 3 NH 3+ oluştuğuna göre reaksiyonun gerçek verimi ve yüzde verimini hesaplayınız. CH 3 NH 2, + H+ → CH 3 NH 3 CH 3 NH 2, : 31, 06 CH 3 NH 3 : 32, 07
Sulu Çözeltilerde reaksiyonlar Çökelme R. Asit Baz R. İndirgenme Yükseltgenme R.
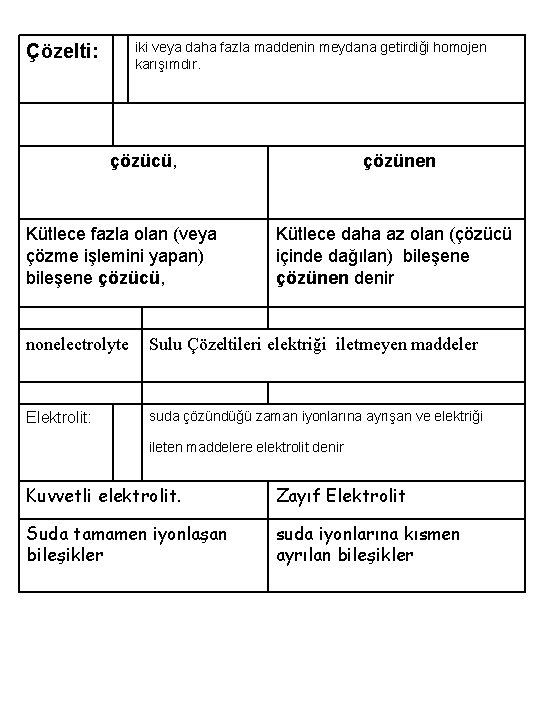
iki veya daha fazla maddenin meydana getirdiği homojen karışımdır. Çözelti: çözücü, Kütlece fazla olan (veya çözme işlemini yapan) bileşene çözücü, çözünen Kütlece daha az olan (çözücü içinde dağılan) bileşene çözünen denir nonelectrolyte Sulu Çözeltileri elektriği iletmeyen maddeler Elektrolit: suda çözündüğü zaman iyonlarına ayrışan ve elektriği ileten maddelere elektrolit denir Kuvvetli elektrolit. Zayıf Elektrolit Suda tamamen iyonlaşan bileşikler suda iyonlarına kısmen ayrılan bileşikler

Mol sayısı m n = ----MA Molarite n M= ------V mol/L m d = -----V gr/m. L Yoğunluk

Çözeltilerin seyreltilmesi Milk x Vilk = mol sayısı = Mson x Vson Milk x Vilk = Mson x Vson

Soru: 23. 4 g Na 2 SO 4 ün suda çözülüp 250. 0 ml ye seyreltilmesiyle oluşan çözeltinin molaritesini hesaplayınız? Na 2 SO 4: 142 Soru: 500 ml 0. 10 M H 2 SO 4 çözeltisi 3. 0 M H 2 SO 4 çözeltisinden nasıl hazırlanır?

Soru: 500 ml 0. 10 M H 2 SO 4 çözeltisi 3. 0 M H 2 SO 4 çözeltisinden nasıl hazırlanır?

Sulu Çözeltilerde reaksiyonlar Çökelme reaksiyonları Bir reaksiyon sonucu katı fazda bir ürün oluşuyorsa bu reaksiyona çökelme (çökme) reaksiyonu denir. Katı fazdaki ürün çökelek olarak adlandırılır. Ag+(aq) + Cl-(aq) → Ag. Cl(s)

Çözünürlük Kuralları çözünen 1 A grup bileşikleri (Na, K, Li, ) ve NH 4+ bileşikleri suda tamamen çözünür. NO 3 (Nitrat), CHCOO- (asetat) , Cl. O 4 (perklorat)bileşikleri suda tamamen çözünür. Cl- Bileşikleri (Ag. Cl, Hg 2 Cl 2, Pb. Cl 2) hariç suda çözünür SO 42+ (Sr SO 4, Ca SO 4 , Ba SO 4 , Pb SO 4 hariç) suda çözünür. Cl-, Br-, I- SO 42 Li+, Na+, K+, Rb+, Cs+ NH 4+ NO 3 CH 3 CO 2 - Cl. O 4 -
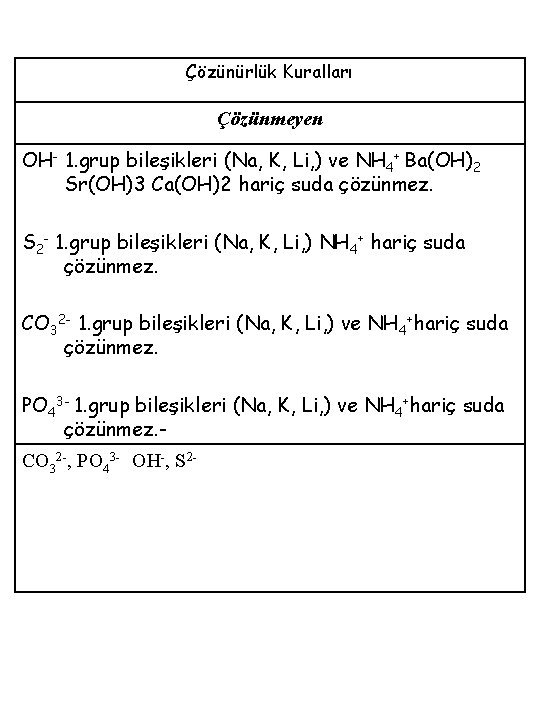
Çözünürlük Kuralları Çözünmeyen OH- 1. grup bileşikleri (Na, K, Li, ) ve NH 4+ Ba(OH)2 Sr(OH)3 Ca(OH)2 hariç suda çözünmez. S 2 - 1. grup bileşikleri (Na, K, Li, ) NH 4+ hariç suda çözünmez. CO 32 - 1. grup bileşikleri (Na, K, Li, ) ve NH 4+hariç suda çözünmez. PO 43 - 1. grup bileşikleri (Na, K, Li, ) ve NH 4+hariç suda çözünmez. CO 32 -, PO 43 - OH-, S 2 -

Soru: aşağıdaki şıklarda meydana gelecek reaksiyonları açıklayınız • Na 2 CO 3 ve Ca. Cl 2 bileşikleri suda çözülüp karıştırıldığında • Cu. SO 4 ve Na. NO 3 bileşikleri suda çözülüp karıştırıldığında

Asit ve Bazlar Asit Baz Ekşi tatları vardır Acı tatları vardır Metalleri ve Karbonat Kayganlık hissi verirler tuzlarını çözerler Metal iyonları ile Çökelti Turnusol kağıdını verirler kırmızıya çevirirler Turnusol kağıdıı maviye çevirirler.

Asit ve Bazlar Asit- Baz Tanımları Arrhenius Asit-Baz Tanımı (1884) Hidrojen içeren ve Suda çözüldüğünde H+ oluşturan maddelere Asit denir. iyonu HCl(aq) H+(aq) + Cl-(aq) OH iyonu içeren ve suda çözüldüğünde OH – iyonu oluşturan maddelere Baz denir. Na. OH (aq) Na+ (aq) + OH -(aq)

Asit ve Bazlar Asit- Baz Tanımları Brønsted-Lowry Asit-Baz Tanımı (1923) H+ iyonu verme eğiliminde olan maddelere asit denir. . HCl + H 2 O Cl– + H 3 O+ H+ iyonu alma eğiliminde olan maddelere baz denir. . NH 3 + H 2 O NH 4+ + OH-

Asit ve Bazlar Lewis asit-baz Tanımı : Baz elektron çifti veren tür, Asit ise elektron çifti alan maddedir B + H+ B - H+ Nötralleşme. Bir asit ile bazın reaksiyona girerek birbirlerinin asit ve bazlığını nötürleştirmesidir. Reaksiyon sonucunda su ve tuz adı verilen iyonik bileşik oluşur HCl + Na. OH H 2 O + Na. Cl
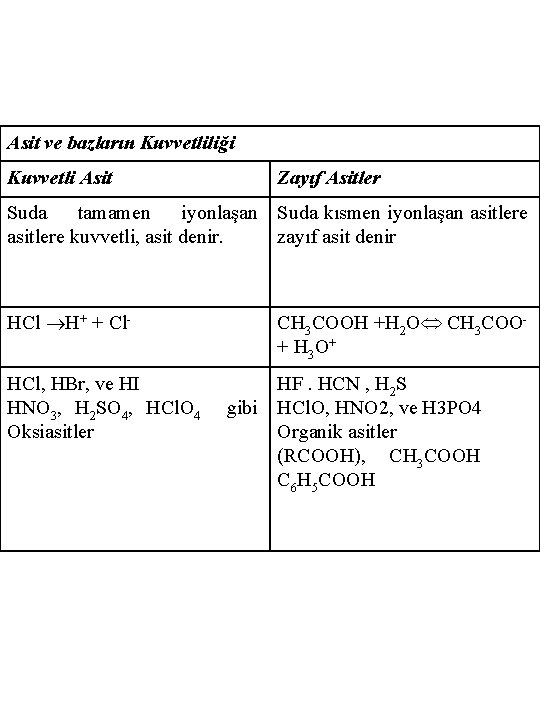
Asit ve bazların Kuvvetliliği Kuvvetli Asit Zayıf Asitler Suda tamamen iyonlaşan Suda kısmen iyonlaşan asitlere kuvvetli, asit denir. zayıf asit denir HCl H+ + Cl. HCl, HBr, ve HI HNO 3, H 2 SO 4, HCl. O 4 Oksiasitler CH 3 COOH +H 2 O CH 3 COO+ H 3 O+ HF. HCN , H 2 S gibi HCl. O, HNO 2, ve H 3 PO 4 Organik asitler (RCOOH), CH 3 COOH C 6 H 5 COOH
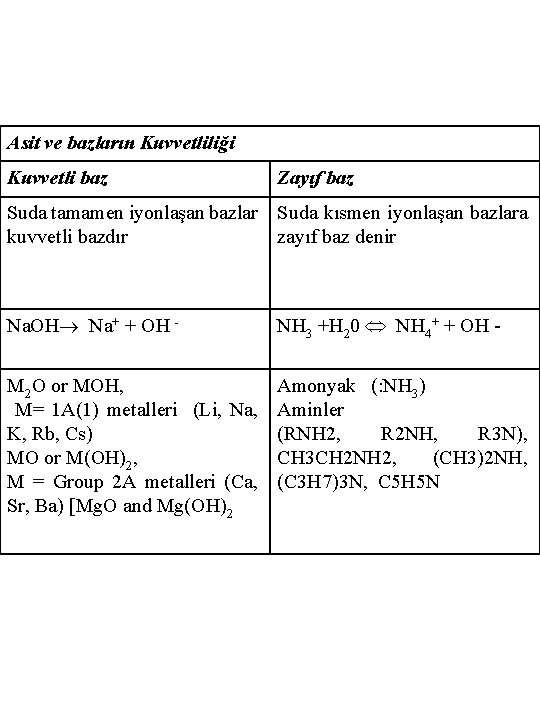
Asit ve bazların Kuvvetliliği Kuvvetli baz Zayıf baz Suda tamamen iyonlaşan bazlar Suda kısmen iyonlaşan bazlara kuvvetli bazdır zayıf baz denir Na. OH Na+ + OH - NH 3 +H 20 NH 4+ + OH - M 2 O or MOH, M= 1 A(1) metalleri (Li, Na, K, Rb, Cs) MO or M(OH)2, M = Group 2 A metalleri (Ca, Sr, Ba) [Mg. O and Mg(OH)2 Amonyak (: NH 3) Aminler (RNH 2, R 2 NH, R 3 N), CH 3 CH 2 NH 2, (CH 3)2 NH, (C 3 H 7)3 N, C 5 H 5 N

• p. H hidronyum iyonu konsantrasyonunun 10 tabanına göre eksi logaritması olarak tarif edilir. p. H = - log[H 3 O+] p. OH hidroksil iyonu konsantrasyonunun 10 tabanına göre eksi logaritması olarak tarif edilir. p. OH = - log[OH-] • p. H = 7. 00 nötr çözelti • p. H < 7. 00 asidik çözelti • p. H > 7. 00 bazik çözelti

İndirgenme Yükseltgenme Reaksiyonları Reaksiyonda iki tür arasında elektron alış verişi oluyorsa bu tür reaksiyonlara indirgenme yükseltgenme reaksiyonları denir. . Elektron alan tür indirgenir elektron veren tür yükseltgenir. Elektron alış verişini göstermek için reaksiyon yarı tepkimelere ayrılır. D Fe 2 O 3(k) + 3 CO(g) → 2 Fe(k) + 3 CO 2(g) Fe 3+ --- metallik demire indirgenir CO(g)---- Karbon dioksite yükseltgenir • Bir tür Yükseltgenirken aynı anda diğer bir tür indirgenir.

Fe 3+ + Cu+ → Fe 2+ + Cu 2+ Fe 3+ + e- → Fe 2+ Cu+ → Cu 2+ + e • İndirgen elektron vericisidir. ( kendi yükseltgenirken diğer türün yükseltgenmesine neden olur. • Yükseltgen elektron alıcısıdır. (kendi indirgenirken diğer türün yükseltgenmesini sağlar)

Yükseltgenme basamakları İyon haline geçmemiş veya herhangi bir bileşik içinde yer almayan Elementlerin değerliği sıfırdır. Bir bileşiğin atomlarının değerliklerinin toplamı sıfırdır. İyonik bir bileşiğin atomlarının değerlikleri toplamı iyonik bileşiğin değerliğine eşittir. 1 A grubu (Li, Na, K, Rb, Cs, Fr) metalleri +1 değerliğine sahptir. 2 A grubu metalleri ise +2. Hidrogenin değerliği genelde +1 dir ancak Na. H Be. H 2 de -1 olur. Flor – 1 değerliğini alır. Halojenler genelde -1 değerliğini (H ve metallerle bileşik yaptıklarında) alırlar Oksijen genelde – 2 değerliğini alır.

Redoks reaksiyonlarını denkleştirme 1 - reaksiyon 2 yarı reaksiyona bölünür 2 - her bir yarı reaksiyon ayrı denkleştirilir - önce indirgenen ve yükseltgenen atom lar denkleştirilir. - Yükseltgenme veya indirgenmeyi göstermek için elektron eklenir - Yükleri denkleştirmek için asidik ortamda H+ eklenip diğer taraftan su eklenir bazik ortamda OH- eklenip diğer tarafa su eklenir kütle ve yük lerin denk olup olmadığı kontrol edilir. 3 - yarı reaksiyonlar birleştirilir. Alınan verilen elektron sayısı eşit olacak şekilde toplanır.

• Soru: Fe 2+ + Mn. O 4 - → denkleştiriniz • Soru: Cl 2 + Cr(OH)3 → Cl- + Cr. O 42 - bazik ortamda denkleştiriniz • Soru: C 2 H 5 OH + Ce 4+ → CO 2 + Ce 3+ asidik ortamda denkleştiriniz Fe 3+ + Mn 2+ asidik ortamda

Titrasyon • Titrasyon – Bir çözeltinin diğer bir çözeltiye azar kontrollü olarak eklenmesidir. • Eşdeğer nokta – Her iki reaktifin tam olarak reaksiyona girdiği tükendiği an. • Indikatör – Eşdeğerlik noktası civarında reaksiyonun bir özelliğine bağlı olarak renk değiştiren madde
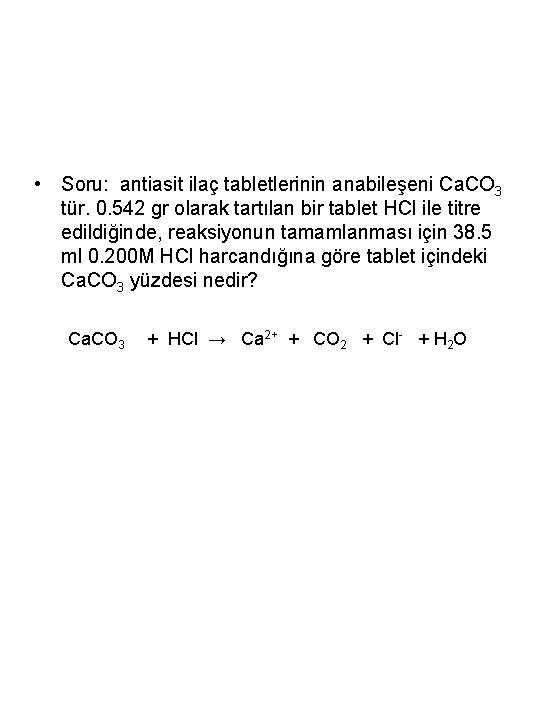
• Soru: antiasit ilaç tabletlerinin anabileşeni Ca. CO 3 tür. 0. 542 gr olarak tartılan bir tablet HCl ile titre edildiğinde, reaksiyonun tamamlanması için 38. 5 ml 0. 200 M HCl harcandığına göre tablet içindeki Ca. CO 3 yüzdesi nedir? Ca. CO 3 + HCl → Ca 2+ + CO 2 + Cl- + H 2 O

• Konsantrasyou bilinmeyen bir permanganat çözeltisinin 28, 97 ml si 0, 1058 g okzalik asit ile tamamen reaksiyona girdiğine göre permanganat çözeltisinin konsantrasyonunu hesaplayınız. • Mn. O 4 - + H 2 C 2 O 4 → Mn 2+ + CO 2 2 Mn. O 4 - + 5 H 2 C 2 O 4 6 H+→ 2 Mn 2+ + 10 CO 2 + 8 H 2 O
- Slides: 37