Kimia Karbon Disampaikan oleh Dra Hartati Soetjipto M
Kimia Karbon Disampaikan oleh : Dra Hartati Soetjipto, M Sc dalam rangka : Pelatihan Pengembangan Pembelajaran bagi Guru-guru Yayasan Del , Medan.

Pengantar. C salah satu unsur penting pd makluk hidup. C merupakan kerangka utama suatu molekul organik. Contoh : C 6 H 12 O 6 – gula C memiliki 6 elektron yg tersebar di kulit pertama 2 elektron dan di kulit ke 2 4 el, yg sebenarnya kulit ke 2 mampu menampung 8 el. C memiliki 4 el valensi. Jadi C mampu menerima atau menyumbangkan 4 el lagi supaya menjadi 8 el atau menjadi ion. C mampu berikatan dengan sesama C maupun atom lain spt H, O, N dll.
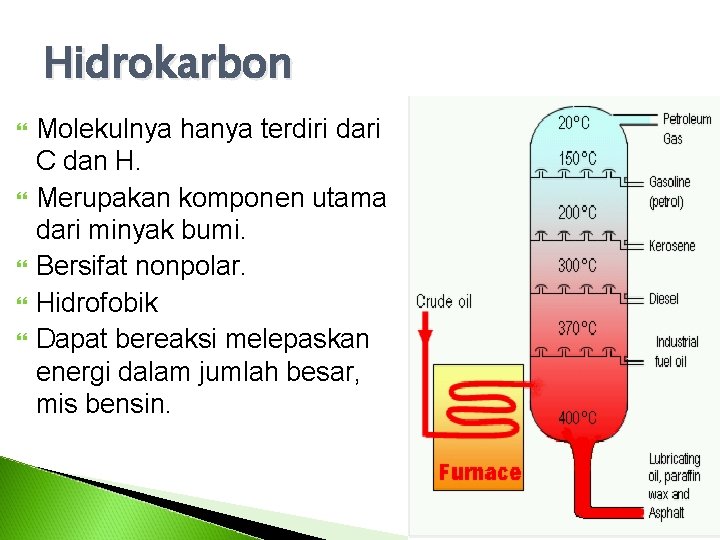
Hidrokarbon Molekulnya hanya terdiri dari C dan H. Merupakan komponen utama dari minyak bumi. Bersifat nonpolar. Hidrofobik Dapat bereaksi melepaskan energi dalam jumlah besar, mis bensin.
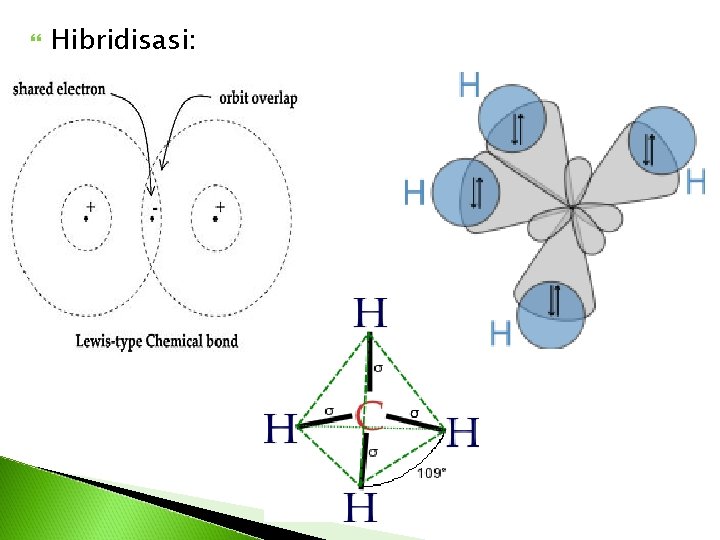
Hibridisasi:
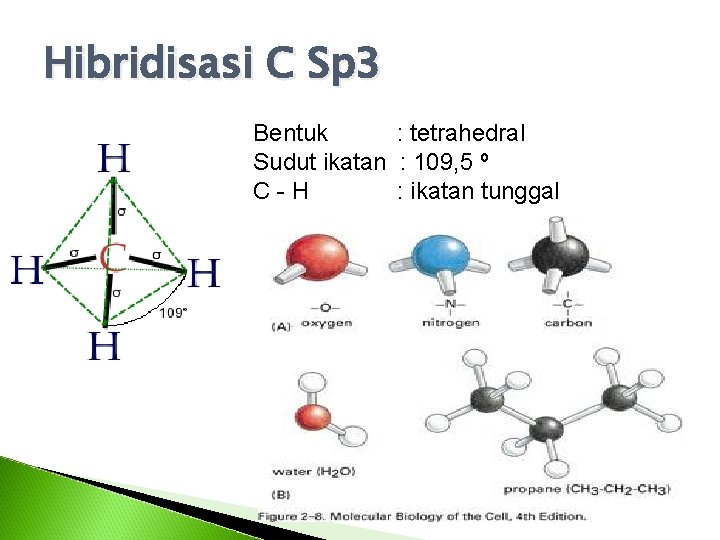
Hibridisasi C Sp 3 Bentuk : tetrahedral Sudut ikatan : 109, 5 º C-H : ikatan tunggal
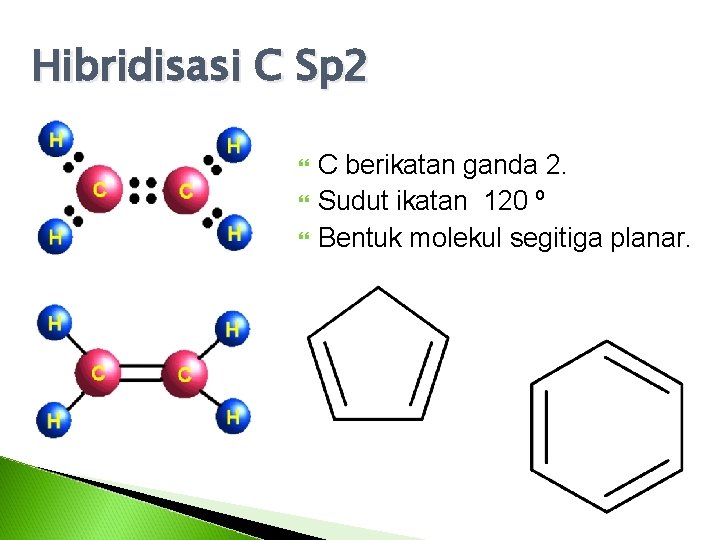
Hibridisasi C Sp 2 C berikatan ganda 2. Sudut ikatan 120 º Bentuk molekul segitiga planar.
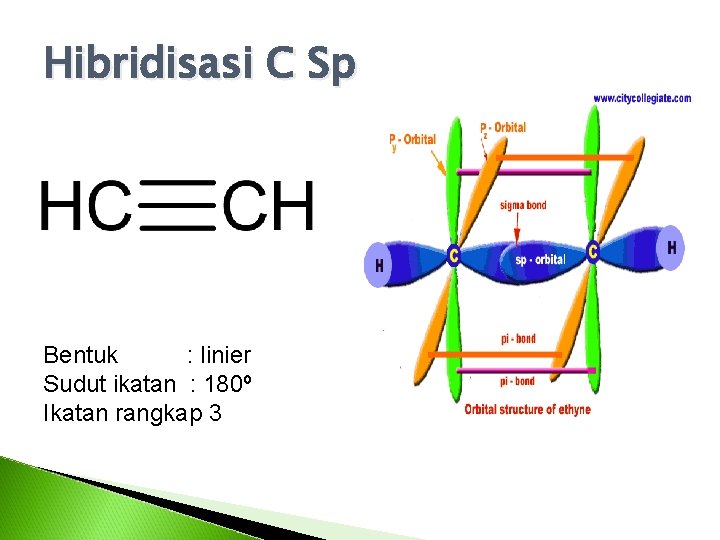
Hibridisasi C Sp Bentuk : linier Sudut ikatan : 180º Ikatan rangkap 3
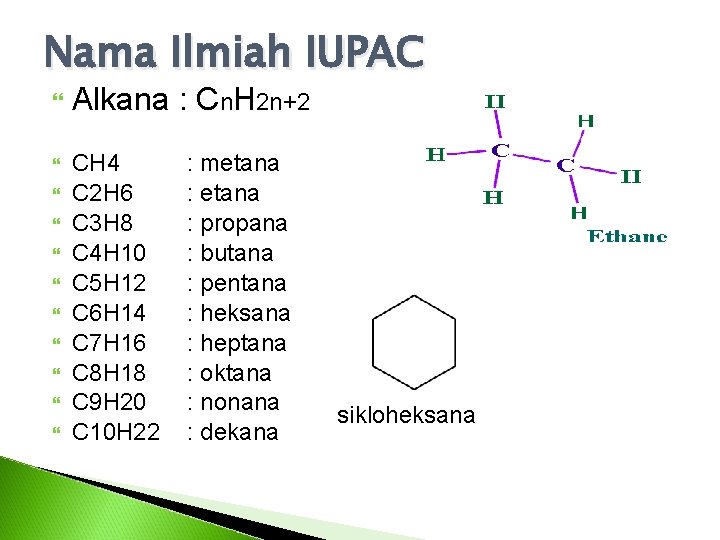
Nama Ilmiah IUPAC Alkana : Cn. H 2 n+2 CH 4 C 2 H 6 C 3 H 8 C 4 H 10 C 5 H 12 C 6 H 14 C 7 H 16 C 8 H 18 C 9 H 20 C 10 H 22 : metana : propana : butana : pentana : heksana : heptana : oktana : nonana : dekana sikloheksana

Isomer Senyawa dengan rumus molekul sama, tetapi memiliki sifat fisik dan kimia berbeda karena letak atom 2 nya berbeda. Rumus umum sama, Rumus bangun berbeda.
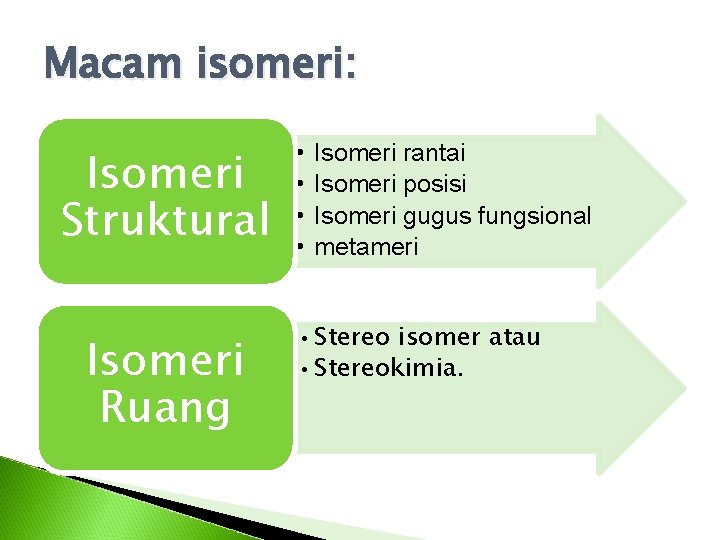
Macam isomeri: Isomeri Struktural Isomeri Ruang • • Isomeri rantai Isomeri posisi Isomeri gugus fungsional metameri • Stereo isomer atau • Stereokimia.

Contoh-contoh Isomer: 1. Isomer rantai : butana dan isobutan 2. Isomer posisi : C 3 H 8 O – propil alkohol dan isopropil alkohol. 3. Isomeri Gugus Fungsi: etanol dan dimetil eter 4. Metameri : isomer yang berbeda gugus alkilnya. Dietileter dan metil propil eter
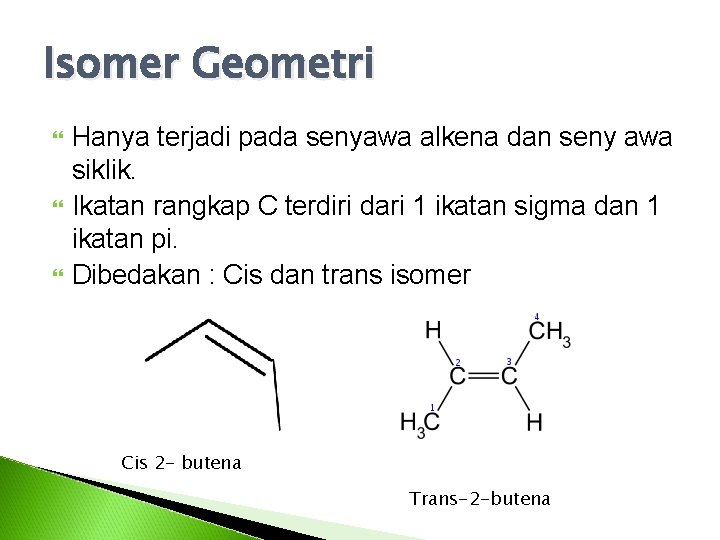
Isomer Geometri Hanya terjadi pada senyawa alkena dan seny awa siklik. Ikatan rangkap C terdiri dari 1 ikatan sigma dan 1 ikatan pi. Dibedakan : Cis dan trans isomer Cis 2 - butena Trans-2 -butena

Isomeri Optik 2 senyawa yang sama tetapi berbeda dalam mempolarisasi cahaya ( searah/+ atau berlawanan /- dengan jarum jam). Memiliki atom C Kiral/asimetri Bersifat aktif optik Memiliki bayangan cermin

Enantiomer ( Bayangan cermin) Sepasang enantiomer memiliki sifat fisik dan kimia yang sama, kecuali dalam hal antaraksi dengan molekul kiral lainnya dan arah pemutaran bidang polarisasi cahaya. Rotasi optik Isomer Optis.

Proyeksi Fischer Emil Fischer dr Jerman pd akhir abad ke 19 menampilkan rumus proyeksi untuk menunjukan penataan ruang untuk /atom gugus disekeliling atom C *. Contoh molekul Gliseraldehide ( 2, 3 -dihidroksi propanal).
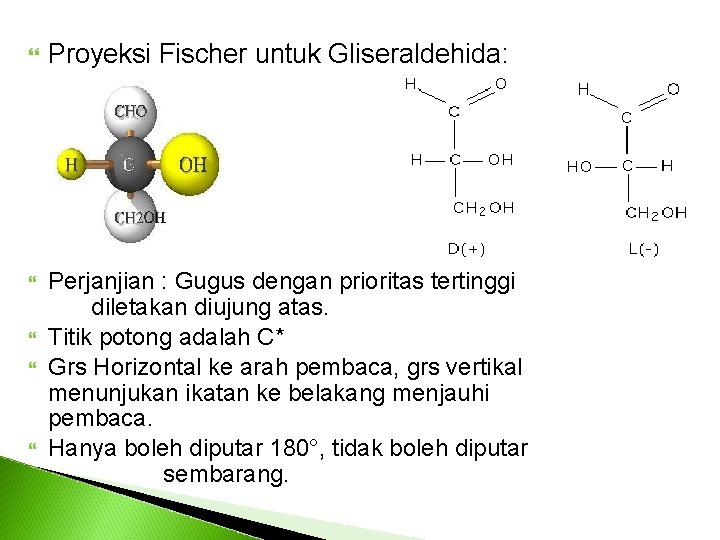
Proyeksi Fischer untuk Gliseraldehida: Perjanjian : Gugus dengan prioritas tertinggi diletakan diujung atas. Titik potong adalah C* Grs Horizontal ke arah pembaca, grs vertikal menunjukan ikatan ke belakang menjauhi pembaca. Hanya boleh diputar 180°, tidak boleh diputar sembarang.

TERIMA KASIH
- Slides: 17