KIMIA ANALITIK Cabang ilmu kimia yang bertugas mengidentifikasi

KIMIA ANALITIK Cabang ilmu kimia yang bertugas mengidentifikasi zat, memisahkannya serta menguraikannya dalam komponen-komponen, menentukan jenis serta jumlahnya.

KIMIA ANALITIK DIBEDAKAN ATAS: 1. KA Kualitatif Analisa yang bertujuan untuk menemukan dan mengidentifikasi jenis unsur, senyawa yang terdapat pada suatu bahan, misalnya: analisa senyawa metabolik sekunder 2. KA Kuantitatif Analisa yang bertujuan untuk menentukan/menetapkan banyaknya suatu unsur atau senyawa yang terdapat dalam suatu sampel dan hasilnya dinyatakan dalam bentuk jumlah atau bilangan, misalnya : analisa volumetri, analisa gravimetri

Langkah-langkah Analisa Kuantitatif: 1. Pengambilan sampel/contoh, yaitu memilih cuplikan dari suatu zat atau bahan yng akan diperiksa (sampel harus mewakili). 2. Mengubah cuplikan menjadi suatu bentuk untuk memungkinkan dilakukan pengukuran, melarutkan, dikeringkan, ataupun ditumbuk. 3. Pengukuran (kimia, fisika, instrumen) 4. Perhitungan dan interpretasi hasil.

VOLUMETRI

Dasar : pengukuran sejumlah reagen yang diketahui konsentrasinya yang dikonsumsi oleh analat/sampel. Ada 3 bentuk analisa titrimetri : Volumetri : didasarkan pengukuran volume larutan yg diketahui konsentrasinya yg diperlukan untuk bereaksi dengan analat. Gravimetri : seperti volumetrik hanya berbeda dalam pengukuran massa reagent disamping volume. Coulometri : didasarkan pengukuran arus listrik.

1. 2. 3. 4. MACAM-MACAM REAKSI VOLUMETRI: Reaksi asam-basa (penetralan): H+Cl- + Na. OH Na+Cl- + H 2 O H+ + OH H 2 O Reaksi oksidasi –reduksi (redoks): Fe 2+ + Ce 4+ Fe 3+ + Ce 3+ 5 C 2 O 42 - + 2 Mn. O 4 - +16 H+ 2 Mn 2+ + 10 CO 2 + 8 H 2 O I 2 + 2 S 2 O 32 2 I- + S 4 O 62 Reaksi pengendapan: Ag+ + Cl Ag. Cl(s) Pb 2+ + Cr. O 42 Pb. Cr. O 4(s) Reaksi pembentukan kompleks: Ag+ + 2 CN Ag(CN)2 Mg 2+ + (EDTA)4 Mg(EDTA)2 -

ISTILAH DALAM TITRIMETRI Larutan Standar / Titrant Standar : larutan yang diketahui konsentrasinya. Ada 2 macam larutan standar primer & standar sekunder. Larutan standar primer: Larutan yang konsentrasinya dapat ditentukan hanya dengan menimbang dan melarutkannya dengan tepat. Larutan standar sekunder: Larutan yang konsentrasinya ditentukan dengan cara titrasi dengan larutan standar primer prosesnya disebut standarisasi / pembakuan

Titrasi : Proses penambahan larutan standart dari buret/ alat lain secara perlahan ke dalam larutan analat sampai terjadi reaksi antara keduanya dengan sempurna. Volume reagent yg diperlukan untuk kesempurnaan titrasi ditentukan dari selisih pembacaan awal dan akhir di buret (volume titrasi). Indikator : Zat yang ditambahkan ke dalam larutan analat untuk mengamati perubahan fisik yang terjadi saat mendekati TE atau TA titrasi

Titik Ekivalent (TE) dalam titrasi: dicapai jika jumlah titrant yang ditambahkan ekivalent secara kimia dengan sejumlah analat dalam sample. Secara teoritis titik ekivalent tidak dapat ditentukan dari percobaan. Titik Akhir (TA) dalam titrasi : kondisi dimana proses titrasi harus dihentikan, karena sudah tercapai kondisi ekivalent antara titrant dan analat. Titik akhir dapat ditentukan dari percobaan karena adanya perubahan sifat fisik larutan dekat TE.

PENENTUAN TITIK AKHIR TITRASI Perhatikan perubahan warna




0. 5 ml 0. 1 ml

Titrasi kembali: jika zat A ditentukan dengan cara penambahan zat B (berlebih), lalu kelebihan B ditentukan dengan titrasi kembali (backtitration) dengan zat C ( standar): A + B (berlebih) hasil reaksi + B sisa + C hasil reaksi Titrasi kembali digunakan jika reaksi A + B hasil reaksi, berjalan sangat lambat. Perhitungannya: {(m. LB. NB) –(m. LC. NC)}. BEA = mg A

Kesalahan Titrasi : Perbedaan volume/massa diantara titik ekivalen dan titik akhir titrasi. Karena 1. Kehilangan cuplikan karena tumpah saat penimbangan, pemindahan larutan, buret bocor, salah pipet. 2. Kontaminasi atau larutan jadi encer karena kurang baik membilas buret, pipet atau labu. 3. Salah mencampurkan larutan setelah diencerkan. 4. Pengotoran pada standar primer 5. Kesalahan menimbang 6. Salah baca buret 7. Salah pemakaian indikator 8. Peralatan ( pipet atau buret) kurang bersih

Syarat analisa titrimetri 1. 2. 3. 4. Reaksi harus stoikiometri (tidak ada reaksi samping) Pada saat mendekati TE reaksi harus sempurna (K >>) Ada cara untuk menentukan bahwa TE /TA sudah tercapai. Reaksi berlangsung cepat , sempurna dalam beberapa menit.

Syarat Larutan Standar Primer 1. 2. 3. 4. 5. 6. 7. Kemurnian tinggi (>99%) atau bila tidak ada maka impuritas harus diketahui dan inert. Stabil terhadap udara Tidak mengandung air hidrat (komposisi tertentu) Mudah dikeringkan, tidak higroskopis (tidak menyerap air dan CO 2)pada waktu penimbangan Harga murah. Dapat larut dalam medium titrasi Berat rumus besar supaya kesalahan penimbangan kecil. Contoh : Na 2 CO 3 , Na 2 B 4 O 7, KHP, HCl.

Cara menyatakan dalam titrasi volumetric � Cara Molar. larutan satu Molar mengandung 1 mol zat terlarut dalam 1 liter larutan. Pada analisa sering digunakan milimol, karena pada titrasi biasanya digunakan larutan dalam jumlah sedikit. � Cara ekivalen: kenormalan suatu larutan yang dinyatakan sebagai jumlah ekivalen per liter larutan. Normalitas= ekiv zat terlarut = mekiv zat terlarut L larutan m. L larutan Ø Reaksi asam-basa : Satu ekiv jumlah gram zat yang menghasilkan/ bereaksi dengan satu mol ion H+. Reaksi redoks: Satu ekiv jumlah gram zat yang menghasilkan / bereaksi dengan 1 mol elektron. Ø

KONSENTRASI LARUTAN Molaritas (M) mol A M= Liter larutan mmol A M= m. L larutan M= mol V Untuk mencari gram zat terlarut: g = M x V x BM

Soal 1 1. Hitung molaritas suatu larutan H 2 SO 4 yang mempunyai densitas 1, 30 g/ml dan mengandung 32, 6% bobot SO 3. BM SO 3=80, 06 • Jawab: 1 liter larutan mengandung 1, 30 g/ml x 1000 ml/L x 0, 326 = 424 g SO 3 (424 g) / (80, 06 g/mol) M= 1 liter = 5, 3 mol/L Karena 1 mol SO 3 menghasilkan dalam air maka ada 5, 3 mol/L H 2 SO 4 dalam larutan itu 2. Berapa gram Na 2 SO 4 (142, 1 g/mol) diperlukan untuk membuat larutan sebanyak 250 m. L dengan konsentrasi 0, 683 M
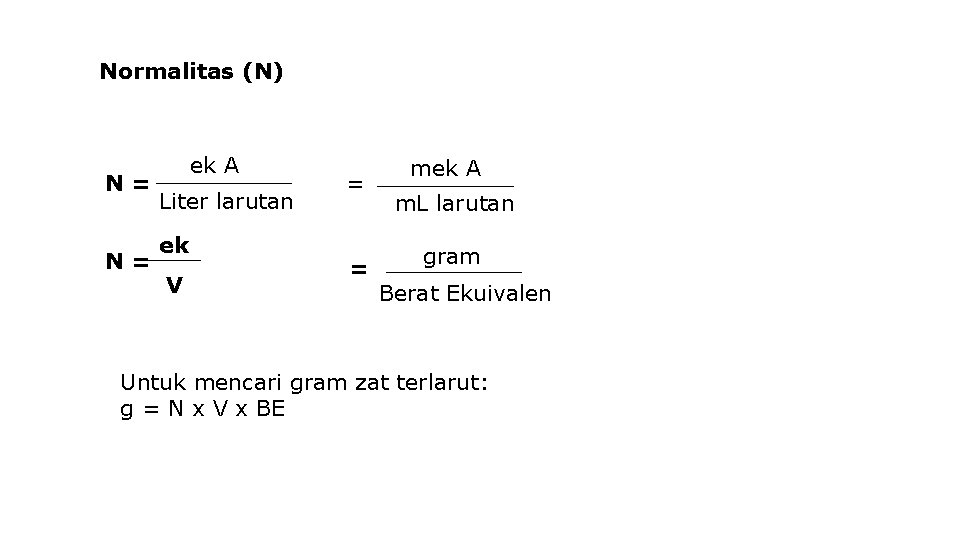
Normalitas (N) N= N= ek A Liter larutan ek V = = mek A m. L larutan gram Berat Ekuivalen Untuk mencari gram zat terlarut: g = N x V x BE

Soal 2: Hitung berapa gram Na 2 CO 3 murni diperlukan untuk membuat 250 ml larutan 0, 150 N. Natrium karbonat itu dititrasi dengan HCl menurut persamaan: CO 32 - + 2 H+ H 2 CO 3 Jawab: tiap Na 2 CO 3 bereaksi dengan 2 H+ , maka berat ekuivalennya setengah BM-nya 106/2 = 53 g/ek jadi, banyaknya Na 2 CO 3 yang diperlukan: ek = g/BE g = (0, 15 ek/L) x (0, 25 L) x (53 g/ek) = 1, 99 g

Persen Berat : gram zat terlarut dalam 100 g larutan %= g zat terlarut x 100% g zat terlarut + g pelarut HCl pekat (BM 36, 5) mempunyai densitas 1, 19 g/ml dan mengandung 37% berat HCl. Berapa ml asam pekat ini harus diambil dan diencerkan menjadi 1 liter untuk membuat larutan 0, 100 M Berapa M HCl pekat? M = mol/L = g/(BM x V) gram HCl = (1, 19 g/ml) x (1000 ml/L) x 0, 37 = 440 g/L M = 440 g / {(36, 5 g/mol) x 1 L }= 12, 055 M g = M x V x BM = (0, 100 mol/L) x (1 L) x (36, 5 g/mol) = 3, 65 gram dalam 1 ml HCl pekat terdapat 1, 19 g/ml HCl x 0, 37 = 0, 44 g/ml ml = 3, 65 g = 8, 3 ml 0, 44 g/ml 0, 1 x 1 V 1= M 2 x V 2 = 12, 055 M 1 = 0, 0083 L = 8, 3 ml

Metode Titrimetri / Volumetri n n Prosedur analisis kimia yang didasarkan pada pengukuran jumlah larutan titran yang bereaksi dengan analit. Larutan titran : larutan yang digunakan untuk mentitrasi, biasanya digunakan suatu larutan standar Larutan standar: larutan yang telah diketahui konsentrasinya titrasi dilakukan dengan menambahkan sedikit demi sedikit titran ke dalam analit

JENIS - JENIS TITRASI n n Titrasi asam - basa Titrasi redoks Titrasi pembentukkan kompleks Titrasi pengendapan

TITRASI ASAM BASA 1. Berapa volume 0. 116 M H 2 SO 4 yang dibutuhkan untuk mentitrasi 25. 0 ml Ba(OH)2 0. 00840 sampai titik ekuvalen. Jawab: mol H+ = mol OHa. ma. va = b. mb. vb 2 x 0, 116 x va = 2 x 0, 0084 x 25 Va = 50 x 0. 0084 2 x 0. 116 Va = 1, 81 ml

2. Kalau 5 ml asam bervalensi 1 dengan kosentrasi 0. 1 M dapat dinetralkan oleh 10 ml larutan KOH (Mr = 56), maka berapa KOH yang ada dalam 1 liter larutan? Jawab: Mol H+ = mol OHM = n = g/mr A x ma x va = b x mb x vb mr 1/1 1 x 0. 1 x 5 = 1 x mb x 10 mb = 0. 05 n = g/mr g = 0. 05 x 56 V = liter = ml/1000 = 2. 8 g
- Slides: 28