KIM TRA BI C P N Hon thnh


KIỂM TRA BÀI CŨ ĐÁP ÁN Hoàn thành các phương trình hóa học sau: a/ Fe + HCl → a/ Fe + 2 HCl → Fe. Cl 2 + H 2 b/ Zn + Cu. SO 4 → c/ Zn + Cu. SO 4 → Zn. SO 4 + Cu c/ Cu + Ag. NO 3 → d/ Cu + 2 Ag. NO 3 → Cu(NO 3)2 + 2 Ag d/ Ag + Cu. SO 4 → e/ Ag + Cu. SO 4 → không phản ứng

THẢO LUẬN NHÓM Dự đoán mức độ hoạt động hóa học của các kim loại sau: Fe; Cu; Ag; Na và H?

THẢO LUẬN NHÓM Hãy đề xuất các thí nghiệm so sánh mức độ hoạt động hóa học của các kim loại sau: 1) Fe với Cu 2) Cu với Ag 3) Fe; Cu với (H) 4) Na với Fe Biết trong phòng thí nghiệm có các hóa chất sau: + Dung dịch Fe. SO 4; Ag. NO 3; Cu. SO 4; HCl; nước. + Kim loại Fe; Cu; Na; Ag và giấy tẩy phenolphtalein.
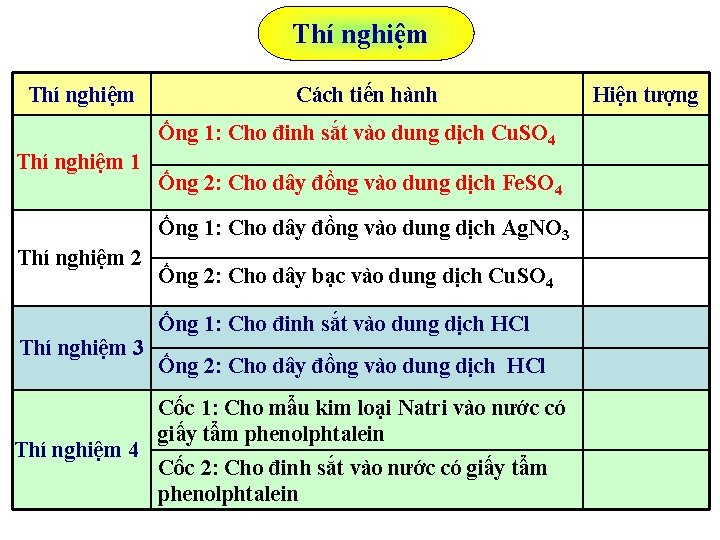
Thí nghiệm Cách tiến hành Ống 1: Cho đinh sắt vào dung dịch Cu. SO 4 Thí nghiệm 1 Ống 2: Cho dây đồng vào dung dịch Fe. SO 4 Ống 1: Cho dây đồng vào dung dịch Ag. NO 3 Thí nghiệm 2 Thí nghiệm 3 Thí nghiệm 4 Ống 2: Cho dây bạc vào dung dịch Cu. SO 4 Ống 1: Cho đinh sắt vào dung dịch HCl Ống 2: Cho dây đồng vào dung dịch HCl Cốc 1: Cho mẩu kim loại Natri vào nước có giấy tẩm phenolphtalein Cốc 2: Cho đinh sắt vào nước có giấy tẩm phenolphtalein Hiện tượng

Chú ý khi làm thí nghiệm: - Không để hóa chất dính vào da tay, quần áo hoặc các bộ phận khác trên cơ thể; - Lượng Na chỉ lấy bằng hạt đỗ xanh; - Dùng ống hút lấy dung dịch các chất vào ống nghiệm khoảng từ 1 – 3 ml.
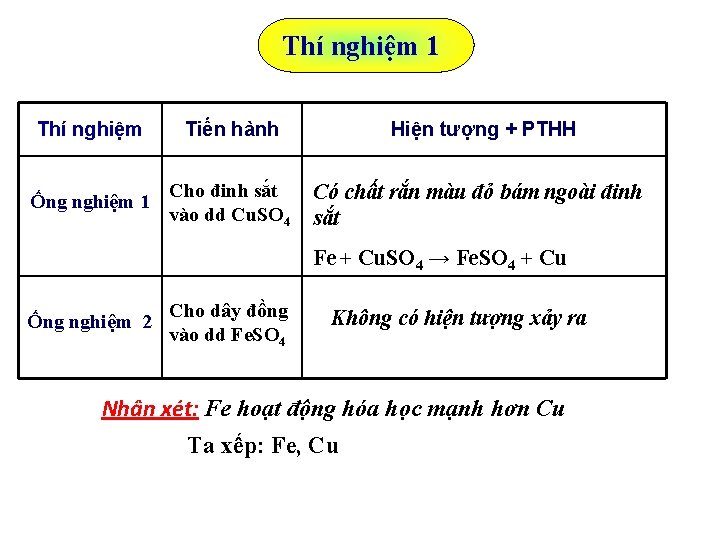
Thí nghiệm 1 Thí nghiệm Tiến hành Hiện tượng + PTHH Ống nghiệm 1 Cho đinh sắt vào dd Cu. SO 4 Có chất rắn màu đỏ bám ngoài đinh sắt Fe + Cu. SO 4 → Fe. SO 4 + Cu Ống nghiệm 2 Cho dây đồng vào dd Fe. SO 4 Không có hiện tượng xảy ra Nhận xét: Fe hoạt động hóa học mạnh hơn Cu Ta xếp: Fe, Cu
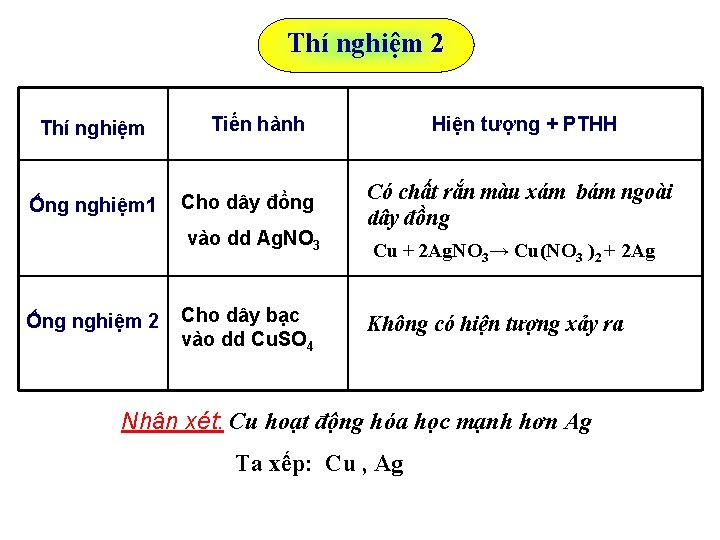
Thí nghiệm 2 Thí nghiệm Ống nghiệm 1 Tiến hành Cho dây đồng vào dd Ag. NO 3 Ống nghiệm 2 Cho dây bạc vào dd Cu. SO 4 Hiện tượng + PTHH Có chất rắn màu xám bám ngoài dây đồng Cu + 2 Ag. NO 3→ Cu(NO 3 )2 + 2 Ag Không có hiện tượng xảy ra Nhận xét: Cu hoạt động hóa học mạnh hơn Ag Ta xếp: Cu , Ag
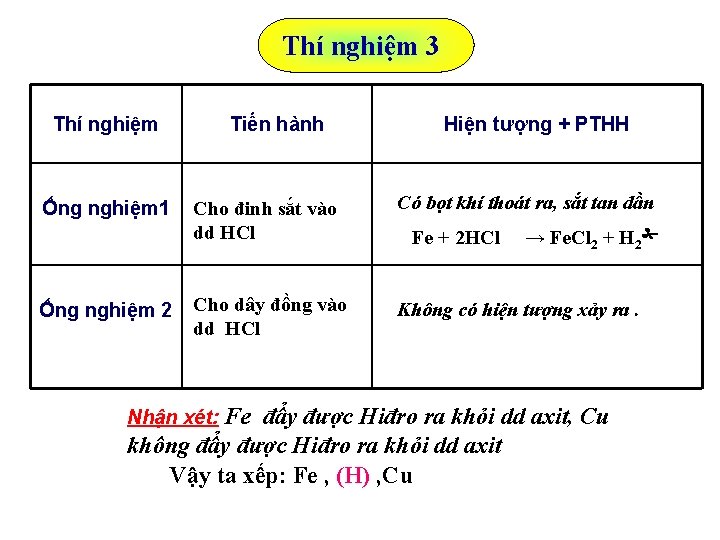
Thí nghiệm 3 Thí nghiệm Ống nghiệm 1 Ống nghiệm 2 Tiến hành Hiện tượng + PTHH Cho đinh sắt vào dd HCl Có bọt khí thoát ra, sắt tan dần Cho dây đồng vào dd HCl Không có hiện tượng xảy ra. Nhận xét: Fe Fe + 2 HCl → Fe. Cl 2 + H 2 đẩy được Hiđro ra khỏi dd axit, Cu không đẩy được Hiđro ra khỏi dd axit Vậy ta xếp: Fe , (H) , Cu
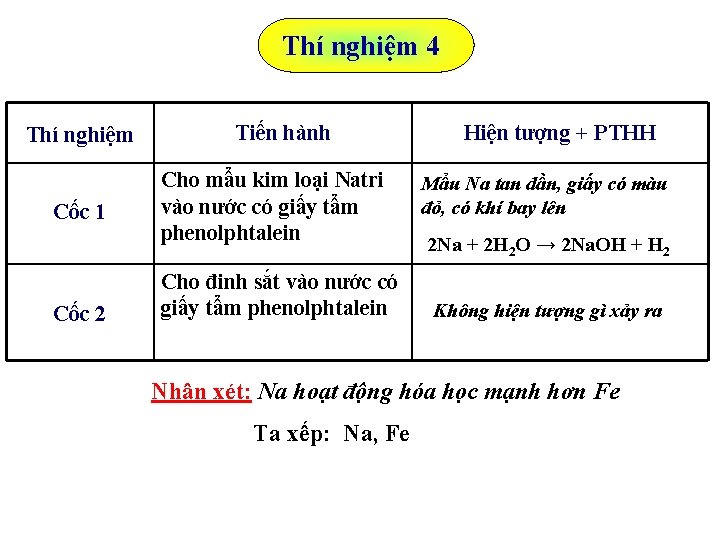
Thí nghiệm 4 Thí nghiệm Cốc 1 Cốc 2 Tiến hành Cho mẩu kim loại Natri vào nước có giấy tẩm phenolphtalein Cho đinh sắt vào nước có giấy tẩm phenolphtalein Hiện tượng + PTHH Mẩu Na tan dần, giấy có màu đỏ, có khí bay lên 2 Na + 2 H 2 O → 2 Na. OH + H 2 Không hiện tượng gì xảy ra Nhận xét: Na hoạt động hóa học mạnh hơn Fe Ta xếp: Na, Fe

Bằng nhiều thí nghiệm khác nhau, người ta đã xếp được các kim loại thành dãy theo chiều giảm dần mức độ hoạt động hóa học như sau : - Dãy HĐHH của một số kim loại: K, Na, Mg, Al, Zn, Fe, Pb, (H), Cu, Ag, Au.
THẢO LUẬN NHÓM: Hoàn thành các nội dung nêu nên ý nghĩa của dãy hđhh trong bảng sau: 1 2 3 4

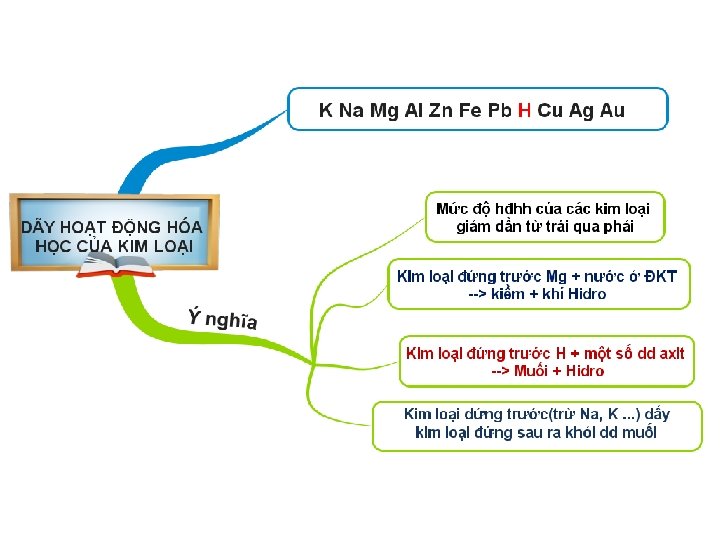
K, Na, Mg, Al, Zn, Fe, Pb, (H), Cu, Ag, Au *Ý nghĩa 1. Mức độ hoạt động hóa học của các kim loại giảm dần từ trái qua phải. 2. Kim loại đứng trước Mg phản ứng với nước ở điều kiện thường tạo thành kiềm và giải phóng khí hiđro. VD: 2 Na + 2 H 2 O → 2 Na. OH + H 2 3. Kim loại đứng trước H phản ứng với một số axit (HCl, H 2 SO 4 loãng …) giải phóng khí H 2 VD: Fe + 2 HCl → Fe. Cl 2 + H 2 4. Kim loại đứng trước (trừ K, Na. . ) đẩy kim loại đứng sau ra khỏi dung dịch muối. VD: Cu + 2 Ag. NO 3 → Cu(NO 3 )2 + 2 Ag
K Na Mg Al Zn Fe Pb (H) Cu Ag Au Khi *Cách Nào ghi May Áo hoạt Zápđộng Sắthóa. Phải Hỏikim. Cụ nhớ dãy học của loại Bạc Vàng

Cuûng coá Bài tập 1 trang 54 SGK Dãy các kim loại nào sau đây được sắp xếp đúng theo chiều hoạt động hóa học tăng dần? A. K, Mg, Cu, Al, Zn, Fe Sai rồi B. Fe, Cu, K, Mg, Al, Zn Sai rồi C. Cu, Fe, Zn, Al, Mg, K Đúng rồi D. Zn, K, Mg, Cu, Al, Fe Sai rồi E. Mg, K, Cu, Al, Fe Sai rồi

Bài 2: Chọn đáp án đứng trước câu trả lời đúng 1. Kim loaïi naøo sau ñaây coù theå taùc duïng vôùi nöôùc ôû ñieàu kieän thöôøng ? A. K B. Fe C. Na D. Caû A vaø C ñeàu ñuùng 2. Nhöõng kim loaïi naøo sau ñaây taùc duïng vôùi dung dòch H 2 SO 4 (loaõng)? A. Fe, Cu B. Zn, Fe C. Ag, Zn D. Cu, Ag

BÀI TẬP VẬN DỤNG Cho 10, 5 gam hỗn hợp gồm 2 kim loại Cu, Zn vào dung dịch H 2 SO 4 loãng, dư, người ta thu được 2, 24 lit khí (đktc) a) Viết PTHH b)Tính khối lượng chất rắn còn lại sau phản ứng c)Tính % kl mỗi kim loại có trong hỗn hợp ban đầu? HƯỚNG DẪN GiẢI Cu không phản ứng với dd H 2 SO 4 loãng PTHH: Zn + H 2 SO 4 → Zn. SO 4 + H 2 0, 1 n. H 2 mzn= 0, 1. 65 = 6, 5 g m. Cucòn lại = 10, 5 – 6, 5 = 4 g %Zn = %Cu= 100% - 61, 9% = 38, 1%

BÀI TẬP VẬN DỤNG Trong những cặp chất sau, cặp nào tác dụng được với nhau? - Viết các PTHH minh hoạ cho các phản ứng. 2 H 2 O 2 KOH + H 2 a)a)K 2+KH+O 2 + 2 HCl Zn. Cl 2 + H 2 b) b) Zn +Zn HCl c) +Cu + HCl Không phản ứng c) Cu HCl + Cu. SO 4 Zn. SO 4 + Cu d) d) Zn +Zn Cu. SO 4 e) +Fe + Mg. Cl 2 Không phản ứng e) Fe Mg. Cl 2 K, Na, Mg, Al, Zn, Fe, Pb, (H), Cu, Ag, Au

HƯỚNG DẪN VỀ NHÀ - Học thuộc dãy HĐHH của kim loại - Ghi nhớ ý nghĩa của dãy - Vận dụng làm bài tập 1, 2, 3, 4 SGK-T 54

Xin c¸m ¬n thÇy c « vµ c¸c em Chóc thÇy c « m¹nh khoÎ Chóc c¸c em häc tèt
- Slides: 22