Kim tra bi c Cu 1 Trnh by

KiÓm tra bµi cò

C©u 1: Tr×nh bµy cÊu t¹o ph©n tö N 2? V× sao ë ®iÒu kiÖn th êng. Nit¬ lµ mét chÊt tr¬ ? ë ®iÒu kiÖn nµo N 2 trë nªn ho¹t ®éng h¬n ? CÊu t¹o ph©n tö N 2 : Liªn kÕt trong ph©n tö N 2 lµ liªn kÕt 3 bÒn v÷ng chÝnh v× vËy mµ ë nhiÖt ®é th êngnit¬ lµ mét khÝ tr¬. ë nhiÖt ®é cao liªn kÕt 3 dÔ bÞ c¾t h¬n khi ®ã nit¬ sÏ trë nªn ho¹t ®éng h¬n. Kiểm tra bài cũ

C©u 2: Nªu nh÷ng tÝnh chÊt ho¸ häc ®Æc tr ng cña N 2. ViÕt ph ¬ngtr×nh ph¶n øng minh ho¹ ? Nh÷ng tÝnh chÊt ho¸ häc ®Æc tr ngcña Nit¬ lµ: N 2 T¸c dông víi H 22 NH 3 + 3 H 2 T¸c dông víi O 2 N 2 + O 2 = 2 NO Q Kiểm tra bài cũ

Giáo án bài 8: Amoniac và muối amoni n n n Giáo viên: NGUYỄN THỊ MINH TRANG Lớp : 11 Ngày :
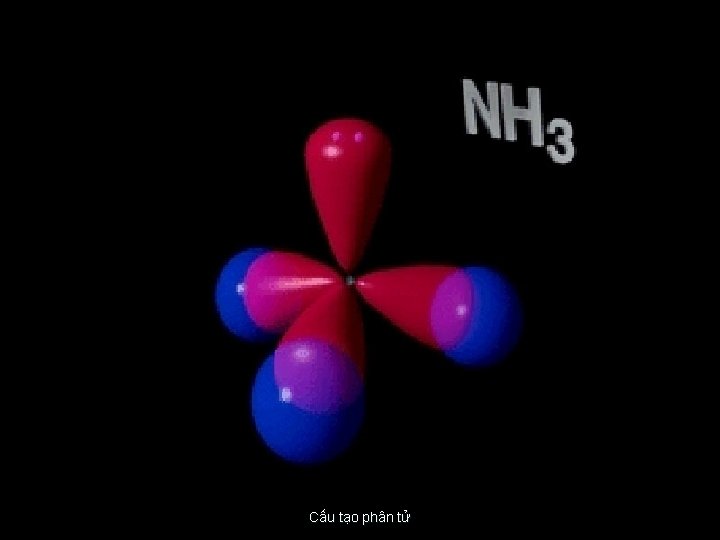
Cấu tạo phân tử

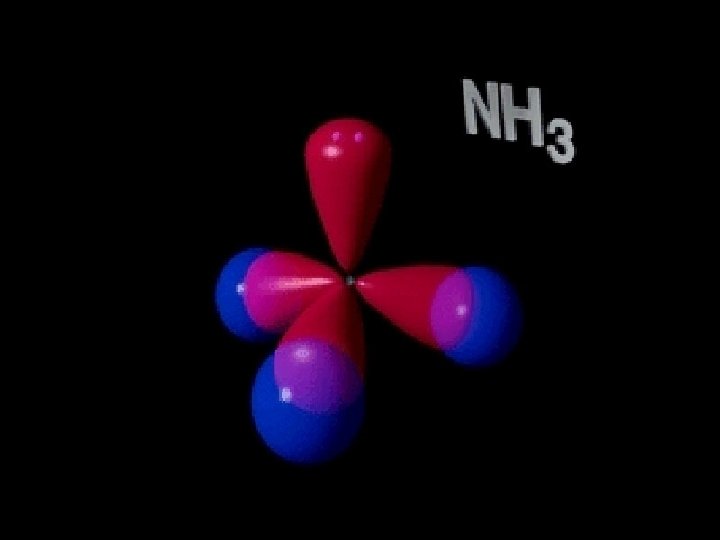
I. CÊu t¹o ph©n tö C «ng thøc ph©n tö : NH 3 Tªn gäi : Amoniac C «ng thøc electron : C «ng thøc cÊu t¹o : M « h×nh ph©n tö : Gi÷a c¸c ph©n tö NH 3 cã c¸c liªn kÕt H. Cấu tạo phân tử

CÊu tróc ph©n tö amoniac Cấu tạo phân tử
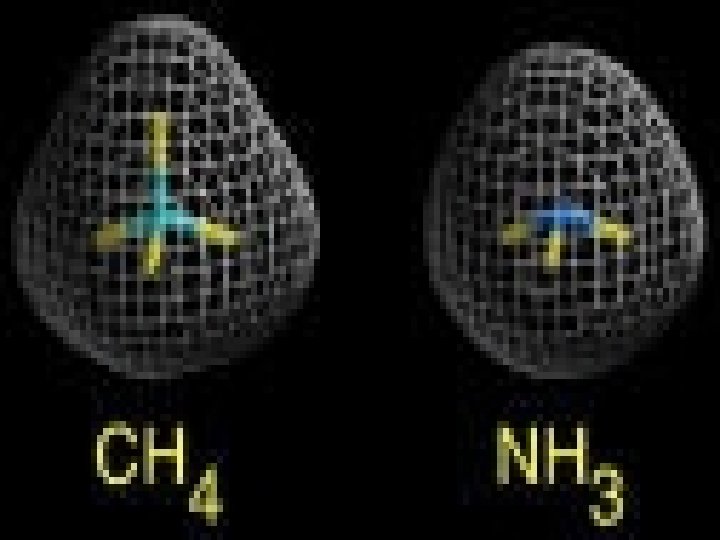
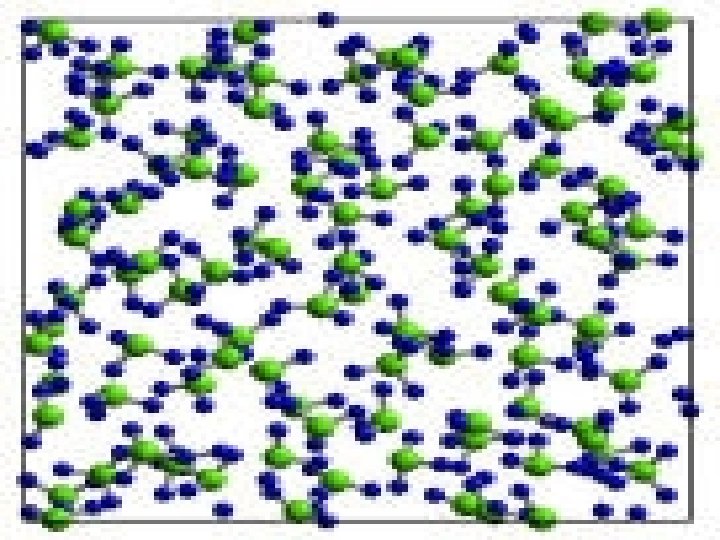

NhËn xÐt Liªn kÕt gi÷a nguyªn tö N vµ 3 nguyªn tö H lµ liªn kÕt céng ho¸ trÞ. CÆp e dïng chung lÖch vÒ phÝa nguyªn tö N. Ba nguyªn tö H ë vÒ cïng mét bªn, do vËy NH 3 lµ mét ph©n tö ph©n cùc. §Çu N d ®iÖn tÝch ©m, ®Çu H d ®iÖn tÝch d ¬ng. Cấu tạo phân tử

II. TÝnh chÊt vËt lÝ NH 3 chÊt khÝ kh «ng mµu, mïi khai vµ xèc, nhÑ h¬n kh «ng khÝ ( D=0. 76 g/l ). Thu NH 3 b» ng ph ¬ngph¸p ®Èy kh «ng khÝ, óp b×nh thu. tohl = 43 o. C tohr = 78 o. C Tan nhiÒu trong n íc. Tính chất vật lí

ThÝ nghiÖm chøng tá NH 3 tan nhiÒu trong n íc Tính chất vật lí


Tính chất hoá học

III. TÝnh chÊt ho¸ häc

1. TÝnh baz¬. a. T¸c dông víi n íc. NH 3 + H 2 O NH 4+ + OH Dung dÞch cã tÝnh baz¬ yÕu : Lµm cho phenolphtalein tõ kh «ng mµu chuyÓn sang mµu hồng. Lµm cho quú tÝm ®æi thµnh mµu xanh. Tính chất hoá học

b. T¸c dông víi axit NH 3 + H+ + HSO 4 = NH 4+ + HSO 4 NH 3 + H+ + SO 42 = NH 4+ + SO 42 Ph¶n øng tæng qu¸t : NH 3 + H+ = NH 4+ NH 3(k) + HCl(k) = NH 4 Cl(h) Ph¶n øng dïng ®Ó nhËn biÕt NH 3 vµ ng îcl¹i. Tính chất hoá học
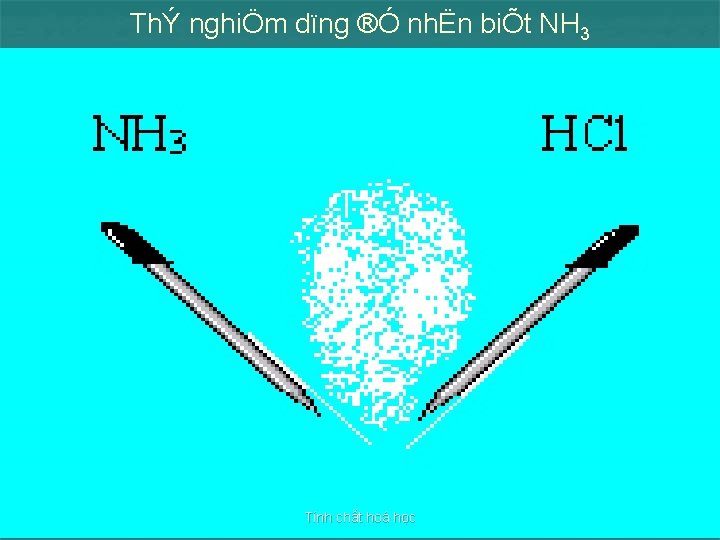
ThÝ nghiÖm dïng ®Ó nhËn biÕt NH 3 Tính chất hoá học

c. T¸c dông víi dung dÞch muèi cña nhiÒu kim lo¹i t¹o hidroxit kÕt tña. Mn+ + n. H 2 O + n. NH 3 = M(OH)n + n. NH 4+ Vd: Fe 2+ + 2 NH 3 + 2 H 2 O Fe(OH)2 + 2 NH 4+ Al 3+ + 3 NH 3 + 3 H 2 O Al(OH)3 + 3 NH 4+ Tính chất hoá học

3. TÝnh khö. Trong ph©n tö NH 3, N cã sè oxi ho¸ lµ 3 lµ sè oxi ho¸ nhá nhÊt cña N do ®ã NH 3 chØ cã tÝnh khö mµ kh «ng thÓ hiÖn tÝnh oxi ho¸. a. T¸c dông víi Cl 2 2 NH 3 + 3 Cl 2 6 HCl + N 2 b. T¸c dông víi O 2 Tính chất hoá học
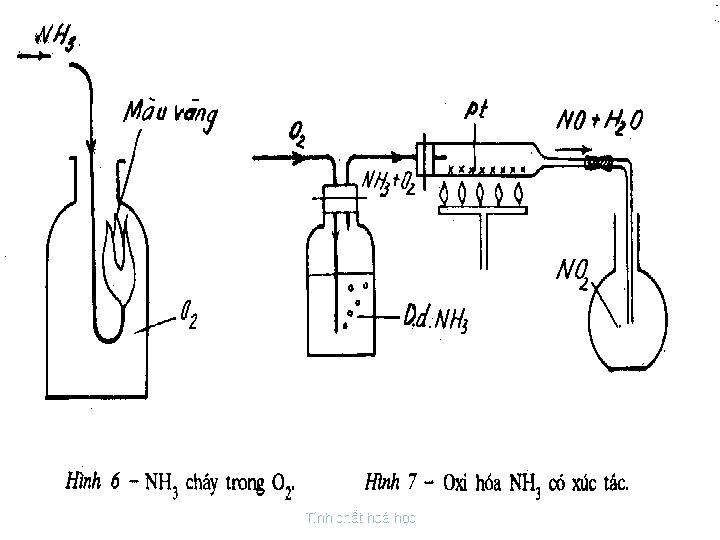
Tính chất hoá học
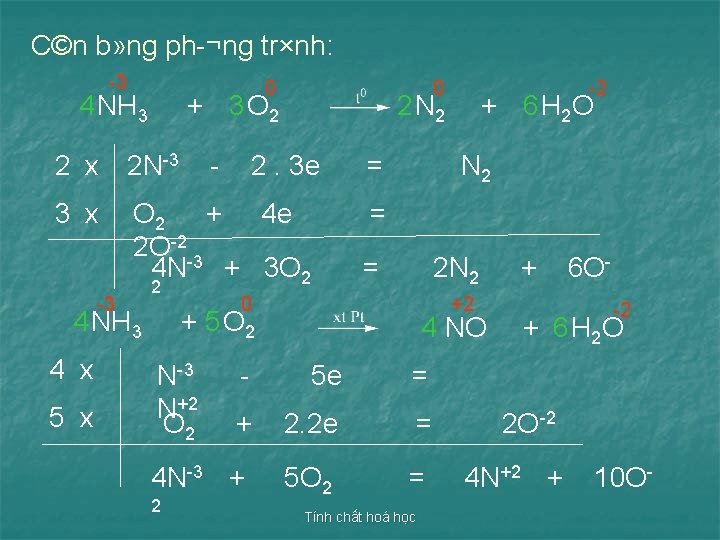
C©n b» ng ph ¬ng tr×nh: 3 0 4 NH 3 0 + 3 O 2 2 N 2 2 x 2 N 3 3 x O 2 + 4 e 2 O 2 3 4 N + 3 O 2 3 2 4 NH NH 3 4 x 5 x 2. 3 e = + 6 H 2 O N 2 = = 2 N 2 0 +2 + 5 O 2 N 3 N+2 O 2 2 4 NO + 2 + 6 H 2 O 5 e = + 2. 2 e = 2 O 2 4 N 3 + 5 O 2 = 4 N+2 + 2 Tính chất hoá học 6 O 10 O

IV. øng dông vµ ®iÒu chÕ.

1. øng dông cña amoniac Amoniac cã nhiÒu øng dông, ®Æc biÖt trong n «ng nghiÖp: Dung dÞch amoniac cã thÓ dông trùc tiÕp lµm ph©n bãn vµ ®Ó s¶n xuÊt ph©n bãn d íi d¹ng muèi Amoni. Dïng ®Ó ®iÒu chÕ c¸c ho¸ chÊt kh¸c nh : HNO 3, x « ®a, ure… §iÒu chÕ hidrazin N 2 H 4 (chÊt ®èt cho tªn löa). NH 3 láng lµ chÊt g©y l¹nh trong m¸y l¹nh. Ứng dụng của Amoniac

2. §iÒu chÕ. a. Trong phßng thÝ nghiÖm * Tõ muèi Amoni: 2 NH 4 Cl + Ca(OH)2 = 2 NH 3 + Ca. Cl 2 + 2 H 2 O * Tõ dd NH 3 ®Ëm ®Æc. Dïng KOH r¾n hoÆc Ca. O míi nung lµm kh « NH 3. Điều chế Amoniac
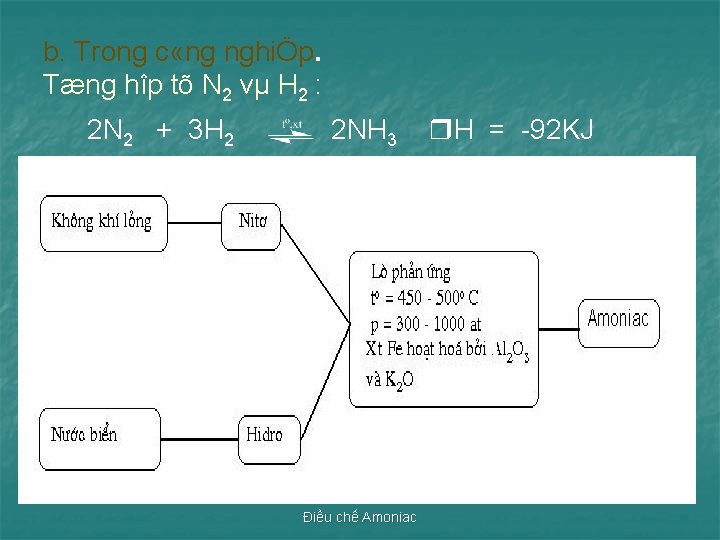
b. Trong c «ng nghiÖp. Tæng hîp tõ N 2 vµ H 2 : 2 N 2 + 3 H 2 2 NH 3 Điều chế Amoniac H = 92 KJ

Điều chế Amoniac

Nhµ m¸y s¶n xuÊt ra amoniac Điều chế Amoniac

Bµi tËp cñng cè

C©u 1: Tõ ®Æc ®iÓm cÊu t¹o ph©n tö, sè oxi ho¸ cña N trong ph©n tö NH 3 cã nhËn xÐt g× vÒ tÝnh chÊt cña NH 3. Cho vÝ dô minh ho¹. §Æc ®iÓm cÊu t¹o: Ph©n tö ph©n cùc: Tan m¹nh trong dung m «i ph©n cùc (H 2 O). Nguyªn tö cã cÆp e tù do: Cã ph¶n øng ho¸ hîp víi axit. T¹o liªn kÕt cho nhËn NH 3 lµ mét baz¬. Cã kh¶ n¨ng t¹o phøc víi mét sè ion kim lo¹i. N cã sè oxi ho¸ 3 do ®ã NH 3 chØ cã tÝnh khö mµ kh «ng cã tÝnh oxi ho¸. Bài tập củng cố

Vd: 2 NH 3 + 3 Cu. O = N 2 + 3 Cu + 3 H 2 O Bài tập củng cố

C©u 2 : So s¸nh tÝnh chÊt gi÷a H 2 S vµ NH 3 cã ®Æc ®iÓm g× gièng nhau vµ kh¸c nhau? Gi¶i thÝch? Gièng nhau: ChØ cã tÝnh khö mµ kh «ng cã tÝnh oxi ho¸. Nguyªn nh©n lµ do c¶ 2 hîp chÊt trªn ®Òu cã nguyªn tè trung t©m mang sè oxi ho¸ ©m nhÊt. Kh¸c nhau: TÝnh khö cña NH 3 yÕu h¬n tÝnh khö cña H 2 S. NH 3 bÒn h¬n H 2 S. (C¨n cø vµo ®é ©m ®iÖn cña 2 nguyªn tè). Bài tập củng cố
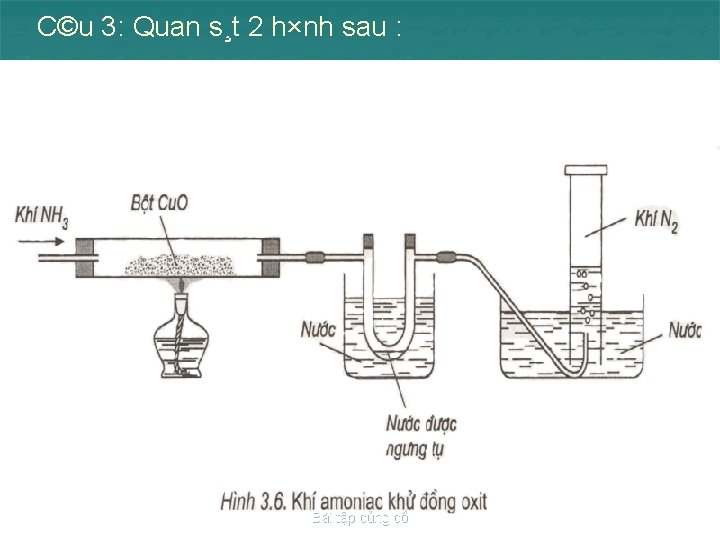
C©u 3: Quan s¸t 2 h×nh sau : Bài tập củng cố

H·y cho biÕt: 1. S¬ ®å thiÕt bÞ ë h×nh nµo dïng ®Ó ®iÒu chÕ NH 3? T¹i sao? 2. Khi ®iÒu chÕ khÝ g× th× cã thÓ dïng c¸c dông cô nh ë h×nh 1, h×nh 2 ? 3. Nªu c¸c ho¸ chÊt cã thÓ dïng ®Ó ®iÒu chÕ H 2, NH 3, Cl 2 nhê c¸c dông cô nh trªn ?
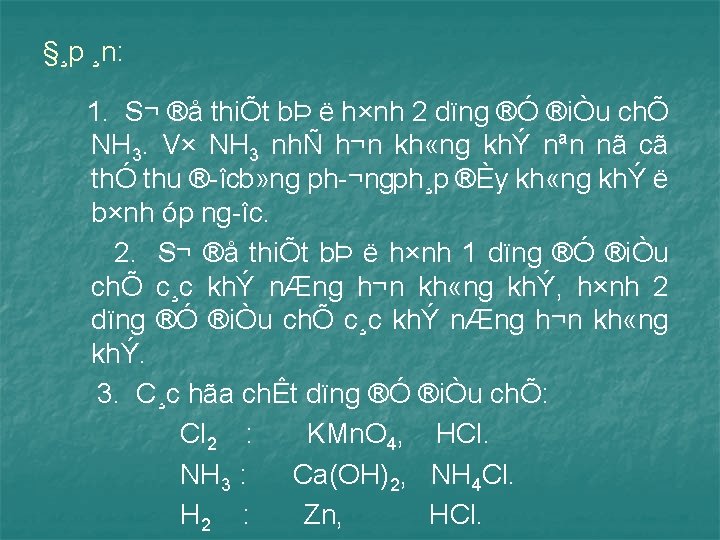
§¸p ¸n: 1. S¬ ®å thiÕt bÞ ë h×nh 2 dïng ®Ó ®iÒu chÕ NH 3. V× NH 3 nhÑ h¬n kh «ng khÝ nªn nã cã thÓ thu ® îcb» ng ph ¬ngph¸p ®Èy kh «ng khÝ ë b×nh óp ng îc. 2. S¬ ®å thiÕt bÞ ë h×nh 1 dïng ®Ó ®iÒu chÕ c¸c khÝ nÆng h¬n kh «ng khÝ, h×nh 2 dïng ®Ó ®iÒu chÕ c¸c khÝ nÆng h¬n kh «ng khÝ. 3. C¸c hãa chÊt dïng ®Ó ®iÒu chÕ: Cl 2 : KMn. O 4, HCl. NH 3 : Ca(OH)2, NH 4 Cl. H 2 : Zn, HCl.

C©u 4: Gi¶i thÝch t¹i sao tr íckhi hµn kim lo¹i ng êi ta th êngdïng NH 4 Cl ®¸nh lªn bÒ mÆt cña kim lo¹i ? V× NH 4 Cl ph©n huû t¹o ra NH 3 cã tÝnh khö t¸c dông víi Oxit kim lo¹i do ®ã nã cã t¸c dông ®¸nh s¹ch bÒ mÆt kim lo¹i ®Ó mèi hµn ® îc bÒn h¬n. NH 4 Cl = NH 3 + HCl 3 Cu. O + 2 NH 3 = 3 Cu + N 2 + 3 H 2 O

C©u 5 : Dung dÞch amoniac cã thÓ hoµ tan d îc Zn(OH)2, lµ do : a. Zn(OH)2 lµ mét hidroxit l ìng tÝnh. b. Zn(OH)2 lµ mét baz¬ Ýt tan. c. Zn(OH)2 cã kh¶ n¨ng t¹o phøc chÊt tan t ¬ngtù nh Cu(OH)2. d. NH 3 lµ mét hîp chÊt cã cùc vµ lµ mét baz¬ yÕu. H·y chän c©u tr¶ lêi ®óng.

C©u 5 : Dung dÞch amoniac cã thÓ hoµ tan d îc Zn(OH)2, lµ do : a. Zn(OH)2 lµ mét hidroxit l ìng tÝnh. b. Zn(OH)2 lµ mét baz¬ Ýt tan. c. Zn(OH)2 cã kh¶ n¨ng t¹o phøc chÊt tan t ¬ngtù nh Cu(OH)2. d. NH 3 lµ mét hîp chÊt cã cùc vµ lµ mét baz¬ yÕu. H·y chän c©u tr¶ lêi ®óng.

Bµi tËp vÒ nhµ C¸c bµi tËp s¸ch gi¸o khoa vµ mét sè bµi tËp trong s¸ch bµi tËp.

C©u 1 : Cã 5 b×nh ®ùng 5 chÊt khÝ riªng biÖt : N 2, O 2, NH 3, Cl 2 vµ CO 2. H·y dùa mét thÝ nghiÖm ®¬n gi¶n ®Ó nhËn ra b×nh ®ùng NH 3. C©u 2 : ViÕt c¸c ph ¬ngtr×nh ph¶n øng thùc hiÖn s¬ ®å chuyÓn ho¸ sau ®©y: KhÝ A Dung dÞch A D + H 2 O C Bài tập về nhà B KhÝ A

C©u 3 : Cho c©n b» ng ho¸ häc : N 2(K) + 3 H 2 2 NH 3(K) Q>0 C©n b» ng sÏ chuyÓn dÞch vÒ chiÒu nµo ? Cã gi¶i thÝch. a. T¨ng nhiÖt ®é. b. Hãa láng amoniac ®Ó t¸ch amoniac ra khái hçn hîp. c. Gi¶m thÓ tÝch cña hçn hîp ph¶n øng. Bài tập về nhà

Chóc c¸c em häc tèt !
- Slides: 43