KESETIMBANGAN KIMIA Kesetimbangan Kimia Laju reaksi maju sama

KESETIMBANGAN KIMIA

Kesetimbangan Kimia Laju reaksi maju sama dengan laju reaksi balik V 1 p A(g + q B(g ⇌ r C(g + s D(g ) ) V 2 V 1 = V 2

Kesetimbangan Kimia A. Jenis Kesetimbangan B. Faktor-faktor yang Mempengaruhi Pergeseran Kesetimbangan C. Aplikasi Kesetimbangan Kimia Dalam Industri D. Tetapan Kesetimbangan
A. Jenis Kesetimbangan 1. Homogen 2. Heterogen
![Kesetimbangan Amonia N 2(g) + 3 H 2(g) ⇌ 2 NH 3(g) 3 [] Kesetimbangan Amonia N 2(g) + 3 H 2(g) ⇌ 2 NH 3(g) 3 []](http://slidetodoc.com/presentation_image_h/f4bd75ef9dd08f73d89e2860a4832f99/image-5.jpg)
Kesetimbangan Amonia N 2(g) + 3 H 2(g) ⇌ 2 NH 3(g) 3 [] 2 1 H 2 NH 3 N 2 V

a. Kesetimbangan Homogen : zat yang direaksikan mempunyai wujud yang sama Contoh: N 2(g) + 3 H 2(g) ⇌ 2 NH 3(g)

b. Kesetimbangan Heterogen : Zat yang direaksikan mempunyai wujud yang berbeda Contoh: 2 C(s) + O 2(g) ⇌ 2 CO(g)

B. Faktor-faktor yang mempengaruhi pergeseran kesetimbangan 1. Konsentrasi 2. Tekanan dan volume 3. Temperatur

1. Konsentrasi a. Konsentrasi reaktan / produk diperbesar maka reaksi kearah lawannya Contoh: Ag+(aq) + Fe 2+(aq) ⇌Fe 3+(aq) + Ag(s) Fe 3+(aq) diperbesar arah reaksi ke kiri

b. Konsentrasi reaktan / produk diperkecil maka reaksi kearah diperkecil Contoh: Ag+(aq) + Fe 2+(aq) ⇌Fe 3+(aq) + Ag(s) Ag+(aq) diperkecil arah reaksi ke kiri Fe 3+(aq) diperkecil arah reaksi ke kanan

c. Jika konsentrasi reaktan / produk dilakukan pengenceran maka reaksi kearah mol yang terbesar Contoh: Ag+(aq) + Fe 2+(aq) ⇌ Fe 3+(aq) + Ag(s) 1+1 1

2. Tekanan a. Tekanan diperbesar arah reaksi ke jumlah mol terkecil b. Tekanan diperkecil arah reaksi ke jumlah mol terbesar Contoh: 2 SO 2(g) + 1 O 2(g) ⇌ 2 SO 3(g) 2 +1 2

3. Temperatur a. Temperatur diperbesar arah reaksi ke endoterm b. Temperatur diperkecil arah reaksi ke eksoterm Contoh: N 2(g)+3 H 2(g) ⇌ 2 NH 3(g); ∆H = -92, 2 k. J Suhu diperkecil arah ke kanan

C. Aplikasi kesetimbangan kimia dalam industri a. Pembuatan Amonia (NH 3) N 2(g)+3 H 2(g) ⇌ 2 NH 3(g) ∆H =-92, 2 k. J Tekanan 350 atm Suhu 5000 C Katalis Fe 3 O 4 (Fe. O dan Fe 2 O 3)

b. Pembuatan Asam Sulfat ( H 2 SO 4) 2 SO 2(g)+O 2(g)⇌2 SO 3(g)∆H=-792, 2 k. J Katalis V 2 O 5 Temperatur 420 0 C Tekanan 1 atm SO 3(g) + H 2 SO 4(l) ⇌ H 2 S 2 O 7(l) + H 2 O(l) ⇌ 2 H 2 SO 4(l)

D. Tetapan Kesetimbangan 1. Tetapan kesetimbangan konsentrasi (Kc) p A(g) + q B(g) ⇌ r C(g) + s D(g)

Contoh : 1. Dalam ruang yang bervolume 2 liter dan temperatur tertentu , terdapat kesetimbangan : 2 A(g) + 3 B(g) ⇌ C(g) + 3 D(g) Setelah pembekuan kesetimbangan, ternyata terdapat 0, 4 mol A; 0, 2 mol B; 0, 3 mol C; dan 0, 4 mol D. Berapa tetapan kesetimbangan Kc ?

Jawab:


2. Tetapan kesetimbangan tekanan (Kp) p A(g) + q B(g) ⇌ r C(g) + s D(g)

Contoh: 1. Harga Kp pada 5000 C untuk reaksi N 2(g) + 3 H 2(g) ⇌ 2 NH 3(g) adalah 1, 5 x 10 -5, berapa Kc? Jawab: ∆n = 2 – ( 1+3 ) mol =-2 t = (5000 C + 273)K = 773 K


Contoh: 2. Pada suhu 4000 C tetapan kesetimbangan untuk reaksi: H 2(g) + I 2(g) ⇌ 2 HI(g) ialah 49. Jika 0, 2 mol gas H 2 dan 0, 2 mol gas I 2 dimasukkan ke dalam suatu wadah tertutup yang bervolume 10 liter. Berapa mol zat-zat pada saat kesetimbangan dicapai?

Jawab: Misalkan gas yang bereaksi = a mol reaksi : H 2(g) + I 2(g) ⇌ 2 HI(g) mula-mula : 0, 2 bereaksi : -a setimbang : 0, 2 -a 0, 2 -a +2 a 2 a
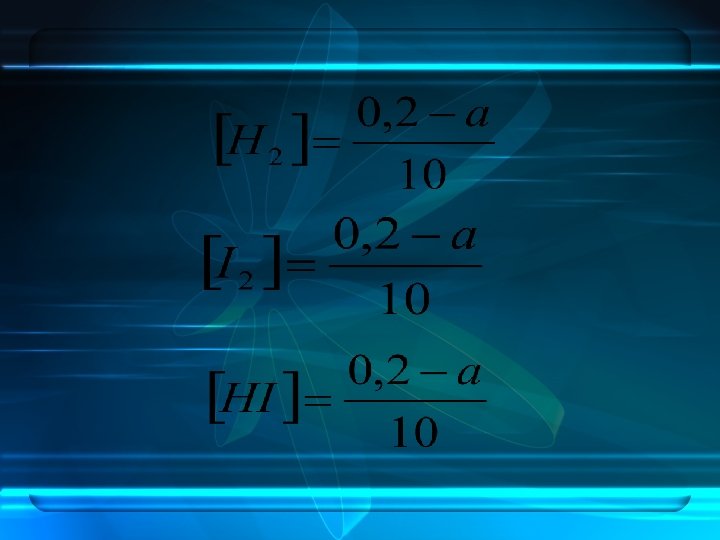


2 a = 7 (0, 2 – a) 2 a = 1, 4 – 7 a 9 a = 1, 4 a = 0, 156 mol Pada saat kesetimbangan terdapat: H 2 =(0, 2 – a)=(0, 2 – 0, 156)= 0, 044 mol I 2 =(0, 2 – a)=(0, 2 – 0, 156)= 0, 044 mol HI = 0, 2 a = (0, 2 x 0, 156) = 0, 312 mol

Pertanyaan: 1. Reaksi kesetimbangan yang berlangsung dalam fase sama disebut kesetimbangan … A. Homogen B. Heterogen

2. Reaksi : N 2(g)+3 H 2(g) ⇌ 2 NH 3(g) Jika konsentrasi N 2 diperbesar maka reaksi akan bergeser kearah … Kanan / Produk

- Slides: 30