KESETIMBANGAN KIMIA Dra M Setyorini M Si Konsep

KESETIMBANGAN KIMIA Dra. M. Setyorini, M. Si

Konsep Kesetimbangan Berdasarkan arah reaksi, jenis reaksi kimia dibedakan menjadi : Reaksi irreversibel ( tidak dapat balik) : hanya berlangsung satu arah, contoh : reaksi pembakaran. Reaksi reversibel (dapat balik) : berlangsung dalam dua arah. Pereaksi semula dapat terbentuk kembali dari zat-zat hasil reaksi. contoh : N 2(g) + 3 H 2(g) 2 NH 3(g) H 2(g) + I 2(g) 2 HI(g)
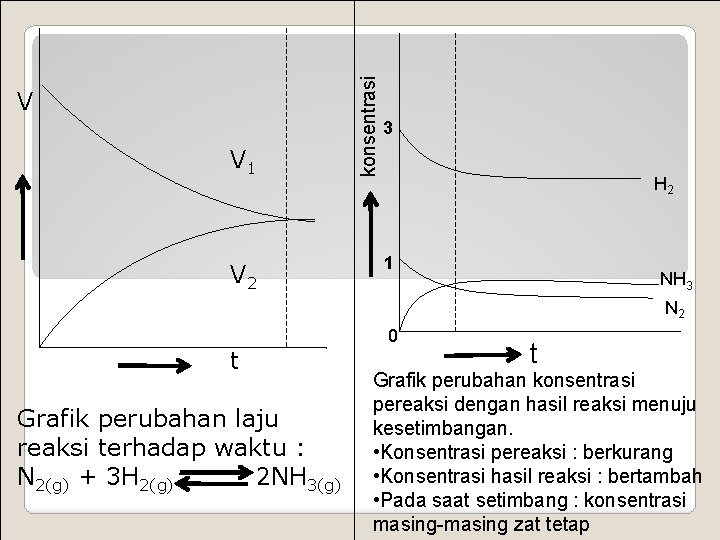
V 1 V 2 konsentrasi V 3 H 2 1 NH 3 N 2 t Grafik perubahan laju reaksi terhadap waktu : N 2(g) + 3 H 2(g) 2 NH 3(g) 0 t Grafik perubahan konsentrasi pereaksi dengan hasil reaksi menuju kesetimbangan. • Konsentrasi pereaksi : berkurang • Konsentrasi hasil reaksi : bertambah • Pada saat setimbang : konsentrasi masing-masing zat tetap

Kesetimbangan tercapai bila V 1 = V 2 Bila laju reaksi maju dan reaksi balik sama besar dan konsentrasi reaktan dan produk tidak lagi berubah seiring berjalannya waktu maka tercapailah : kesetimbangan kimia (keadaan setimbang : chemical equilibrium) Ciri keadaan setimbang Berlangsung dalam sistem tertutup Dinamis Tidak terjadi perubahan makroskopis
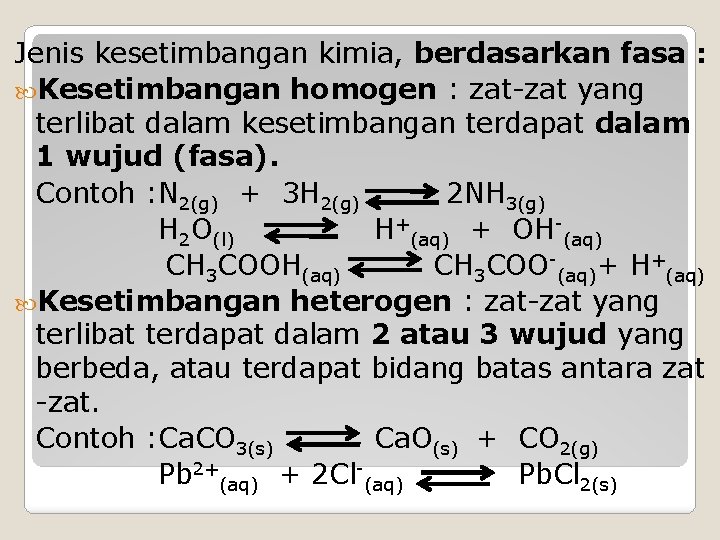
Jenis kesetimbangan kimia, berdasarkan fasa : Kesetimbangan homogen : zat-zat yang terlibat dalam kesetimbangan terdapat dalam 1 wujud (fasa). Contoh : N 2(g) + 3 H 2(g) 2 NH 3(g) H 2 O(l) H+(aq) + OH-(aq) CH 3 COOH(aq) CH 3 COO-(aq)+ H+(aq) Kesetimbangan heterogen : zat-zat yang terlibat terdapat dalam 2 atau 3 wujud yang berbeda, atau terdapat bidang batas antara zat -zat. Contoh : Ca. CO 3(s) Ca. O(s) + CO 2(g) Pb 2+(aq) + 2 Cl-(aq) Pb. Cl 2(s)

Konstanta Kesetimbangan Pada sistem : H 2(g) + I 2(g) 2 HI(g), ada 3 pendekatan untuk mencapai sistem kesetimbangan (T=445 o. C, V=0, 8 L)
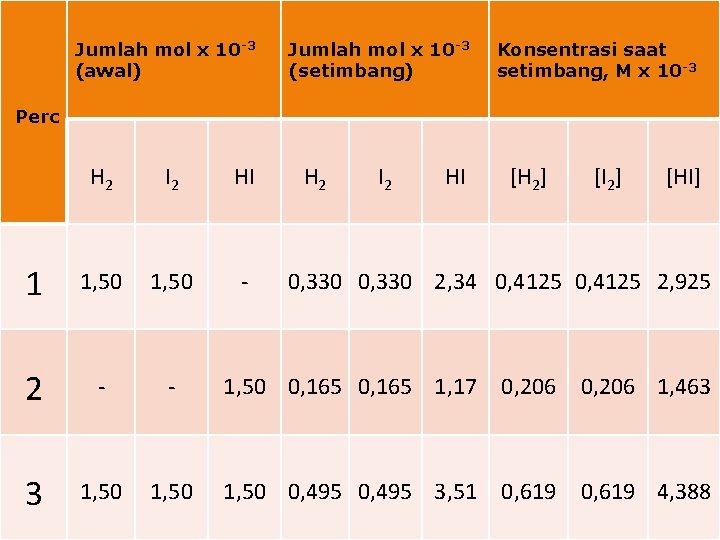
Jumlah mol x 10 -3 (awal) Jumlah mol x 10 -3 (setimbang) Konsentrasi saat setimbang, M x 10 -3 Perc H 2 I 2 HI [H 2] [I 2] [HI] 1 1, 50 - 2 - - 1, 50 0, 165 1, 17 0, 206 1, 463 3 1, 50 0, 495 3, 51 0, 619 4, 388 0, 330 2, 34 0, 4125 2, 925
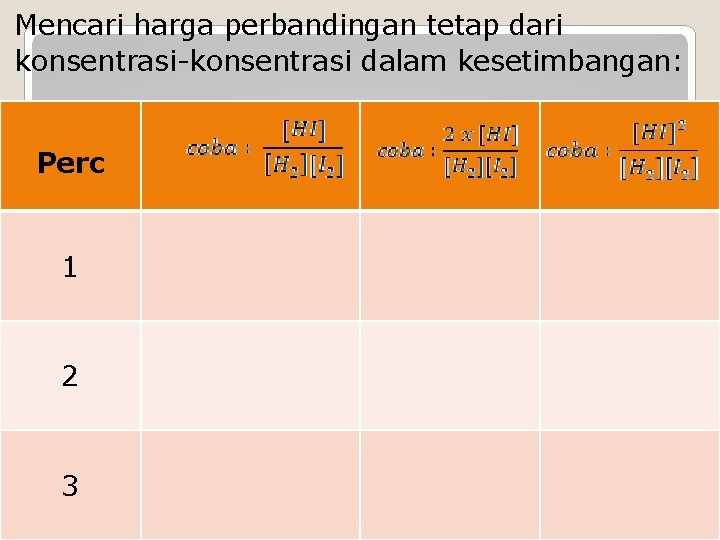
Mencari harga perbandingan tetap dari konsentrasi-konsentrasi dalam kesetimbangan: Perc 1 2 3

Persamaan yang memberikan hasil yang tetap : Kc = Konstanta kesetimbangan Perhatikan : pangkat 2 untuk HI, sama dengan koefisien stoikiometri, sehingga: a. A + b. B c. C + d. D (pada suhu tetap) (1864) Cato Maximillian Gulberg dan Peter Wage

Harga K diasumsikan lewat mekanisme satu tahap elementer : A + 2 B AB 2 Laju reaksi maju : Laju f = kf [A][B]2 Laju reaksi balik : kr [AB 2] Pada saat kesetimbangan :

Karena Kf dan Kr : konstanta pada suhu tertentu, perbandingannya juga adalah suatu konstanta = Kc K>>>1 : kesetimbangan jauh ke arah kanan/produk K<<<1 : kesetimbangan ke arah kiri/reaktan

Beberapa Cara Untuk Menyatakan Konstanta Kesetimbangan Konstanta reaktan dan produk dapat dinyatakan dalam satuan yang berbeda. Spesi yang bereaksi tidak selalu berada dalam fase sama ada lebih satu cara menyatakan “K”.

Kesetimbangan Homogen Contoh : N 2 O 4(g) 2 NO 2(g) 1. Kc : menyatakan bahwa konsentrasi spesi yang bereaksi dalam mol/L 2. Keterangan : PNO 2 dan PN 2 O 4 : tekanan parsial kesetimbangan (atm) Kp : menyatakan bahwa konsentrasi kesetimbangan dinyatakan dalam tekanan
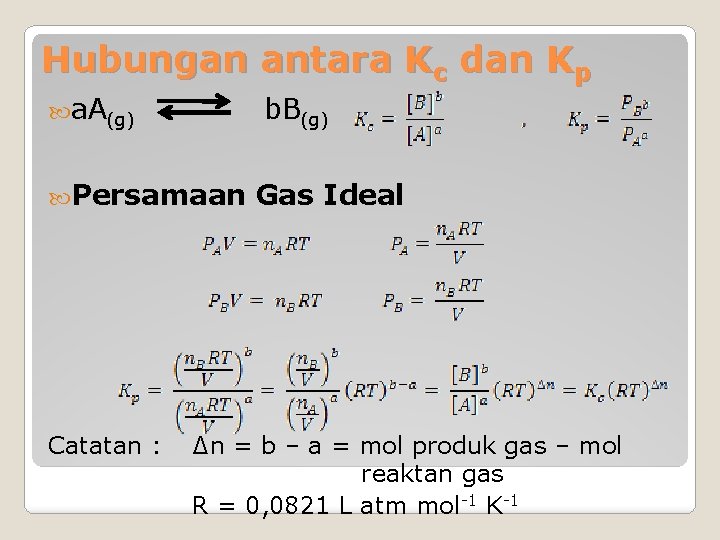
Hubungan antara Kc dan Kp a. A(g) b. B(g) Persamaan Catatan : Gas Ideal ∆n = b – a = mol produk gas – mol reaktan gas R = 0, 0821 L atm mol-1 K-1

Umumnya Kp ≠ Kc, kecuali ∆n = 0 Pada reaksi : CH 3 COOH(aq) + H 2 O(l) Catatan CH 3 COO-(aq) + H 3 O+(aq) : K tidak mempunyai satuan

Kesetimbangan Heterogen Contoh Catatan : Ca. CO 3(s) Ca. O(s) + CO 2(g) : konsentrasi padatan merupakan sifat intensif : tidak bergantung pada banyaknya zat yang ada sehingga [Ca. CO 3] dan [Ca. O] adalah konstanta

Hubungan yang melibatkan K Hubungan Kc dengan persamaan kimia setara 2 SO 2(g) + O 2(g) 2 SO 3(g) Kc = 2, 82 x 102, pada 1000 K 2 SO 3(g) 2 SO 2(g) + O 2(g) Kc =. . . ? SO 2(g) + ½ O 2(g) SO 3(g) Kc =. . . ?


Penggabungan K N 2(g) + O 2(g) 2 NO(g) Kc= 4, 1 x 10 -31. . . (1) N 2(g) + ½ O 2(g) N 2 O(g) Kc= 2, 4 x 10 -18. . . (2) N 2 O(g) + ½ O 2(g) 2 NO(g) Kc=. . . . ? (3)

Pers. (3) dicari (1) N 2(g) + O 2(g) (2) N 2 O(g) dengan : N 2(g) Bersih : N 2 O(g) + ½ O 2(g) Kc(3) =. . . . ? Kc(1) 2 NO(g) + ½ O 2(g) Kc(1)= 4, 1 x 10 -31 2 NO(g)

Menentukan nilai Tetapan Kesetimbangan “K” ditentukan melalui percobaan, misalnya : membekukan kesetimbangan, menurunkan suhu reaksi secara tiba-tiba sehingga reaksi berhenti. Untuk gas , K ditentukan dengan mengukur tekanan campuran.
Contoh 1: CH 4 dapat diperoleh dari gas CO dengan gas H 2 menurut persamaan : CO(g) + 3 H 2(g) CH 4(g) + H 2 O(g) Ke dalam suatu ruangan 10 L, mula-mula dimasukkan 1 mol gas CO, 3 mol gas H 2 dan katalis, kemudian dipanaskan hingga 1200 K. Setelah tercapai keadaan setimbang sistem dibekukan dan ternyata terdapat 0, 387 mol H 2 O a. Tentukan susunan kesetimbangan pada suhu 1200 K ! b. Harga K pada suhu tersebut !
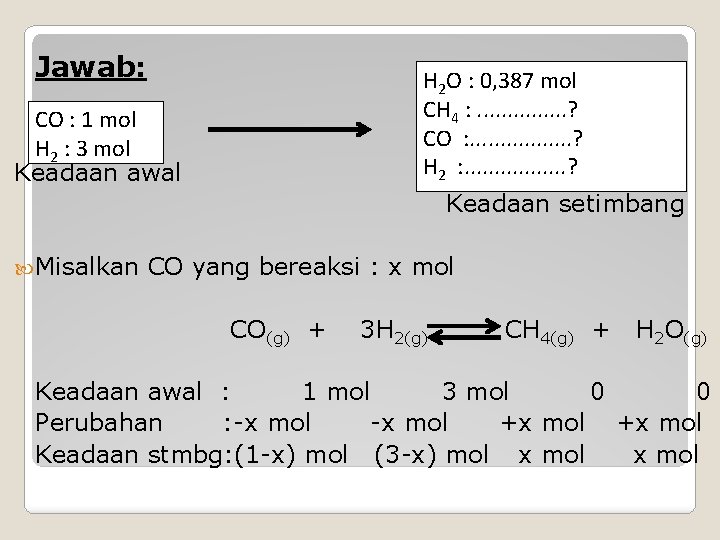
Jawab: H 2 O : 0, 387 mol CH 4 : . . . . ? CO : . . . . ? H 2 : . . . . ? CO : 1 mol H 2 : 3 mol Keadaan awal Keadaan setimbang Misalkan CO yang bereaksi : x mol CO(g) + 3 H 2(g) CH 4(g) + H 2 O(g) Keadaan awal : 1 mol 3 mol 0 0 Perubahan : -x mol +x mol Keadaan stmbg: (1 -x) mol (3 -x) mol x mol

Susunan kesetimbangan : CO = 1 - 0, 3897 mol =. . . . mol H 2 = 3 – (3. 0, 387) mol =. . . mol CH 4 =. . . mol H 2 O =. . . mol K =. . . Contoh 2: Sebanyak 10 mol gas N 2 dicampurkan dengan 40 mol gas H 2 dalam suatu ruangan 10 L, kemudian dipanaskan pada suhu 427 o C sehingga sebagian bereaksi membentuk NH 3 menurut kesetimbangan : N 2(g) + 3 H 2(g) 2 NH 3(g) ∆H = -92 k. J Apabila tekanan total campuran pada keadaan kesetimbangan adalah 230 atm, tentukan Kp dan Kc pada suhu 426 o C !

Jawab : Dengan persamaan gas ideal, jumlah mol gas dalam campuran dapat dihitung : Misal jumlah mol N 2 yang bereaksi adalah x mol, susunan kesetimbangan : N 2(g) + Keadaan awal : 10 mol Perubahan : -x mol Keadaan stmbg: (10 -x)mol 3 H 2(g) 40 mol -3 x mol (40 -3 x)mol 2 NH 3(g) 0 +2 x mol

Jumlah mol gas pada saat setimbang = 40 mol ( 10 -x ) + ( 40 -3 x ) + 2 x = 40 mol x =5 Susunan kesetimbangan : N 2 = (10 -5) mol = 5 mol; H 2 = (40 -15) mol = 25 mol; NH 3 = (2. 5) mol = 10 mol Perbandingan tekanan parsial gas sama dengan perbandingan mol Perbandingan gas N 2 : H 2 : NH 3 = 5 : 25 : 10 = 1 : 5 : 2 Jadi : PH 2 =. . . . . ? Kp =. . . . . ? PNH 3 =. . . . . ? Kc =. . . . . ?

Makna K a. Memberi informasi tentang posisi kesetimbangan Contoh : 2 H 2(g) + O 2(g) 2 H 2 O(g) Kc = 3 x 1081 pada 25 o. C Reaksi ini dapat dianggap : tuntas ke kanan ½ N 2(g) + ½ O 2(g) 2 NO(g) Kc = 1 x 10 -15 pada 25 o. C Reaksi ini hanya membentuk sedikit sekali gas NO Kc atau Kp >>> : reaksi ke kanan hampir sempurna Kc atau Kp <<< : reaksi ke kanan berlangsung sedikit

b. Mempredikasi arah reaksi Contoh : Kc untuk reaksi : H 2(g) + I 2(g) 2 HI(g) adalah 54, 3 pada 430 o. C. Dalam suatu percobaan dimasukkan 0, 234 mol H 2, 0, 146 mol I 2, dan 1, 98 mol HI dalam wadah 1 L pada suhu 430 o. C. Apakah campuran tersebut setimbang ? Bila tidak, ke arah mana reaksi bersihnya membentuk lebih banyak H 2 dan I 2 atau membentuk lebih banyak HI ?
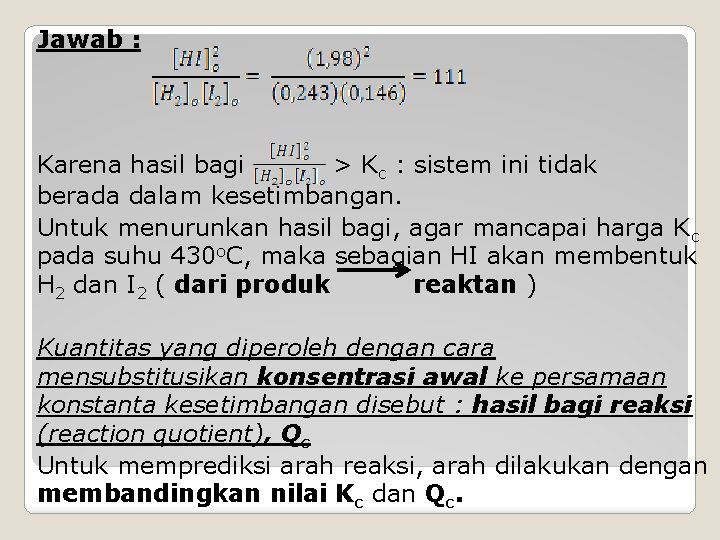
Jawab : Karena hasil bagi > Kc : sistem ini tidak berada dalam kesetimbangan. Untuk menurunkan hasil bagi, agar mancapai harga K c pada suhu 430 o. C, maka sebagian HI akan membentuk H 2 dan I 2 ( dari produk reaktan ) Kuantitas yang diperoleh dengan cara mensubstitusikan konsentrasi awal ke persamaan konstanta kesetimbangan disebut : hasil bagi reaksi (reaction quotient), Qc Untuk memprediksi arah reaksi, arah dilakukan dengan membandingkan nilai Kc dan Qc.
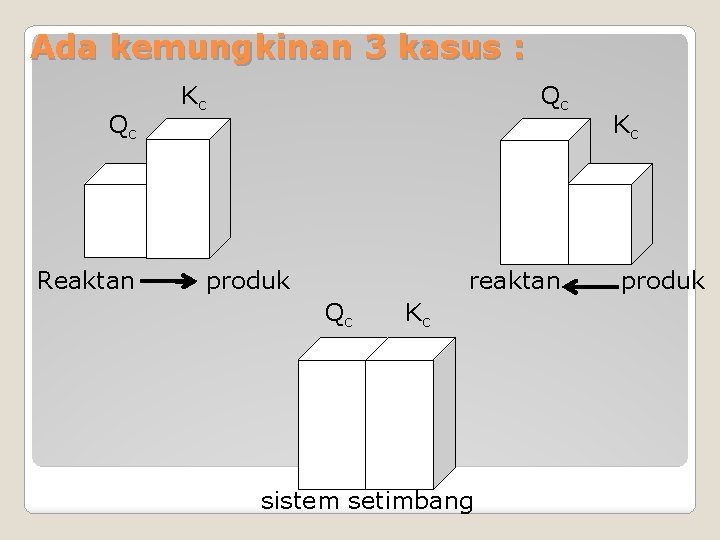
Ada kemungkinan 3 kasus : Qc Reaktan Kc Qc produk reaktan Qc Kc sistem setimbang Kc produk

Qc < Kc : Perbandingan konsentrasi awal produk terhadap reaktan terlalu kecil. Untuk mencapai kesetimbangan reaktan harus diubah menjadi produk. Sistem bergeser dari kiri ke kanan untuk mencapai kesetimbangan. Qc = Kc : Sistem berada pada kesetimbangan. Qc > Kc : Perbandingan konsentrasi awal produk terhadap reaktan terlalu besar. Untuk mencapai kesetimbangan produk harus diubah menjadi reaktan. Sistem bergeser dari kiri ke kanan untuk mencapai kesetimbangan.

Faktor-faktor yang mempengaruhi Kesetimbangan Perubahan kondisi percobaan dapat mengganggu kesetaraan dan menggeser posisi kesetimbangan Variabel percobaan yang dapat diatur : a. Konsentrasi b. Tekanan dan volume c. Suhu d. Katalis Asas Le Chatelier : “ Bila terhadap suatu kesetimbangan dilakukan suatu tindakan (aksi) maka sistem itu akan mengadakan reaksi yang cenderung mengurangi pengaruh aksi tersebut”.

Perubahan konsentrasi Jika konsentrasi salah satu komponen diperbesar, maka reaksi sistem adalah mengurangi komponen tersebut. Sebaliknya jika konsentrasi salah satu komponen diperkecil maka reaksi sistem adalah menambah komponen itu. Contoh : Pada sistem kesetimbangan : Fe. SCN 2+(aq Fe 3+(aq) + SCN-(aq) Merah kuning-pucat tak berwarna Ke arah mana kesetimbangan bergeser dan bagaimana perubahan warna campuran jika : a. Ditambahkan sedikit Na. SCN dalam larutan b. Ditambahkkan [Fe(NO 3)3] ke dalam larutan c. Ditambahkan sedikit kristal H 2 C 2 O 4 Jawab : . . . .

Pengaruh tekanan dan volume Jika dalam suatu sitem kesetimbangan sistem diperbesar atau volume diperkecil, maka kesetimbangan akan bergeser ke pihak reaksi yang jumlah koefisiennya kecil dan sebaliknya. Contoh : N 2(g) + 3 H 2(g) 2 NH 3(g) Ke arah manakah pergeseran kesetimbangan jika pada suhu tetap volume diperbesar (tekanan diperkecil) ? Jawab : . . .

Pengaruh suhu Jika pada suatu sistem kesetimbangan dinaikkan maka sistem kesetimbangan akan bergeser ke pihak reaksi yang menyerap kalor (endoterm) dan sebaliknya. Contoh : N 2 O 4(g) 2 NO 2(g)∆Ho = 58, 0 k. J Ke arah manakah reaksi bergeser jika suhu dinaikkan ? Jawab : . . . . Pengaruh katalis a. Katalis tidak mengubah K b. Mempercepat tercapainya keadaan setimbang

Kesetimbangan Dissosiasi adalah peristiwa penguraian suatu zat menjadi beberapa zat lain yang lebih sederhana dan peristiwa penguraiannya merupakan reaksi kesetimbangan. Contoh kesetimbangan dissosiasi gas : 2 H 2 O(g) 2 H 2(g) + O 2(g) 2 NH 3(g) N 2(g) + 3 H 2(g) N 2 O 4(g) 2 NO 2(g)

dissosiasi (α) : perbandingan mol zat yang berdissosiasi dengan mol zat mula-mula sebelum dissosiasi. Derajad Harga α berkisar dari 0 s/d 1 α = 0 : zat belum terdissosiasi α = 1 : zat berdissosiasi sempurna Kesetimbangan dissosiasi terjadi jika 0<α<1

Contoh 1 Dalam ruangan V liter dipanaskan a mol gas NH 3 sampai suhu tertentu hingga berdissosiasi dengan derajad dissosiasi sebesar α. Bagaimana susunan gas-gas pada saat kesetimbangan ? Jawab : Reaksi dissosiasinya : 2 NH 3(g) N 2(g) + 3 H 2(g) Mula-mula : a mol 0 0

Jika mula-mula terdapat a mol gas NH 3 dan derajad ionisasi α. Reaksi : 2 NH 3(g) N 2(g) + 3 H 2(g) Mula-mula : a mol 0 0 Perubahan : -aα mol ½ aα mol 3/2 aα mol Setimbang : a- aα mol ½ aα mol 3/2 aα mol =a(1 - α) mol Jadi susunan gas-gas pada saat setimbang : NH 3 : a(1 - α) mol N 2 : ½ aα mol H 2 : 3/2 aα mol

Contoh 2 Dalam ruang 5 L dipanaskan 0, 8 mol gas SO 3 sampai suhu tertentu hingga berdissosiasi sebagian setelah kesetimbangan tercapai, dalam ruang terdapat 0, 3 mol gas oksigen. Tentukan : Derajad ionisasi SO 3 Harga tetapan kesetimbangan K Jawab : . .

Kesetimbangan Dalam Industri Proses pembuatan gas amoniak menurut Haber-Bosch Prof. Fritz Haber (1868 -1934), Jerman, orang pertama yang berhasil mensintesis amoniak dari gas nitrogen dan hidrogen. Proses ini disempurnakan oleh Karl Bosch (1874 -1940). Reaksi : N 2(g) + 3 H 2(g) 2 NH 3(g) ∆H = -92, 6 k. J

1. Pengaruh suhu : suhu tinggi, bergeser ke kiri (endoterm), sehingga untuk memperoleh NH 3 max. suhu tidak boleh terlalu tinggi. 2. Pengaruh tekanan : jumlah koefisien kiri > kanan, maka jumlah NH 3 bertambah jika tekanan dinaikkan. 3. Pemakaian katalis : untuk mempercepat tercapainya kesetimbangan dipakai katalis : oksida-oksida besi.

Agar NH 3 yang dihasilkan maksimal : 1. Suhu tidak terlampau tinggi (sekitar 500 o. C) 2. Tekanan sangat tinggi : 500 – 1000 atm 3. Selama proses berlangsung : Gas N 2 dan H 2 ditambahkan secara terus menerus NH 3 yang dihasilkan dipisahkan dengan pengembunan sehingga reaksi bersih selalu bergeser ke kanan.
Proses pembuatan Asam sulfat melalui proses kontak Pembuatan H 2 SO 4 dengan cara mengoksidasi gas SO 2 dengan gas O 2 dari udara dengan katalis V 2 O 5 Reaksi : 2 SO 2(g) + O 2(g) 2 SO 3(g) ∆H = -98 k. J Tahap selanjutnya : SO 3 dilarutkan dalam H 2 SO 4 pekat membentuk pirosulfat H 2 SO 4(aq) + SO 3(aq) H 2 S 2 O 7(l) + H 2 O(l) 2 H 2 SO 4(aq)

Tahap penting : reaksi kesetimbangan dan eksoterm Agar reaksi max : a. Suhu 500 o. C b. Katalis : V 2 O 5 c. Tekanan 1 atm (sesungguhnya tekanan tinggi akan menguntungkan produksi SO 3, tetapi ternyata tidak diimbangi dengan hasil yang memadai)
- Slides: 45