Kesetimbangan dalam Sistem Nonideal Teori DebyeHuckel Struktur Larutan

Kesetimbangan dalam Sistem Non-ideal

Teori Debye–Huckel Struktur Larutan Ionik Encer Zarut dalam larutan encer nonelektrolit telah cukup dijelaskan secara termodinamik oleh persamaan, = 0 + RT ln m (7. 56) Potensial kimia adalah jumlah dari dua suku: yang pertama, 0, tidak bergantung pada komposisi, dan yang kedua bergantung pada komposisi. Persamaan (7. 56) cukup bagus untuk hampir semua nonelektrolit pada konsentrasi tidak lebih dari 0, 1 m, dan untuk kebanyakan yang lain ia tidak bagus bahkan pada konsentrasi yang tinggi. Pernyataan sederhana dalam persamaan (7. 56) tidak cukup bermanfaat untuk larutan elektrolit; ditemukan penyimpangan bahkan pada konsentrasi 0, 001 m, bahkan jika persamaan (7. 56) dimodifikasi untuk mengatasi perhitungan beberapa ion yang dihasilkan.




Dengan mengetahui nilai Ws, kita dapat memperoleh nilai Wi jika kita berhasil dalam menghitung W. Untuk menghitung W pertama kita harus menghitung a, lihat persamaan (7. 58). Sebelum mengerjakan perhitungan kita dapat memperkirakan secara beralasan bahwa Wi akan negative. Perhatikan suatu ion positif: ia menarik ion negative dan menolak ion positif lainnya. Sebagai hasilnya adalah ion negative, secara rata, sedikit lebih dekat ke ion positive dibanding ion positive yang lain. Hal ini berakibat ion memiliki energi Gibbs yang lebih rendah dibanding jika ia tidak bermuatan; itulah sebabnya kita tertarik pada energi relative terhadap spesies yang tidak bermuatan, Wi negative.
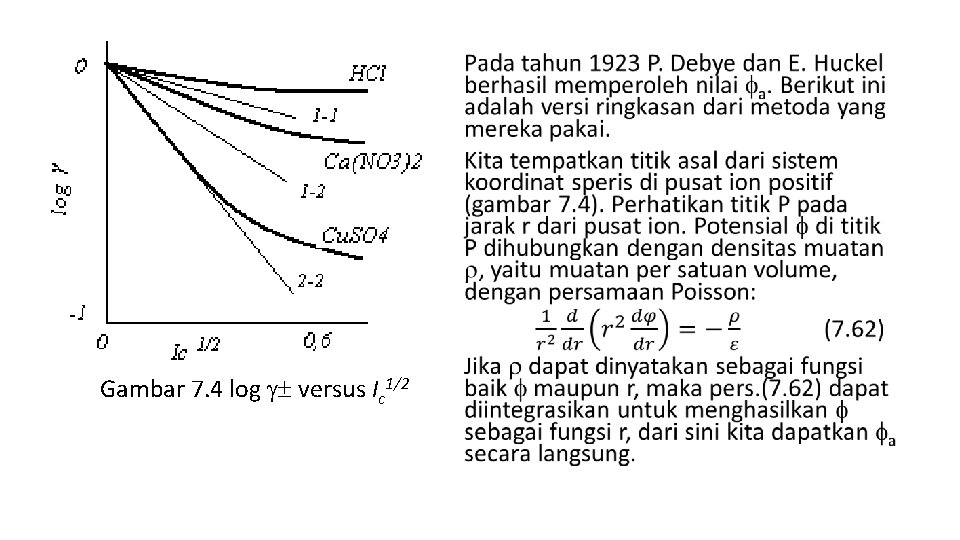
Gambar 7. 4 log versus Ic 1/2










Gambar 7. 4 menunjukkan variasi dari log 10 dengan Ic; kurva padat adalah data eksperimen; garis putus adalah nilai prediksi oleh hukum pembatas, persamaan (7. 82). Gambar 7. 4 log versus Ic 1/2

Pendekatan yang diperlukan dalam teori membatasi validitasnya, hanya terhadap larutan yang sangat encer. Dalam praktek, penyimpangan dari hukum pembatas menjadi cukup besar dalam konsentrasi antara 0, 005 sampai 0, 01 mol/L. Persamaan yang lebih akurat telah diturunkan hingga memperluas teori ke konsentrasi sedikit lebih tinggi. Tetapi, sebagaimana sebelumnya tidak ada persamaan teoritis yang cukup yang dapat memprediksi perilaku larutan dalam konsentrasi yang lebih tinggi dari 0, 01 mol/L Teori Debye-Huckel menyediakan suatu representasi yang akurat tentang perilaku terbatas dari koefisien aktifitas dalam larutan ionic encer. Selain itu, ia menghasilakn gambaran dari struktur larutan ionic. Kita telah menyinggung fakta bahwa awan ion negative sedikit lebih dekat ke ion positif daripada ion positif itu sendiri, yang terdesak menjauh. Dalam hal ini, setiap ion dikelilingi oleh atmosfir dari ion yang muatannya berlawanan; muatan total pada atmosfir ini adalah sama, tetapi tandanya berlawanan. Jejari rata dari atmosfir ionic ini adalah 1/x; yang disebut panjang Debye. Karena x berbanding lurus terhadap akar pangkat dua dari kekuatan ion, pada kekuatan ionic yang tinggi, atmosfir tersebut lebih dekat ke ion disbanding pada kekuatan ionic rendah. Konsep atmosfir ionic ini dan matematikanya dihubungkan dengan telah banyaknya manfaat yang luar biasa dalam menjelaskan banyak aspek dari perilaku larutan elektrolit.


Gambar 7. 5 Fungsi f (r) adalah fungsi distribusi muatan dalam atmosfir. Plot f (r) terhadap r tampak dalam gambar 7. 5. Maksimum pada kurva muncul pada rmax =1/x, panjang Debye. Dalam elektrolit bertipe valensi simetris, 1: 1; 2: 2; dan lainnya, kita boleh mengatakan bahwa f (r) merepresentasikan probabilitas persatuan tebal dr untuk menemukan kesetimbangan ion dalam lapisan speris pada jarak r dari pusat ion. Dalam larutan berkekuatan ionic tinggi penggabungan ke ion pusat sangat dekat, 1/x adalah kecil; pada kekuatan ionic yang lebih rendah 1/x adalah besar dan penggabungan menjauh.

Kesetimbangan dalam Larutan Ionik •



Pada persamaan yang terakhir, eksponensial telah diekspansikan dalam deret. Penghitungan untuk asam asetat 0, 1 molal, K = 1, 75 x 10 -5, menunjukkan bahwa derajat dissosiasi bertambah sekitar 4%. Pengaruh tersebut kecil karena dissosiasi tidak menghasilkan banyak ion. Jika sejumlah besar elektrolit inert, salah satunya tidak mengandung baik ion H+ maupun A-, ditambahkan ke dalam larutan asam lemah, lalu akan dihasilkan pengaruh yang cukup berarti pada dissosiasinya. Perhatikan larutan asam lemah dalam 0, 1 mol KCl, sebagai contoh. Kekuatan ionic larutan ini terlalu besar untuk menggunakan hukum pembatas, tetapi nilai dapat diestimasi dari Tabel 7. 1 Tabel tersebut menunjukkan bahwa untuk elektrolit 1: 1 nilai dalam 0, 1 molal larutan adalah kira 0, 8. Kita dapat mengasumsikan bahwa ini adalah nilai yang cukup beralasan untuk ion H+ dan A- dalam 0, 1 molal larutan KCl.



Soal-soal • Nilai Kf dalam larutan sukrosa (C 12 H 22 O 11) pada berbagai konsentrasi m/(mol/kg) 0, 10 0, 20 0, 50 1, 00 1, 50 2, 00 Kf/(K kg/mol) 1, 88 1, 90 1, 96 2, 06 2, 17 2, 30 a) Hitunglah aktifitas air dalam tiap larutan b) Hitunglah koefisien aktifitas air dalam tiap larutan c) Plotkan nilai a dan terhadap fraksi mol air dalam larutan d) Hitunglah aktifitas dan koefisien aktifitas sukrosa dalam 1 molal larutan. • Konstanta hukum Henry untuk chloroform dalam acetone pada 35, 17 o. C adalah 1, 99 jika tekanan uap adalah dalam atm, dan konsentrasi chloroform dalam fraksi mol. Tekanan parsial chloroform pada berbagai nilai fraksi mol adalah: XCHCl 3 0, 059 0, 123 0, 185 PCHCl 3 9, 2 20, 4 31, 9 Jika a = x, dan 1 jika x 0, hitunglah nilai a dan untuk chloroform dalam ketiga larutan itu.

• Pada konsentrasi yang sama seperti di soal no 2, tekanan parsial acetone adalah 323, 2; 299, 3; dan 275, 4 mm. Hg. Tekanan uap acetone murni adalah 344, 5 mm. Hg. Hitunglah aktifitas acetone dan koefisien aktifitas dalam ketiga larutan ini (a = = x, dan 1 jika x 1) • Kesetimbangan cair-uap dalam sistem, isopropil alkohol-benzena, dipelajari meliputi komposisi pada 25 o. C. Uapnya dapat dianggap gas ideal. X 1 adalah fraksi mol isopropil alcohol dalam cairan, dan p 1 adalah tekanan parsial alkohol dalam uap. Datanya adalah x 1 1, 000 0, 924 0, 836 P 1/mm. Hg 44, 0 42, 2 39, 5 a). Hitunglah aktifitas rasional dari isopropil alcohol pada x 1 = 1, 000, x 1 = 0, 924, dan x 1 = 0, 836 b). Hitunglah koefisien aktifitas rasional dari isopropil alcohol pada tiga komposisi di a). c) Pada x 1 = 0, 836 hitunglah jumlah yang dengannya potensial kimia alkohol berbeda dari jika ia dalam larutan ideal.

- Slides: 29