KESETIMBANGAN ASAMBASA Konstanta Hasil Kali Ionion Air H

KESETIMBANGAN ASAM-BASA Konstanta Hasil Kali Ion-ion Air H 2 O + H 2 O k H 3 O+(aq) + OH-(aq) Sangat kecil berarti konsentrasi H 2 O dapat dianggap konstan atau [H+] [OH-] Kw = (1, 2 x 10 -7) x (1, 0 x 10 -7) = 1, 0 x 10 -14 (25 o. C) 1
![Kriteria Larutan Asam, Basa dan Netral Jika [H+] > [OH-] Larutan asam [H+] = Kriteria Larutan Asam, Basa dan Netral Jika [H+] > [OH-] Larutan asam [H+] =](http://slidetodoc.com/presentation_image/45885dcf711659caffa317263106f588/image-2.jpg)
Kriteria Larutan Asam, Basa dan Netral Jika [H+] > [OH-] Larutan asam [H+] = [OH-] Larutan netral [H+] < [OH-] Larutan basa Contoh soal : Suatu sampel darah diketahui mempunyai [H+] = 4, 6 x 10 -8 M. Hitung konsentrasi molar [OH-] dan tentukan jenis larutan. Jawab : Kw 1, 0 x 10 -14 Maka [OH-] = [H+] [OH-] = 1, 0 x 10 -14 = 4, 6 x 10 -8 x [OH-] = 2, 2 X 10 -7 mol/L Latihan : Larutan baking soda Na. HCO 3 mempunyai [OH-] = 7, 8 x 10 -6 mol/L. Berapa [H+] ? Apakah bersifat asam, basa atau netral ? 2
![Konsep p. H adalah nilai – log [H+] atau p. H = - log Konsep p. H adalah nilai – log [H+] atau p. H = - log](http://slidetodoc.com/presentation_image/45885dcf711659caffa317263106f588/image-3.jpg)
Konsep p. H adalah nilai – log [H+] atau p. H = - log [H+] Jika p. H < 7 , larutan bersifat asam, p. H > 7 , larutan bersifat basa, p. H = 7 , larutan netral. Skala p. H beberapa larutan : Gambar. The p. H scale p. H Asam dan Basa Kuat Asam kuat dan basa kuat terdiossosiasi sempurna : p. H = -log [H+] Contoh : Berapa p. H larutan Na. OH 0, 0026 M (25 o. C) ? Jawab : p. OH = -log (2, 6 x 10 -3) = 3 -log 2, 6 = 2, 59 p. H = 14 – p. OH = 14 – 2, 59 = 11, 41 3

Latihan : Hitung p. H 0, 020 M HCl Pengukuran p. H dapat dilakukan dengan : p. H meter, kertas atau larutan indikator Tabel. p. H, [H+], [OH-], dan p. OHa 4
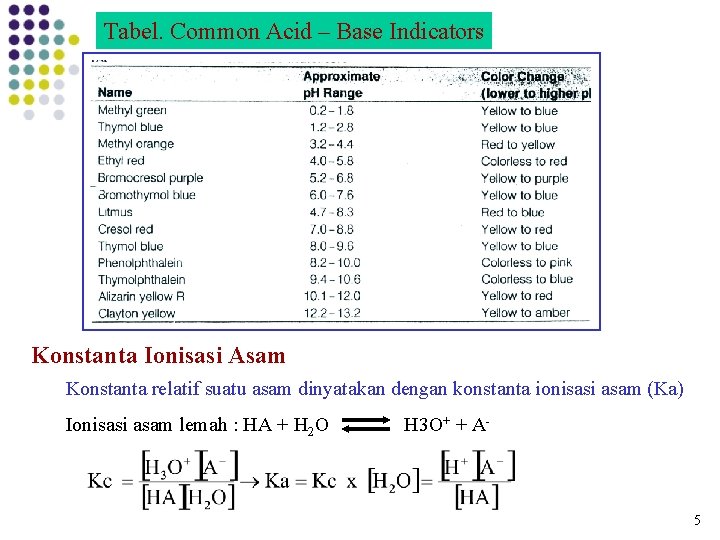
Tabel. Common Acid – Base Indicators Konstanta Ionisasi Asam Konstanta relatif suatu asam dinyatakan dengan konstanta ionisasi asam (Ka) Ionisasi asam lemah : HA + H 2 O H 3 O+ + A- 5

Tabel Kb Values for Basess 6

Contoh soal : p. H 0, 100 M larutan asam format pada 25 o. C adalah 2, 38. Hitung Ka ? Jawab : [H+] = 10 -p. H = 10 -2, 38 = 4, 2 x 10 -3 mol/L HCHO 2 H+ + CHO 2 Kons. Awal Perubahan Kons. Setimbang Ka < 10 -3 Ka > 1 Ka 1 - 10 -3 0, 100 -0, 0042 0, 096 0 +0, 0042 : asam lemah : asam kuat : asam sedang 7

Latihan : • Konsentrasi asam asetat / asam cuka adalah 0, 75 M. Hitung [H+] dan p. H nya. • Vitamin B, asam nikotinat HC 2 H 4 NO 2, merupakan asam lemah dengan Ka = 1, 4 x 10 -5. Berapakah [H+] dan p. H larutan 0, 010 M ? Persentase ionisasi asam lemah Jumlah HA yang terionisasi Persentase ionisasi = Jumlah HA awal Contoh soal : Berapakah persentase ionisasi asam asetat 0, 10 M ? (Ka = 1, 8 x 10 -5) 8
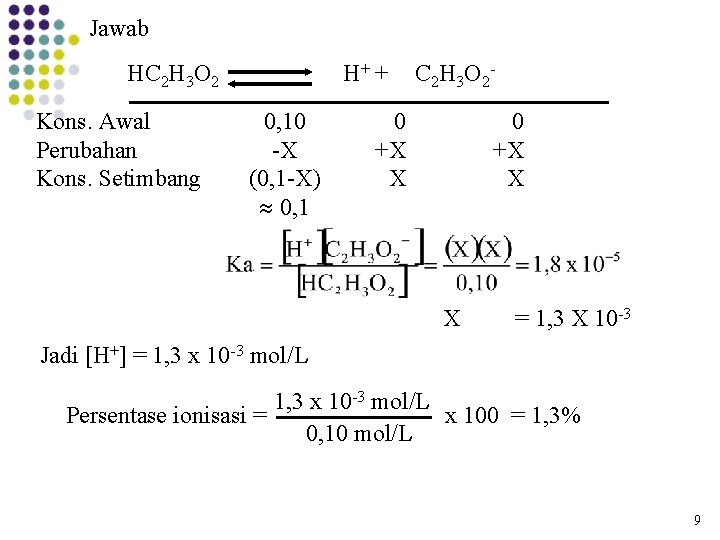
Jawab HC 2 H 3 O 2 Kons. Awal Perubahan Kons. Setimbang H+ + 0, 10 -X (0, 1 -X) 0, 1 C 2 H 3 O 2 - 0 +X X X = 1, 3 X 10 -3 Jadi [H+] = 1, 3 x 10 -3 mol/L Persentase ionisasi = x 100 = 1, 3% 0, 10 mol/L 9
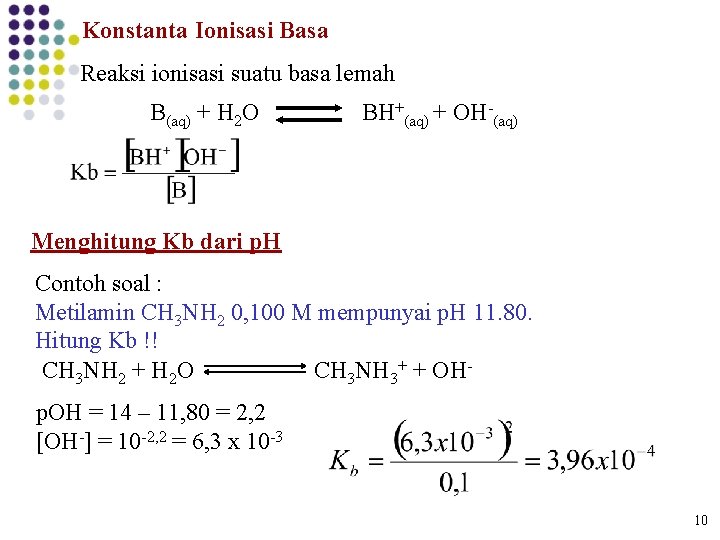
Konstanta Ionisasi Basa Reaksi ionisasi suatu basa lemah B(aq) + H 2 O BH+(aq) + OH-(aq) Menghitung Kb dari p. H Contoh soal : Metilamin CH 3 NH 2 0, 100 M mempunyai p. H 11. 80. Hitung Kb !! CH 3 NH 2 + H 2 O CH 3 NH 3+ + OHp. OH = 14 – 11, 80 = 2, 2 [OH-] = 10 -2, 2 = 6, 3 x 10 -3 10

p. Ka dan p. Kb p. Ka = -log Ka makin besar p. Ka, asam makin lemah p. Kb = -log makin besar p. Kb, basa makin lemah Ka x Kb = Kw (untuk pasangan asam – basa konjugat) • Basa konjugat suatu asam sangat lemah adalah basa relatif kuat • Asam konjugat suatu basa sangat kuat adalah basa relatif lemah Latihan : • HIO mempunyai p. Ka 10, 6. Pka HBr. O = 8, 64. Mana asam yang lebih lemah • p. Ka asam asetat pada suhu 25 o. C = 4, 47. Berapa p. Kb basa konjugatnya C 2 H 3 O 2 -. Tulis pers. Kesetimbangannya. 11

Buffer (Penyangga p. H) Larutan buffer : Larutan yang dapat mempertahankan p. H bila ditambahkan sedikit asam atau sedikit basa Umumnya terdiri atas : asam lemah HA dan basa konjugatnya Ap. H larutan Buffer atau 12

Kesetimbangan pada Larutan Buffer CH 3 COOH + H 2 O CH 3 COO- + H 3 O+ Jika rasio [HA]/[A-] meningkat maka [H 3 O+] meningkat Jika rasio [HA]/[A-] turun maka [H 3 O+] turun

Contoh soal : Suatu larutan buffer dibuat dengan cara mencampur 0, 11 M Na. C 2 H 3 O 3 (Na-asetat) dan asam asetat 0, 090 M. Hitung p. H ! Jawab : Kapasitas Buffer Adalah : Ukuran kemampuan buffer menahan perubahan p. H ditentukan oleh ukuran molaritas komponen-komponen yang terlibat 13

Contoh Soal • Hitung p. H larutan buffer terdiri dari 0, 50 M CH 3 COOH dan 0, 50 M CH 3 COONa • Berapa p. H setelah penambahan 0, 020 mol Na. OH padat kedalam 1 L larutan buffer diatas • Berapa p. Hsetelah penambahan 0, 20 mol HCl ke 1 L larutan buffer (a) Diketahui Ka = 1, 8 x 10 -5, asumsi volume tidak berubah CH 3 COOH + H 2 O Mula Berubah Setimbang 0, 50 -x 0, 50 -x - 0, 50 – x ≈ 0, 50 dan 0, 50 + x ≈ 0, 50 CH 3 COO- + H 3 O+ 0, 50 +x 0, 50+x
![(a) (b) Setelah penambahan 0, 020 mol Na. OH ke 1 L Larutan [OH-] (a) (b) Setelah penambahan 0, 020 mol Na. OH ke 1 L Larutan [OH-]](http://slidetodoc.com/presentation_image/45885dcf711659caffa317263106f588/image-16.jpg)
(a) (b) Setelah penambahan 0, 020 mol Na. OH ke 1 L Larutan [OH-] = 0, 020 mol/1 L = 0, 020 M CH 3 COOH + OHMula Tambahn Setelah th 0, 50 0, 48 0, 020 0 CH 3 COO- + H 2 O 0, 50 0, 52 0 -

CH 3 COOH + H 2 O Mula Berubah Setimbang 0, 48 -x 0, 48 -x - CH 3 COO- + H 3 O+ 0, 52 +x 0, 52+x 0 +x x Asumsi 0, 48 – x ≈ 0, 48 dan 0, 52 + x ≈ 0, 52 (c) Dengan cara yang sama p. H pada soal (c) menjadi 4, 70

Hidrolisis Ion - Ion • • • Anion asam lemah terhidrolisis, asam kuat tidak Logam golongan IA dan IIA (Kec. Be) tidak terhidrolisis Ion amonium terhidrolisis larutan sedikit asam p. H Larutan Garam Contoh : Hitung p. H larutan (K-asetat) 0, 15 M, Kb = 5, 7 x 10 -10 Jawab. C 2 H 3 O 2 - + H 2 O HC 2 H 3 O 2 + OHKonsentrasi Awal Perubahan 0, 15 -X Konsentrasi setimbang (0, 15 -X) 0, 15 0 +X (X+y) (X-y) 16

Maka x = 9, 2 x 10 -6 p. OH = -log (9, 2 x 10 -6) = 5, 04 maka p. H = 14 -5, 04 = 8, 96 Hidrilisis Anion Poliprotik Contoh soal : Hitung p. H larutan Na 2 CO 3 0, 15 M Jawab. CO 32 - + H 2 O HCO 3 - + OH- Konsentrasi Awal Perubahan 0, 15 -X 0 +X Konsentrasi setimbang (0, 15 -X) 0, 15 (X) 17
![[OH-] = 5, 7 x 10 -3 ; p. OH = -log (5, 7 [OH-] = 5, 7 x 10 -3 ; p. OH = -log (5, 7](http://slidetodoc.com/presentation_image/45885dcf711659caffa317263106f588/image-20.jpg)
[OH-] = 5, 7 x 10 -3 ; p. OH = -log (5, 7 x 10 -3) = 2, 24 maka p. H = 14 – 2, 24 = 11, 76 18
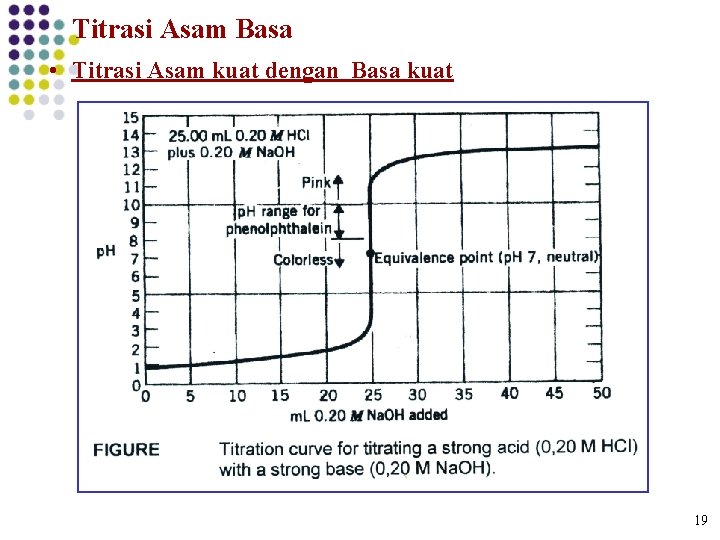
Titrasi Asam Basa • Titrasi Asam kuat dengan Basa kuat 1 19
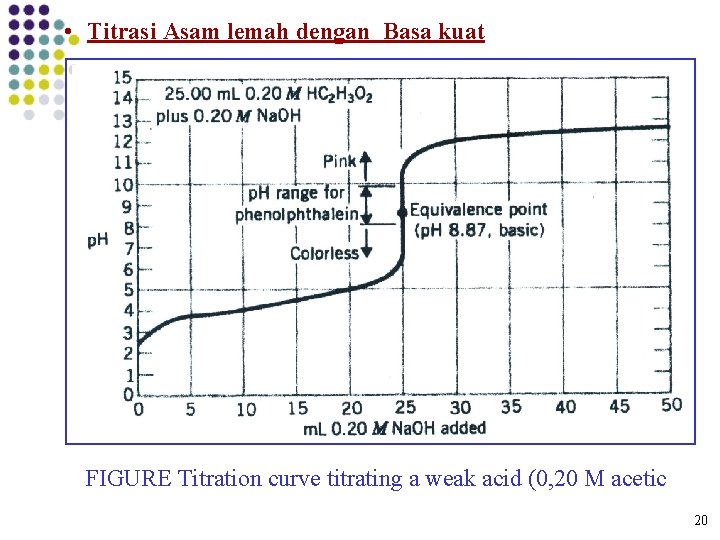
• Titrasi Asam lemah dengan Basa kuat FIGURE Titration curve titrating a weak acid (0, 20 M acetic 20
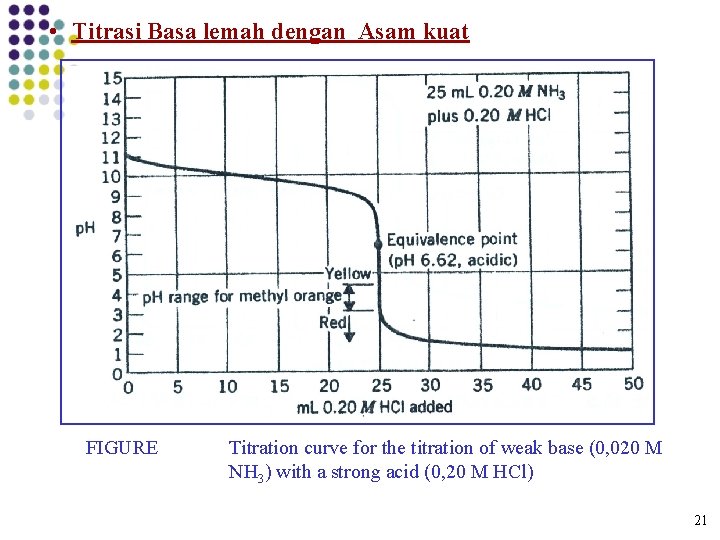
• Titrasi Basa lemah dengan Asam kuat FIGURE Titration curve for the titration of weak base (0, 020 M NH 3) with a strong acid (0, 20 M HCl) 21

Contoh soal : Hitung p. H larutan hasil sesudah 20, 00 m. L Na. OH 0, 2 M Ditambahkan dengan 25, 00 m. L HC 2 H 3 O 2 0, 2 M Jawab. Jml mol asam lar. Asal = 25 m. L asam x 0, 20 mol HC 2 H 3 O 2 1000 m. L asam = 0, 0050 mol HC 2 H 3 O 2 Jml mol Na. OH yang ditambahkan = 20, 00 m. L x 0, 20 mol Na. OH 1000 m. L larutan = 0, 0040 mol Na. OH Sisa asam : 0, 005 mol – 0 m 0040 mol = 0, 0010 mol HC 2 H 3 O 2 22

p. H larutan buffer Na-asetat : p. H = p. Ka + log = 4, 74 + log [anion] [asam] [0, 004] [0, 001] = 5, 34 23
![Kesetimbangan Kelarutan Ag. Cl (s) Ksp = [Ag+][Cl-] Mg. F 2 (s) Ag 2 Kesetimbangan Kelarutan Ag. Cl (s) Ksp = [Ag+][Cl-] Mg. F 2 (s) Ag 2](http://slidetodoc.com/presentation_image/45885dcf711659caffa317263106f588/image-26.jpg)
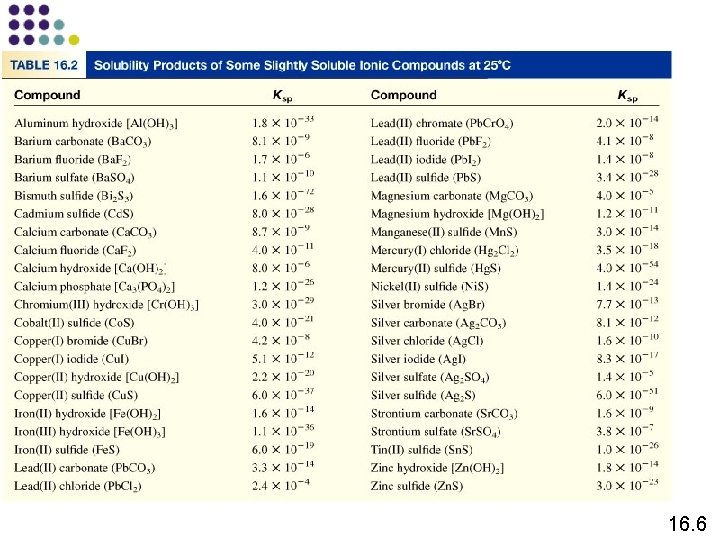
Kesetimbangan Kelarutan Ag. Cl (s) Ksp = [Ag+][Cl-] Mg. F 2 (s) Ag 2 CO 3 (s) Ca 3(PO 4)2 (s) Ag+ (aq) + Cl- (aq) Ksp adalah Konstanta hasil kali kelarutan Mg 2+ (aq) + 2 F- (aq) Ksp = [Mg 2+][F-]2 2 Ag+ (aq) + CO 32 - (aq) Ksp = [Ag+]2[CO 32 -] 3 Ca 2+ (aq) + 2 PO 43 - (aq) Ksp = [Ca 2+]3[PO 43 -]2 Pelarutan suatu padatan ionik dalam larutan aqueous: Q < Ksp Larutan tak jenuh Q = Ksp Larutan jenuh Q > Ksp Larutan lewat jenuh Tidak mengendap Terbentuk endapan 16. 6
16. 6
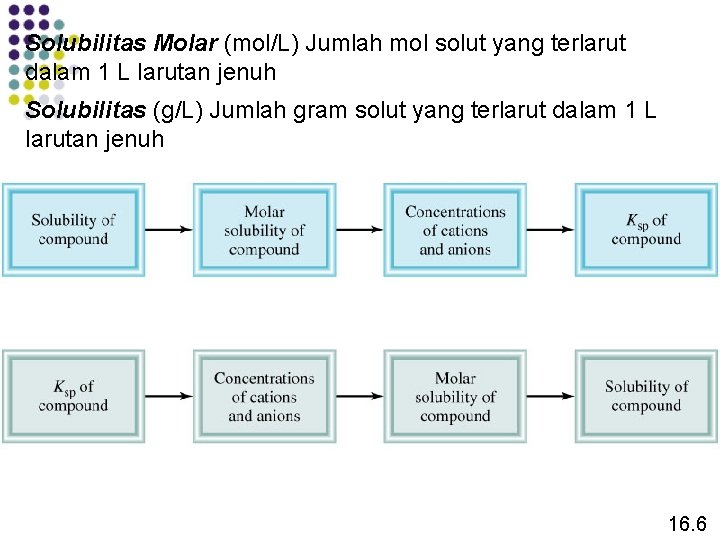
Solubilitas Molar (mol/L) Jumlah mol solut yang terlarut dalam 1 L larutan jenuh Solubilitas (g/L) Jumlah gram solut yang terlarut dalam 1 L larutan jenuh 16. 6

Berapa solubilitas of perak klorida dalam g/L ? Ag. Cl (s) Mula (M) Berubah (M) Equilibrium (M) [Ag+] = 1. 3 x 10 -5 M Ag+ (aq) + Cl- (aq) 0. 00 +s +s s s [Cl-] = 1. 3 x 10 -5 M Ksp = 1. 6 x 10 -10 Ksp = [Ag+][Cl-] Ksp = s 2 s = Ksp s = 1. 3 x 10 -5 mol Ag. Cl 143. 35 g Ag. Cl Solubilitas Ag. Cl = x = 1. 9 x 10 -3 g/L 1 L soln 1 mol Ag. Cl 16. 6
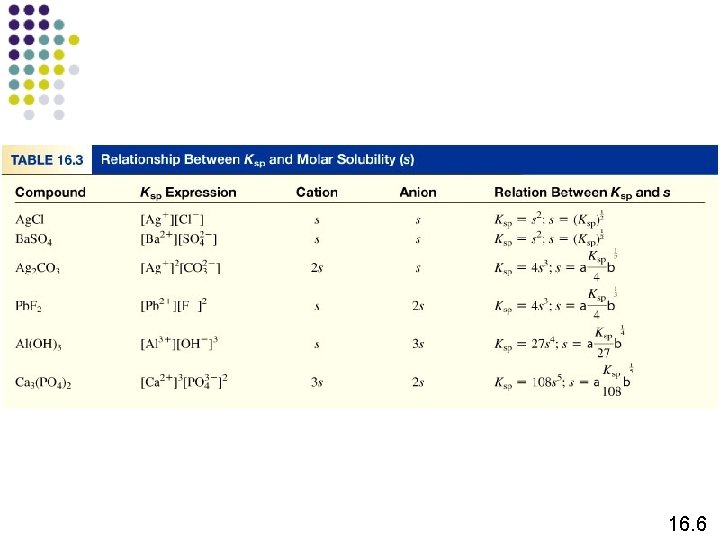
16. 6

Jika 2. 00 m. L larutan Na. OH 0. 200 M ditambahkan ke 1. 00 L larutan 0. 100 M Ca. Cl 2, Apakah akan terjadi pengendapan? Ion-ion yangada dalam larutan: Na+, OH-, Ca 2+, Cl-. Ca(OH)2 satu-satunya yang mungkin larut (aturan solubilitas). Apakah Q > Ksp for Ca(OH)2? [Ca 2+]0 = 0. 100 M [OH-]0 = 4. 0 x 10 -4 M Q = [Ca 2+]0[OH-]02 = 0. 10 x (4. 0 x 10 -4)2 = 1. 6 x 10 -8 Ksp = [Ca 2+][OH-]2 = 8. 0 x 10 -6 Q < Ksp Tidak ada precipitate yang terbentuk 16. 6

Berapa konsentrasi Ag yang dibutuhkan untuk mengendapkan HANYA Ag. Br dalam larutan yang mengandung baik Br- dan Cl- Pada konsentrasi 0. 02 M? Ag. Br (s) Ag+ (aq) + Br- (aq) Ksp = 7. 7 x 10 -13 Ksp = [Ag+][Br-] -13 K 7. 7 x 10 sp -11 M = = 3. 9 x 10 [Ag+] = 0. 020 [Br-] Ag. Cl (s) [Ag+] Ag+ (aq) + Cl- (aq) Ksp = 1. 6 x 10 -10 Ksp = [Ag+][Cl-] Ksp 1. 6 x 10 -10 -9 M = = 8. 0 x 10 = 0. 020 [Cl-] 3. 9 x 10 -11 M < [Ag+] < 8. 0 x 10 -9 M 16. 7

Pengaruh Ion Senama dan Solubilitas The presence of a common ion decreases the solubility of the salt. Berapa solubilitas molar Ag. Br dalam (a) air murni dan (b) 0. 0010 M Na. Br? Na. Br (s) Na+ (aq) + Br- (aq) Ag. Br (s) Ag+ (aq) + Br- (aq) [Br-] = 0. 0010 M Ksp = 7. 7 x 10 -13 Ag. Br (s) Ag+ (aq) + Br- (aq) s 2 = Ksp [Ag+] = s s = 8. 8 x 10 -7 [Br-] = 0. 0010 + s 0. 0010 Ksp = 0. 0010 x s s = 7. 7 x 10 -10 16. 8
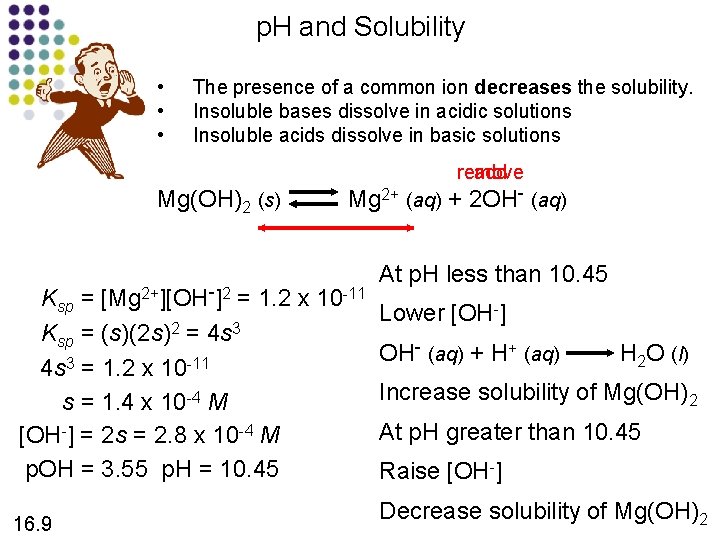
p. H and Solubility • • • The presence of a common ion decreases the solubility. Insoluble bases dissolve in acidic solutions Insoluble acids dissolve in basic solutions add remove Mg(OH)2 (s) Mg 2+ (aq) + 2 OH- (aq) Ksp = [Mg 2+][OH-]2 = 1. 2 x 10 -11 Ksp = (s)(2 s)2 = 4 s 3 = 1. 2 x 10 -11 s = 1. 4 x 10 -4 M [OH-] = 2 s = 2. 8 x 10 -4 M p. OH = 3. 55 p. H = 10. 45 16. 9 At p. H less than 10. 45 Lower [OH-] OH- (aq) + H+ (aq) H 2 O (l) Increase solubility of Mg(OH)2 At p. H greater than 10. 45 Raise [OH-] Decrease solubility of Mg(OH)2
- Slides: 34