Kesetimbangan Asam dan Basa 1 Sifatsifat AsamBasa Air

Kesetimbangan Asam dan Basa 1
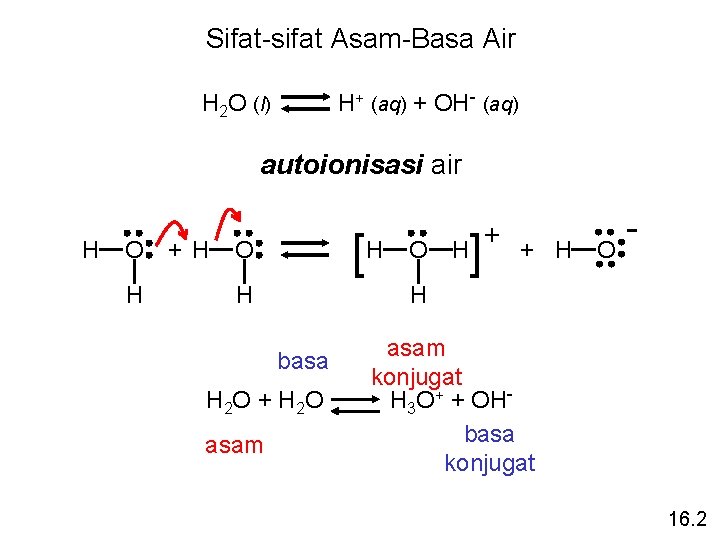
Sifat-sifat Asam-Basa Air H+ (aq) + OH- (aq) H 2 O (l) autoionisasi air H O H + H [H O H ] H + H O - H basa H 2 O + H 2 O asam O + asam konjugat H 3 O+ + OHbasa konjugat 16. 2
![Konstanta Hasilkali Ion Air H 2 O (l) H+ (aq) + OH- (aq) [H+][OH-] Konstanta Hasilkali Ion Air H 2 O (l) H+ (aq) + OH- (aq) [H+][OH-]](http://slidetodoc.com/presentation_image_h/9d3900c9f834f2ae633d11c1faaab4d3/image-3.jpg)
Konstanta Hasilkali Ion Air H 2 O (l) H+ (aq) + OH- (aq) [H+][OH-] Kc = [H 2 O] = konstan Kc[H 2 O] = Kw = [H+][OH-] Konstanta hasilkali ion air (Kw) adalah hasilkali antara konsentrasi molar ion H+ dan ion OH- pada suhu tertentu. Larutan bersifat [H+] = [OH-] netral Pada suhu 250 C Kw = [H+][OH-] = 1, 0 x 10 -14 [H+] > [OH-] asam [H+] < [OH-] basa
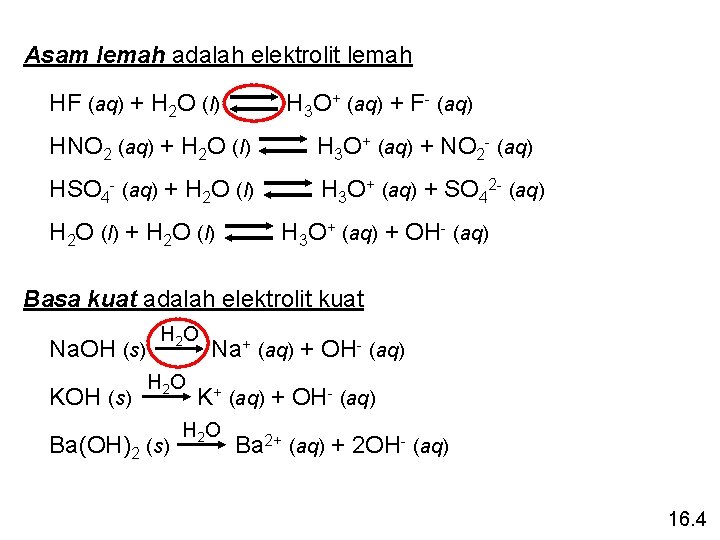
Asam lemah adalah elektrolit lemah HF (aq) + H 2 O (l) H 3 O+ (aq) + F- (aq) HNO 2 (aq) + H 2 O (l) H 3 O+ (aq) + NO 2 - (aq) HSO 4 - (aq) + H 2 O (l) H 3 O+ (aq) + SO 42 - (aq) H 2 O (l) + H 2 O (l) H 3 O+ (aq) + OH- (aq) Basa kuat adalah elektrolit kuat Na. OH (s) KOH (s) H 2 O Ba(OH)2 (s) Na+ (aq) + OH- (aq) K+ (aq) + OH- (aq) H 2 O Ba 2+ (aq) + 2 OH- (aq) 16. 4

Basa lemah adalah elektrolit lemah (NH 3) F- (aq) + H 2 O (l) NO 2 - (aq) + H 2 O (l) OH- (aq) + HF (aq) OH- (aq) + HNO 2 (aq) Pasangan asam-basa konjugat: • Jika asamnya kuat, basa konjugatnya sangat lemah. • H 3 O+ adalah asam terkuat yang dapat berada di dalam larutan berair. • Ion OH- adalah basa terkuat yang dapat berada di dalam larutan berair. 16. 4

16. 4
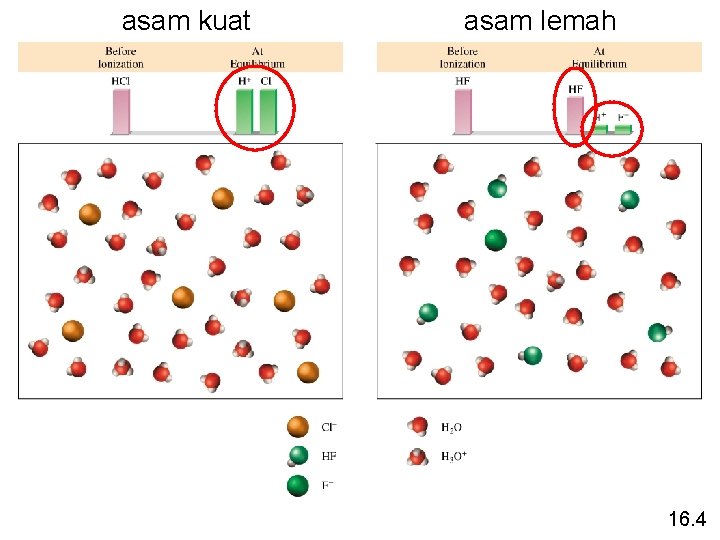
asam kuat asam lemah 16. 4
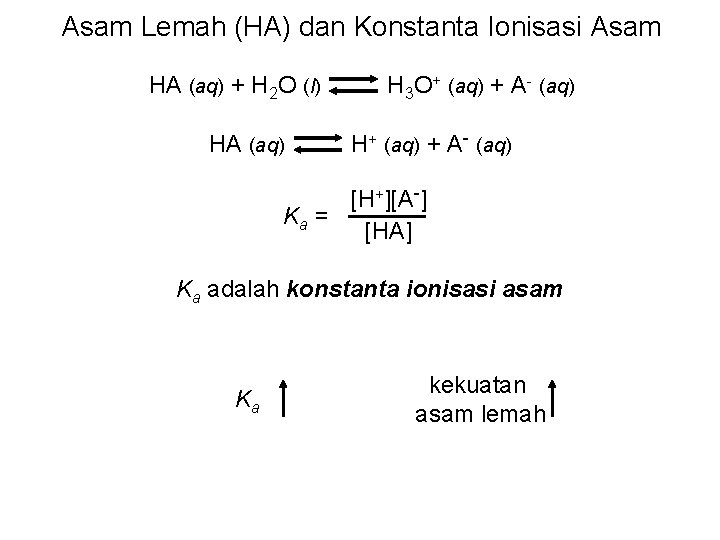
Asam Lemah (HA) dan Konstanta Ionisasi Asam HA (aq) + H 2 O (l) HA (aq) H 3 O+ (aq) + A- (aq) H+ (aq) + A- (aq) [H+][A-] Ka = [HA] Ka adalah konstanta ionisasi asam Ka kekuatan asam lemah

16. 5
![Berapakah p. H dari larutan 0, 5 M HF (pada 250 C)? +][F-] [H Berapakah p. H dari larutan 0, 5 M HF (pada 250 C)? +][F-] [H](http://slidetodoc.com/presentation_image_h/9d3900c9f834f2ae633d11c1faaab4d3/image-10.jpg)
Berapakah p. H dari larutan 0, 5 M HF (pada 250 C)? +][F-] [H = 7, 1 x 10 -4 Ka = HF (aq) H+ (aq) + F- (aq) [HF] HF (aq) Awal (M) Perubahan (M) Akhir (M) 0, 50 0, 00 -x +x +x 0, 50 - x x 2 = 7, 1 x 10 -4 Ka = 0, 50 - x Ka H+ (aq) + F- (aq) x 2 = 7, 1 x 10 -4 0, 50 [H+] = [F-] = 0, 019 M [HF] = 0, 50 – x = 0, 48 M Ka << 1 0, 50 – x 0, 50 x 2 = 3, 55 x 10 -4 x = 0, 019 M p. H = -log [H+] = 1, 72

Kapan kita boleh menggunakan aproksimasi? Ka << 1 0, 50 – x 0, 50 Jika x lebih kecil daripada 5% dari konsentrasi awal. x = 0, 019 Lebih kecil dari 5% 0, 019 M x 100% = 3, 8% 0, 50 M Aproksiomasi ok. Berapakah p. H dari larutan 0, 05 M HF (pada 250 C)? x 2 Ka = 7, 1 x 10 -4 x = 0, 006 M 0, 05 Lebih dari 5% 0, 006 M x 100% = 12% 0, 05 M Aproksimasi tidak ok. Harus menggunakan persamaan kuadrat atau metode pendekatan berjenjang untuk mencari nilai x.

Menyelesaikan Soal-soal ionisasi asam lemah: 1. Tentukan spesi-spesi yang dapat mempengaruhi p. H. • Pada sebagian besar soal, anda dapat mengabaikan autoionisasi air. • Abaikan [OH-] karena p. H ditentukan oleh [H+]. 2. Nyatakan konsentrasi kesetimbangan dari semua spesi dalam konsentrasi awal dan satu variabel x. 3. Tulis Ka dalam konsentrasi-konsentrasi kesetimbangannya. Setelah mengetahui nilai Ka, kita dapat mencari x. 4. Hitunglah konsentrasi dari semua spesi dan/atau p. H larutan. 16. 5

Berapakah p. H dari 0, 122 M asam monoprotik yang nilai Ka-nya 5, 7 x 10 -4? Awal (M) Perubahan (M) Akhir (M) HA (aq) H+ (aq) + A- (aq) 0, 122 0, 00 -x +x +x 0, 122 - x x 2 = 5, 7 x 10 -4 Ka = 0, 122 - x Ka x 2 = 5, 7 x 10 -4 0, 122 0, 0083 M x 100% = 6, 8% 0, 122 M Ka << 1 0, 122 – x 0, 122 x 2 = 6, 95 x 10 -5 x = 0, 0083 M Lebih dari 5% Aproksimasi tidak ok.

x 2 = 5, 7 x 10 -4 Ka = 0, 122 - x ax 2 + bx + c =0 x = 0, 0081 Awal (M) Perubahan (M) Akhir (M) x 2 + 0, 00057 x – 6, 95 x 10 -5 = 0 -b ± b 2 – 4 ac x= 2 a x = - 0, 0081 HA (aq) H+ (aq) + A- (aq) 0, 122 0. 00 0, 00 -x +x +x 0, 122 - x x x [H+] = x = 0, 0081 M p. H = -log[H+] = 2, 09
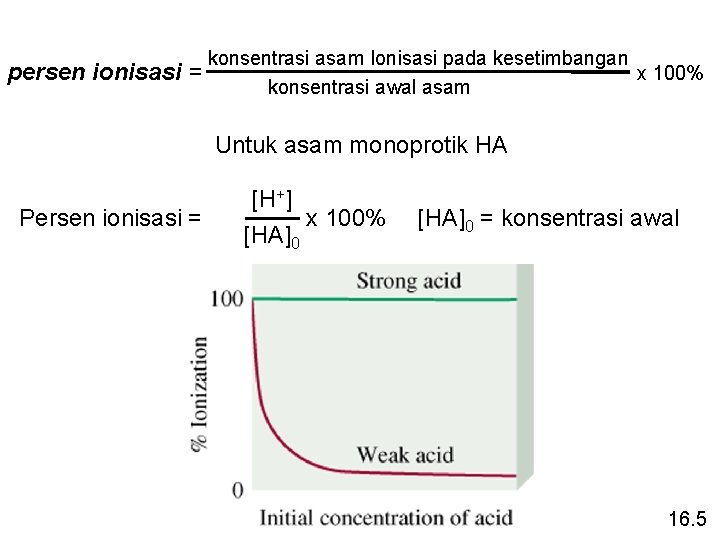
persen ionisasi = konsentrasi asam Ionisasi pada kesetimbangan x 100% konsentrasi awal asam Untuk asam monoprotik HA Persen ionisasi = [H+] [HA]0 x 100% [HA]0 = konsentrasi awal 16. 5
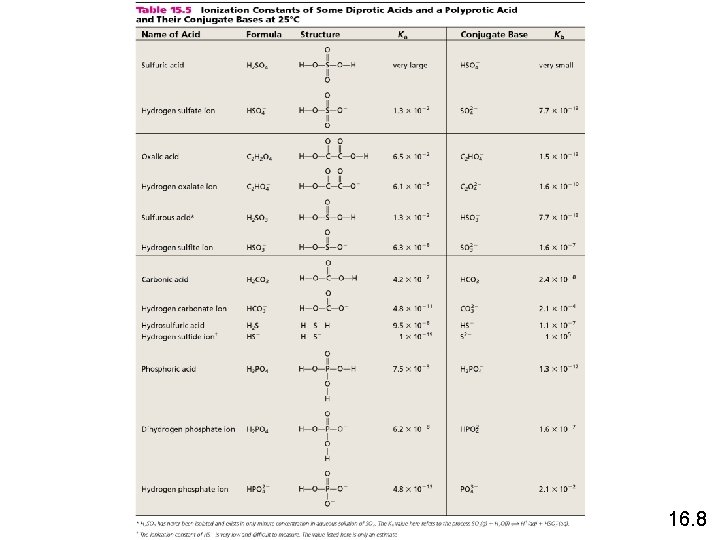
16. 8
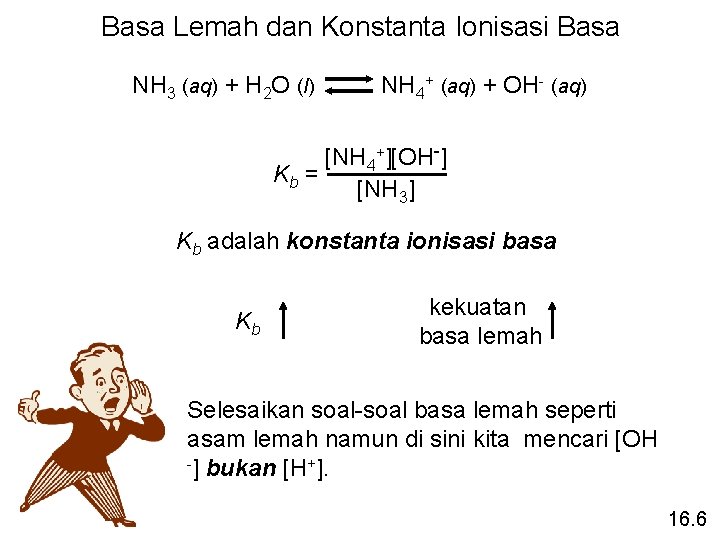
Basa Lemah dan Konstanta Ionisasi Basa NH 3 (aq) + H 2 O (l) NH 4+ (aq) + OH- (aq) [NH 4+][OH-] Kb = [NH 3] Kb adalah konstanta ionisasi basa Kb kekuatan basa lemah Selesaikan soal-soal basa lemah seperti asam lemah namun di sini kita mencari [OH -] bukan [H+]. 16. 6

Konstanta disosiasi-basa Kb mengacu pada kesetimbangan yang terjadi ketika basa lemah ditambahkan ke dalam air. Amonia dan amina adalah molekul-molekul yang paling umum yang bertindak sebagai basa lemah. Sebagian besar anion bertindak sebagai basa lemah.
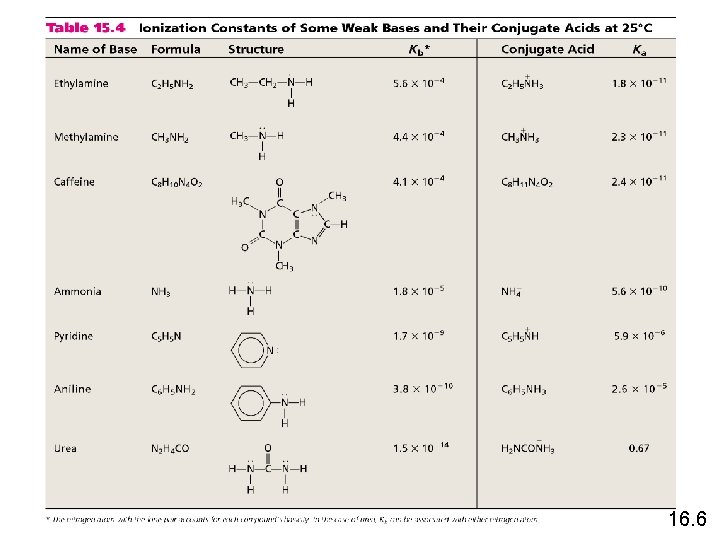
16. 6
![Menentukan p. H dari Kb dan [B] awal Soal: Amonia adalah zat pembersih yang Menentukan p. H dari Kb dan [B] awal Soal: Amonia adalah zat pembersih yang](http://slidetodoc.com/presentation_image_h/9d3900c9f834f2ae633d11c1faaab4d3/image-20.jpg)
Menentukan p. H dari Kb dan [B] awal Soal: Amonia adalah zat pembersih yang paling umum digunakan dalam rumah tangga dan termasuk basa lemah, dengan Kb = 1, 8 x 10 -5. Berapakah p. H dari larutan 1, 5 M NH 3?
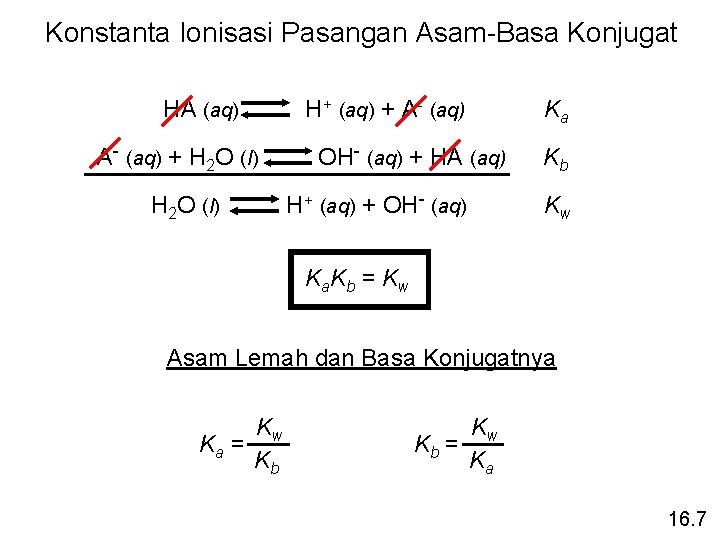
Konstanta Ionisasi Pasangan Asam-Basa Konjugat HA (aq) A- (aq) + H 2 O (l) H+ (aq) + A- (aq) OH- (aq) + HA (aq) H+ (aq) + OH- (aq) Ka Kb Kw K a. K b = K w Asam Lemah dan Basa Konjugatnya Kw Ka = Kb Kw Kb = Ka 16. 7

Semua anion dapat bekerja sebagai basa lemah kecuali anion yang merupakan basa konjugat dari asam kuat.

Menentukan p. H suatu Larutan Garam Soal: Natrium sianida dalam air dapat menghasilkan larutan basa. Berapakah p. H dalam larutan 0, 25 M Na. CN? Ka HCN = 4, 9 x 10 -10 Petunjuk: Kita harus mencari p. H larutan dari ion sianida, CN -, yang bertindak sebagai basa dalam air.

Reaksi antara anion atau kation suatu garam, atau keduanya, dengan air disebut hidrolisis garam. Hidolisis mempengaruhi p. H larutan garam. Kation: Semua kation akan menghasilkan asam dalam air kecuali kation dari golongan 1 dan 2. Anion: Beberapa bersifat asam HSO 4 Anion yg merupakan basa konjugat dari asam kuat bersifat netral. (Cl-, NO 3 -, …) Yang lainnya bersifat basa.
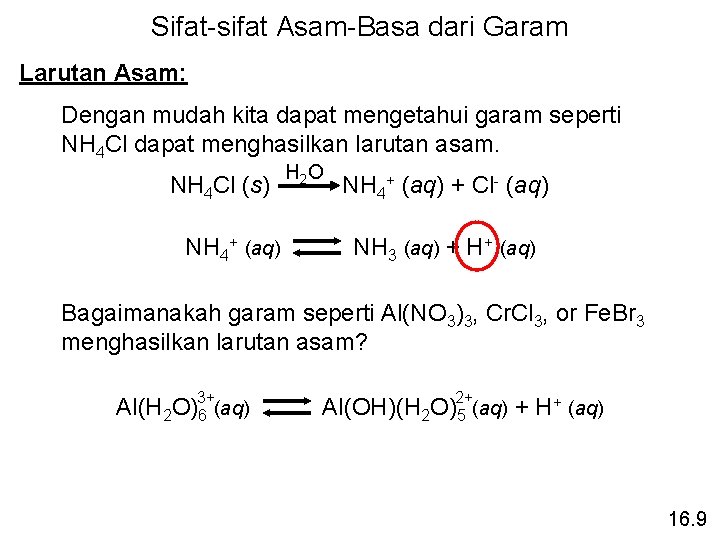
Sifat-sifat Asam-Basa dari Garam Larutan Asam: Dengan mudah kita dapat mengetahui garam seperti NH 4 Cl dapat menghasilkan larutan asam. NH 4 Cl (s) NH 4+ (aq) H 2 O NH 4+ (aq) + Cl- (aq) NH 3 (aq) + H+ (aq) Bagaimanakah garam seperti Al(NO 3)3, Cr. Cl 3, or Fe. Br 3 menghasilkan larutan asam? Al(H 2 O)3+ 6 (aq) + (aq) Al(OH)(H 2 O)2+ (aq) + H 5 16. 9
- Slides: 25