Keseimbangan Asam Basa Dra Asterina MS Teori Asam

Keseimbangan Asam Basa Dra. Asterina, MS
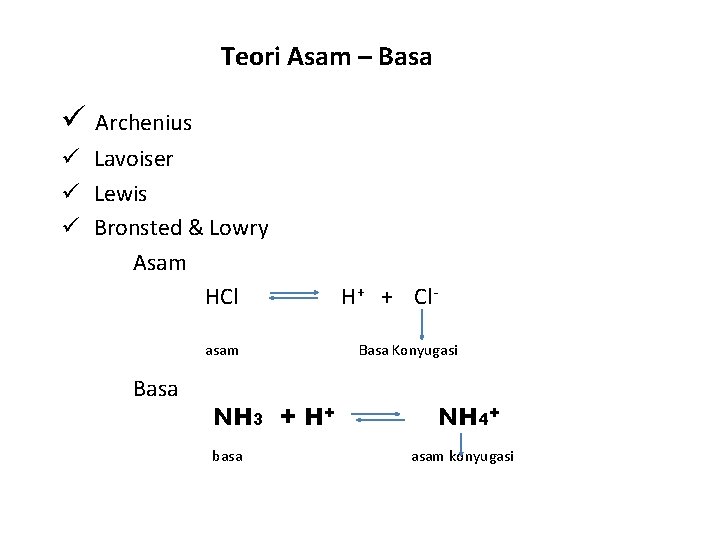
Teori Asam – Basa ü Archenius ü Lavoiser ü Lewis ü Bronsted & Lowry Asam HCl asam Basa NH 3 + H+ basa H+ + Cl. Basa Konyugasi NH 4+ asam konyugasi

Asam yang telah memberikan protonnya → Basa Konyugasi Basa yang telah menerima Proton → Asam Konyugasi

Tata Nama Asam : Ø Hx (tidak mengandung O) Ø Hox (mengandung O) HX : di berikan nama berdasarkan gugus sisa asam, di berikan akhiran ida contoh : HCL Asam klorida HOX : di beri nama sesuai nama asam utama, di berikan akhiran at Contoh: HCl. O 2 HCl. O 3 asam hipoklorit asam klorat asam utama asam perklorat

Basa : Ø HX (tanpa O) Ø HOX (mengandung O) HX : diberi nama sesuai nama trivial (penemu) contoh : NH 3 Amoniak HOX : diberi akhiran hidroksid contoh : Natrium hidroksida
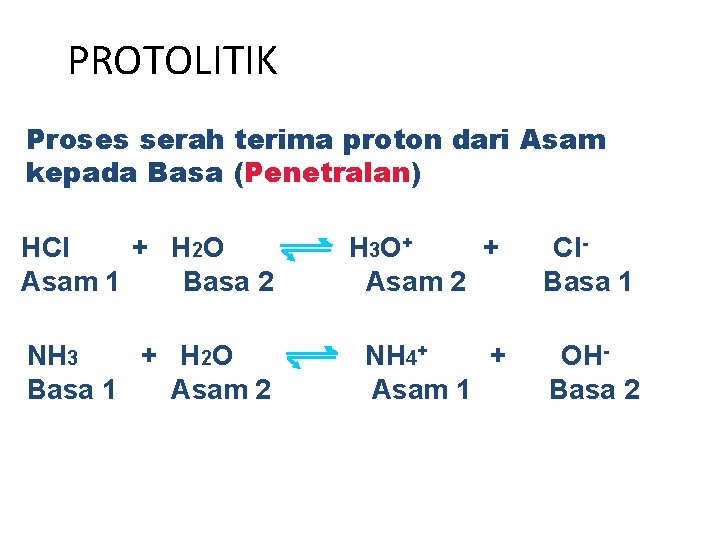
PROTOLITIK Proses serah terima proton dari Asam kepada Basa (Penetralan) HCl + H 2 O Asam 1 Basa 2 H 3 O + + Asam 2 Cl. Basa 1 NH 3 + H 2 O Basa 1 Asam 2 NH 4+ + Asam 1 OHBasa 2

Kekuatan Asam – Basa Asam HX (tidak mengandung O) HOX (mengandung O) Asam HX Ø Tergantung pada mudah atau tidak H+ lepas Ø Mudah atau tidak H+ lepas tergantung pada Sifat Elektronegatif contoh : H 3 P > H 2 S > HCl Ø Jari – jari atom contoh : HCl > HBr > HI

Asam HOX : Tergantung pada bilangan oksidasi unsur contoh : H 2 SO 4 > H 2 SO 3 Kekuatan asam juga tergantung pada nilai Ka Basa Tergantung pada sifat elektropositif unsur. contoh : Na. OH > Ca(OH)2 > N(OH)3

Mudah atau tidaknya H lepas tergantung pada : 1. Sifat Elektronegatif Dalam skala : Asam bertambah kuat bila X semakin elektronegatif. Contoh : HCl > H 2 S > H 3 P 2. Ukuran Jari – jari Dalam 1 golongan : Asam bertambah kuat bila jari - jari bertambah besar Contoh : HI > HCl > HF

Mudah atau tidaknya H lepas tergantung pada : q Sifat Elektromagnetik X * Bertambah kuat elektron ditarik dari H, bertambah mudah H lepas contoh : HOCl > HOBr > HO I q Untuk asam-asam yang berasal dari unsur non logam yang sama, kekuatan asam tergantung pada bil oksidasi unsur non logam yang terletak ditengah Contoh : H 2 SO 4 > H 2 SO 3

Kekuatan Asam juga ditentukan oleh tetapan asam (Ka) Hx Ka = H + + X(H+ ) (X- ) (Hx)
![Pengertian p. H = - log [ H+ ] PH = 7 → larutan Pengertian p. H = - log [ H+ ] PH = 7 → larutan](http://slidetodoc.com/presentation_image/0603eb70211b008e3e1c87acdfbc4222/image-12.jpg)
Pengertian p. H = - log [ H+ ] PH = 7 → larutan netral PH = < 7 → larutan asam PH = > 7 → larutan basa
![Perhitungan Ø Asam Kuat p. H = - Log [H+] contoh : p. H Perhitungan Ø Asam Kuat p. H = - Log [H+] contoh : p. H](http://slidetodoc.com/presentation_image/0603eb70211b008e3e1c87acdfbc4222/image-13.jpg)
Perhitungan Ø Asam Kuat p. H = - Log [H+] contoh : p. H HCl 0, 01 M = 2 p. H H 2 SO 4 0, 01 M = 2 – log 2 Ø Basa Kuat p. H = - Log [OH-] contoh : p. OH Na. OH 0, 001 M = 3 Ø Asam Lemah p. H = Contoh : p. H CH 3 COOH 0, 1 M (Ka = 10 -5) p. H = =3

Hidrolisis Garam di bagi atas 4 golongan : 1. Berasal dari asam kuat dan basa kuat contoh : Na. Cl tidak mengalami hidrolisis (p. H = 7) 2. Berasal dari asam kuat dan basa lemah contoh : NH 4 Cl (p. H < 7) 3. Berasal dari asam lemah dan basa kuat contoh : Na. CN (p. H > 7) 4. Berasal dari asam lemah dan basa lemah Garam ini mengalami hidrolisi total

Larutan Buffer Larutan yang mengandung : Ø Asam lemah dengan garamnya Ø Basa lemah dengan garamnya Asam lemah dengan garamnya : contoh : CH 3 COOH dengan CH 3 COONa [H+] = Ka. p. H = p. Ka + Log
![Basa lemah dengan garamnya contoh : NH 4 OH dengan NH 4 Cl [OH-] Basa lemah dengan garamnya contoh : NH 4 OH dengan NH 4 Cl [OH-]](http://slidetodoc.com/presentation_image/0603eb70211b008e3e1c87acdfbc4222/image-16.jpg)
Basa lemah dengan garamnya contoh : NH 4 OH dengan NH 4 Cl [OH-] = Kb. p. OH = p. Kb + log

Keseimbangan Asam Basa Dalam tubuh • Didalam tubuh gas CO 2 dapat berereksi dengan air membentuk asam karbonat, disamping itu asam dapat berasal dari proses metabolisme. • Asam ada yang mudah terurai dalam tubuh, misalnya H 2 CO 3 dan ada yang tidak dapat terurai, misalnya asam laktat • Keseimbangan asam basa dalam tubuh perlu dijaga, karena adanya perubahan ion Hidrogen atau p. H sedikit saja dari nilai normal dapat menyebabkan gangguan kesetimbangan dalam tubuh dan dapat menyebabkan kematian. Keseimbangan Asam Basa dalam tubuh tergantung pada konsentrasi ion H+ Konsentrasi ion Hidrogen cairan ekstraseluler dalam keadaan normal = 4 x 10 -8 M p. H = 7, 4 p. H normal darah arteri = 7, 4

Gangguan Keseimbangan asam Basa 1. 2. 3. 4. Asidosis metabolik Alkalosis metabolik Asidosis Respiratorik Alkalosis Respitorik Proses metabolisme Proses respirasi Asidosis metabolik dan alkalosis metabolik, salah satu penyebabnya karena ketidak seimbangan dalam pembentukan dan pembuangan asam basa oleh ginjal Asidosis respiratorik dan alkalosis respiratorik terutama Di sebabkan oleh kelainan pada pernafasan

Bila (H+) > (H+) normal dan p. H < p. H normal disebut Asidosis bila (H+) < (+) normal dan p. H > p. H disebut Alkalosis. Batas p. H yangmasih dapat ditanggulangi oleh tubuh adalah 7 – 8. Bila p. H < 7 dan > 8 dapat menyebabkan kematian.
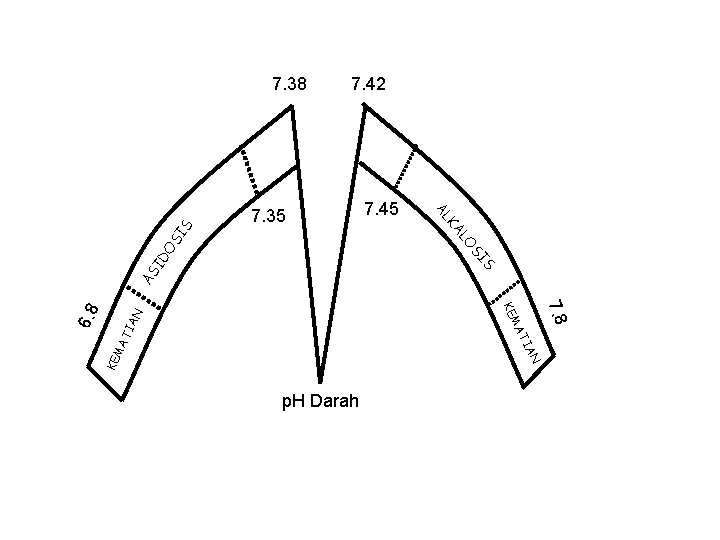
7. 42 OS O S AS ID SI AN KE N MA A TI TI MA p. H Darah 7. 8 KE 6. 8 7. 45 L KA 7. 35 AL IS 7. 38

Tubuh menggunakan 3 sistem untuk mengendalikan keseimbangan asam – basa yaitu: 1. Sistem Penyangga (Buffer) Ø Ø Mencegah perubahan ion Hidrogen secara berlebihan Dapat bekerja beberapa detik untuk mencegah perubahan ion Hidrogen 2. Sistem pernafasan Ø Ø Ø Mengatur perlepasan gas CO 2 melalui pernafasan Mengatur H 2 CO 3 dalam tubuh Memerlukan waktu beberapa menit Jika (H+) berubah, pusat pernapasan segera terangsang untuk mengubah kecepatan pengeluaran gas CO 2 dari cairan tubuh, sehingga (H+) kembali normal , memerlukan waktu 3 sampai 12 menit 3. Ginjal Ø Mengatur kelebihan asam atau basa Ø Bekerja beberapa jam sampai beberapa hari

Larutan Buffer dan fungsinya dalam tubuh Ø Buffer Bikarbonat (H 2 CO 3 / BHCo 3) Terdiri dari campuran H 2 CO 3 dan Na. HCO 3 Kelebihan H+ di ikat oleh HCO 3 H+ + HCO 3 H 2 CO 3 Buffer ini terdapat dalam semua cairan tubuh berperan penting dalam menunjang keseimbangan asam – basa Ø Buffer Protein Sangat penting untuk menetralkan kelebihan asam karbonat dalam plasma Protein + H+ H- Protein Ø Buffer Phosfat Terdiri dari binatrium dan mononatrium fosfat (Na 2 HPO 4 dan Na. H 2 PO 4 ). Sangat penting untuk sel darah merah dan ginjal H 3 PO 4= + H+ H 3 PO 4 -

Ø Buffer Hemoglobin Sangat penting untuk menetralkan kelebihan H 2 CO 3 dalam eritrosit carbonic CO 2 + H 2 O anhidrase H 2 CO 3 + Hb H 2 CO 3 HCO 3 - + H+Hb. O H 2 CO 3 + Hb. O 2 HCO 3 - + H+Hb. O Persamaan Henderson – Hassebalch Untuk sistem buffer bikarbonat CH 2 CO 3 / HCO 3[H+] = Ka. p. H = p. Ka + Log [HCO -] 3 [H CO ] 2 3

H 2 CO 3 berasal dari CO 2 + H 20 karena sebagian CO 2 terlarut dalam plasama di rubah menjadi H 2 CO 3 Konsentrasi CO 2 terlarut ekivalent dengan PCO 2 3 sehingga p. H = p. Ka + Log HCO S x PCO [ ] 2 S = Kons. Kelarutan PCO 2 = tekanan Parsial gas CO 2 PCO 2 = normal = 40 mm. Hg Dalam keadaan normal perbandingan antara [HCO 3 -] dengan H 2 CO 3 cairan ekstra celulair = 20 : 1
![Contoh soal : Bila di ketahui [HCO 3 -] = 24 M eq/liter PCO Contoh soal : Bila di ketahui [HCO 3 -] = 24 M eq/liter PCO](http://slidetodoc.com/presentation_image/0603eb70211b008e3e1c87acdfbc4222/image-25.jpg)
Contoh soal : Bila di ketahui [HCO 3 -] = 24 M eq/liter PCO 2 = 40 mm. Hg S = 0, 03 p. Ka = 6, 1 + Log 24 0, 03 x 40 p. H = p. Ka =p. Ka 6, 1 + Log 241, 2 =6, 1 +Log 120 = 7, 4 normal
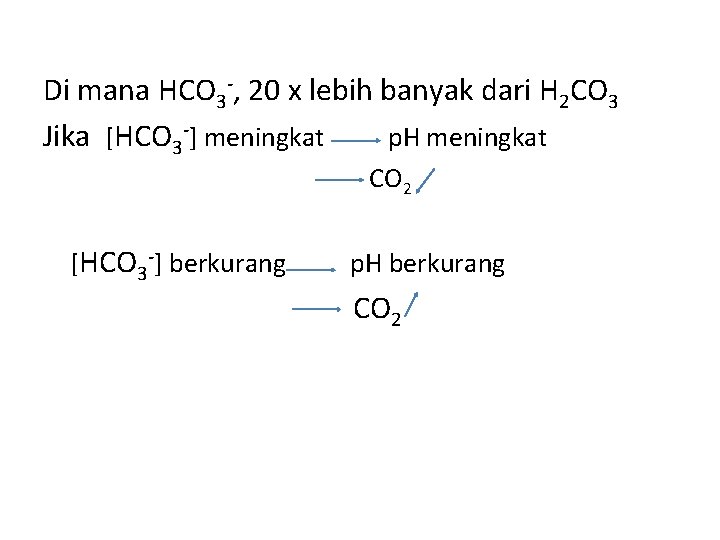
Di mana HCO 3 -, 20 x lebih banyak dari H 2 CO 3 Jika [HCO 3 -] meningkat p. H meningkat CO 2 [HCO 3 -] berkurang p. H berkurang CO 2

TERIMA KASIH
- Slides: 27