Kemisk jmvikt Lite fram och tillbaka HaberBoschmetoden Jmviktsekvationen

Kemisk jämvikt Lite fram och tillbaka
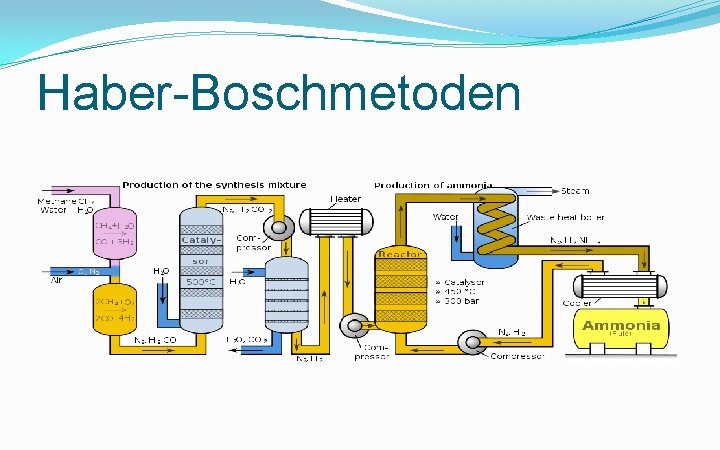
Haber-Boschmetoden

Jämviktsekvationen �Eller Guldberg-Waages lag (norrmän) �Eller massverkans lag

Jämviktsekvationen �Eller Guldberg-Waages lag (norrmän) �Eller massverkans lag �a. A

Jämviktsekvationen �Eller Guldberg-Waages lag (norrmän) �Eller massverkans lag �a. A + b. B

Jämviktsekvationen �Eller Guldberg-Waages lag (norrmän) �Eller massverkans lag �a. A + b. B ↔

Jämviktsekvationen �Eller Guldberg-Waages lag (norrmän) �Eller massverkans lag �a. A + b. B ↔ c. C

Jämviktsekvationen �Eller Guldberg-Waages lag (norrmän) �Eller massverkans lag �a. A + b. B ↔ c. C + d. D

Jämviktsekvationen �Eller Guldberg-Waages lag (norrmän) �Eller massverkans lag �a. A + b. B ↔ c. C + d. D

Jämviktsekvationen �Eller Guldberg-Waages lag (norrmän) �Eller massverkans lag �a. A + b. B ↔ c. C + d. D

Jämviktsekvationen �Eller Guldberg-Waages lag (norrmän) �Eller massverkans lag �a. A + b. B ↔ c. C + d. D �Sidan 60 i Fo. T

Exempel �N 2 + 3 H 2 ↔ 2 NH 3 � 2 SO 3 ↔ 2 SO 2+ O 2

Förändra jämvikten �Le Chateliers princip �Om man gör en förändring i ett system i jämvikt sker en nettoreaktion – en jämviktsförskjutning – så att förändringen motverkas.

Förändra jämvikten �Haber-Bosch-metoden: �N 2 + 3 H 2 ↔ 2 NH 3 �Öka trycket �En nettoreaktion sker åt höger eftersom antalet molekyler då minskar vilket sänker trycket �Därför bör man ha så högt tryck som är praktiskt möjligt: 300 bar

Förändra jämvikten �Haber-Bosch-metoden: �N 2 + 3 H 2 ↔ 2 NH 3 + 92 k. J �Öka temperaturen �En nettoreaktion sker åt vänster eftersom då tas energi upp �Därför bör man ha så låg temperatur som är praktiskt möjligt: 3 -400 °C

Katalysator �Förändrar inte jämviktens läge

Syra-bas-jämvikter

Definitioner �En syra är en protongivare �En bas är en protontagare

Syra-baspar �Mot varje syra svarar en bestämd bas �syra ↔ H+ + bas �HCl ↔ H+ + Cl– �H 2 O ↔ H+ + OH– �H 3 O+ ↔ H+ + H 2 O �NH 4+ ↔ H+ + NH 3
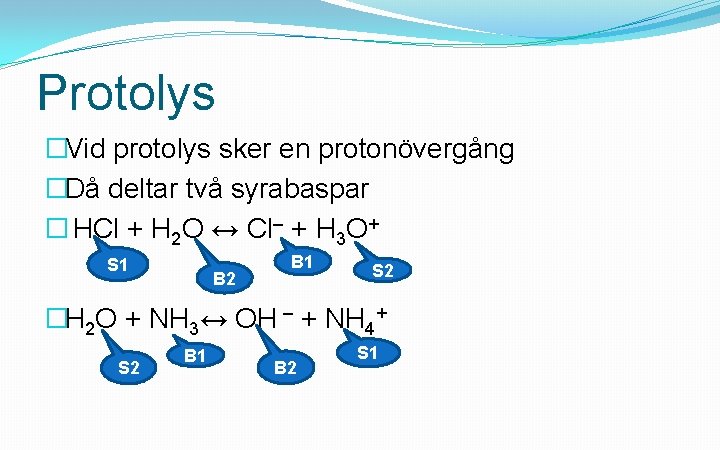
Protolys �Vid protolys sker en protonövergång �Då deltar två syrabaspar � HCl + H 2 O ↔ Cl– + H 3 O+ S 1 B 2 B 1 S 2 �H 2 O + NH 3↔ OH – + NH 4+ S 2 B 1 B 2 S 1

Syrakonstanten Ka �H 2 O + HA ↔ H 3 O+ + A– �Slå upp syrakonstant i ”Formler och Tabeller”

Beräkning �Vad blir p. H i en liter vatten om man sprutar ner 9 gram myrsyra i det?

Vattnets autoprotolys �Vid protolys sker en protonövergång �Då deltar två syrabaspar • H 2 O + H 2 O ↔ OH – + H 3 O+ S 1 B 2 B 1 S 2 �En amfolyt kan fungera både som syra och som bas �HCO 3 –
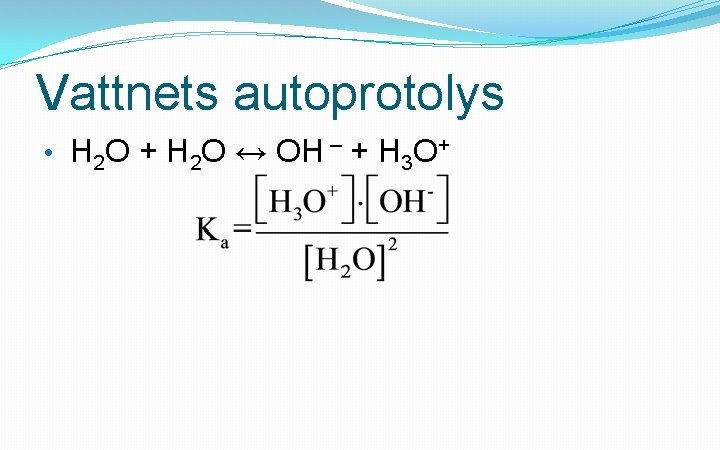
Vattnets autoprotolys • H 2 O + H 2 O ↔ OH – + H 3 O+

Vattnets autoprotolys • H 2 O + H 2 O ↔ OH – + H 3 O+ • Kw = 10 -14 (mol/dm 3)2
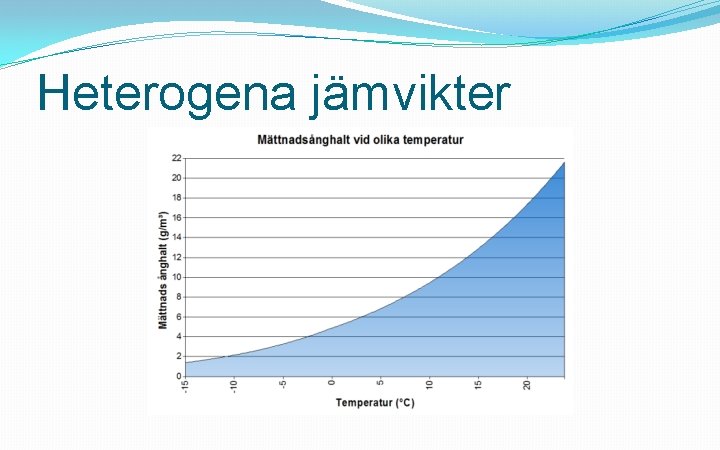
Heterogena jämvikter
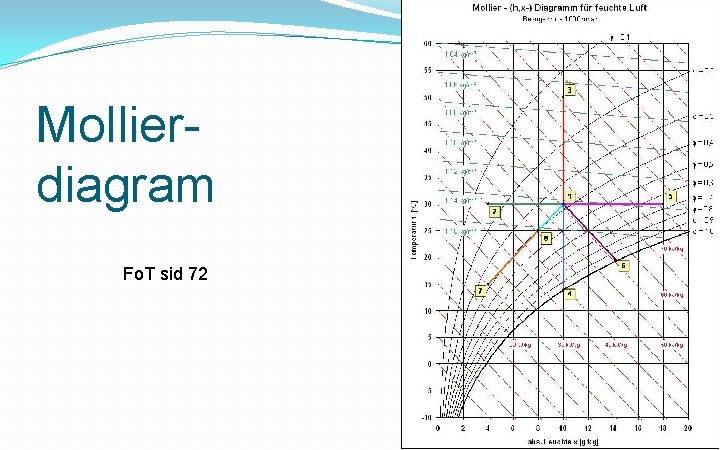
Mollierdiagram Fo. T sid 72
- Slides: 27