Kemi atommodeller isotop Syfte Knna till hur en










- Slides: 18

Kemi – atommodeller, isotop

Syfte • Känna till hur en atom är uppbyggd • Veta vilka partiklar påverkar atomens massa • Veta elektronernas roll i kemiska reaktioner • Kunna skriva formel på grundämnen och kemiska föreningar

Viktiga begrepp • Grundämne och kemisk förening • Elementpartiklar • Atom och jon • Laddning • Atomnummer • Masstal • Isotop

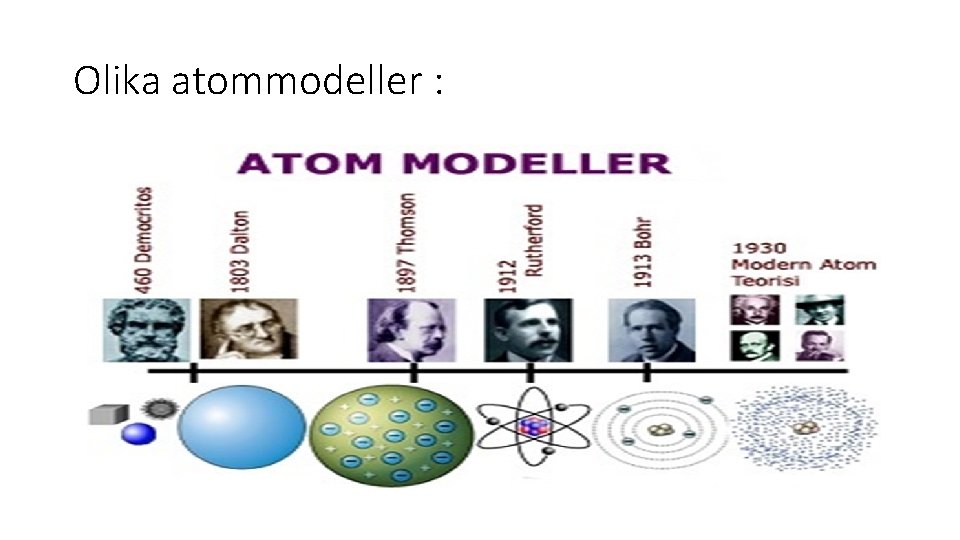
Olika atommodeller :

Att sortera atomer : • John Dalton 1805 : olika ämne har olika vikt • Jöns Jacob Berzelius 1818: tabell med relativa atomvikter • Dimitri Mendelejev 1869 : första periodiska systemet • Marie Curie - Sklodowska 1896 : Radioaktiviteten – atom är inte odelbar!

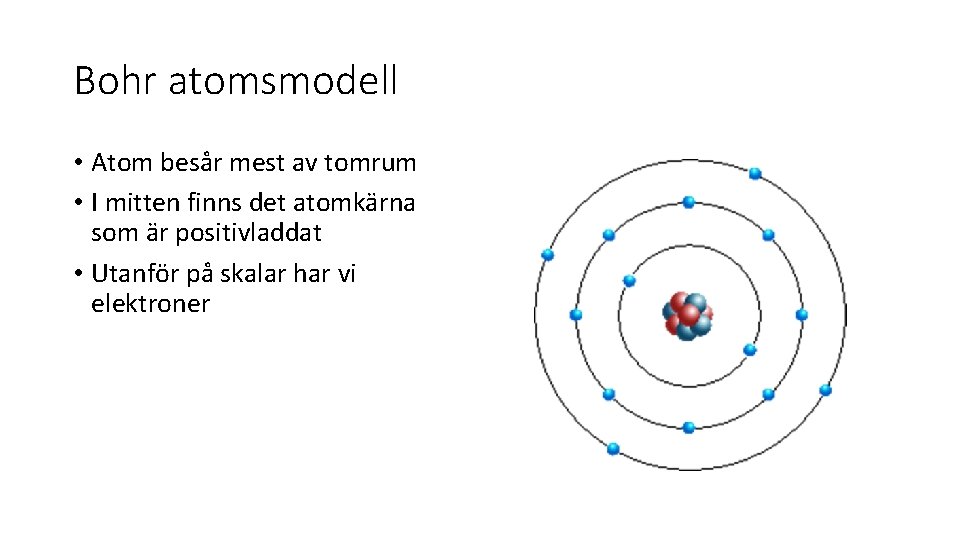
Bohr atomsmodell • Atom besår mest av tomrum • I mitten finns det atomkärna som är positivladdat • Utanför på skalar har vi elektroner

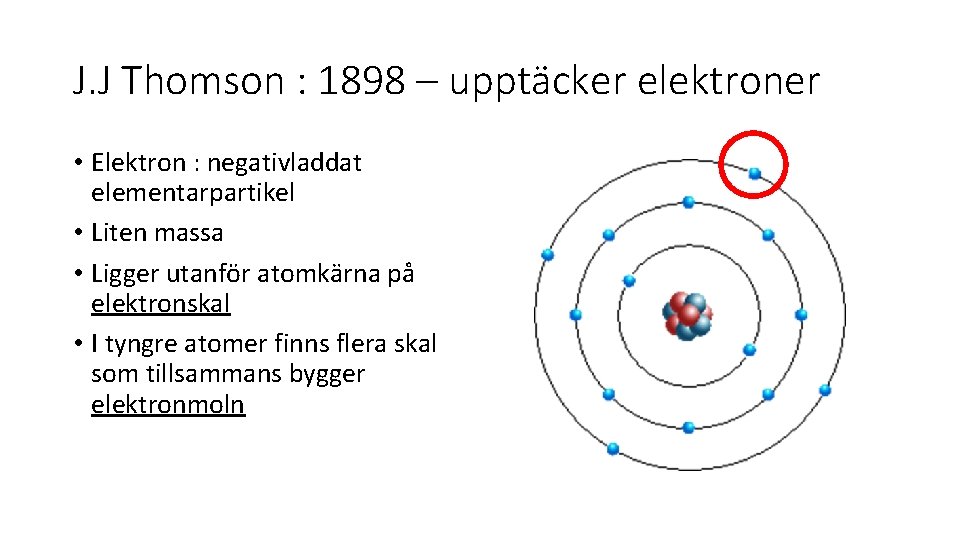
J. J Thomson : 1898 – upptäcker elektroner • Elektron : negativladdat elementarpartikel • Liten massa • Ligger utanför atomkärna på elektronskal • I tyngre atomer finns flera skal som tillsammans bygger elektronmoln

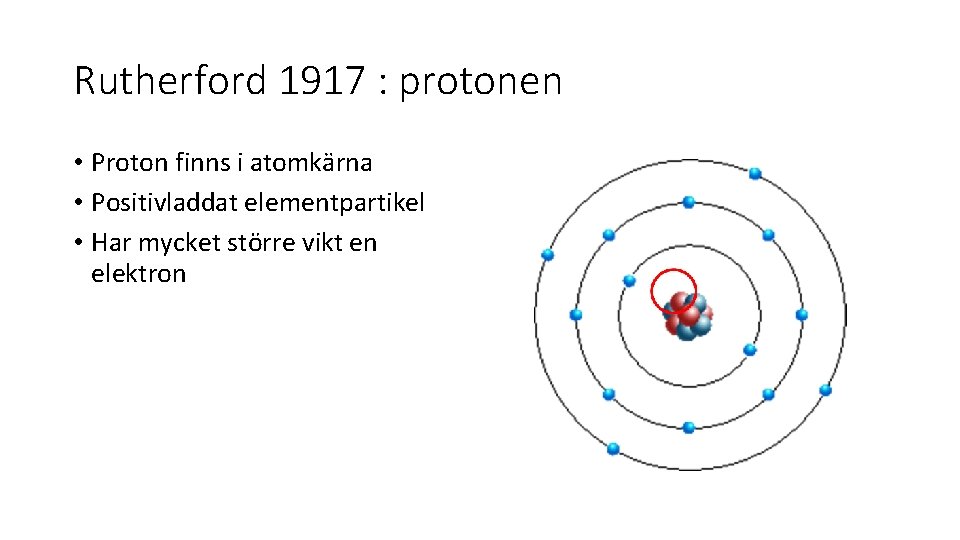
Rutherford 1917 : protonen • Proton finns i atomkärna • Positivladdat elementpartikel • Har mycket större vikt en elektron

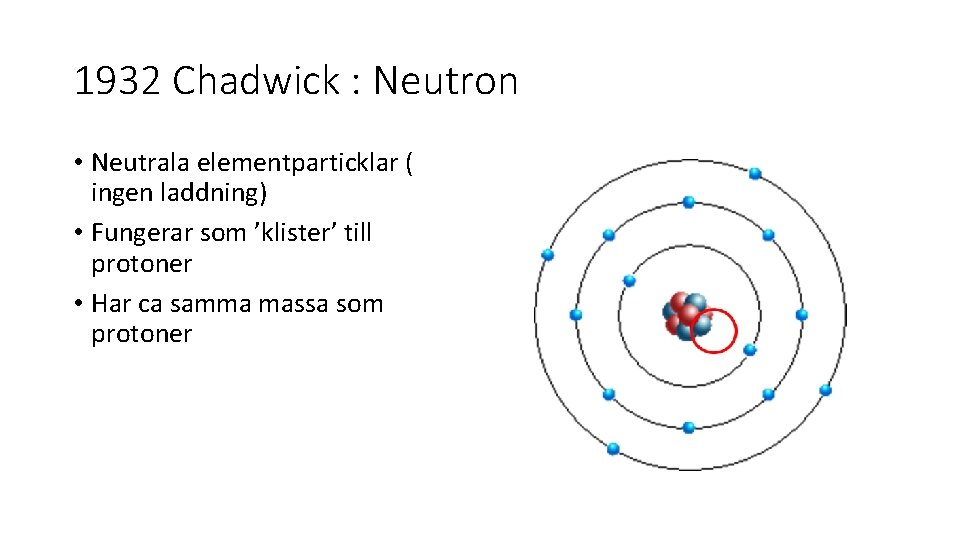
1932 Chadwick : Neutron • Neutrala elementparticklar ( ingen laddning) • Fungerar som ’klister’ till protoner • Har ca samma massa som protoner

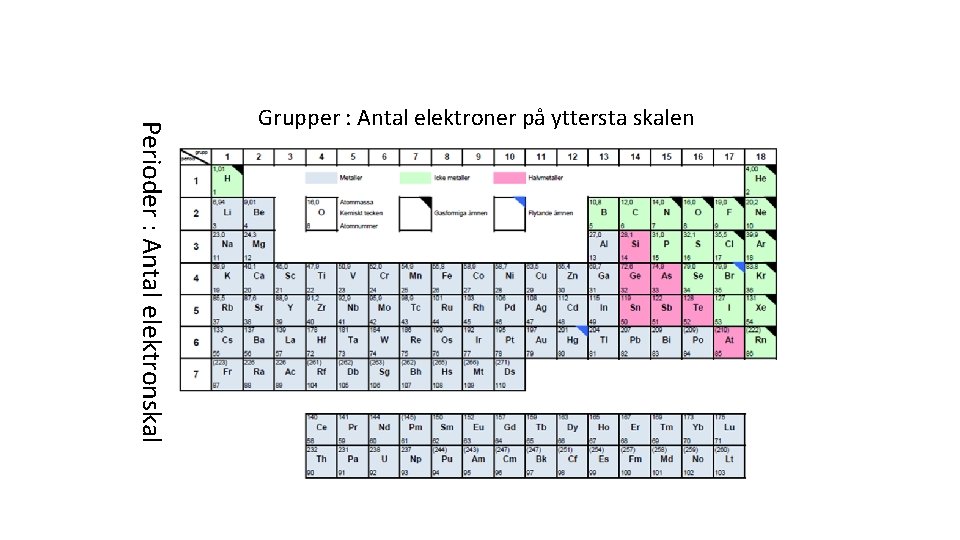
Perioder : Antal elektronskal Grupper : Antal elektroner på yttersta skalen

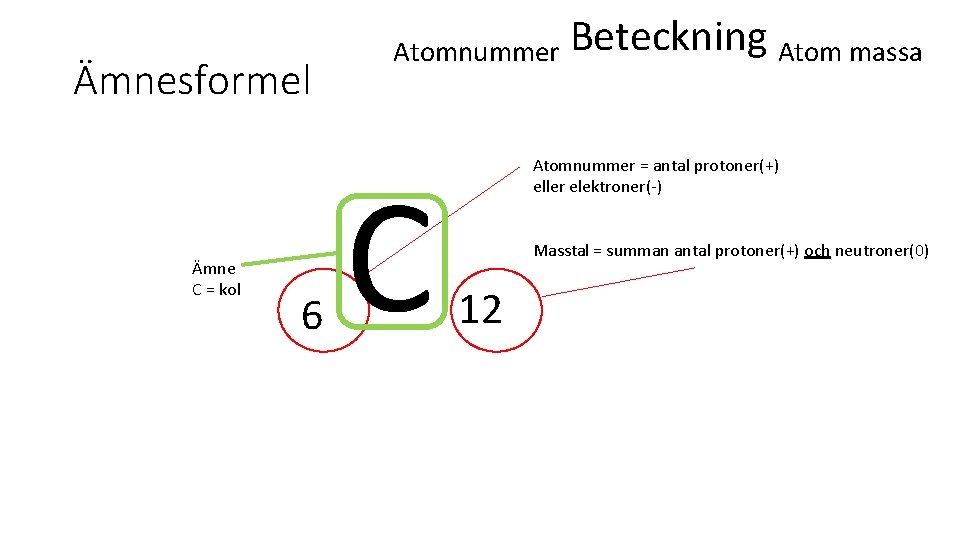
Ämnesformel Ämne C = kol 6 Atomnummer C Beteckning Atom massa Atomnummer = antal protoner(+) eller elektroner(-) Masstal = summan antal protoner(+) och neutroner(0) 12

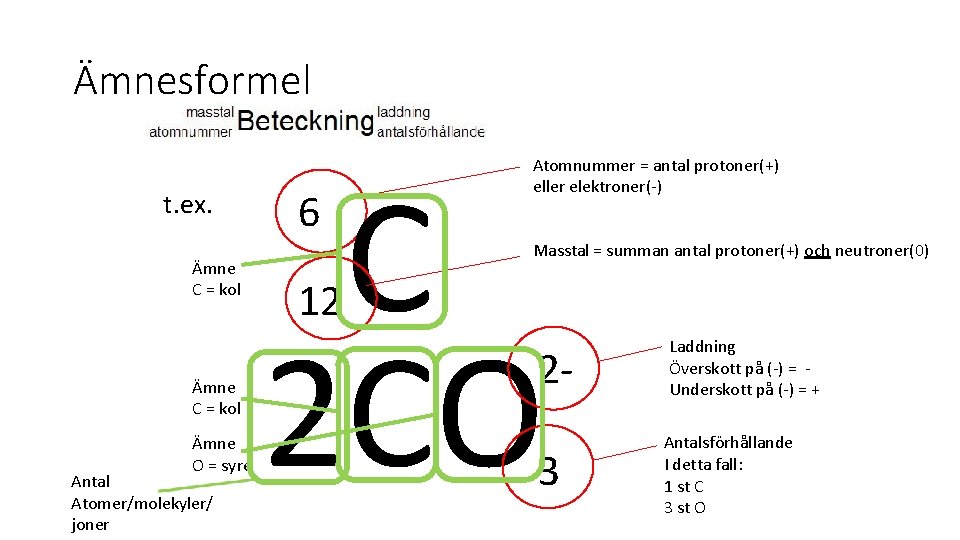
Ämnesformel t. ex. Ämne C = kol Ämne O = syre Antal Atomer/molekyler/ joner C 2 CO 6 Atomnummer = antal protoner(+) eller elektroner(-) Masstal = summan antal protoner(+) och neutroner(0) 12 23 Laddning Överskott på (-) = Underskott på (-) = + Antalsförhållande I detta fall: 1 st C 3 st O

Övning • Skriva formel

Var finns elektroner? Utanför atomkärna på elektronskal : • Det finns flera skalar runt om atomkärna • Räckans från atomkärna utåt och kallas för K, L, M…. • Maximal antal elektroner på olika skalar definierar vi med formel 2 : Antal e =2⋅n , där n står för skalens nummer (period i periodiska systemet) • Yttersta skalet i varje atom kan innehålla högst 8 elektroner (valenselektroner)

Övning : fylla tabellen

Rita elektrontilldelning (elektronkonfiguration) i atomer : • H • O • Na • Cl

Ädelgas konfiguration • Ädelgaser finns i grupp 18 • Reagerar inte med andra ämne • Har komplett fyllda elektronskal

Isotoper • Alla atomer i vis grundämne har fast antal protoner (atomnummer) • Visa kan ha mer eller mindre antal neutroner – isotoper • Den förändring kan avgöra isotopens unika egenskaper • Fördjupning : Läs mer om hur kan man avgöra ålder i fossil med hjälp av C-14