Kelvin Clapeyro n CALOR uma forma de energia














- Slides: 25

Kelvin Clapeyro n CALOR é uma forma de energia em transito de um ponto a outro do espaço. Boyle Charle s

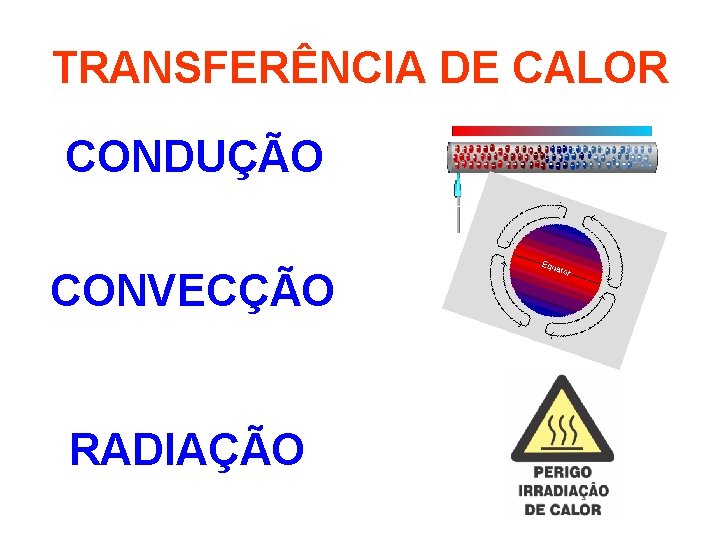
TRANSFERÊNCIA DE CALOR CONDUÇÃO CONVECÇÃO RADIAÇÃO



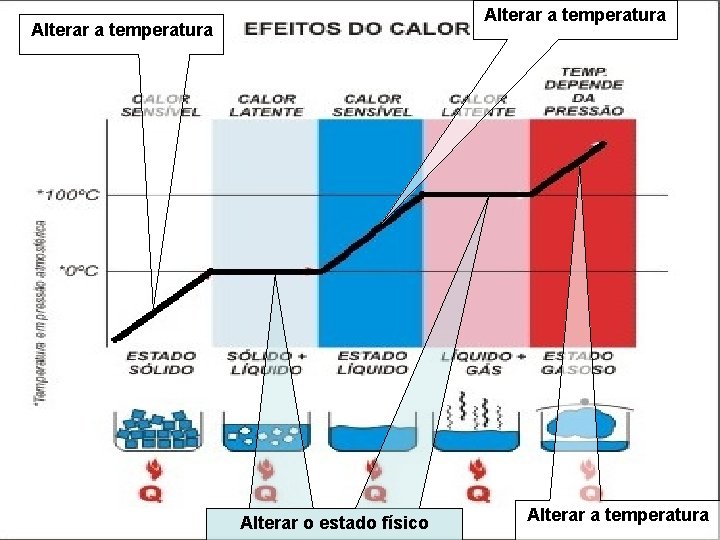
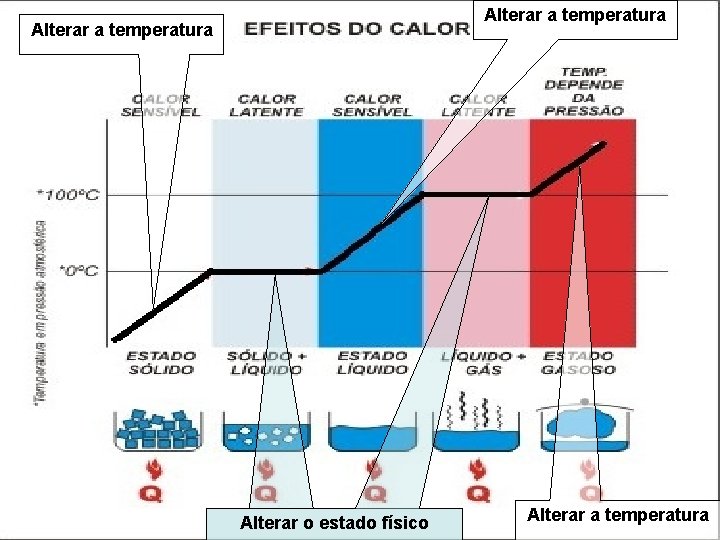
Alterar a temperatura Alterar o estado físico Alterar a temperatura

Calor SENSÍVEL: SENSÍVEL Altera a TEMPERATURA do corpo LATENTE: LATENTE Altera o ESTADO FÍSICO do corpo

Quantidade de Calor Sensível (Q) trocada entre dois ou mais corpos Q = m. c. T Onde Q é a quantidade de calor recebido (Q>0) ou cedido (Q<0); m é a massa do material; T é a variação de temperatura; c é o CALOR ESPECÍFICO DA SUBST NCIA. Num determinado estado físico

Unidade do calor específico Q = m. c. T

Alterar a temperatura Alterar o estado físico Alterar a temperatura

Calor SENSÍVEL: SENSÍVEL Altera a TEMPERATURA do corpo LATENTE: LATENTE Altera o ESTADO FÍSICO do corpo

IA R É A D S O C I ÍS A T ES F S DO T A M

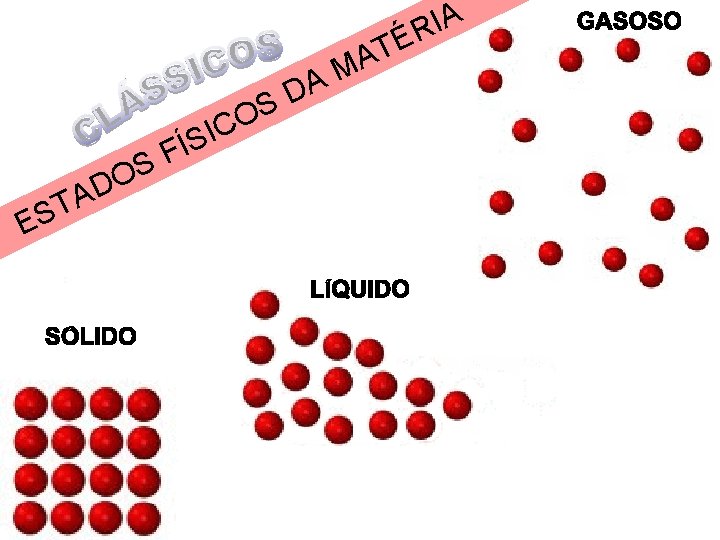
ESTADOS FÍSICOS

ESTADOS FÍSICOS Gás de quarks

opriedades dos estados da matéria Table 9 propriedade Estado da Matéria Sólido Liquido Gás (Vapor) indefinida i) FORMA definida indefinida ii) VOLUME definido iii) Interação Molecular iv) Exemplos indefinido Muito forte. Forte. Moléculas fixas Moléculas ligadas. fraca Na. Cl Zn. SO 4 H 2 O Petróleo H 2 , CO 2 Ar (puro)

Plasma, é um gás ionizado constituído de elétrons livres, íons e átomos neutros, em proporções variadas. ☼ Principalmente nas estrelas (altas Temperaturas); ☼ Também a “baixas temperaturas” (sob ação de campos eletromagnéticos).

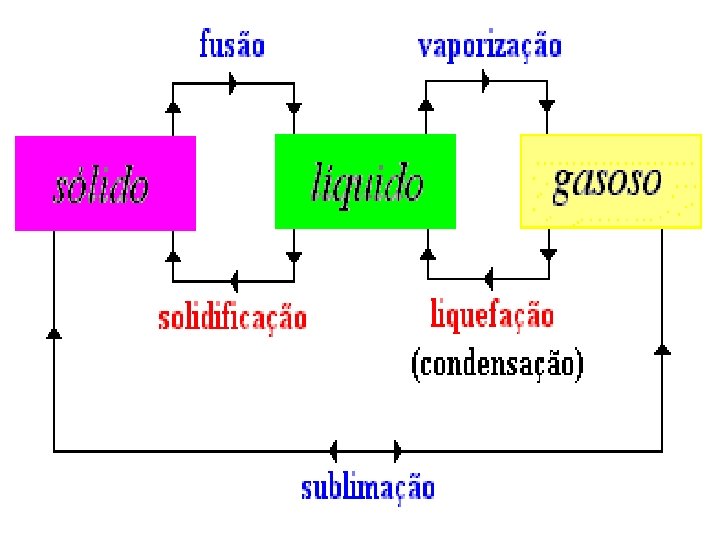
MUDANÇAS DE ESTADO MUDANÇAS DE ESTADO

MUDANÇAS DE ESTADO


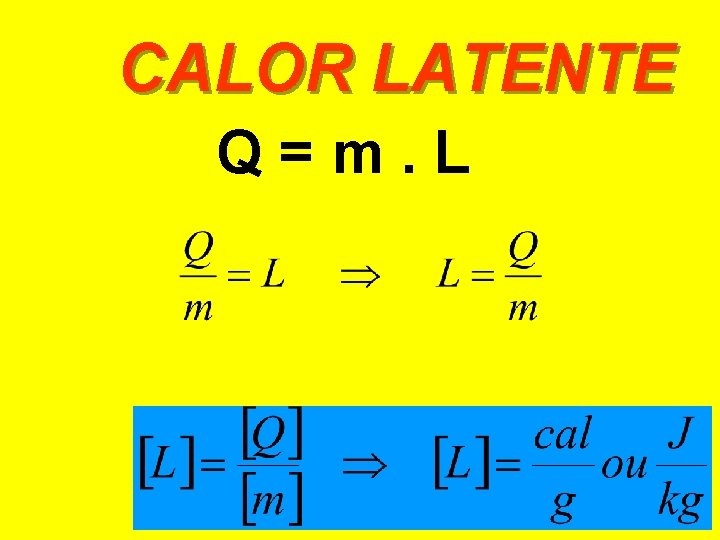
QUANTIDADE DE CALOR LATENTE A quantidade de calor latente que um objeto qualquer deve receber (ceder) para mudar de estado físico depende: Da massa do objeto (m); Do material do qual o objeto é feito (L) Q=m. L onde L é o calor latente do material.

Que = Ma. La!

CALOR LATENTE Q=m. L

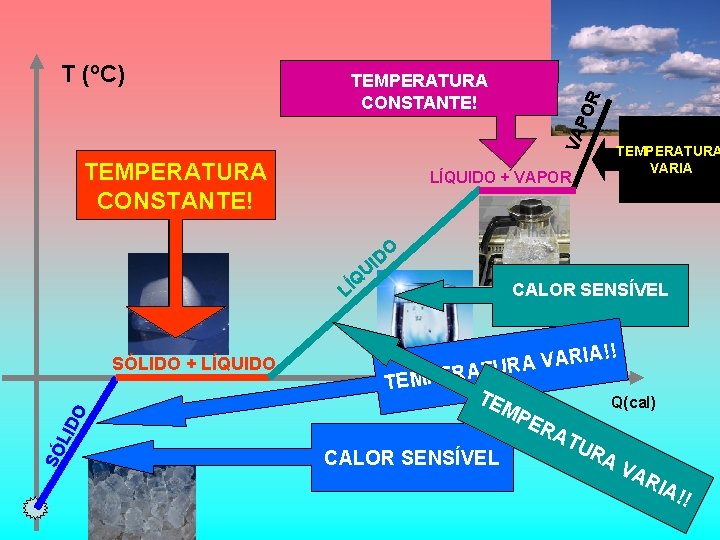
PO R CALOR LATENTE TEMPERATURA CONSTANTE! VA T (o. C) CALOR TEMPERATURA CONSTANTE! LATENTE CALOR TEMPERATURA VARIA SENSÍVEL LÍQUIDO + VAPOR O D UI Q LÍ !! TEMPE ARIA V A R U RAT TE MP SÓ LID O SÓLIDO + LÍQUIDO CALOR SENSÍVEL ER Q(cal) AT UR AV AR IA! !

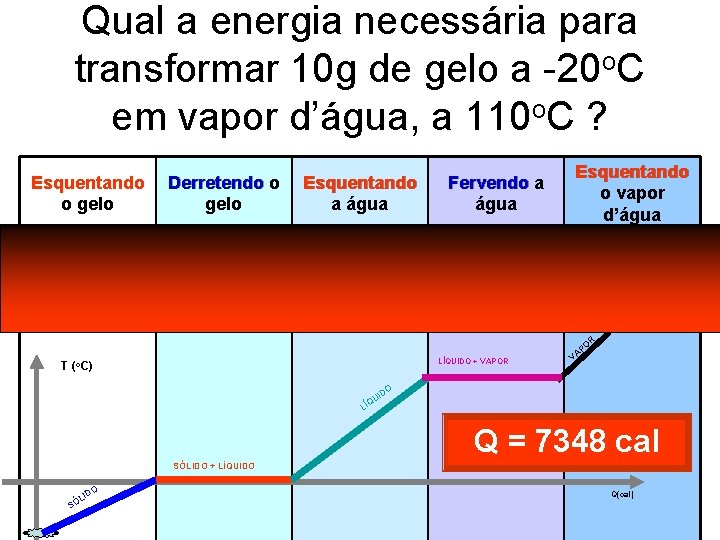
Qual a energia necessária para transformar 10 g de gelo a -20 o. C em vapor d’água, a 110 o. C ? Esquentando o gelo Derretendo o gelo Esquentando a água Fervendo a água Esquentando o vapor d’água Q 1=m. c. T Q 1 = 10. 0, 5. 20 Q 1 = 100 cal Q 2 = m. L Q 2 = 10. 80 Q 2 = 800 cal Q 3 = m. c. T Q 3 = 10. 1. 100 Q 3 = 1000 cal Q 4 = m. L Q 4 = 10. 540 Q 4 = 5400 cal Q 5 = m. c. T Q 5 = 10. 0, 48. 10 Q 5 = 48 cal R LÍQUIDO + VAPOR T (o. C) O AP V DO UI Q LÍ Q = 7348 cal SÓLIDO + LÍQUIDO L SÓ O ID Q(cal)

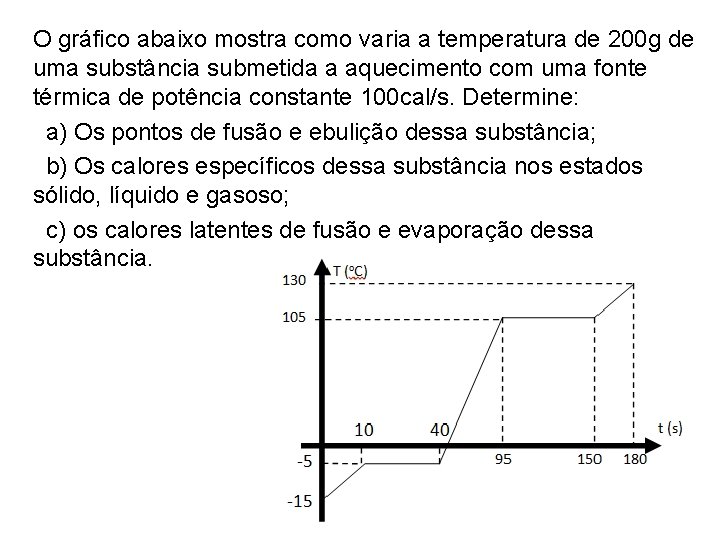
O gráfico abaixo mostra como varia a temperatura de 200 g de uma substância submetida a aquecimento com uma fonte térmica de potência constante 100 cal/s. Determine: a) Os pontos de fusão e ebulição dessa substância; b) Os calores específicos dessa substância nos estados sólido, líquido e gasoso; c) os calores latentes de fusão e evaporação dessa substância.

Lição de casa TRAZER LIVRO Livro: Problemas e testes, pg. 169 exs. 1 a 6