Katera Chemii Nieorganicznej i Analitycznej Zakad Elektroanalizy i















![Polimery z przewodnictwem elektronowym Nazwa Metoda polimeryzacji Przewodnictwo [S/cm] chem 102 -105 Polipirol elech/chem Polimery z przewodnictwem elektronowym Nazwa Metoda polimeryzacji Przewodnictwo [S/cm] chem 102 -105 Polipirol elech/chem](https://slidetodoc.com/presentation_image_h/95b7eac8f3136a0a1f3cd998ee0ee5b9/image-28.jpg)



- Slides: 36

Katera Chemii Nieorganicznej i Analitycznej Zakład Elektroanalizy i Elektrochemii UŁ Ul. Tamka 12, 91 -403 Łódź

ELEKTROCHEMIA ZWIĄZKÓW ORGANICZNYCH TROCHĘ HISTORII - ZAMIAST WSTĘPU DOBÓR WARUNKÓW DO PRZEPROWADZENIA PROCESÓW ELEKTROCHEMICZNYCH APARATURA DO PROWADZENIA ELEKTROLIZY PODSTAWOWE MECHANIZMY REAKCJI ELEKTROCHEMICZNYCH PODSTAWOWE TYPY REAKCJI ELEKTROCHEMICZNYCH ZWIĄZKÓW ORGANICZNYCH ANODOWE REAKCJE PODSTAWIENIA NUKLEOFILOWEGO KATODOWE REAKCJE PODSTAWIANIA ELEKTROFILOWEGO ANODOWE REAKCJE PRZYŁĄCZENIA KATODOWE REAKCJE PRZYŁĄCZANIA ELEKTROFILOWEGO ANODOWE REAKCJE ELIMINACJI KATODOWE REAKCJE ELIMINACJI ANODOWE REAKCJE DIMERYZACJI KATODOWE REAKCJE ELEKTROKATALITYCZNE ANODOWE REAKCJE ELEKTROKATALITYCZNE KATODOWE REAKCJE PRZYŁĄCZANIA REAKCJE ELEKTRODOWE Z ELEKTROREGENACJĄ JEDNEGO Z SUBSTRATÓW REAKCJE PRZEKSZTAŁCANIA GRUP FUNKCYJNYCH POLIMERY PRZEWODZĄCE

Trochę historii 1780 - Luigi Galvani odkrywa zjawisko potencjału elektrochemicznego 1799 - Alesandro Volta prezentuje swoje ogniwo 1834 - Reakcja Faraday'a 2 CH 3 COO- - 2 e → 2 CO 2 + 3 H 2 O 1855 - Reakcja Kolbe’go 2 RCOO- - 2 e → R–R + 2 CO 2

Trochę historii – pierwsze technologie elektrochemiczne organiczne Elektrosynteza czteroetylku ołowiu Roztwór elektrolitu to etylowy chlorek magnezowy (związek Grignarda) w eterze, anoda Pb, katoda stalowa. 4(C 2 H 5)Mg. Cl + Pb → (C 2 H 5)4 Pb + 4 Mg. Cl+ + 4 e Mg. Cl+ + 2 e → Mg + Clmagnez z katody jest zawracany do reakcji Grignarda C 2 H 5 Cl + Mg → (C 2 H 5)Mg. Cl Drugim historycznym już przykładem reakcji elektrosyntezy organicznej jest elektrochemiczna polimeryzacja akrylonitrylu. Była to technologia opracowana w USA w czasie drugiej wojny światowej i wykorzystywana m. in. do otrzymywania trwałych włókien polimerowych do produkcji na potrzeby wojska (np. spadochrony) 2 CH 2=CHCN + 2 H 2 O + 2 e → -[(CHCH)2 CN]n- + 2 OH 2 H 2 O → O 2 + 4 H+ + 4 e

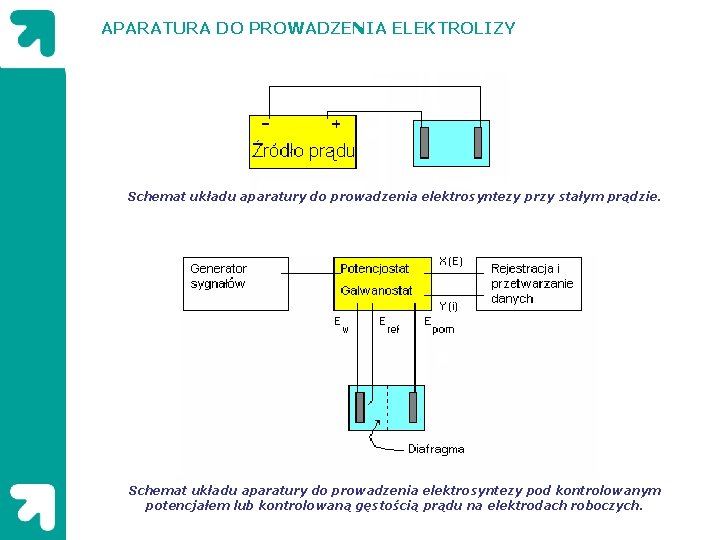
APARATURA DO PROWADZENIA ELEKTROLIZY Schemat układu aparatury do prowadzenia elektrosyntezy przy stałym prądzie. Schemat układu aparatury do prowadzenia elektrosyntezy pod kontrolowanym potencjałem lub kontrolowaną gęstością prądu na elektrodach roboczych.

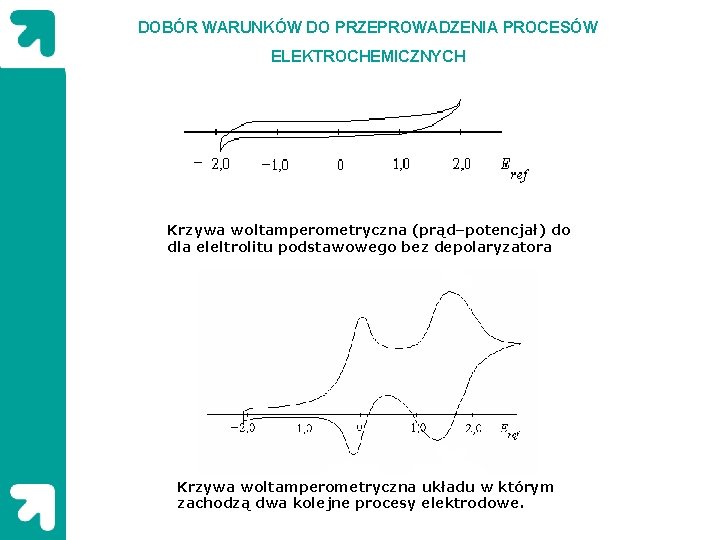
DOBÓR WARUNKÓW DO PRZEPROWADZENIA PROCESÓW ELEKTROCHEMICZNYCH Krzywa woltamperometryczna (prąd–potencjał) do dla eleltrolitu podstawowego bez depolaryzatora Krzywa woltamperometryczna układu w którym zachodzą dwa kolejne procesy elektrodowe.

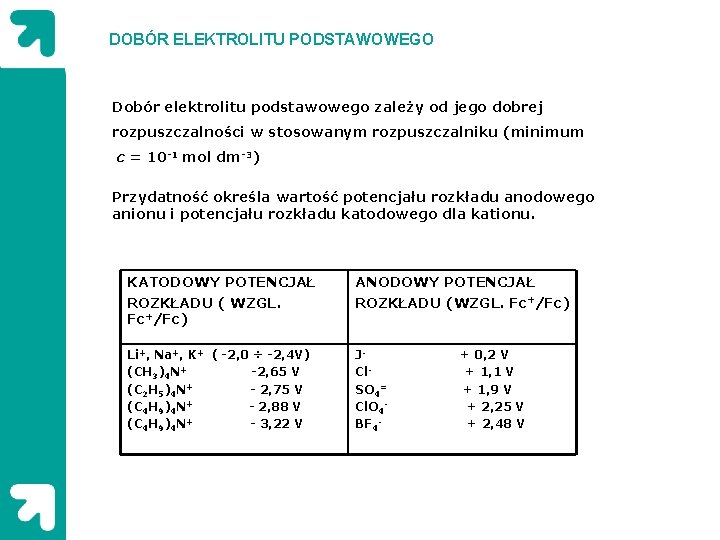
DOBÓR ELEKTROLITU PODSTAWOWEGO Dobór elektrolitu podstawowego zależy od jego dobrej rozpuszczalności w stosowanym rozpuszczalniku (minimum c = 10 -1 mol dm-3) Przydatność określa wartość potencjału rozkładu anodowego anionu i potencjału rozkładu katodowego dla kationu. KATODOWY POTENCJAŁ ROZKŁADU ( WZGL. Fc+/Fc) ANODOWY POTENCJAŁ ROZKŁADU (WZGL. Fc+/Fc) Li+, Na+, K+ ( -2, 0 ÷ -2, 4 V) (CH 3)4 N+ -2, 65 V (C 2 H 5)4 N+ - 2, 75 V (C 4 H 9)4 N+ - 2, 88 V (C 4 H 9)4 N+ - 3, 22 V J- + 0, 2 V Cl- + 1, 1 V SO 4= + 1, 9 V Cl. O 4 - + 2, 25 V BF 4 - + 2, 48 V

Materiały katodowe Najbardziej popularne materiały katodowe to: rtęć (obecnie ogranicza się jej stosowanie ze względu na toksycze właściwości) ołów, cyna, tytan, miedź, żelazo, glin, platyna, nikiel, różnego typu elektrody węglowe (grafitowe), elektrody kompozytowe (układy Pb / Pb. O 2, Ti / Ti. O 2 , Cu/ Ni/Ti / Ti. O 2 itp. . ) elektrody modyfikowane. Zakresy katodowego zastosowania katody rtęciowej w różnych rozpuszczalnikach i w różnych elektrolitach podstawowych.

Materiały anodowe Jako materiał anodowy najczęściej stosowana jest platyna i jej stopy z innymi platynowcami (Ir, Pd, Rh) Elektroda złota, a właściwie elektroda kompozytowa Au/Au 2 O 3 Innego typu elektrody jak np. Pb / Pb. O 2, Ti / Ti. O 2, Ti /(Ti. O 2 + Cr 2 O 3), Ti/(Ti. O 2+Co 3 O 4) itd. Elektrody modyfikowane.

Materiały anodowe Zakresy robocze elektrody platynowej w różnych rozpuszczalnikach. Stężenie elektrolitów podstawowych c = 0, 1 mol/dm 3

PODSTAWOWE MECHANIZMY ELEKTROCHEMICZNYCH REAKCJI ZWIĄZKÓW CHEMICZNYCH I. Mechanizm E (elektrodowy) - proces przeniesienia ładunku: Ox + ne ⇄ Red Ox + ne → Red II. Mechanizm CE. Proces elektrodowy, który jest poprzedzony reakcją chemiczną Z ⇄ Ox Ox + ne ⇄ Red III. Mechanizm EC. Proces, w którym reakcja elektrodowa poprzedza reakcję chemiczną: Ox + ne ⇄ Red ⇄ Z IV. Mechanizn ECE. Dwa procesy elektrodowe są rozdzielone reakcją chemiczną: Ox 1 + n 1 e ⇄ Red 1 (E 01) Red 1 ⇄ Ox 2 + n 2 e ⇄ Red 2 (E 02)

PODSTAWOWE TYPY REAKCJI ELEKTROCHEMICZNYCH ZWIĄZKÓW ORGANICZNYCH ANODOWE REAKCJE PODSTAWIENIA NUKLEOFILOWEGO Anodowe reakcje podstawienia mogą przebiegać według kilku różnych mechanizmów. Poniżej przedstawiony jest ogólny schemat podstawienia rodnikowego: Nu- - e → Nu. + RH → R. + HNu R. + Nu. → RNu R. + e → R+ R+ + Nu- → RNu I droga II droga Przykładem może być reakcja chlorowania. Proces ten zachodzi według mechanizmu EC. Z innych możliwych mechanizmów można wymienić atak odczynnika nukleofilowego na karbokation aromatyczny. Pt, CH 3 CN + Et 4 NCl 35% 55%

KATODOWE REAKCJE PODSTAWIANIA ELEKTROFILOWEGO RX + E+ + 2 e → RE + XReakcja ta zachodzi według mechanizmu EC: RX + 2 e → R + XR- + E+ → RE Jako przykład może służyć reakcja otrzymywania kwasu fenyloacetylowego z chlorku benzylu w DMF na platynie w obecności CO 2. Ph—CH 2— Cl + CO 2 + 2 e→ Ph—CH 2— CO 2 - + Cl. Hg, DMF

Schemat przedstawiający różnorodność reakcji katodowego podstawienia elektrofilowego

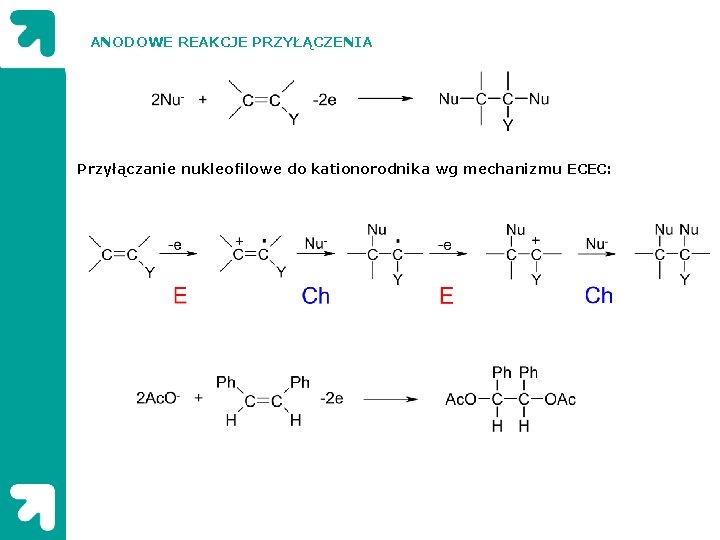
ANODOWE REAKCJE PRZYŁĄCZENIA Przyłączanie nukleofilowe do kationorodnika wg mechanizmu ECEC:

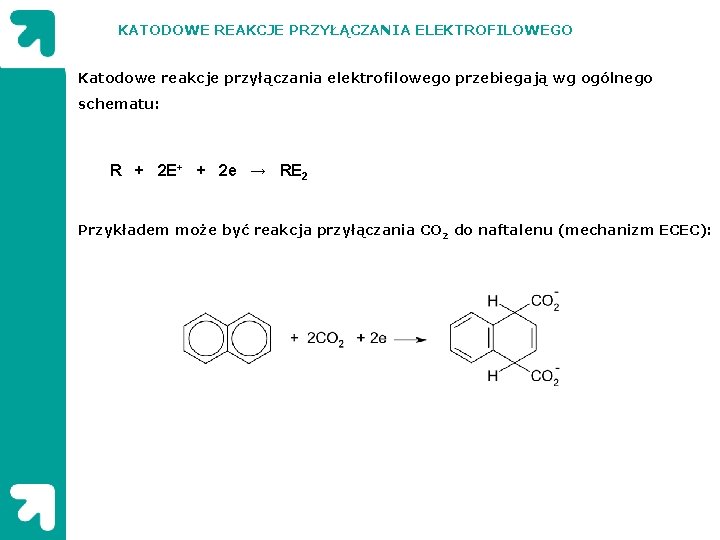
KATODOWE REAKCJE PRZYŁĄCZANIA ELEKTROFILOWEGO Katodowe reakcje przyłączania elektrofilowego przebiegają wg ogólnego schematu: R + 2 E+ + 2 e → RE 2 Przykładem może być reakcja przyłączania CO 2 do naftalenu (mechanizm ECEC):

ANODOWE REAKCJE ELIMINACJI Ten typ reakcji dotyczy przede wszystkim eliminacji cząsteczek CO 2 ze związków organicznych zgodnie ze schematem: RCO 2 - 2 e → CO 2 + R+ R+ H+ + (cykloalkany) Przykład reakcji: CH 3—CH 2—CO 2 + 2 e → CO 2 + CH 3—CH 2+

KATODOWE REAKCJE ELIMINACJI W przypadku tych reakcji i przebieg i produkty zależą od rodzaju wiązania, które ulega rozpadowi: RX + H+ + 2 e ⇄ RH + X- I przykład: degradacja IV-rzędowych kationów amoniowych i fosfoniowych: R 3 N+−CH 2−Ph + 2 e + H+ → R 3 N + Ph−CH 3 + Ph−CH 2−P−Ph 3 + 2 e + H+ → Ph−CH 3 + P(Ph)3 II przykład: eliminacja wiązania -S-O- (również mechanizm ECEC) - Ar−SO 3−OR + 2 e + H+ → Ar. SO 2 + ROH

ANODOWE REAKCJE DIMERYZACJI Cechą charakterystyczną tych reakcji jest tworzenie wiązań typu X-X, czyli np. wiązań C – C, S – S, N – N. Klasycznym przykładem takich reakcji jest reakcja utleniania anionów Karboksylowych nazwana reakcją Kolbego. Proces zachodzi zgodnie wg mechanizmu EC ze schematem: R−CO 2 - e → R. + CO 2 2 R. → R−R W przypadku mieszaniny dwóch anionów karboksylowych otrzymuje się trzy produkty: R−CO 2 + R’−CO 2 - 2 e → CO 2 + ( R−R’ R’−R’)

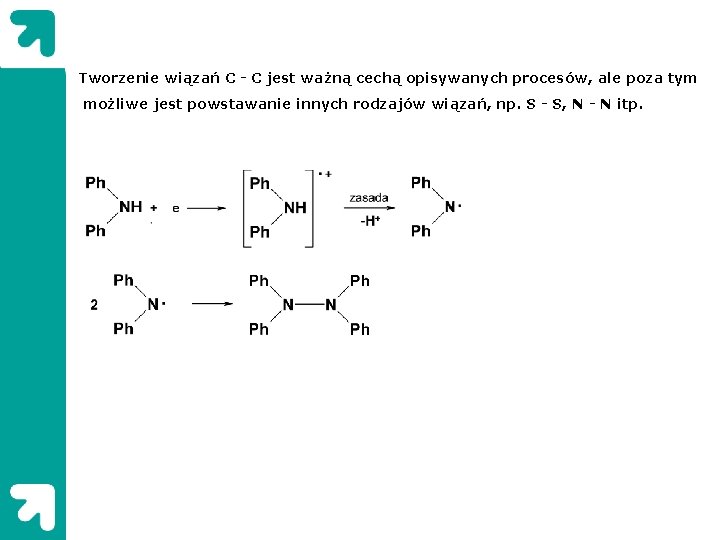
Tworzenie wiązań C - C jest ważną cechą opisywanych procesów, ale poza tym możliwe jest powstawanie innych rodzajów wiązań, np. S - S, N - N itp.

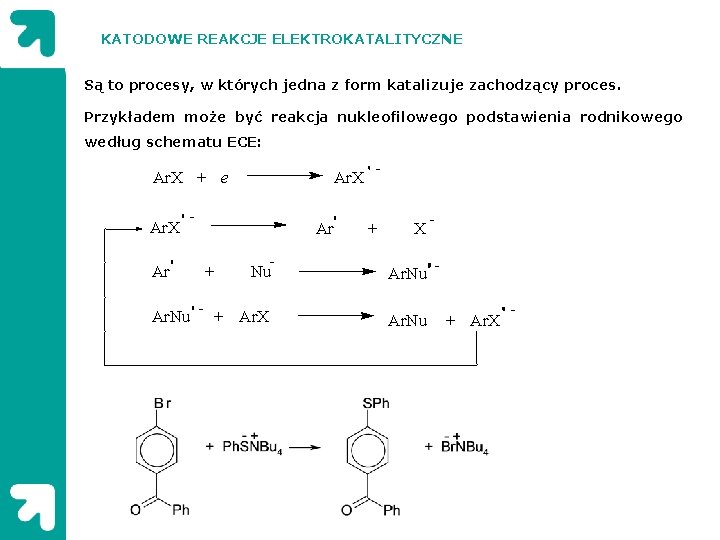
KATODOWE REAKCJE ELEKTROKATALITYCZNE Są to procesy, w których jedna z form katalizuje zachodzący proces. Przykładem może być reakcja nukleofilowego podstawienia rodnikowego według schematu ECE: Ar. X + e Ar. X - Ar Ar Ar. Nu + X Nu Ar. Nu + Ar. X Ar. Nu + - + Ar. X -

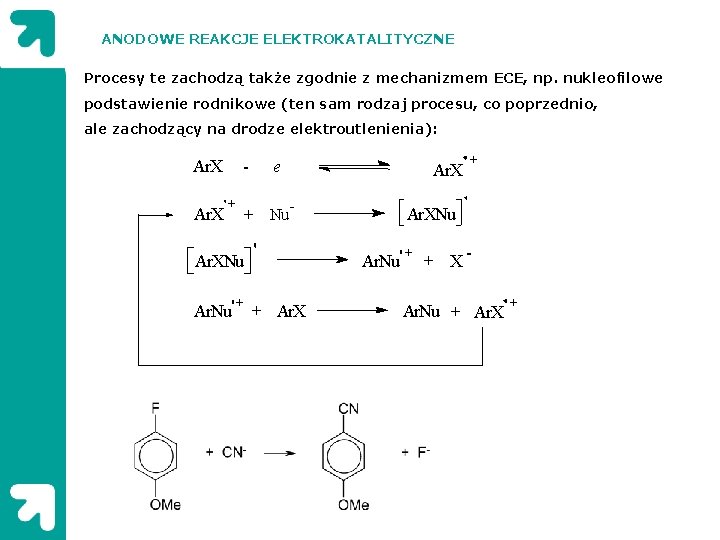
ANODOWE REAKCJE ELEKTROKATALITYCZNE Procesy te zachodzą także zgodnie z mechanizmem ECE, np. nukleofilowe podstawienie rodnikowe (ten sam rodzaj procesu, co poprzednio, ale zachodzący na drodze elektroutlenienia): Ar. X + e + Nu Ar. XNu Ar. Nu + + Ar. XNu Ar. Nu + + X Ar. Nu + Ar. X +

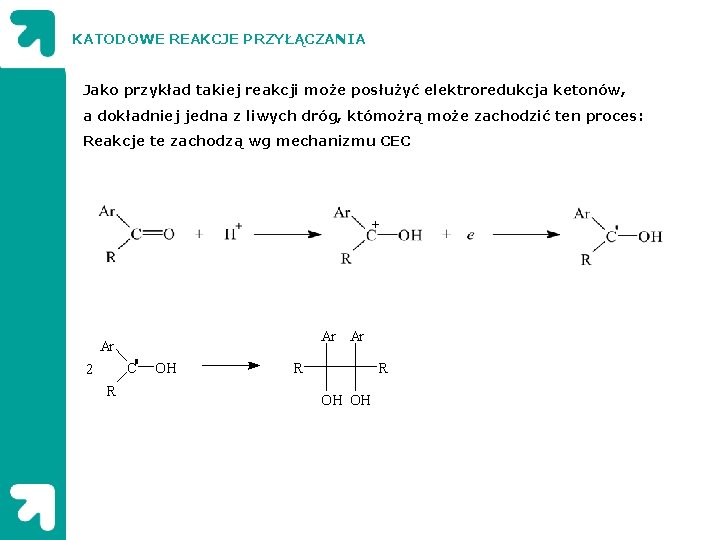
KATODOWE REAKCJE PRZYŁĄCZANIA Jako przykład takiej reakcji może posłużyć elektroredukcja ketonów, a dokładniej jedna z liwych dróg, któmożrą może zachodzić ten proces: Reakcje te zachodzą wg mechanizmu CEC + Ar Ar Ar C 2 R OH R R OH OH

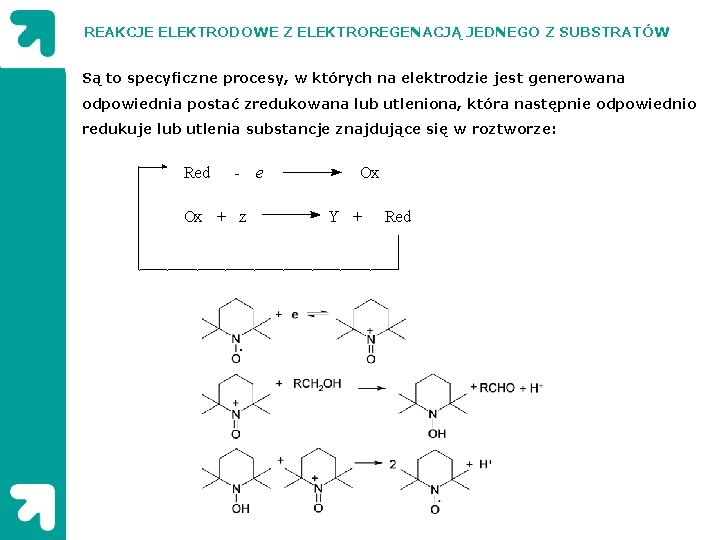
REAKCJE ELEKTRODOWE Z ELEKTROREGENACJĄ JEDNEGO Z SUBSTRATÓW Są to specyficzne procesy, w których na elektrodzie jest generowana odpowiednia postać zredukowana lub utleniona, która następnie odpowiednio redukuje lub utlenia substancje znajdujące się w roztworze: Red - e Ox + z Ox Y + Red

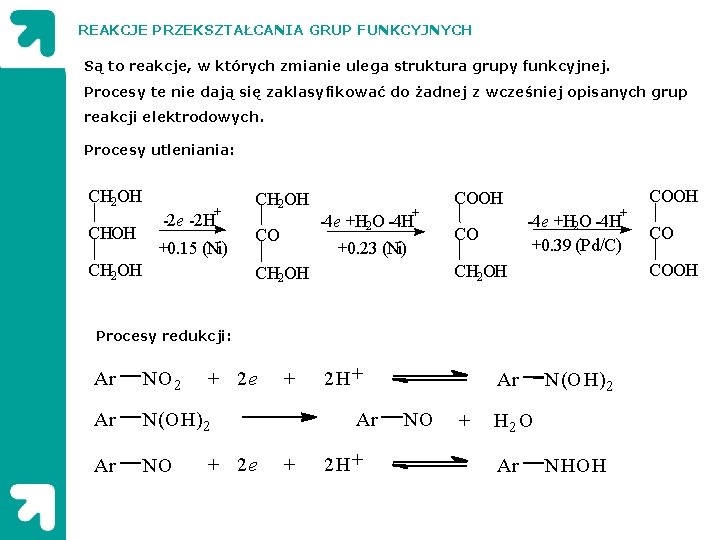
REAKCJE PRZEKSZTAŁCANIA GRUP FUNKCYJNYCH Są to reakcje, w których zmianie ulega struktura grupy funkcyjnej. Procesy te nie dają się zaklasyfikować do żadnej z wcześniej opisanych grup reakcji elektrodowych. Procesy utleniania: CH 2 OH CHOH + -2 e -2 H +0. 15 (Ni) CH 2 OH CO + -4 e +H 2 O -4 H +0. 23 (Ni) COOH + -4 e +H 2 O -4 H +0. 39 (Pd/C) CO Procesy redukcji: Ar NO 2 + 2 e Ar N(O H)2 Ar NO + 2 e + 2 H+ Ar NO + N(O H)2 H 2 O Ar CO COOH CH 2 OH COOH NHO H

Polimery Przewodzące Definicje i podział polimerów przewodzących Polimery przewodzące – substancje wielokoczasteczkowe zdolne do przewodzenia prądu elektrycznego Polimery z przewodnictwem jonowym – substancje polimerowe w których przewodnictwo odbywa się poprzez ruch jonów, zalicza się je do przewodników drugiego rodzaju. Przykładem może być odpowiednio spreparowany Nafion. Polimery z przewodnictwem elektronowym –substancje polimerowe w których przewodnictwo odbywa się poprzez ruch elektronów lub dziur, zalicza się je do przewodników pierwszego rodzaju. Przykładem mogą być polianilina, plipirol.

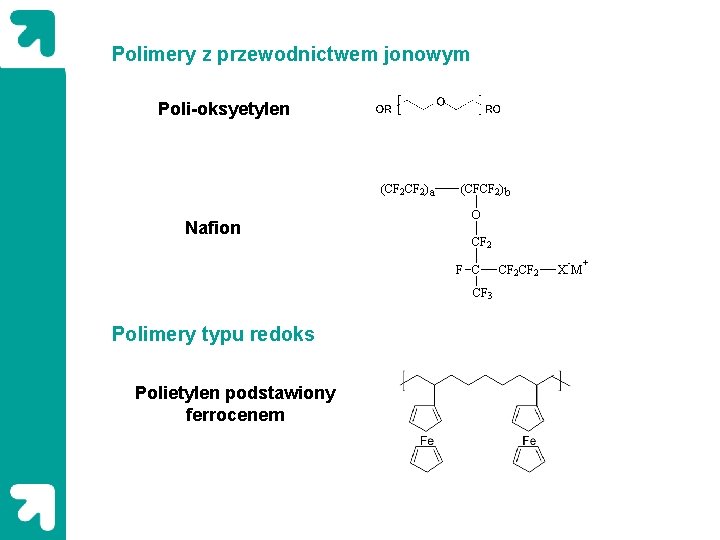
Polimery z przewodnictwem jonowym Poli-oksyetylen Nafion Polimery typu redoks Polietylen podstawiony ferrocenem
![Polimery z przewodnictwem elektronowym Nazwa Metoda polimeryzacji Przewodnictwo Scm chem 102 105 Polipirol elechchem Polimery z przewodnictwem elektronowym Nazwa Metoda polimeryzacji Przewodnictwo [S/cm] chem 102 -105 Polipirol elech/chem](https://slidetodoc.com/presentation_image_h/95b7eac8f3136a0a1f3cd998ee0ee5b9/image-28.jpg)
Polimery z przewodnictwem elektronowym Nazwa Metoda polimeryzacji Przewodnictwo [S/cm] chem 102 -105 Polipirol elech/chem 100 Politiofen elech/chem 106 elech - elech/chem 100 Poliacetylen Poli-(3, 4 -etylenodioxytiofen) PEDOT Polianilina Struktura

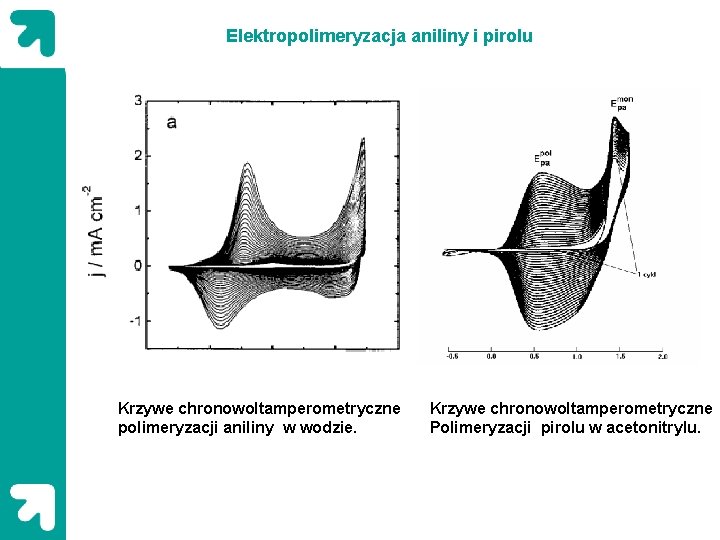
Elektropolimeryzacja aniliny i pirolu Krzywe chronowoltamperometryczne polimeryzacji aniliny w wodzie. Krzywe chronowoltamperometryczne Polimeryzacji pirolu w acetonitrylu.

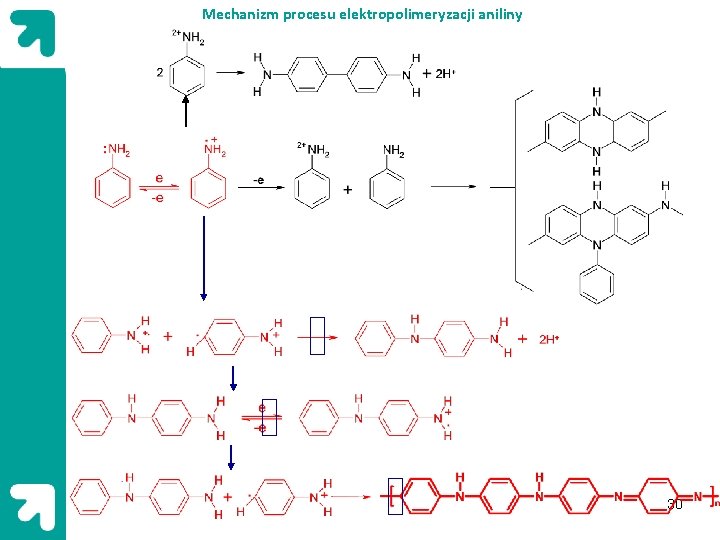
Mechanizm procesu elektropolimeryzacji aniliny 30

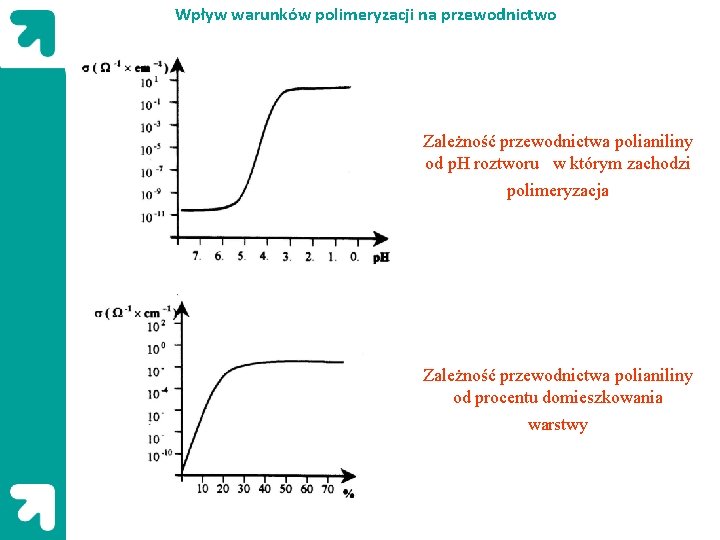
Wpływ warunków polimeryzacji na przewodnictwo Zależność przewodnictwa polianiliny od p. H roztworu w którym zachodzi polimeryzacja Zależność przewodnictwa polianiliny od procentu domieszkowania warstwy

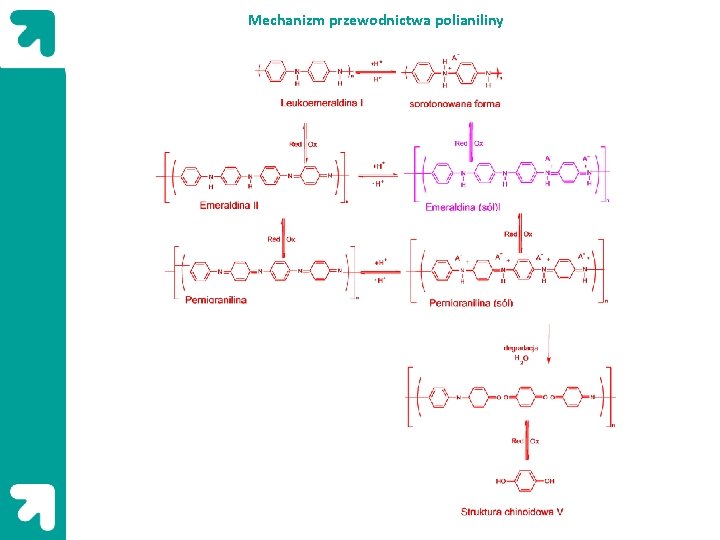
Mechanizm przewodnictwa polianiliny

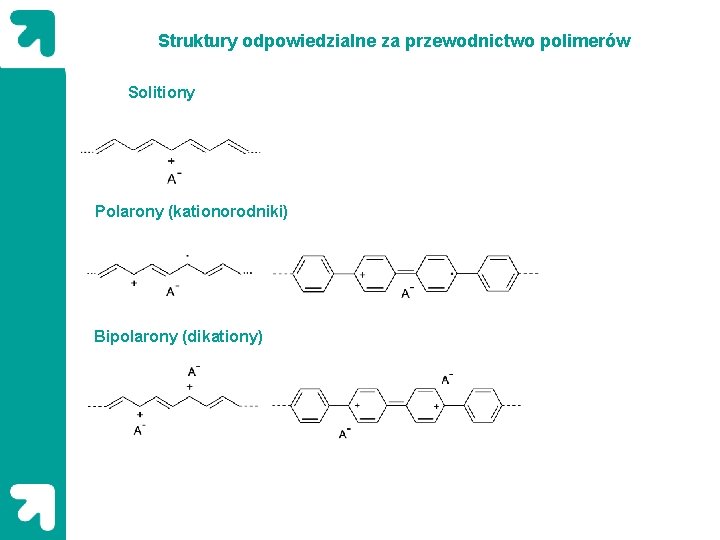
Struktury odpowiedzialne za przewodnictwo polimerów Solitiony Polarony (kationorodniki) Bipolarony (dikationy)

POLIANILINA Właściwości • • • Stabilna od 0 – 300 C Przewodnictwo od 10 -3 d 0 10 S/cm Praktycznie nierozpuszczalna w rozpuszczalnikach organicznych Wykazuje właściwości katalityczne (izomeryzacja butadienu) PANI otrzymywana w środowisku kwaśnym jest elektroaktywna przy p. H < 3 i nieelektroaktywna przy p. H > 4 Właściwości półprzewodnikowe Zastosowania • • • Wytwarzanie baterii i akumulatorów Budowa tranzystorów Otrzymywanie powłok pochłaniających promieniowanie mikrofalowe Budowa czujników chemicznych i elektrochemicznych Pokrycia, opakowania i tkaniny antystatyczne Elektrody modyfikowane

Literatura 1. H. Lund, O. Hammerich, Organic Electrochemistry, Fourth Edition, CRC Press, 2001 2. A. Tallec, Electrochimie organique synthèses et mécanismes, Paris: Masson, 1985 3. G. Inzelt, Conducting polymers, ed. F. Scholz, Springer, Berlin, 2008 4. H. Scholl, T. Błaszczyk , " Elektrochemia - Zarys teorii i praktyki", Wyd. U Ł , 1998 5. A. J. Bard, G. Inzelt, F. Scholz, Electrochemical Dictionary Springer, 2008

Dziękuję za uwagę