KARBONYLOV SLOUENINY Vypracoval Klra Urbanov Malostransk gymnzium Tento

KARBONYLOVÉ SLOUČENINY Vypracoval: Klára Urbanová Malostranské gymnázium Tento projekt je financován z prostředků Evropského sociálního fondu a rozpočtu hl. města Prahy v rámci Operačního programu Praha Adaptabilita. Praha & EU: Investujeme do vaší budoucnosti
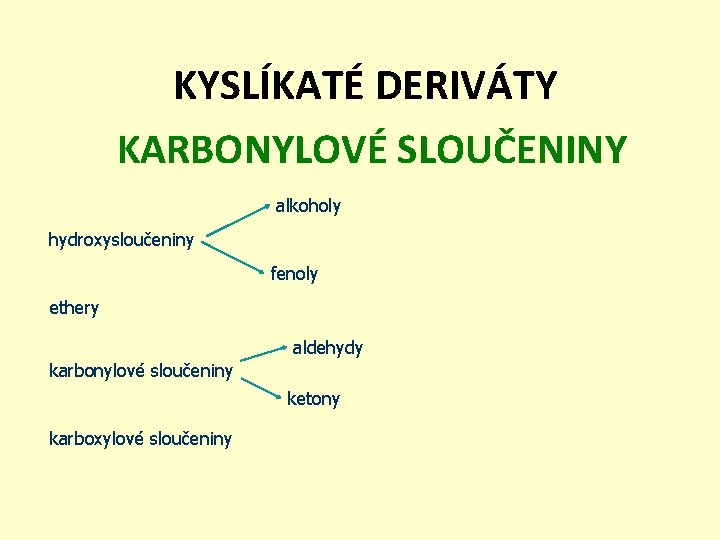
KYSLÍKATÉ DERIVÁTY KARBONYLOVÉ SLOUČENINY alkoholy hydroxysloučeniny fenoly ethery aldehydy karbonylové sloučeniny ketony karboxylové sloučeniny
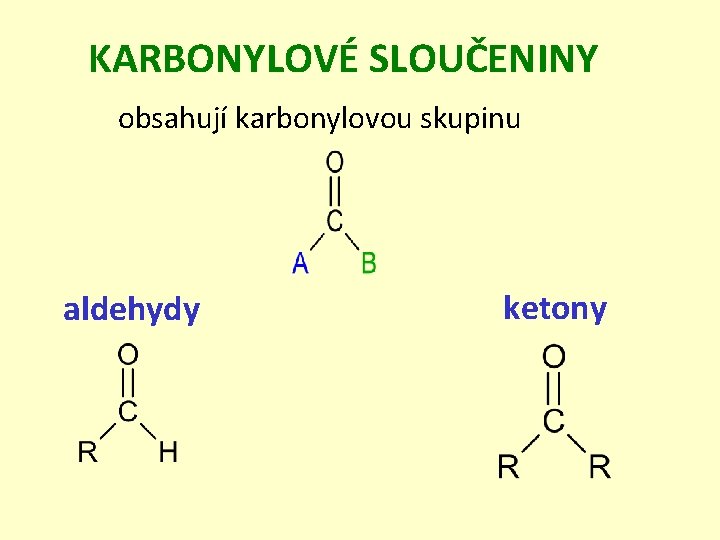
KARBONYLOVÉ SLOUČENINY obsahují karbonylovou skupinu aldehydy ketony
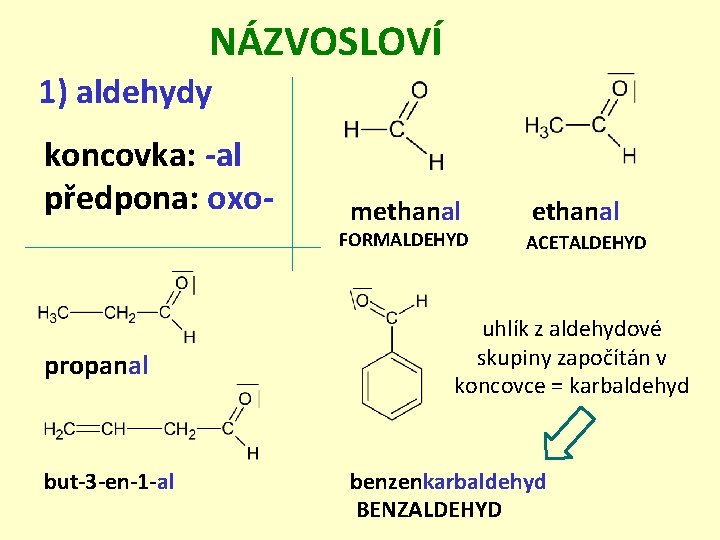
NÁZVOSLOVÍ 1) aldehydy koncovka: -al předpona: oxo- methanal FORMALDEHYD propanal but-3 -en-1 -al ethanal ACETALDEHYD uhlík z aldehydové skupiny započítán v koncovce = karbaldehyd benzenkarbaldehyd BENZALDEHYD
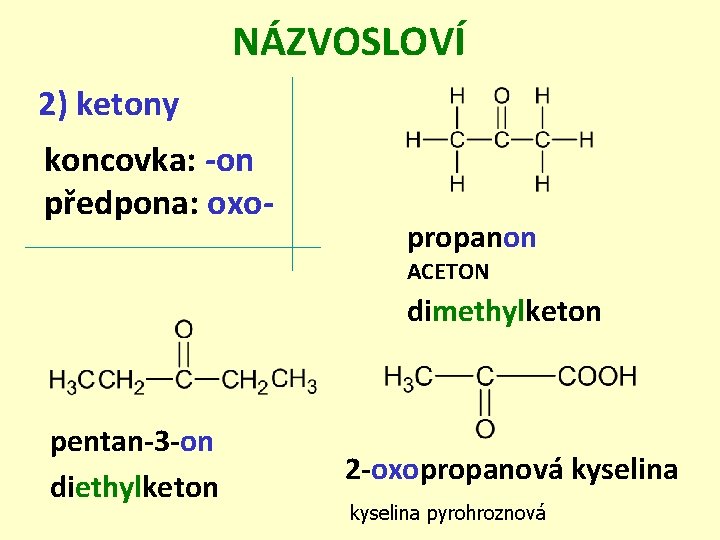
NÁZVOSLOVÍ 2) ketony koncovka: -on předpona: oxo- propanon ACETON dimethylketon pentan-3 -on diethylketon 2 -oxopropanová kyselina pyrohroznová
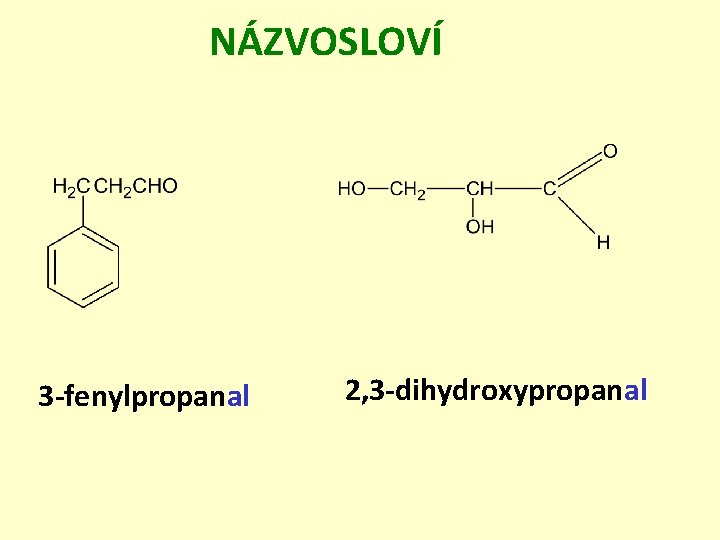
NÁZVOSLOVÍ 3 -fenylpropanal 2, 3 -dihydroxypropanal

FYZIKÁLNÍ VLASTNOSTI • nižší aldehydy i ketony jsou kapaliny (výjimkou je plynný formaldehyd) • vyšší jsou pevné látky Methan CH 4 Methanal HCHO Methanol CH 3 OH t. t. -182, 5 °C t. v. -161, 6 °C t. t. - 117, 0 °C t. v. -19, 3 °C t. t. -97, 7 °C t. v. 64, 7 °C Ethan C 2 H 6 Ethanal CH 3 CHO Ethanol C 2 H 5 OH t. t. -183, 3 °C t. v. -88, 7 °C t. t. - 124, 0 °C t. v. 20, 2 °C t. t. - 114, 4 °C t. v. 78, 3 °C

FYZIKÁLNÍ VLASTNOSTI • mají vyšší teploty varu než příslušné nenasycené uhlovodíky, ale nižší než odpovídající alkoholy (netvoří vodíkové můstky) • nižší aldehydy i ketony jsou ve vodě rozpustné, rozpustnost klesá s rostoucí molekulovou hmotností Roztok fomaldehydu [obr. 1]

FYZIKÁLNÍ VLASTNOSTI • nižší aldehydy pronikavě zapáchají, • vyšší aldehydy a některé ketony mají příjemnou vůni VANILIN [obr. 2] [obr. 3]
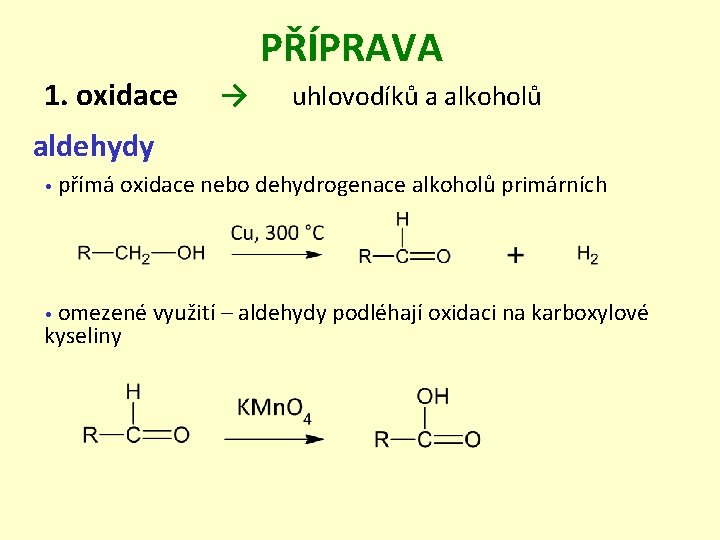
PŘÍPRAVA 1. oxidace → uhlovodíků a alkoholů aldehydy • přímá oxidace nebo dehydrogenace alkoholů primárních omezené využití – aldehydy podléhají oxidaci na karboxylové kyseliny •
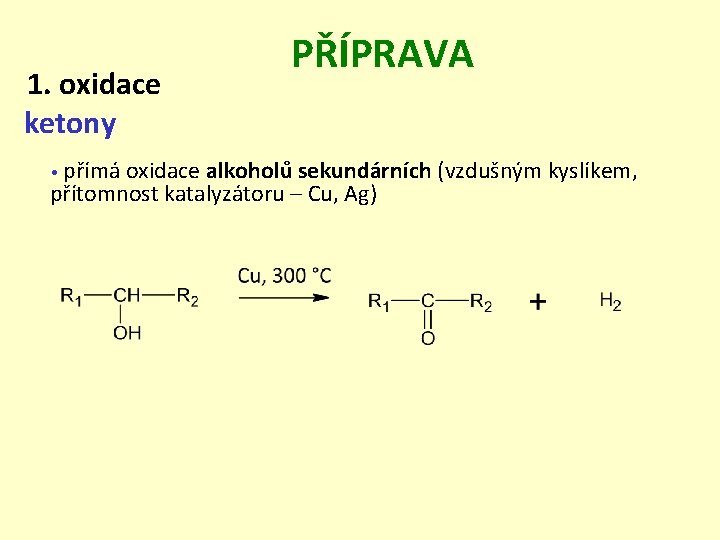
1. oxidace ketony PŘÍPRAVA přímá oxidace alkoholů sekundárních (vzdušným kyslíkem, přítomnost katalyzátoru – Cu, Ag) •
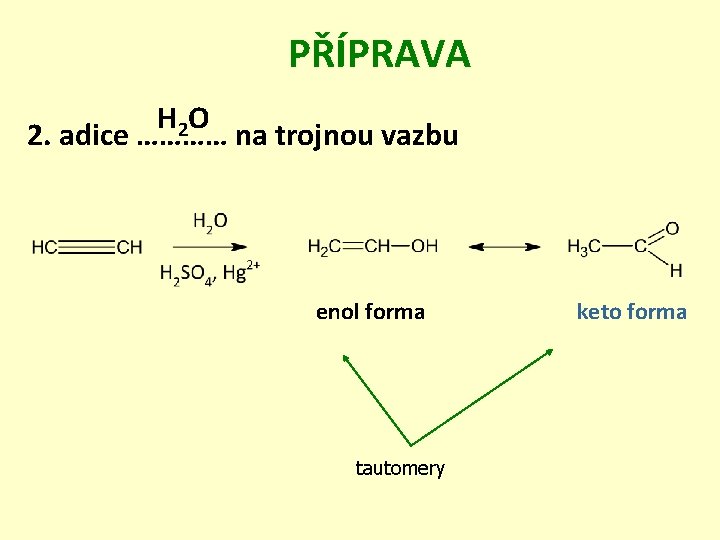
PŘÍPRAVA H 2 O 2. adice ………… na trojnou vazbu enol forma tautomery keto forma
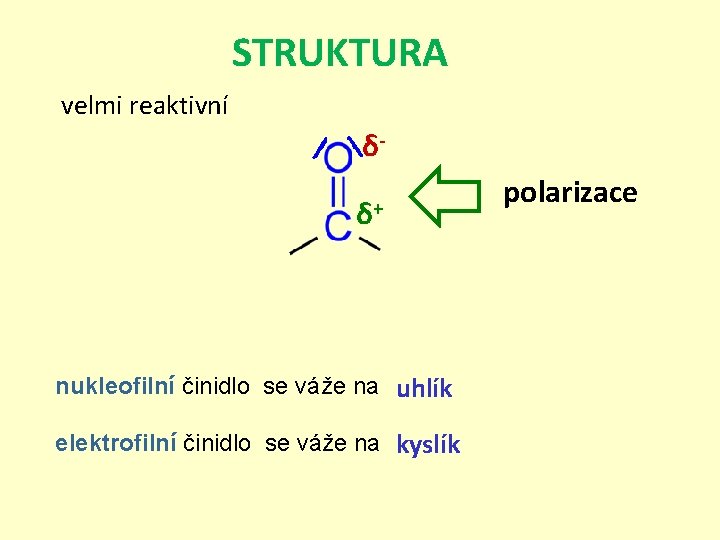
STRUKTURA velmi reaktivní δδ+ nukleofilní činidlo se váže na uhlík elektrofilní činidlo se váže na kyslík polarizace
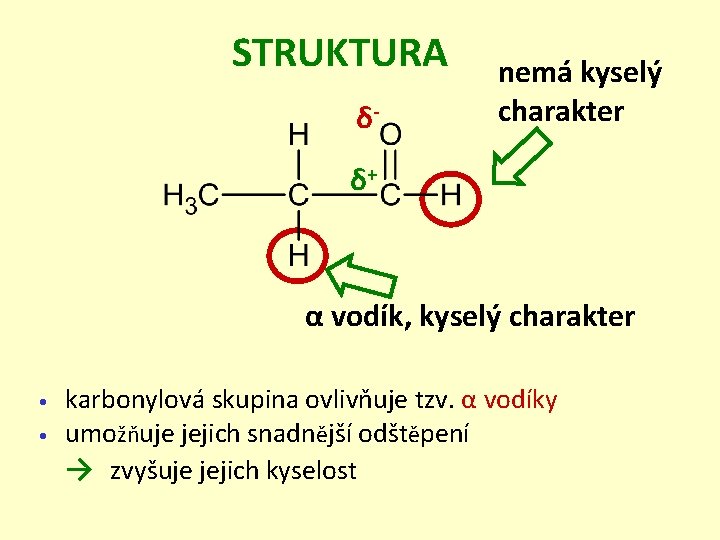
STRUKTURA δ- nemá kyselý charakter δ+ α vodík, kyselý charakter • • karbonylová skupina ovlivňuje tzv. α vodíky umožňuje jejich snadnější odštěpení → zvyšuje jejich kyselost
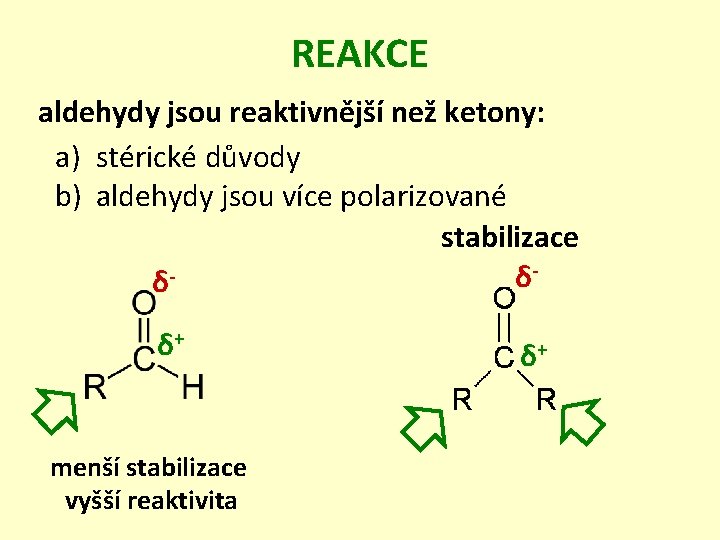
REAKCE aldehydy jsou reaktivnější než ketony: a) stérické důvody b) aldehydy jsou více polarizované stabilizace δ δ δ+ menší stabilizace vyšší reaktivita δ+

REAKCE 1. nukleofilní adice na karbonylovou skupinu a) adice vody b) adice alkoholu – vznik poloacetalů a acetalů nukleofil: záporný náboj: OH-, CNvolný e- pár: H 2 O, R-OH, NH 3, R-NH 2, 2. substituce na α uhlíku a) aldolová kondenzace b) jodoformová reakce 3. oxidace 4. redukce
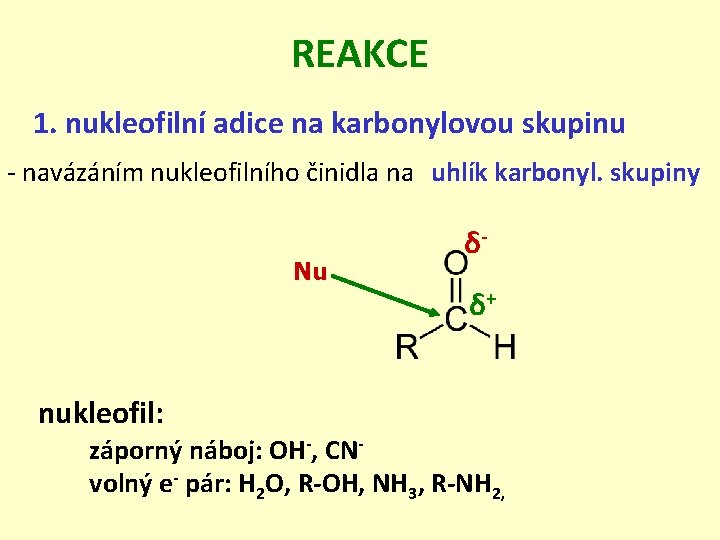
REAKCE 1. nukleofilní adice na karbonylovou skupinu - navázáním nukleofilního činidla na uhlík karbonyl. skupiny Nu δδ+ nukleofil: záporný náboj: OH-, CNvolný e- pár: H 2 O, R-OH, NH 3, R-NH 2,
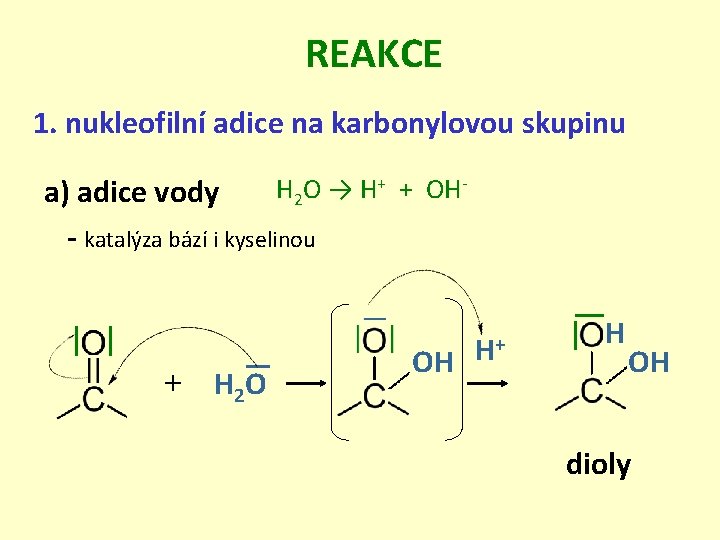
REAKCE 1. nukleofilní adice na karbonylovou skupinu H 2 O → H+ + OHa) adice vody - katalýza bází i kyselinou + H 2 O OH H+ H OH dioly
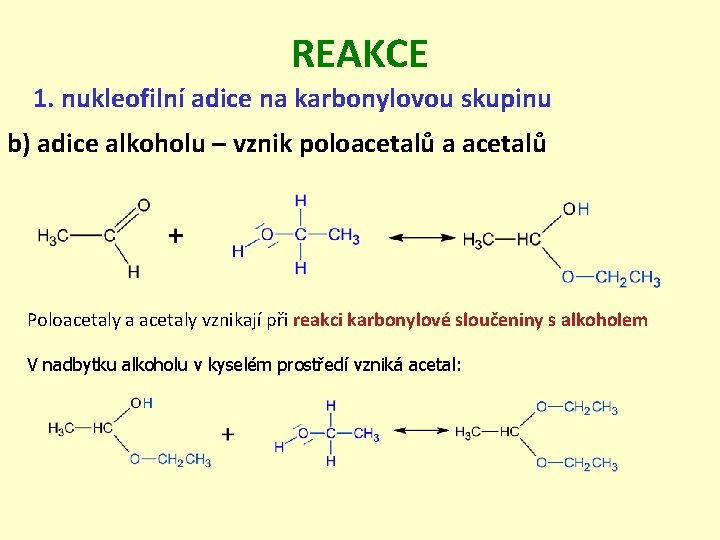
REAKCE 1. nukleofilní adice na karbonylovou skupinu b) adice alkoholu – vznik poloacetalů a acetalů Poloacetaly a acetaly vznikají při reakci karbonylové sloučeniny s alkoholem. V nadbytku alkoholu v kyselém prostředí vzniká acetal:

REAKCE 1. nukleofilní adice na karbonylovou skupinu a) adice vody b) adice alkoholu – vznik poloacetalů a acetalů nukleofil: záporný náboj: OH-, CNvolný e- pár: H 2 O, R-OH, NH 3, R-NH 2, 2. substituce na α uhlíku a) aldolová kondenzace b) jodoformová reakce 3. oxidace 4. redukce
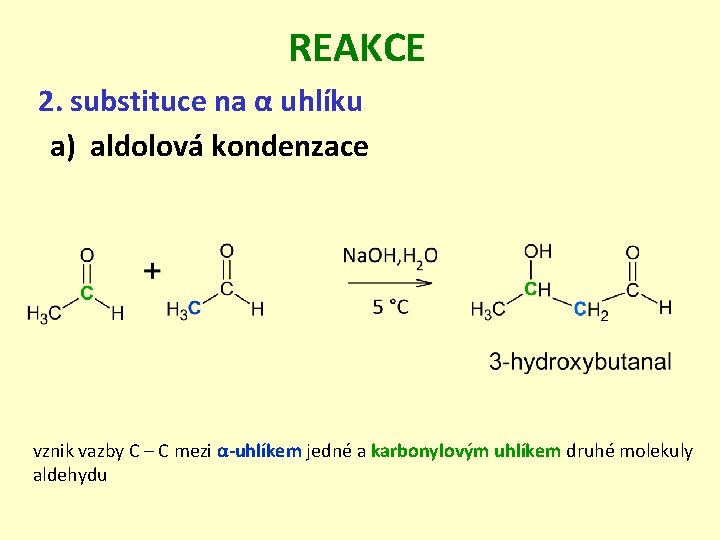
REAKCE 2. substituce na α uhlíku a) aldolová kondenzace vznik vazby C – C mezi α-uhlíkem jedné a karbonylovým uhlíkem druhé molekuly aldehydu
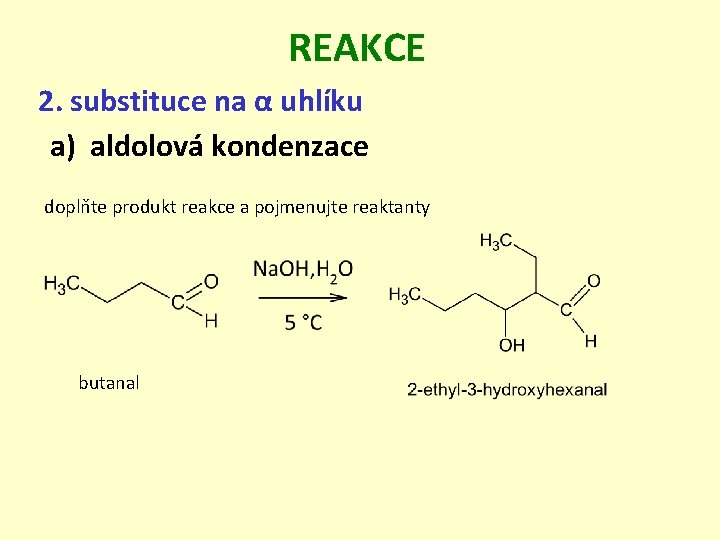
REAKCE 2. substituce na α uhlíku a) aldolová kondenzace doplňte produkt reakce a pojmenujte reaktanty butanal
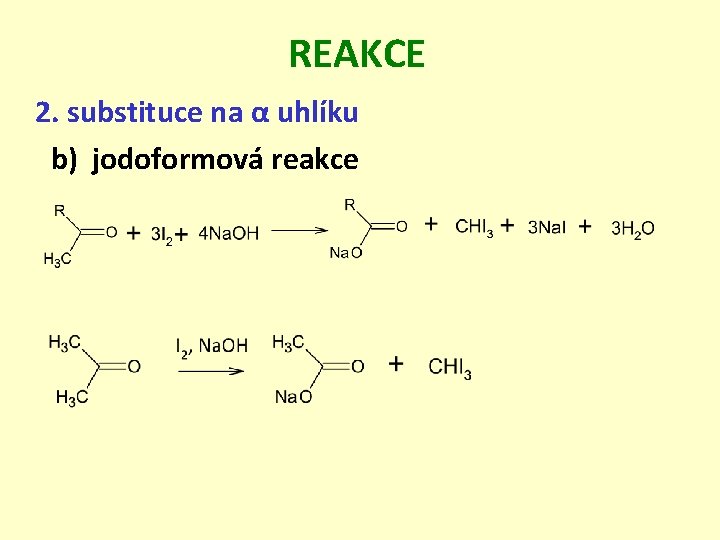
REAKCE 2. substituce na α uhlíku b) jodoformová reakce

REAKCE 2. substituce na α uhlíku b) jodoformová reakce CH 3 CH 2 OH CH 3 CHO + I 2 + Na. OH CHI 3+ HCOONa HCHO/CH 3 OH + I 2+Na. OH nevzniká nic

REAKCE 1. nukleofilní adice na karbonylovou skupinu a) adice vody b) adice alkoholu – vznik poloacetalů a acetalů nukleofil: záporný náboj: OH-, CNvolný e- pár: H 2 O, R-OH, NH 3, R-NH 2, 2. substituce na α uhlíku a) aldolová kondenzace b) jodoformová reakce 3. oxidace 4. redukce
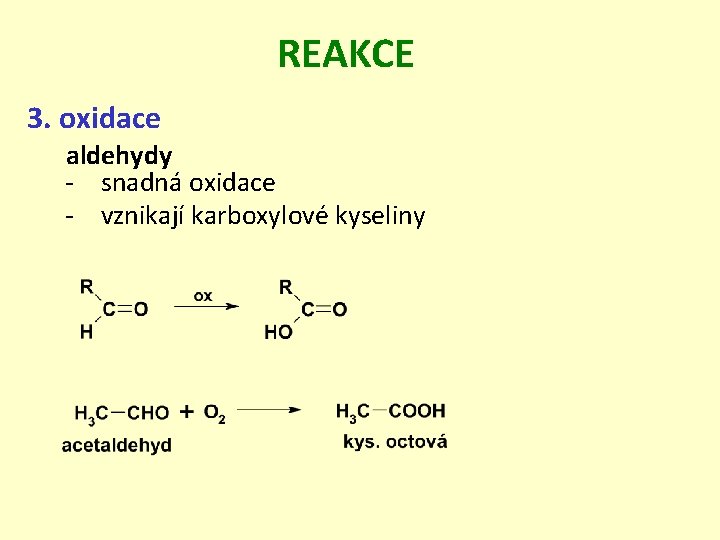
REAKCE 3. oxidace aldehydy - snadná oxidace - vznikají karboxylové kyseliny
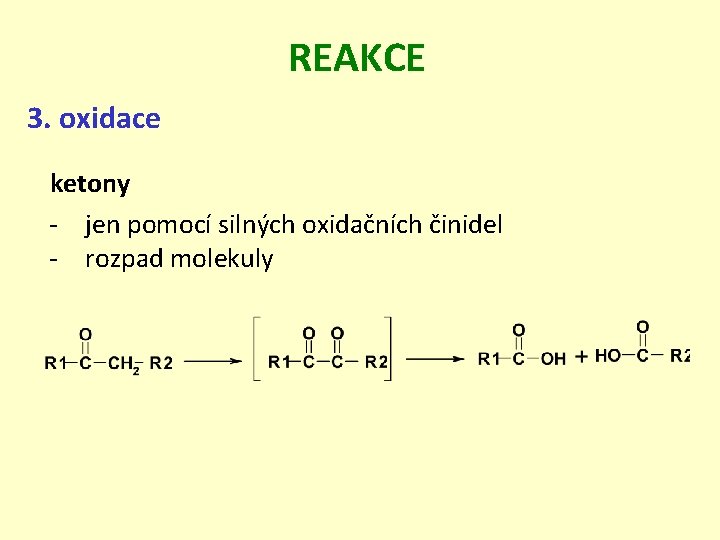
REAKCE 3. oxidace ketony - jen pomocí silných oxidačních činidel - rozpad molekuly
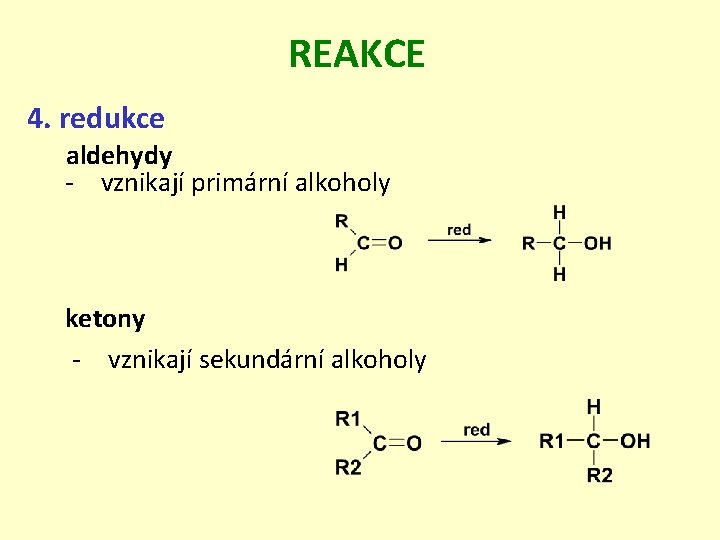
REAKCE 4. redukce aldehydy - vznikají primární alkoholy ketony - vznikají sekundární alkoholy
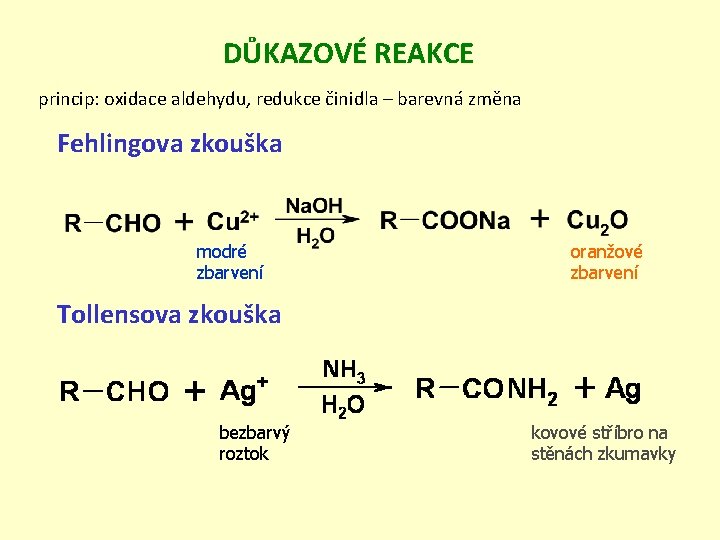
DŮKAZOVÉ REAKCE princip: oxidace aldehydu, redukce činidla – barevná změna Fehlingova zkouška modré zbarvení oranžové zbarvení Tollensova zkouška bezbarvý roztok kovové stříbro na stěnách zkumavky

DŮKAZOVÉ REAKCE Schiffova reakce • tato reakce využívá reakce karbonylové skupiny se Schiffovým činidem roztok červeného barviva fuchsinu je odbarven hydrogensiřičitanem nebo oxidem siřičitým • Schiffovo činidlo se s aldehydem barví opět do fialova [obr. 4] [obr. 5] Hugo (Ugo) Schiff

ZÁSTUPCI

VÝSKYT - hojně v přírodě - složky chuťových látek a vonných silic - řada metabolicky významná [obr. 7] [obr. 6]
![mařinka vonná KUMARIN [obr. 9] tonkové boby [obr. 8] VANILIN [obr. 10] vanilovník plocholistý mařinka vonná KUMARIN [obr. 9] tonkové boby [obr. 8] VANILIN [obr. 10] vanilovník plocholistý](http://slidetodoc.com/presentation_image/47e1fa71720fa9eab525df7327b60676/image-33.jpg)
mařinka vonná KUMARIN [obr. 9] tonkové boby [obr. 8] VANILIN [obr. 10] vanilovník plocholistý
![Amygdalin [obr. 11] [obr. 12] [obr. 13] BENZALDEHYD Amygdalin [obr. 11] [obr. 12] [obr. 13] BENZALDEHYD](http://slidetodoc.com/presentation_image/47e1fa71720fa9eab525df7327b60676/image-34.jpg)
Amygdalin [obr. 11] [obr. 12] [obr. 13] BENZALDEHYD
![vitamín A – retinal - retinaldehyd Rakytník řešetlákový [obr. 14] 3, 7 -dimethyl-9 -(2, vitamín A – retinal - retinaldehyd Rakytník řešetlákový [obr. 14] 3, 7 -dimethyl-9 -(2,](http://slidetodoc.com/presentation_image/47e1fa71720fa9eab525df7327b60676/image-35.jpg)
vitamín A – retinal - retinaldehyd Rakytník řešetlákový [obr. 14] 3, 7 -dimethyl-9 -(2, 6, 6 -trimethylcyklohexen-1 -yl) nona-2, 4, 6, 8 -tetraenal

Methanal formaldehyd HCHO Je bezbarvý plyn, ostrého zápachu. Je toxický, žíravý a karcinogenní! V praxi se používá jeho 40% roztok – formalín Je jedním z metabolitů methanolu zodpovědným za jeho toxicitu. [obr. 15]

Ethanal (acetaldehyd), CH 3–CHO, je bezbarvá, hořlavá kapalina štiplavého zápachu. Snadno polymerizuje na metaldehyd. Ten lze použít jako tuhý podpalovač (suchý líh) do lihových turistických vařičů.

Propanon (aceton), CH 3–CO–CH 3, je vysoce hořlavá a dráždivá látka. Je výborným ředidlem barev rozpouštědlem některých lepidel. Produkty reakce acetonu s halogeny mají slzotvorné účinky.
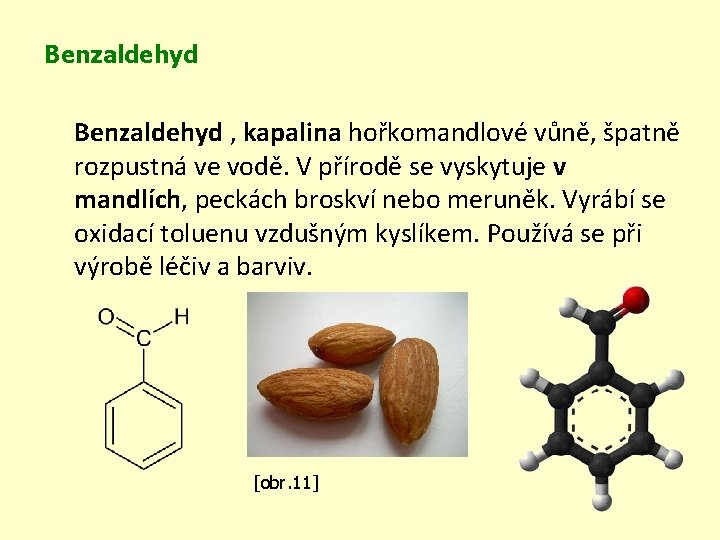
Benzaldehyd , kapalina hořkomandlové vůně, špatně rozpustná ve vodě. V přírodě se vyskytuje v mandlích, peckách broskví nebo meruněk. Vyrábí se oxidací toluenu vzdušným kyslíkem. Používá se při výrobě léčiv a barviv. [obr. 11]
![Odkazy: [obr. 1] http: //upload. wikimedia. org/wikipedia/commons/b/bc/NHM_formaldehyde. jpg [obr. 2] http: //www. e-cukrovinky. cz/e-cukrovinky/eshop/25 Odkazy: [obr. 1] http: //upload. wikimedia. org/wikipedia/commons/b/bc/NHM_formaldehyde. jpg [obr. 2] http: //www. e-cukrovinky. cz/e-cukrovinky/eshop/25](http://slidetodoc.com/presentation_image/47e1fa71720fa9eab525df7327b60676/image-40.jpg)
Odkazy: [obr. 1] http: //upload. wikimedia. org/wikipedia/commons/b/bc/NHM_formaldehyde. jpg [obr. 2] http: //www. e-cukrovinky. cz/e-cukrovinky/eshop/25 -1 -Na-vareni-a-peceni [obr. 3] http: //www. biovanilka. cz/ [obr. 4] http: //www. foodcolors. in/basic-fuchsin-828181. html [obr. 5] http: //canov. jergym. cz/cinidla/s. htm [obr. 6] http: //www. tilligerryhabitat. org. au/ [obr. 7] http: //www. rosliny-nasiona. pl/egzotyczne-rosliny/231 -eukaliptus-galkowy-eucalyptus-globulus-iloc-nasion-10 -szt. html [obr. 8] http: //cs. wikipedia. org/wiki/Sv%C 3%ADzel_vonn%C 3%BD [obr. 9] http: //cs. wikipedia. org/wiki/Tonkov%C 3%A 9_boby#mediaviewer/Soubor: Tonka_Beans. jpg [obr. 10] http: //cs. wikipedia. org/wiki/Vanilovn%C 3%ADk_plocholist%C 3%BD#mediaviewer/Soubor: Vanilla_planifolia_1. jpg [obr. 11] http: //cs. wikipedia. org/wiki/Mandle_(plod)#mediaviewer/Soubor: Almonds 02. jpg [obr. 12] http: //cs. wikipedia. org/wiki/Mandlo%C 5%88#mediaviewer/Soubor: Illustration_Prunus_dulcis 0. jpg [obr. 13] http: //en. wikipedia. org/wiki/Prunus_armeniaca#mediaviewer/File: Apricot_and_cross_section. jpg [obr. 14] http: //cs. wikipedia. org/wiki/Rakytn%C 3%ADk_%C 5%99 e%C 5%A 1 etl%C 3%A 1 kov%C 3%BD#mediaviewer/Soubor: Hippoph ae_rhamnoides. jpg [obr. 15] http: //eshop. mach-chemikalie. cz/product_info. php? products_id=66
- Slides: 40