Karboksilne kiseline Nastavni predmet Organska kemija Ekoloki tehniar3

Karboksilne kiseline Nastavni predmet: Organska kemija Ekološki tehničar-3. razred Trajanje: 2 sata Autor: Zorica Majić, prof.

Dragi učenici i drage učenice, kako bismo vam olakšali učenje za vas smo pripremili materijale za samostalni rad. U ovoj prezentaciji su sadržaji koji se odnose na nastavni predmet: Organska kemija Također prezentacija sadrži i zadatke za vježbu. Na kraju prezentacije nalaze se pitanja za ponavljanje gradiva. Vaši nastavnici će vam također pružati podršku u učenju na daljinu.

KARBOKSILNE KISELINE
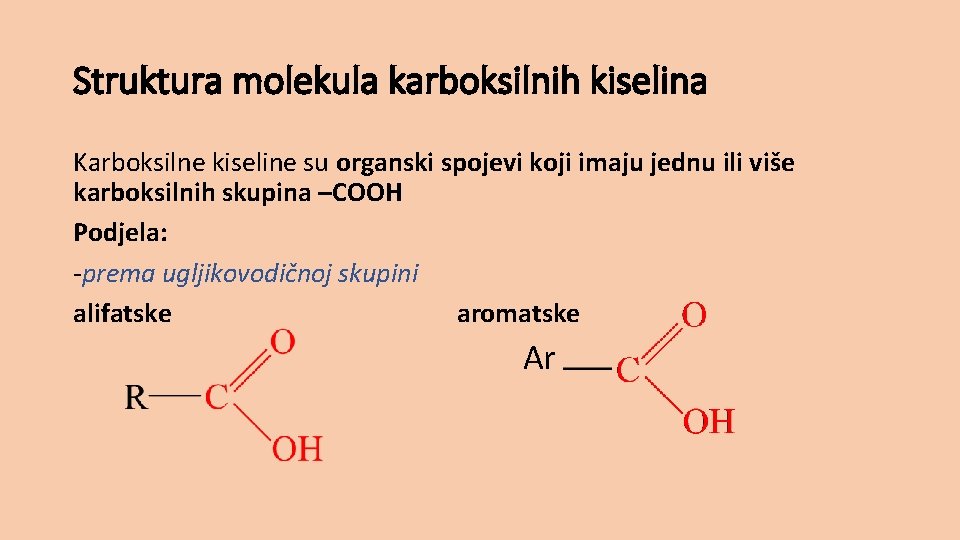
Struktura molekula karboksilnih kiselina Karboksilne kiseline su organski spojevi koji imaju jednu ili više karboksilnih skupina –COOH Podjela: -prema ugljikovodičnoj skupini alifatske aromatske Ar
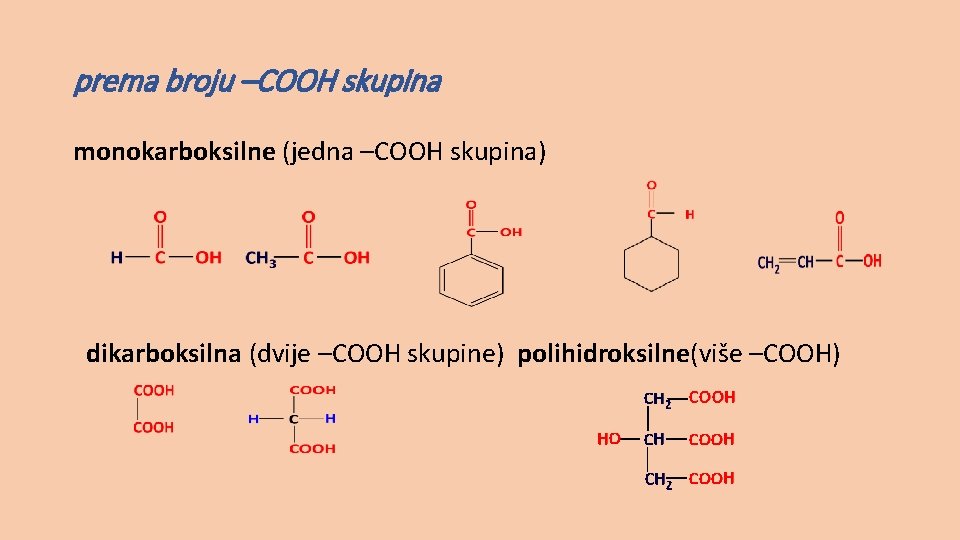
prema broju –COOH skupina monokarboksilne (jedna –COOH skupina) dikarboksilna (dvije –COOH skupine) polihidroksilne(više –COOH)
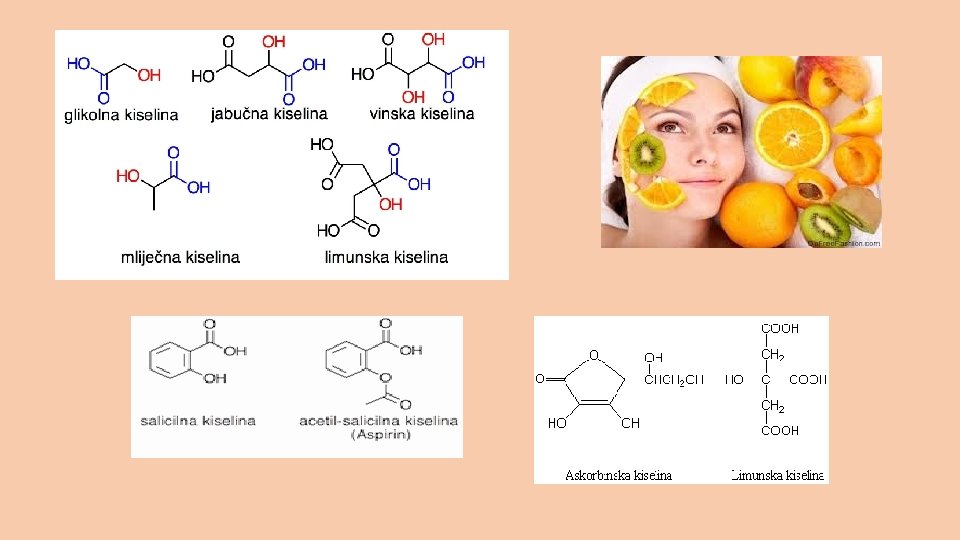

Nomenklatura alifatskih karboksilnih kiselina • Sustavna imena-imenu najduljeg ugljikovodika doda se nastavak –ska kiselina (karbonilni ugljik u lancu ima broj 1!)

Nomenklatura karboksilnih kiselina

Imena aromatskih karboksilnih kiselina • Imenu aromatskog dijela molekule doda se nastavak karboksilna kiselina
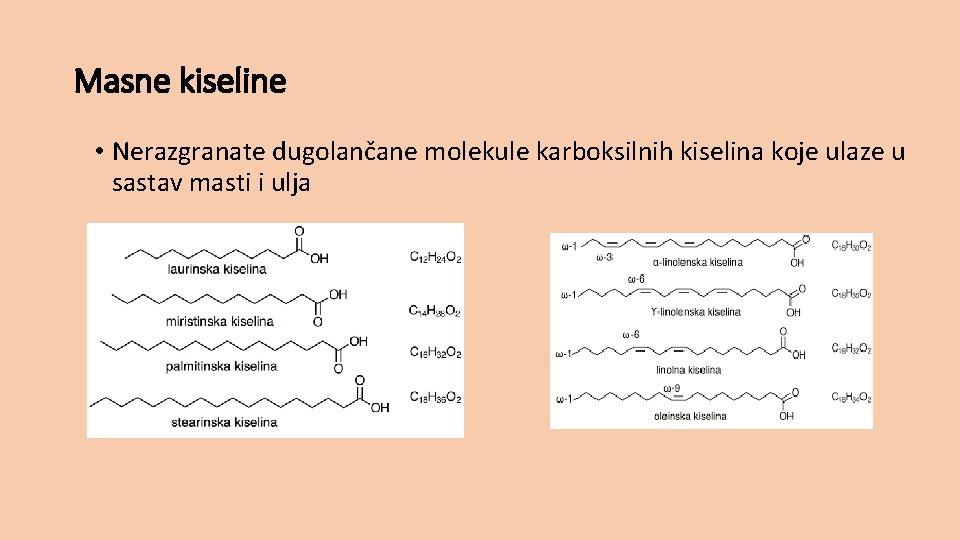
Masne kiseline • Nerazgranate dugolančane molekule karboksilnih kiselina koje ulaze u sastav masti i ulja

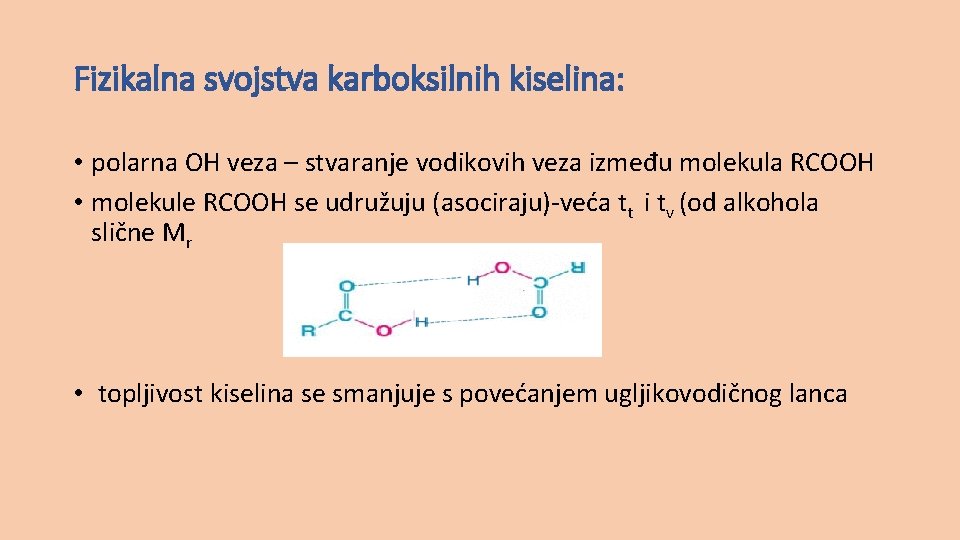
Fizikalna svojstva karboksilnih kiselina: • polarna OH veza – stvaranje vodikovih veza između molekula RCOOH • molekule RCOOH se udružuju (asociraju)-veća tt i tv (od alkohola slične Mr • topljivost kiselina se smanjuje s povećanjem ugljikovodičnog lanca
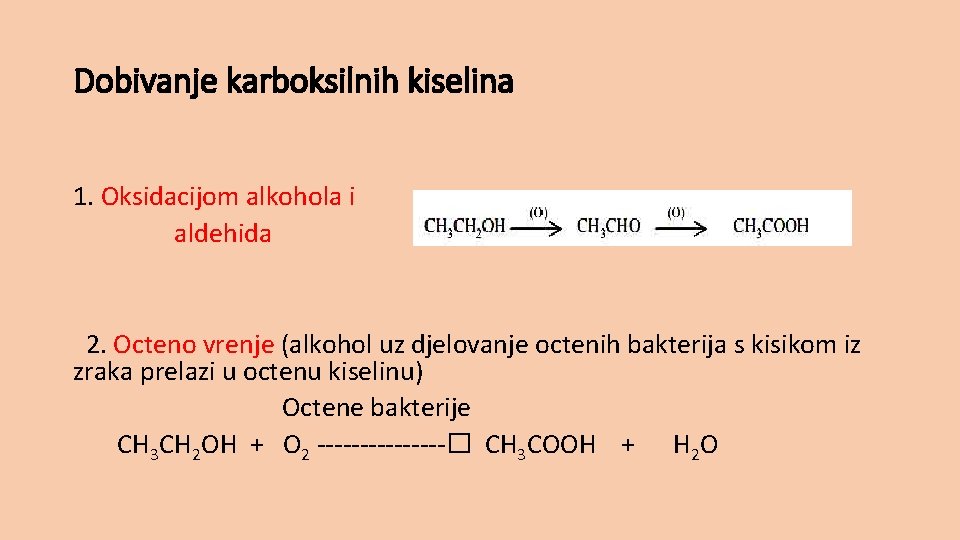
Dobivanje karboksilnih kiselina 1. Oksidacijom alkohola i aldehida 2. Octeno vrenje (alkohol uz djelovanje octenih bakterija s kisikom iz zraka prelazi u octenu kiselinu) Octene bakterije CH 3 CH 2 OH + O 2 --------� CH 3 COOH + H 2 O

Kemijska svojstva karboksilnih kiselina: 1. Kiselost (posljedica disocijacije kiselina u vodenim otopinama)-povećava se koncentracija oksonijevih iona, H 3 O+ HCOOH + H 2 O→ H 3 O+ + HCOOkarboksilatni ion Jakost karboksilnih kiselina iskazuje se konstantom disocijacije, Ka Ka(HCOOH)= 3, 77 Ka(CH 3 COOH)=4, 76 2. Neutralizacija s bazama nastaju soli topljive u vodi- karboksilati HCOOH + Na. OH → HCOONa + H 2 O natrijev formijat

Imena soli karboksilnih kiselina: • dobiju se tako da se osnovnom ugljikovodiku doda nastavak- oat ili kod cikličkih kiselina- karboksilat npr. soli metanske kiseline metanoati ( formijati) etanske kiseline etanoati ( acetati ) benzenkarboksilne kiseline – benzenkarboksilati (benzoati)

Uporaba karboksilnih kiselina: • Metanska ili mravlja kiselina(HCOOH) -bezbojna i bistra tekućina oštra mirisa - u doticaju s kožom stvara crvenilo i plikove - prvi put izolirana iz mrava, kao sredstvo za obranu nalazi se u žarnicama meduza, pčela i kopriva -soli formijati (lat. formica= mrav)

Etanska ili octena kiselina (CH 3 COOH) • bistra bezbojna tekućina oštra mirisa • na 17 ⁰C , 99, 5%-tna kristalizira- ledena octena kiselina • dobro otapalo i sirovina za sintezu plastični masa, lijekova, boja • 9%-tna otopina-ocat • koristi se za konzerviranje povrća, • zakiseljavanja salata i jela • soli acetati (lat. acetum= ocat)
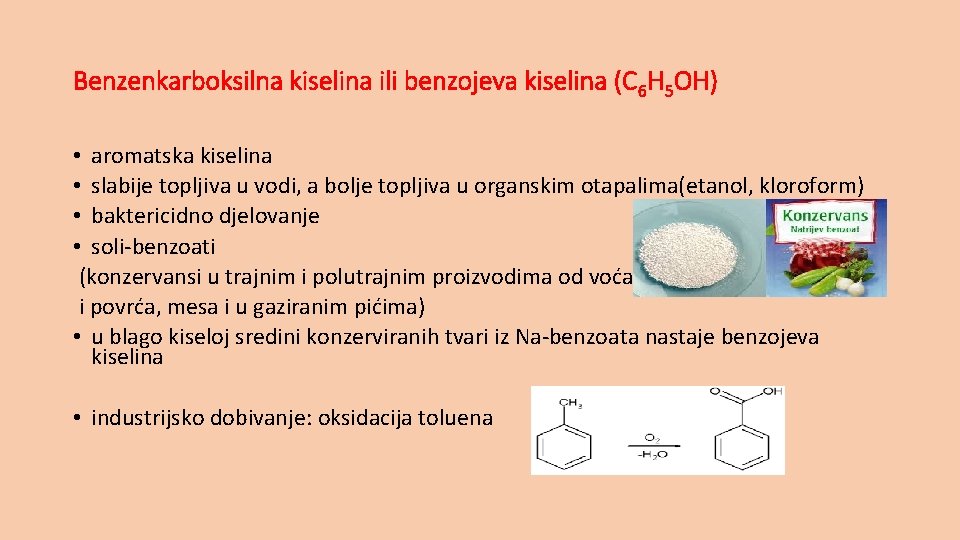
Benzenkarboksilna kiselina ili benzojeva kiselina (C 6 H 5 OH) • aromatska kiselina • slabije topljiva u vodi, a bolje topljiva u organskim otapalima(etanol, kloroform) • baktericidno djelovanje • soli-benzoati (konzervansi u trajnim i polutrajnim proizvodima od voća i povrća, mesa i u gaziranim pićima) • u blago kiseloj sredini konzerviranih tvari iz Na-benzoata nastaje benzojeva kiselina • industrijsko dobivanje: oksidacija toluena

Pitanja za ponavljanje Dopuni slijedeće tvrdnje: 1. Funkcionalna skupina karboksilnih kiselina je________ 2. Karboksilne kiseline koje ulaze u sastav masti i ulja zovu se ______ 3. Najjednostavnija aromatska karboksilna kiselina je _______ 4. Neutralizacijom karboksilnih kiselina s bazom nastaju ____i ______ 5. Soli metanske kiseline nazivaju se _______, a soli etanske kiseline_________
- Slides: 19