karakteristik unsurunsur penting kegunaan dan bahayanya serta terdapatnya



karakteristik unsur-unsur penting, kegunaan dan bahayanya, serta terdapatnya di alam

Mengidentifikasi kelimpahan unsur utama dan transisi di alam dan produk yang mengandung unsur tersebut

1. Mengidentifikasi keberadaan unsur-unsur yang ada di alam terutama di Indonesia (gas mulia, halogen, alkali tanah, aluminium, karbon, silikon, belerang, krom, tembaga, seng, besi, oksigen dan nitrogen) 2. Mengidentifikasi produk-produk yang mengandung zat tersebut

Unsur-unsur golongan utama dan transisi

KELIMPAHAN UNSUR DAN SIFATNYA

KELIMPAHAN UNSUR DALAM KULIT BUMI Unsur Oksigen Silikon % massa 49, 2 25, 67 Unsur % massa Titanium 058 Klorin 0, 19 Aluminium 7, 50 Fosforus 0, 11 Besi 4, 71 Mangan 0, 09 Kalsium 3, 39 Karbon 0, 08 Natrium 2, 63 Belerang 0, 06 Kalium 2, 40 Barium 0, 04 Magnesium 1, 93 Nitrogen 0, 03 Higrogen 0, 87 Fluorin 0, 02

Komposisi Udara Bersih dan Kering KOMPONEN KONSENTRASI (%) Nirogen 78, 09 Oksigen 20, 94 Argon 0, 934 Karbondioksida 0, 0315 Neon 0, 0018 Helium 0, 00052 Metana 0, 00012 Kripton 0, 0001 Karbon monoksida 0, 00001 Dinitrogen monoksida 0, 00005 Hidrogen 0, 00005 Xenon 0, 000008 Nitrogen dioksida 0, 000002

SEBAGIAN BESAR UNSUR DI ALAM BERADA DALAM BENTUK SENYAWA OKSIDA, SULFAT, POSPAT, KARBONAT, HALIDA DAN SILIKAT DAN SEBAGIAN KECIL BERADA DI ALAM DALAM KEADAAN BEBAS

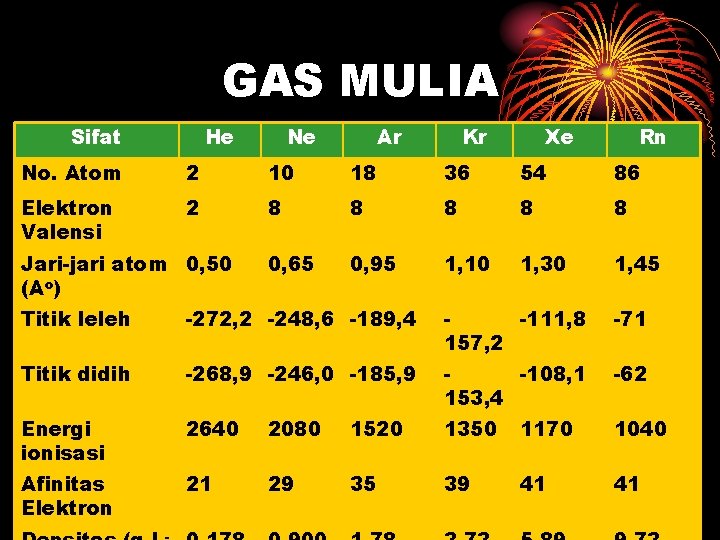
GAS MULIA Sifat He Ne Ar Kr Xe Rn No. Atom 2 10 18 36 54 86 Elektron Valensi 2 8 8 8 0, 65 0, 95 1, 10 1, 30 1, 45 Jari-jari atom 0, 50 (Ao) Titik leleh -272, 2 -248, 6 -189, 4 -111, 8 157, 2 -71 Titik didih -268, 9 -246, 0 -185, 9 -108, 1 153, 4 -62 Energi ionisasi 2640 2080 1520 1350 1170 1040 Afinitas Elektron 21 29 35 39 41 41

Gas Mulia • Mengapa gas Mulia sukar bereaksi (stabil) ? • Mengapa titik leleh dan titik didih gas mulia sangat rendah ? • Berdasarkan literatur, mengapa hanya Kr dan Xe saja yang dapat disintesa senyawanya ? , dan sebutkan contoh senyawanya ! • Tentukan jenis hibridisasi dan bentuk geometri molekul dari senyawa, • Xe. F 4

HALOGEN F F Cl Cl Br Br I I
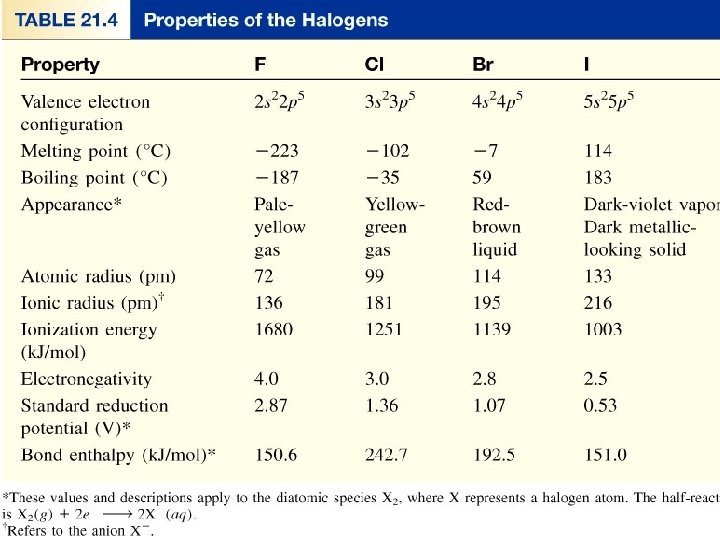

Daya Oksidasi Halogen dan Daya Reduksi Ion Halida • Berdasarkan Harga Eo nya urutan daya oksidasi gas halogen F 2 > Cl 2 > Br 2 > I 2 • Daya reduksi ion halidanya F- < Cl- < Br-< IDapatkah reaksi berikut berlangsung: Cl 2 + KBr Br- + I 2 F- + Cl 2

• Struktur molekul Halogen F 2 + + Cl 2 + Br 2 + I 2 Bagaimana anda dapat menjelaskan kereaktifan gas-gas halogen berdasarkan harga energi ikatannya ? + +

Wujud dan Warna Gas Halogen. Bagaimana anda menjelaskan kenaikan titik leleh dan titik didih dari atas ke bawah ? Berdasarkan titik leleh dan titik didihnya, ramalkan wujud unsur halogen pada suhu kamar ( 25 o. C ). + + F 2 + + Cl 2 + + Br 2 + + I 2

Kelarutan Halogen dalam air • Halogen adalah senyawa non polar yang berarti tidak larut dalam air. Berarti hanya larut dalam pelarut Organik/ non polar. (CCl 4) • Bila halogen laru tdalam air, itu karena halogen bereaksi dengan air. 2 F 2 + 2 H 2 O 4 HF + O 2 • Cl 2 , Br 2 dan I 2 sukar larut dalam air. • I 2 mudah larut dalam larutan KI, karena akan membentuk ion poli iodida. I 2 + I - I 3 -

• Kereaktifan unsur Halogen Keraktifan unsur halogen (non logam) dapat dilihat dari harga Avinitas elektron atau keelektronegatifannya. • Halogen hampir dapat bereaksi dengan semua unsur. a. Dengan Gas Hidrogen. H 2 + X 2 2 HX b. Dengan unsur logam. 2 M + n. X 2 2 MXn

Bereaksi dengan unsur non logam lain seperti Si, P, S dan Sn. Dengan Silikon: Si + F 2 Si. F 4 Dengan Pospor: P + Cl 2(terbatas) PCl 3 P + Cl 2(berlebih) PCl 5 Dengan hidrokarbon : CH 4 + Cl 2 CH 3 Cl + HCl Dengan larutan Basa (Na. OH) Cl 2 + Na. OH Na. Cl + Na. Cl. O + H 2 O Cl 2 + Na. OHpanas Na. Cl + Na. Cl. O 3 + H 2 O

Halogen dapat memiliki bil. Oksidasi -1 s/d +7 Bilok Nama Fluor Clor Brom Iod -1 Halida HF HCl HBr HI 0 Unsur F 2 Cl 2 Br 2 I 2 +1 Hipoha lit - Cl. O- Br. O- IO- +3 Halit - Cl. O 2 - Br. O 2 - IO 2 - +5 Halat - Cl. O 3 - Br. O 3 - IO 3 - +7 Perhal at - Cl. O 4 - Br. O 4 - IO 4 -

KEKUATAN ASAM OKSI HALOGEN • Kekuatan asam oksihalida semakin kuat dengan bertambahnya jumlah atom Oksigen O H ׃ Cl O H ׃ Cl O O H ׃ O O Diantara ikatan-ikatan tersebut manakah yang paling mudah putus. (paling mudah melepaskan ion H+) Cl O O
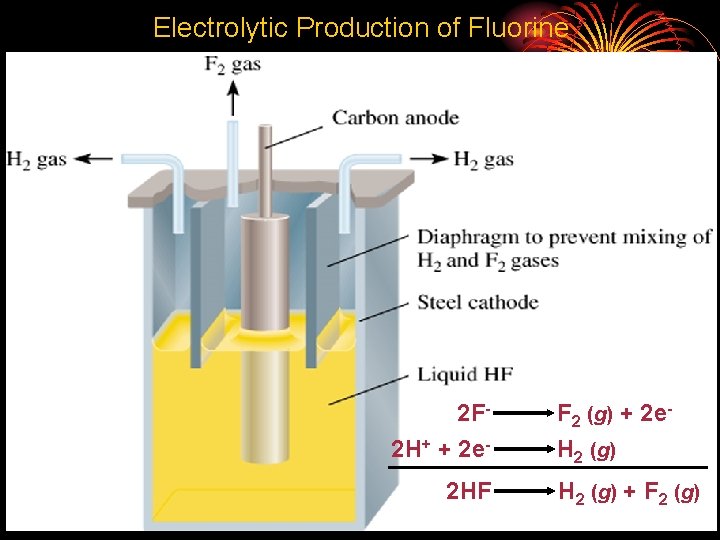
Electrolytic Production of Fluorine 2 F 2 H+ + 2 e 2 HF F 2 (g) + 2 e. H 2 (g) + F 2 (g)
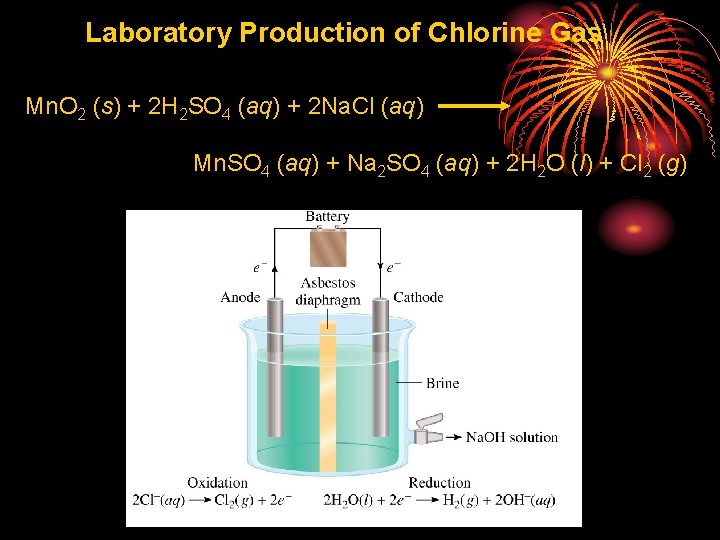
Laboratory Production of Chlorine Gas Mn. O 2 (s) + 2 H 2 SO 4 (aq) + 2 Na. Cl (aq) Mn. SO 4 (aq) + Na 2 SO 4 (aq) + 2 H 2 O (l) + Cl 2 (g)
- Slides: 25

















































