Kapittel N Den romlige formen til molekyler Hybridisering

Kapittel N Den romlige formen til molekyler. Hybridisering av atomorbitaler

Lewisstrukturer • Elektronprikkformler for molekyler eller ioner kalles Lewisstrukturer. • Bindingselektronene tegnes som streker, mens ledige elektronpar tegnes med prikker. • Oktettregelen skal så langt det er mulig være oppfylt når vi tegner Lewisstrukturer.
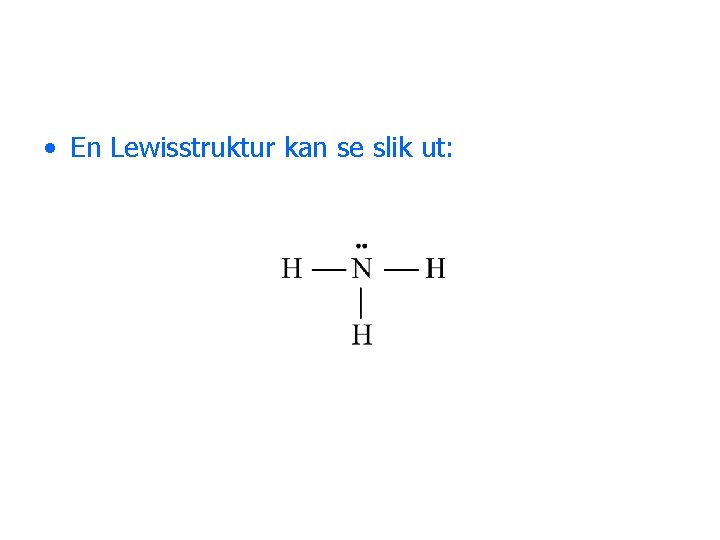
• En Lewisstruktur kan se slik ut:
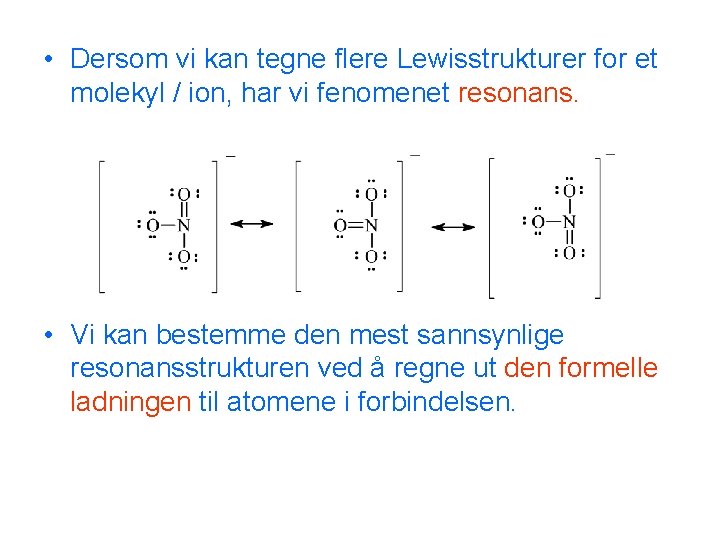
• Dersom vi kan tegne flere Lewisstrukturer for et molekyl / ion, har vi fenomenet resonans. • Vi kan bestemme den mest sannsynlige resonansstrukturen ved å regne ut den formelle ladningen til atomene i forbindelsen.

Unntak fra oktettregelen • Det fins stoffer der oktettregelen ikke er oppfylt. Vi kan ha • Ufullstendig oktett, der vi har færre enn 8 elektroner i ytre skall. • Utvidet oktett, der vi har flere enn 8 elektroner i ytre skall. I slike forbindelser puttes elektroner inn i ledige d-orbitaler fra det samme elektronskallet.

VSEPR-teori • Vi kan bestemme den romlige formen til molekyler ved hjelp av VSEPR-teorien. • Den går ut på at elektronskyene til bindingselektronene vil stille seg inn i maksimal avstand fra hverandre. • Vi må også ta hensyn til frastøtingskreftene fra ledige elektronpar.

Hybridisering • VSEPR-teorien vil gi oss vinkler mellom elektronskyene i en forbindelse som vi ikke finner hos de frie atomene som lager denne forbindelsen. • Når forbindelsen dannes, vil elektronskyene til atomene (orbitalene) gå sammen og lage hybridorbitaler. Disse vil stille seg inn med de riktige vinklene.
- Slides: 7