Kapittel J Atomenes elektronstruktur Problemer med Bohrs atommodell

Kapittel J Atomenes elektronstruktur

Problemer med Bohrs atommodell • Bohrs modell sier oss at elektronene går rundt atomkjerna i faste baner. Men ved en slik bevegelse må de etter hvert miste energi. • Siden dette ikke skjer, må Bohrs modell være feil. • Lang tids forsking og tankevirksomhet måtte til!
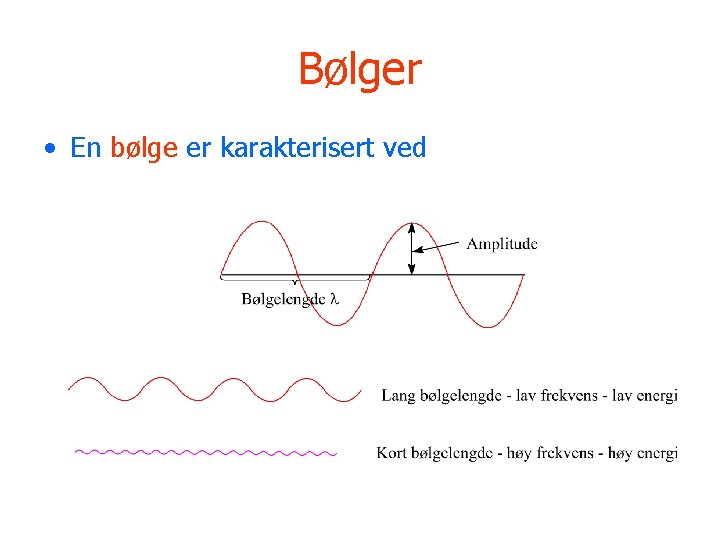
Bølger • En bølge er karakterisert ved

• Det elektromagnetiske spektrum strekker seg fra radiobølger med bølgelengder på 1012 nm via synlig lys (750 nm – 400 nm) ned til gammastråler med bølgelengder på 10 -2 nm. • 1 nm = 10 -9 m.

Max Planck • Når et svart legeme varmes opp, sender det ut lys med stadig høyere energi. • Planck antok at energien ikke kan ha alle verdier, men har helt bestemte energier E gitt ved E = h f, der h kalles Plancks konstant.

Bølge-partikkeldualismen • Hva er lys? • Lys oppfører seg som en bølge når det støter på minimale hindringer. • Einstein fant ut at lys oppfører seg som en liten partikkel (foton) når det enten blir sendt ut eller tatt opp av en gjenstand (fotoelektrisk effekt).

• Grunnstoff sender ut lys med karakteristiske farger (og dermed bølgelengder) når de tilføres energi. • Niels Bohr antok at elektronet tar opp en helt bestemt energi og går over i en annen bane med høyere energi (eksitasjon). • Det faller straks tilbake til grunntilstanden, og gir da denne energien fra seg i form av lys – synlig eller usynlig.

Hydrogenatomet • Bohr utledet en formel som ga energien til lyset som ble sendt ut fra hydrogenatomet. Det stemte fremragende med det vi kan observere.

Louis de Broglie • Bohrs modell stemte dessverre ikke så godt for atomer med flere enn ett elektron. • De Broglie antok at bølge-partikkeldualismen også gjaldt for elektronet – som dermed kunne ha bølgeegenskaper.

Werner Heisenberg • Werner Heisenberg fant ut at det ikke er mulig å bestemme posisjonen til et elektron helt nøyaktig. • Jo mer nøyaktig vi kjenner farten til en partikkel, desto mindre nøyaktig kjenner vi posisjonen. • Vi kan derfor bare snakke om sannsynligheter for å treffe på et elektron et bestemt sted rundt atomkjerna.

• Erwin Schrödinger klarte å stille opp likningen som beskriver elektronbevegelsen rundt et hydrogenatom. • Løsningene av denne likningen gir oss energinivåene til hydrogenatomet – som har fått navnet atomorbitaler. En orbital angir altså sannsynligheten for å treffe på et elektron rundt atomkjerna. • Orbitalene er karakterisert ved tre tall – kvantetallene.

Kvantetallene • Hovedkvantetallet n angir størrelsen på orbitalene. • Bikvantetallet l angir formen på orbitalene. • Det magnetiske kvantetallet ml angir retningen av orbitalene ut fra atomkjerna.

• Elektroner med samme verdi av n ligger i samme elektronskall, som har fått betegnelsene K, L, M, N osv. • Elektroner med samme verdi av l ligger i samme underskall, som har fått betegnelsene s, p, d og f. • Elektroner med samme verdi av ml ligger i samme orbital. Disse betegnes med en kombinasjon av tall og bokstaver (3 s, 2 p, 3 d, 4 f osv). • K-skallet er nr. 1, L-skallet er nr. 2 osv.
- Slides: 13