Kapitel 14 Syror och baser Kapitel 14 Innehll

Kapitel 14 Syror och baser
Kapitel 14 Innehåll 14. 1 14. 2 14. 3 14. 4 14. 5 14. 6 14. 7 14. 8 14. 9 14. 10 14. 11 14. 12 Syror och baser Syrastyrka p. H-skalan Beräkna p. H för en stark syra Beräkna p. H för en svag syra Baser Flerprotoniga syror Syra-basegenskaper hos salter Molekylstrukturens inverkan på syra-basegenskaper Syra-basegenskaper hos oxider Lewis-syror och baser: ett vidgat syra-basbegrepp En övergripande strategi för att lösa syrabasproblem Copyright © Cengage Learning. All rights reserved 2

Avsnitt 14. 1 Syror och baser Syra-basbegrepp • Arrhenius: Syror producerar H 3 O+-joner i lösningar, baser producerar OHˉ-joner. • Brønsted-Lowry: Syror är protondonatorer, baser är protonacceptorer. HCl + H 2 O → Clˉ + H 3 O+ syra bas Return to TOC Copyright © Cengage Learning. All rights reserved 3
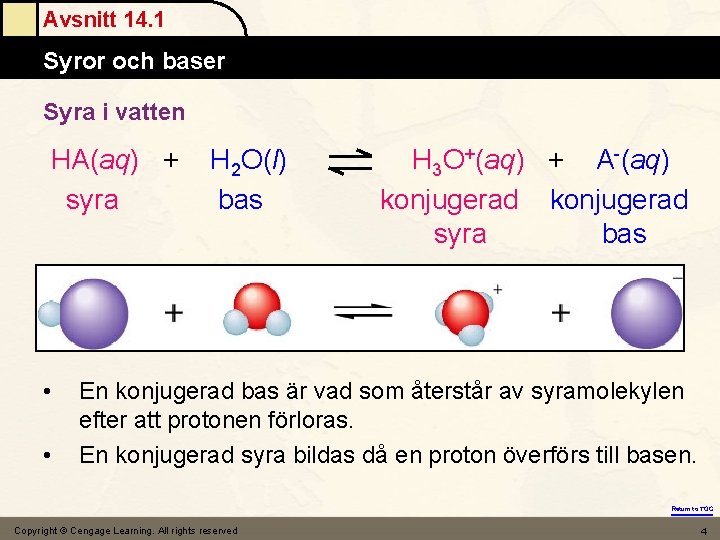
Avsnitt 14. 1 Syror och baser Syra i vatten HA(aq) + syra • • H 2 O(l) bas H 3 O+(aq) + A-(aq) konjugerad syra bas En konjugerad bas är vad som återstår av syramolekylen efter att protonen förloras. En konjugerad syra bildas då en proton överförs till basen. Return to TOC Copyright © Cengage Learning. All rights reserved 4

Avsnitt 14. 1 Syror och baser Syrakonstanten (Ka) HA(aq) + H 2 O(l) ⇌ H 3 O+(aq) + A (aq) Return to TOC Copyright © Cengage Learning. All rights reserved 5

Avsnitt 14. 2 Atomic Masses Syrastyrka Starka och svaga syror • Starka syror: § Syrajämvikten är starkt förskjuten åt höger. § Producerar en mycket svag konjugerad bas. • Svag syra: § Syrajämvikten är förskjuten åt vänster. § Ju svagare syra desto starkare konjugerad bas. Return to TOC Copyright © Cengage Learning. All rights reserved 6

Avsnitt 14. 2 Atomic Masses Syrastyrka Stark syra • Dess jämvikt är kraftigt förskjuten åt höger. HNO 3(aq) ⇌ H+(aq) + NO 3ˉ(aq) • Åtföljs av en svag konjugerad bas. (NO 3ˉ) Return to TOC Copyright © Cengage Learning. All rights reserved 7

Avsnitt 14. 2 Atomic Masses Syrastyrka Svag syra • Jämvikten är förskjuten åt vänster. CH 3 COOH(aq) ⇌ H+(aq) + CH 3 COOˉ(aq) • Åtföljs av en starkare bas än vatten: CH 3 COOˉ(aq) Return to TOC Copyright © Cengage Learning. All rights reserved 8
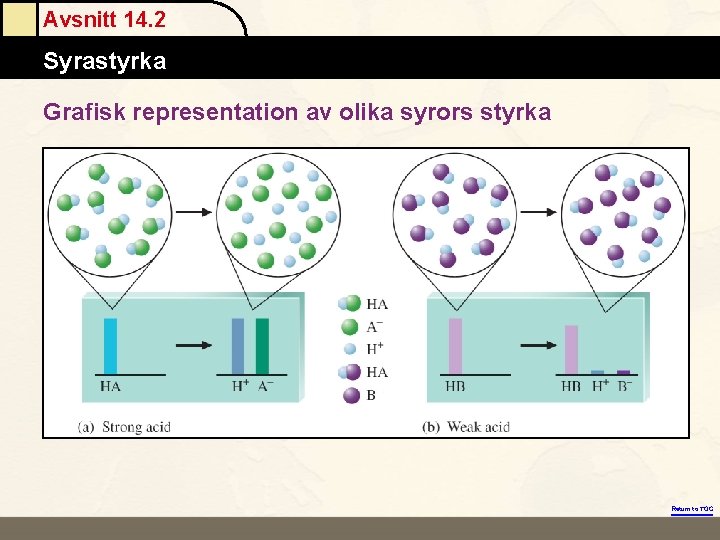
Avsnitt 14. 2 Atomic Masses Syrastyrka Grafisk representation av olika syrors styrka Return to TOC

Avsnitt 14. 2 Atomic Masses Syrastyrka Svag syra – svag elektrolyt • innehåller få joner, • bara delvis dissocierad. • leder dåligt elektrisk ström Return to TOC
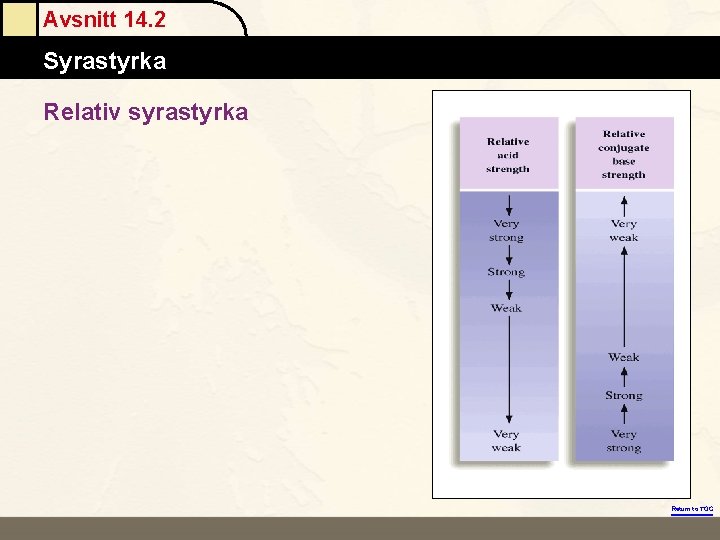
Avsnitt 14. 2 Atomic Masses Syrastyrka Relativ syrastyrka Return to TOC

Avsnitt 14. 2 Atomic Masses Syrastyrka Värdet på Ka Return to TOC Copyright © Cengage Learning. All rights reserved 12

Avsnitt 14. 2 Atomic Masses Syrastyrka Svaga syror Return to TOC Copyright © Cengage Learning. All rights reserved 13

Avsnitt 14. 2 Atomic Masses Syrastyrka Övning Ordna följande species enligt stigande styrka som konjugerad bas. F-, Cl-, NO 2 -, CN- Return to TOC Copyright © Cengage Learning. All rights reserved 14

Avsnitt 14. 2 Atomic Masses Syrastyrka Konceptkoll HA(aq) + H 2 O(l) syra bas H 3 O+(aq) + A-(aq) konjugerad syra bas Hur skrivs jämviktsuttrycket för syrareaktionen ovan? Return to TOC Copyright © Cengage Learning. All rights reserved 15
Avsnitt 14. 3 The Mole p. H-skalan Begrepp på p. H skalan • p. H = 7; neutral • p. H > 7; basisk § Ju högre p. H desto mer basisk. • p. H < 7; sur § Ju lägre p. H desto surare. Return to TOC Copyright © Cengage Learning. All rights reserved 16

Avsnitt 14. 3 The Mole p. H-skalan Vattnets autoprotolys • Vatten är en amfotär förening (den kan fungera både som en syra och en bas). H 2 O + H 2 O ⇌ H 3 O+ + OH syra 1 bas 2 syra 2 bas 1 Kw = [H 3 O+] [OH ] = 1 10 14 vid 25°C Return to TOC Copyright © Cengage Learning. All rights reserved 17

Avsnitt 14. 3 The Mole p. H-skalan Vattnets autoprotolys Return to TOC Copyright © Cengage Learning. All rights reserved 18

Avsnitt 14. 3 The Mole p. H-skalan Vad är p. H? • • • p. H log[H+] p. H i vatten antar värden typiskt mellan 0 och 14. Kw = 1. 00 10 14 = [H+] [OH ] p. Kw = 14. 00 = p. H + p. OH Då p. H stiger, sjunker p. OH (summan = 14. 00). I neutralt vatten (p. H = 7) är [H+] = [OH ] = 1. 00 10 7 Return to TOC Copyright © Cengage Learning. All rights reserved 19

Avsnitt 14. 3 The Mole p. H-skalan p. H för några vattenlösningar Return to TOC

Avsnitt 14. 3 The Mole p. H-skalan Övning Beräkna p. H för följande koncentrationer av H+ och OHˉ. a) 1. 0 × 10– 4 M H+ p. H = 4. 00 b) 0. 040 M OH– p. H = 12. 60 Return to TOC Copyright © Cengage Learning. All rights reserved 21
Avsnitt 14. 3 The Mole p. H-skalan Övning En lösnings p. H-värde uppmäts till 5. 85. Vad är [H+] i lösningen? [H+] = 1. 4 × 10– 6 M Return to TOC Copyright © Cengage Learning. All rights reserved 22
Avsnitt 14. 4 Beräkna p. H för en stark syra Viktiga steg vid syra-basberäkningar • Vilka ämnen finns i lösningen? • Vilka är de viktigaste reaktionerna som sker? § Är det en jämviktsreaktion (med dubbelpil) eller en reaktion som sker fullt ut (enkelpil)? § Låt alla reaktioner utom jämvikterna reagera fullt ut och lös därefter jämviktssystemet. • Beräkna p. H om det är det som det frågas efter. Return to TOC Copyright © Cengage Learning. All rights reserved 23
Avsnitt 14. 4 Beräkna p. H för en stark syra Konceptkoll En vattenlösning innehåller 2. 0 x 10– 3 M HCl. Vilka molekyler och joner finns i lösningen? H+, Cl–, H 2 O Beräkna p. H = 2. 70 Return to TOC Copyright © Cengage Learning. All rights reserved 24
Avsnitt 14. 4 Beräkna p. H för en stark syra Konceptkoll Beräkna p. H hos en 1. 5 x 10– 11 M vattenlösning av HCl. p. H = 7. 00 Return to TOC Copyright © Cengage Learning. All rights reserved 25
Avsnitt 14. 5 Beräkna p. H för en svag syra Lösningsprocedur 1. Lista upp de viktigaste molekylerna och jonerna i lösningen 2. Notera vilka ämnena som kan producera H+ (eller OHˉ) och skriv ner reaktionslikheterna. 3. Avgör på basen av Ka den dominerande H+ donatorn vid jämvikt. 4. Skriv upp jämviktsuttrycket för den dominerande jämviketen. 5. Lista utgångskoncentrationerna i den dominerande jämvikten. Return to TOC Copyright © Cengage Learning. All rights reserved 26
Avsnitt 14. 5 Beräkna p. H för en svag syra Lösningsprocedur (forts) 6. Avgör förändringen från utgångssituationen till jämvikt (som “x”). 7. Teckna jämviktskoncentrationerna som funktionav förändringen (x). 8. För in jämviktskoncentrationerna i jämviktsuttrycket. 9. Bestäm x ur andragradsekvationen (alt. bestäm x den “enkla vägen” och verifiera lösningen m. h. a. 5% regeln). 10. Beräkna [H+] och p. H ur jämviktsdefinitionen Return to TOC Copyright © Cengage Learning. All rights reserved 27
Avsnitt 14. 5 Beräkna p. H för en svag syra Konceptkoll Beakta en 0. 80 M vattenlösning av den svaga syran HCN (Ka = 6. 2 x 10– 10). Vilka är de dominerande molekylerna/jonerna i lösningen? HCN, H 2 O Return to TOC Copyright © Cengage Learning. All rights reserved 28
Avsnitt 14. 5 Beräkna p. H för en svag syra Låt oss tänka på saken • Varför är inte H+ eller CN– dominerande? Return to TOC Copyright © Cengage Learning. All rights reserved 29

Avsnitt 14. 5 Beräkna p. H för en svag syra Beakta följande HCN(aq) + H 2 O(l) H 3 O+(aq) + CN–(aq) Ka = 6. 2 x 10 -10 H 2 O(l) + H 2 O(l) H 3 O+(aq) + OH–(aq) Kw = 1. 0 x 10 -14 • Vilken jämvikt dominerar p. H? Förklara. Return to TOC Copyright © Cengage Learning. All rights reserved 30
Avsnitt 14. 5 Beräkna p. H för en svag syra Övning Beräkna p. H för en 0. 100 M vattenlösning av HOCl(aq) (vätehypoklorit/underklorsyrlighet) Ka = 3. 5 x 10 -8 Return to TOC Copyright © Cengage Learning. All rights reserved 31

Avsnitt 14. 5 Beräkna p. H för en svag syra Dissociationsgrad mängd dissocierad (M) 100% % dissociation = initial koncentration (M) Return to TOC Copyright © Cengage Learning. All rights reserved 32
![Avsnitt 14. 5 Beräkna p. H för en svag syra Utspädning, dissociationsgrad och [H+] Avsnitt 14. 5 Beräkna p. H för en svag syra Utspädning, dissociationsgrad och [H+]](http://slidetodoc.com/presentation_image_h2/a89e219c0950c175ece0427901e477fa/image-33.jpg)
Avsnitt 14. 5 Beräkna p. H för en svag syra Utspädning, dissociationsgrad och [H+] Return to TOC Copyright © Cengage Learning. All rights reserved 33

Avsnitt 14. 5 Beräkna p. H för en svag syra Övning • Beräkna dissociationsprocenten för ättikssyra i de nedanstående lösningarna: – 1. 00 M CH 3 COOH – 0. 10 M CH 3 COOH Return to TOC Copyright © Cengage Learning. All rights reserved 34

Avsnitt 14. 6 Baser Definitioner • • Arrhenius: baser genererar OH– joner i lösning. Brønsted–Lowry: baser är protontagare. I en basisk lösning vid 25°C är p. H > 7. Jonföreningar som innehåller OH– kan generellt betraktas som starka baser. § Li. OH, Na. OH, KOH, Ca(OH)2 • p. OH = –log[OH–] • p. H = 14. 00 – p. OH Return to TOC Copyright © Cengage Learning. All rights reserved 35

Avsnitt 14. 6 Baser Basstyrka • Termerna “stark” och “svag” används analogt för baser och syror • Stark bas = fullständigt dissocierad molekyl Na. OH(aq) → Na+(aq) + OHˉ(aq) • Svag bas = jämvikten förskjuten åt vänster CH 3 NH 2(aq) + H 2 O(l) ⇌ H 3 CNH 3+(aq) + OHˉ(aq) Return to TOC Copyright © Cengage Learning. All rights reserved 36
Avsnitt 14. 6 Baser Övning Beräkna p. H för en 5. 0 x 10 -2 M Na. OHlösning. Return to TOC Copyright © Cengage Learning. All rights reserved 37

Avsnitt 14. 6 Baser Baskonstanten (Kb) B(aq) + H 2 O(l) ⇌ BH+(aq) + OH (aq) Kb = BH + OH B Return to TOC Copyright © Cengage Learning. All rights reserved 38
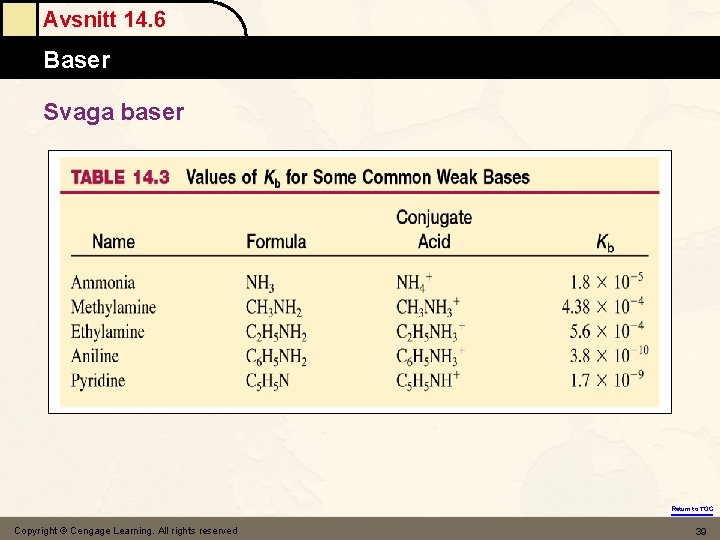
Avsnitt 14. 6 Baser Svaga baser Return to TOC Copyright © Cengage Learning. All rights reserved 39
Avsnitt 14. 6 Baser Övning Beräkna p. OH och p. H för en 1. 00 M vattenlösning av metylamin (CH 3 NH 2). Kb = 4. 38 x 10 -4 Return to TOC Copyright © Cengage Learning. All rights reserved 40

Avsnitt 14. 7 Flerprotoniga syror Syror med fler än ett surt väte • Kan donera fler än en proton per syramolekyl. • Dissocierar alltid stegvis, en proton i taget. • Den konjugerade basen från det första steget blir syran i det andra steget. • För en svag flerprotonig syra gäller: Ka 1 > Ka 2 > Ka 3 • För de flesta flerprotoniga syror i vattenlösning är det endast det första dissociationssteget som bestämmer p. H i lösningen. Return to TOC Copyright © Cengage Learning. All rights reserved 41

Avsnitt 14. 7 Flerprotoniga syror Syror med fler än ett surt väte. . . kan avge flera H+ per molekyl. Return to TOC Copyright © Cengage Learning. All rights reserved 42
Avsnitt 14. 7 Flerprotoniga syror Övning Beräkna p. H för 1. 00 M vattenlösning av H 3 PO 4. Ka 1 = 7. 5 x 10 -3 Ka 2 = 6. 2 x 10 -8 Ka 3 = 4. 8 x 10 -13 p. H = 1. 08 Return to TOC Copyright © Cengage Learning. All rights reserved 43

Avsnitt 14. 7 Flerprotoniga syror Konceptkoll Beräkna jämviktskoncentrationen av PO 43 - i en 1. 00 M vattenlösning av H 3 PO 4. Ka 1 = 7. 5 x 10 -3 Ka 2 = 6. 2 x 10 -8 Ka 3 = 4. 8 x 10 -13 [PO 43 -] = 3. 6 x 10 -19 M Return to TOC Copyright © Cengage Learning. All rights reserved 44
Avsnitt 14. 8 Syra-basegenskaper hos salter Salter • Är jonföreningar. • Dissocierar till joner då de löses upp i vatten. – jonerna kan sedan ha syra-basegenskaper. Return to TOC Copyright © Cengage Learning. All rights reserved 45

Avsnitt 14. 8 Syra-basegenskaper hos salter p. H kan ändras då ett salt löses i vatten 1. NH 4 Cl(s) NH 4+(aq) + Clˉ(aq) 2. NH 4+(aq) + H 2 O(l) ⇌ NH 3 (aq) + H 3 O+ (aq) p. H = -log[H 3 O+] Return to TOC Copyright © Cengage Learning. All rights reserved 46
Avsnitt 14. 8 Syra-basegenskaper hos salter Neutrala saltlösningar • Saltet av en stark syra och en stark bas ger neutral lösning. § KCl, Na. NO 3 Return to TOC Copyright © Cengage Learning. All rights reserved 47
Avsnitt 14. 8 Syra-basegenskaper hos salter Basiska saltlösningar • Uppstår om anjonen i ett salt är en konjugerad bas till en svag syra. § Na. F, KC 2 H 3 O 2 § Kw = Ka × Kb Ø använd Kb då p. H ska beräknas. Return to TOC Copyright © Cengage Learning. All rights reserved 48
Avsnitt 14. 8 Syra-basegenskaper hos salter Sura saltlösningar • Uppstår om katjonen i ett salt är en konjugerad syra till en svag bas. § NH 4 Cl § Kw = Ka × Kb Ø Använd Ka för beräkning av p. H. Return to TOC Copyright © Cengage Learning. All rights reserved 49
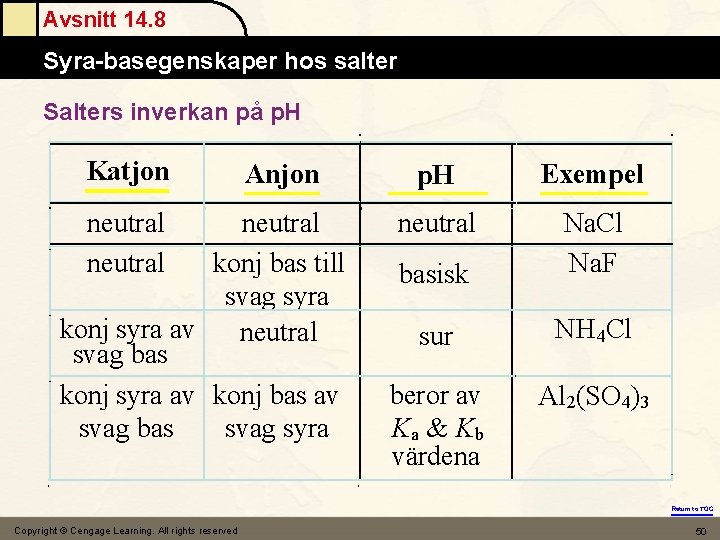
Avsnitt 14. 8 Syra-basegenskaper hos salter Salters inverkan på p. H Katjon neutral Anjon neutral konj bas till svag syra konj syra av neutral svag bas konj syra av konj bas av svag bas svag syra p. H Exempel neutral basisk Na. Cl Na. F sur NH 4 Cl beror av Ka & Kb värdena Al 2(SO 4)3 Return to TOC Copyright © Cengage Learning. All rights reserved 50

Avsnitt 14. 8 Syra-basegenskaper hos salter Bestämning av p. H i saltlösningar av svaga “föräldrar” Return to TOC Copyright © Cengage Learning. All rights reserved 51
Avsnitt 14. 8 Syra-basegenskaper hos salter Övning Beräkna p. H för 0. 30 M Na. F(aq) (för HF är Ka = 7. 2 10 -4) Return to TOC Copyright © Cengage Learning. All rights reserved 52
Avsnitt 14. 8 Syra-basegenskaper hos salter Konceptkoll Arrangera följande 1. 0 M lösningar från lägst till högst p. H. HBr Na. CN Na. Cl Na. OH NH 3 HF NH 4 Cl HCN HBr, HF, HCN, NH 4 Cl, Na. CN, NH 3, Na. OH Return to TOC Copyright © Cengage Learning. All rights reserved 53
Avsnitt 14. 9 Molekylstrukurens effekt på syra-basegenskaperna Observationer • Två faktorer styr syrastyrkan hos binära föreningar: § Jonkaraktären (hög ger stark syra) § Bindningsenergin (låg ger stark syra) Return to TOC Copyright © Cengage Learning. All rights reserved 54

Avsnitt 14. 9 Molekylstrukurens effekt på syra-basegenskaperna Bindnings- och syrastyrka för vätehalider Return to TOC Copyright © Cengage Learning. All rights reserved 55

Avsnitt 14. 9 Molekylstrukurens effekt på syra-basegenskaperna Syror som innehåller syre: Oxosyror • Innehåller den funktionella gruppen H–O–X. • Syrastyrkan ökar med antalet syreatomer som är bundna med centralatomen. • Ju större elektronegativitet hos X desto större förmåga att dra elektroner från syret och ju högre syrastyrka hos molekylen. Return to TOC Copyright © Cengage Learning. All rights reserved 56

Avsnitt 14. 9 Molekylstrukurens effekt på syra-basegenskaperna Några oxosyror och deras Ka-värden Return to TOC Copyright © Cengage Learning. All rights reserved 57

Avsnitt 14. 9 Molekylstrukurens effekt på syra-basegenskaperna Elektronegativiteten hos X och Ka-värdet för molekylen Return to TOC Copyright © Cengage Learning. All rights reserved 58

Avsnitt 14. 10 Syra-basegenskaper hos oxider Sura oxider • Oxider av icke-metaller § O-X bindningen är stark och kovalent. SO 2, NO 2, CO 2 • Då en H-O-X grupp löses i vatten kommer O-X bindningen förbli. Det är den relativt svaga H-O bindningen som bryts varpå det frigörs en proton. Return to TOC Copyright © Cengage Learning. All rights reserved 59

Avsnitt 14. 10 Syra-basegenskaper hos oxider Basiska oxider • Oxider av metaller: § O-X bindningen har jonkaraktär. K 2 O, Ca. O • Om X har låg elektronegativitet bryts O-X bindningen i vattenlösningen varpå syreatomen reagerar med vattenmolekylerna och generar en basisk lösning. Return to TOC Copyright © Cengage Learning. All rights reserved 60

Avsnitt 14. 11 Lewis-syror och baser: ett vidgat syra-basbegrepp Lewis syrabasbegrepp • Lewissyra: elektronparmottagare • Lewisbas: elektronpardonator Lewissyra Lewisbas Return to TOC Copyright © Cengage Learning. All rights reserved 61

Avsnitt 14. 11 Lewis-syror och baser: ett vidgat syra-basbegrepp Tre parallella modeller för syrabasbegreppet Return to TOC Copyright © Cengage Learning. All rights reserved 62
- Slides: 62