Kap 17 Temperatur og varme 1 Temperatur og













- Slides: 18

Kap 17 Temperatur og varme 1

Temperatur og varme Definisjon av varme Varme (Heat) : Energi-overføring pga temperatur-differenser Energi-overføring T 1 T 2 T 1 > T 2 2

Temperatur Varm - Kald Varm Kald Makroskopisk T 1 T 2 Mikroskopisk T 1 > T 2 0 0 C 40 0 C 10 0 C 30 0 C Varm Kald 3

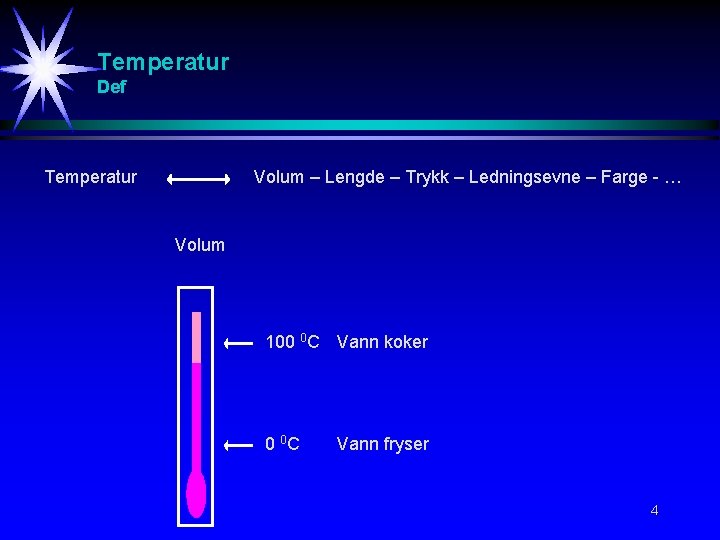
Temperatur Def Temperatur Volum – Lengde – Trykk – Ledningsevne – Farge - … Volum 100 0 C Vann koker 0 0 C Vann fryser 4

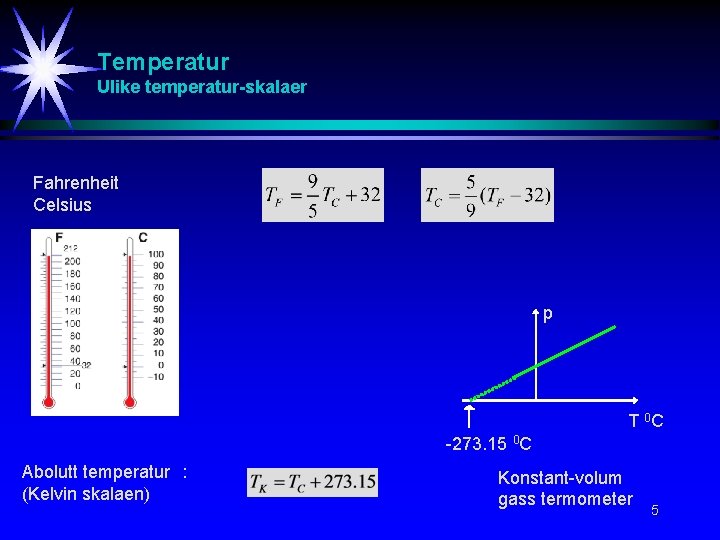
Temperatur Ulike temperatur-skalaer Fahrenheit Celsius p T 0 C -273. 15 0 C Abolutt temperatur : (Kelvin skalaen) Konstant-volum gass termometer 5

Temperatur Ulike temperatur-skalaer K C F Vann koker 373 100 212 Vann fryser 273 0 32 CO 2 til fast stoff 195 -78 -109 Oksygen til væske 90 -183 -298 Absolutt nullpunkt 0 -273 -460 6

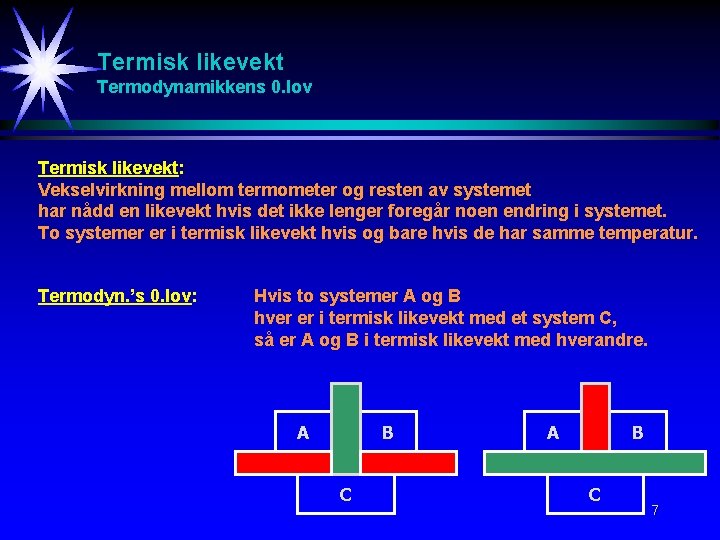
Termisk likevekt Termodynamikkens 0. lov Termisk likevekt: Vekselvirkning mellom termometer og resten av systemet har nådd en likevekt hvis det ikke lenger foregår noen endring i systemet. To systemer er i termisk likevekt hvis og bare hvis de har samme temperatur. Termodyn. ’s 0. lov: Hvis to systemer A og B hver er i termisk likevekt med et system C, så er A og B i termisk likevekt med hverandre. A B C 7

Termisk utvidelse Lineær utvidelse L 0 T T + T L 0 + L L Lengde-utvidelsen er proporsjonal med opprinnelig lengde L 0 og temperatur-endringen T 8

Termisk utvidelse Volum utvidelse T T + T V 0 + L Volum-utvidelsen er proporsjonal med opprinnelig volum V 0 og temperatur-endringen T 9

Termisk utvidelse Sammenheng mellom lineær utvidelse og volum utvidelse T V 0 L 0 T + T V 0 + L L 0 + L 10

Varme (Heat) Energioverføring pga temperaturforskjell Varm T 1 Kald T 2 T 1 > T 2 T 1 T 2 Varme: Energioverføring pga temperaturforskjell 11

Spesifikk varme 1 kalori (1 cal) er den varmemengden (energien) Q som trengs for å varme opp 1 gram vann fra 14. 5 0 C til 15. 5 0 C. 1 cal = 4. 186 J Den varmemengden Q som trengs for å varme opp en masse m fra T til T + T er proporsjonal med massen m og temperaturdiff T. Spesifikk varmekapasitet c: 12

Mol - Molar masse 1 mol av et stoff er den mengden substans som inneholder like mange elementære enheter (molekyler) som det er atomer i 0. 012 kg karbon 12 C. Antall molekyler i ett mol kalles Avogadros tall NA. Den molare masse M av et stoff er massen av ett mol av stoffet = massen av ett molekyl m multiplisert med Avogadros tall NA: 13

Molar varmekapasitet Ofte er det mer hensiktsmessig å beskrive en substans i antall mol n i stedet for vha massen m. Massen m av et stoff er lik massen pr mol M multiplisert med antall mol n Molar varmekapasitet: 14

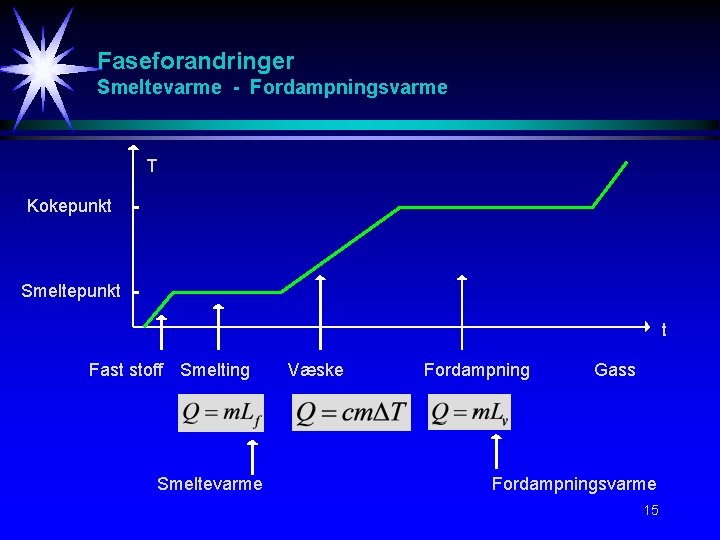
Faseforandringer Smeltevarme - Fordampningsvarme T Kokepunkt Smeltepunkt t Fast stoff Smelting Smeltevarme Væske Fordampning Gass Fordampningsvarme 15

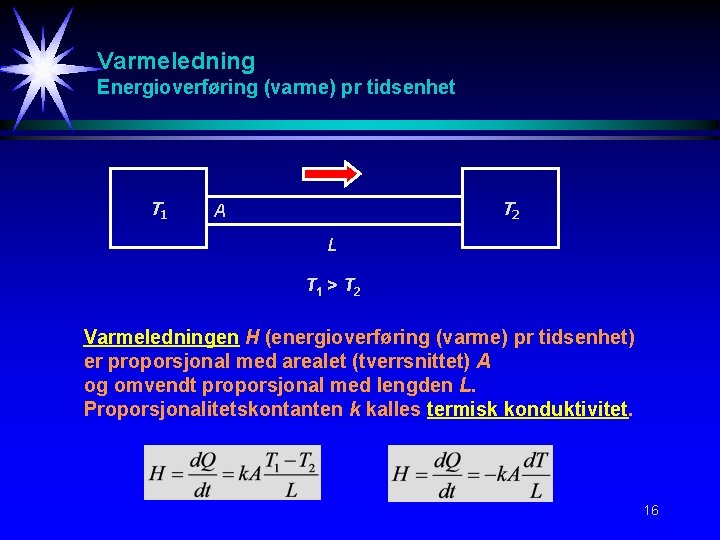
Varmeledning Energioverføring (varme) pr tidsenhet T 1 T 2 A L T 1 > T 2 Varmeledningen H (energioverføring (varme) pr tidsenhet) er proporsjonal med arealet (tverrsnittet) A og omvendt proporsjonal med lengden L. Proporsjonalitetskontanten k kalles termisk konduktivitet. 16

Termisk resistans: 17

Stråling Energioverføring (varme) vha elektromagnetiske bølger Stråling (radiation) er energioverføring (varme) vha elektromagnetiske bølger. Varmeledningen H er i dette tilfellet proporsjonal med arealet A og fjerde potens av temperaturen T. Varmeledningen er også avhengig av overflaten og beskrives vha en størrelse e kalt emisiviteten ( [0, 1]). Proporsjonalitetskontanten er en fundamental fysisk kontant kalt Stefan-Boltzmann konstant. 18