Kalor Hk Termodinamika Bima Wicaksono Kelas XII IPA

Kalor & Hk Termodinamika Bima Wicaksono Kelas XII IPA SMA Muhammadiyah 7 Surabaya 11/30/2020 1
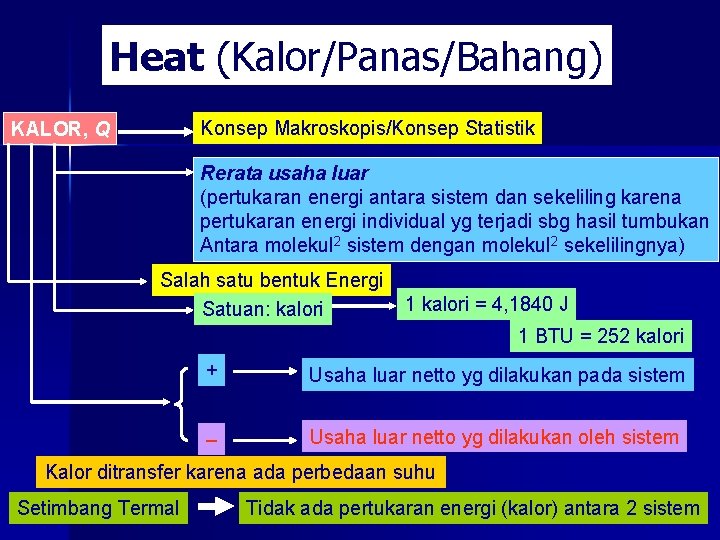
Heat (Kalor/Panas/Bahang) Konsep Makroskopis/Konsep Statistik KALOR, Q Rerata usaha luar (pertukaran energi antara sistem dan sekeliling karena pertukaran energi individual yg terjadi sbg hasil tumbukan Antara molekul 2 sistem dengan molekul 2 sekelilingnya) Salah satu bentuk Energi Satuan: kalori 1 kalori = 4, 1840 J 1 BTU = 252 kalori + Usaha luar netto yg dilakukan pada sistem – Usaha luar netto yg dilakukan oleh sistem Kalor ditransfer karena ada perbedaan suhu Setimbang Termal 2 Tidak ada pertukaran energi (kalor) antara 2 sistem

Kapasitas Kalor dan Kalor Jenis Kalor untuk menaikkan suhu zat sebanding dengan perubahan suhu dan massanya C = Kapasitas Kalor Zat = energi kalor untuk menaikkan suhu per derajat c = Kalor Jenis Zat = Kapasitas Kalor per satuan massa Kapasitas Kalor molar Kalor yang diserap oleh satu mole bahan untuk menghasilkan satu derajat suhu Kapasitas kalor pada tekanan konstan Hubungan Kapasitas kalor pada volume konstan Gas ideal mengalami transformasi adiabatis berlaku 3 Akan dibuktikan kemudian
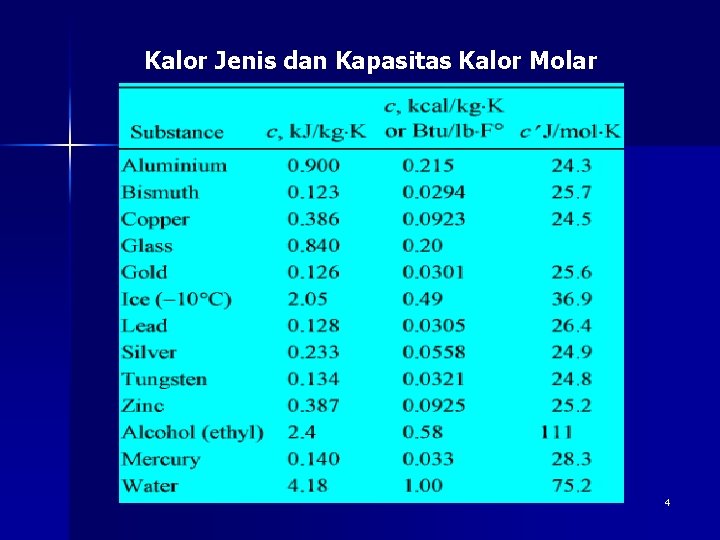
Kalor Jenis dan Kapasitas Kalor Molar 4
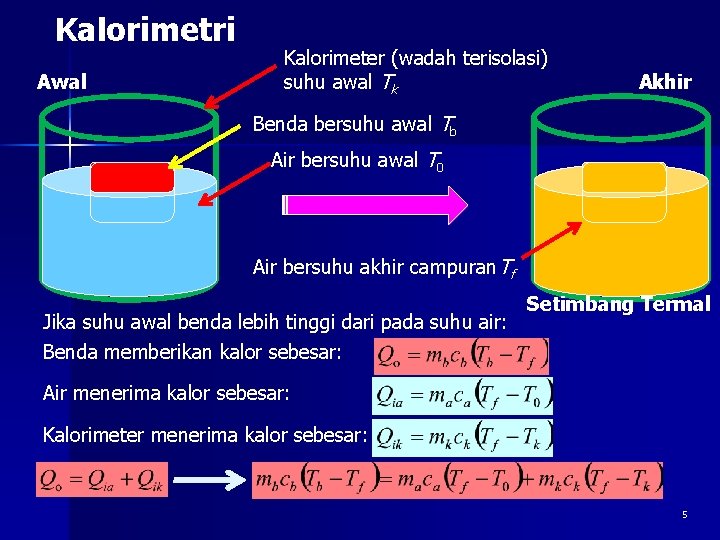
Kalorimetri Awal Kalorimeter (wadah terisolasi) suhu awal Tk Akhir Benda bersuhu awal Tb Air bersuhu awal T 0 Air bersuhu akhir campuran. Tf Jika suhu awal benda lebih tinggi dari pada suhu air: Benda memberikan kalor sebesar: Setimbang Termal Air menerima kalor sebesar: Kalorimeter menerima kalor sebesar: 5
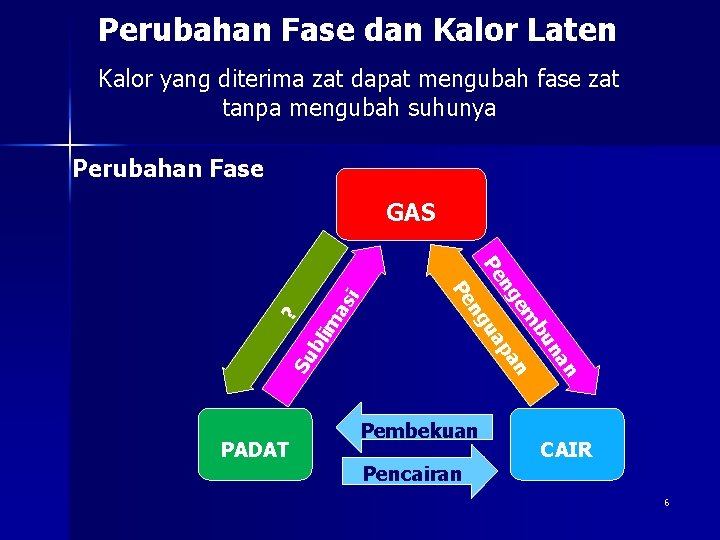
Perubahan Fase dan Kalor Laten Kalor yang diterima zat dapat mengubah fase zat tanpa mengubah suhunya Perubahan Fase GAS as i im ua Su bl ? ng n na bu em n ng pa Pe Pe PADAT Pembekuan CAIR Pencairan 6
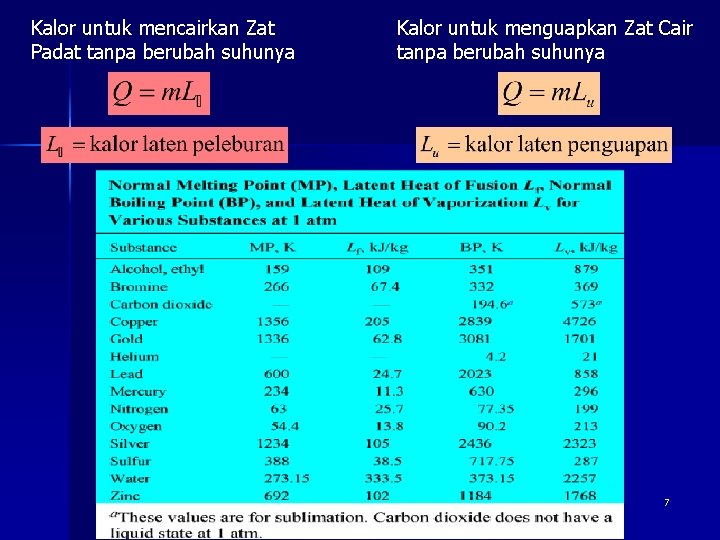
Kalor untuk mencairkan Zat Padat tanpa berubah suhunya Kalor untuk menguapkan Zat Cair tanpa berubah suhunya 7

Transfer Kalor/Energi Termis Cara transfer kalor 1. Konduksi lewat interaksi antar atom/molekul 2. Konveksi via perpindahan massa/ media fluida 3. Radiasi bentuk pancaran elektromagnetik 11/30/2020 8
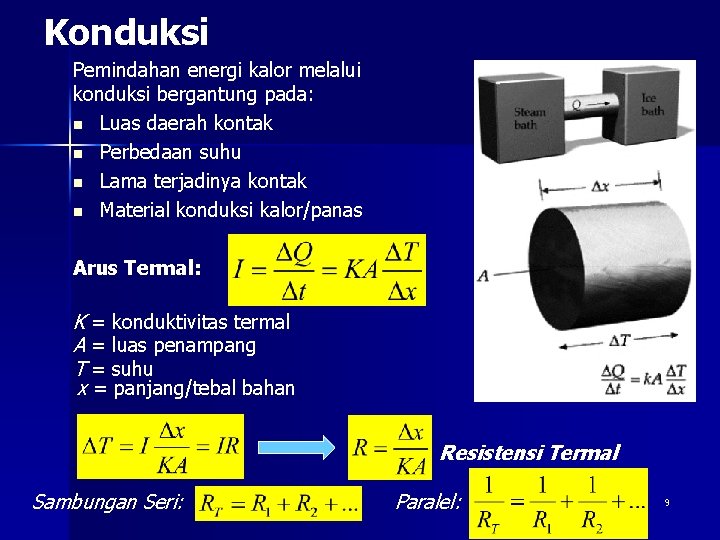
Konduksi Pemindahan energi kalor melalui konduksi bergantung pada: n Luas daerah kontak n Perbedaan suhu n Lama terjadinya kontak n Material konduksi kalor/panas Arus Termal: K = konduktivitas termal A = luas penampang T = suhu x = panjang/tebal bahan Resistensi Termal Sambungan Seri: Paralel: 9

Nilai Konduktivitas Termal Bahan 10

Konveksi Laju aliran energi kalor dari tubuh manusia ke udara sekitar (dalam J/s) v = kecepatan udara (medium perambatan) Ts = suhu permukaan (kulit) Ta = suhu udara 11/30/2020 11

Radiasi Hukum Stefan-Boltzman e = emisivitas (kemampuan pancaran kalor) suatu permukaan Nilai emisivitas antara 0 dan 1 = konstanta Stefan-Boltzman = 5, 6703 x 10– 8 W/m 2. K 4 T = suhu dalam Kelvin 11/30/2020 12

Evaporasi Penguapan/evaporasi juga dapat menghantarkan energi kalor Laju evaporasi energi kalor dari tubuh: (dalam J/s) p = tekanan (atm) p = kecepatan mediun perambatan (udara) 11/30/2020 13

Metabolisme sebagai konversi energi Kandungan/konversi energi berbagai macam bahan Karbohidrat dari Tumbuhan: -Sukrosa 3, 94 kkal/g -Glukosa 3, 74 kkal/g -Glikogen 4, 19 kkal/g -Tepung 4, 18 kkal/g Pada Manusia -Protein/Karbohidrat 4, 1 kkal/g -Lemak 9, 3 kkal/g 11/30/2020 Lemak Hewan/Tumbuhan -Rata-rata 9, 3 kkal/g Protein Hewan/Tumbuhan -Rata-rata 5, 6 kkal/g

Efek Kalor n Efek Fisik pemuaian peningkatan hambatan listrik penurunan konduktivitas listrik n Efek Kimia peningkatan kecepatan reaksi peningkatan permeabilitas membran peningkatan metabolisme n Efek Biologis akibat gabungan efek fisik dan kimia peningkatan sel darah putih fenomena reaksi peradangan pelebaran pembuluh darah peningkatan sirkulasi darah peningkatan tekanan kapiler peningkatan tekanan O 2 dan CO 2 dalam darah penurunan p. H darah

Hukum Termodinamika Hukum 11/30/2020 Pertama Kedua Ketiga ke Nol 16

Hukum Pertama Termodinamika Kalor netto yang ditambahkan pada suatu sistem sama dengan perubahan energi internal sistem ditambah usaha yang dilakukan sistem Q = U + W U = energi dalam Q = kalor W = usaha oleh sistem W ext= usaha luar pada sistem = W 11/30/2020 17
![Hk I Termodinamika Kasus: Jika sistem membentuk siklus [transformasi siklis] Jika transformasi adiabatis Jika Hk I Termodinamika Kasus: Jika sistem membentuk siklus [transformasi siklis] Jika transformasi adiabatis Jika](http://slidetodoc.com/presentation_image_h/c33be94c4223442a1752eeedce21e0a2/image-18.jpg)
Hk I Termodinamika Kasus: Jika sistem membentuk siklus [transformasi siklis] Jika transformasi adiabatis Jika tak ada usaha dilakukan sistem [transformasi isokoris] 11/30/2020 18
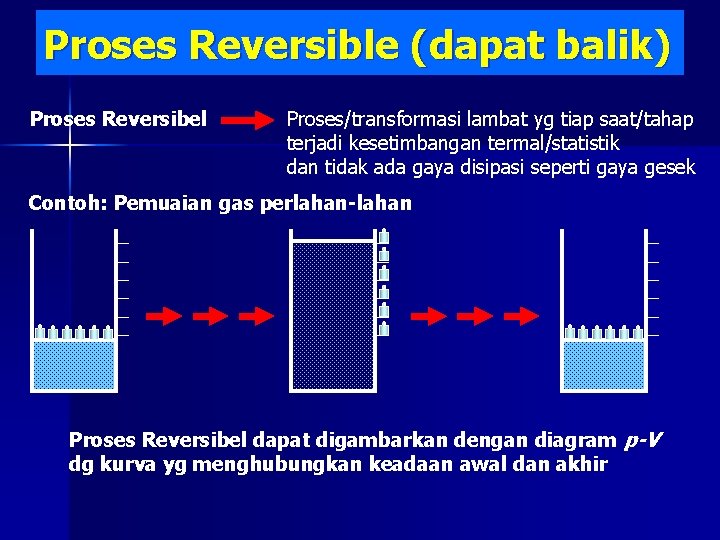
Proses Reversible (dapat balik) Proses Reversibel Proses/transformasi lambat yg tiap saat/tahap terjadi kesetimbangan termal/statistik dan tidak ada gaya disipasi seperti gaya gesek Contoh: Pemuaian gas perlahan-lahan Proses Reversibel dapat digambarkan dengan diagram p-V dg kurva yg menghubungkan keadaan awal dan akhir
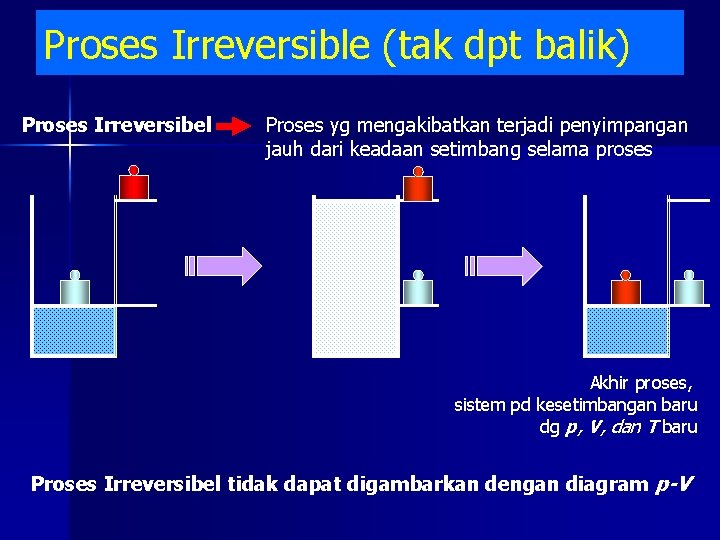
Proses Irreversible (tak dpt balik) Proses Irreversibel Proses yg mengakibatkan terjadi penyimpangan jauh dari keadaan setimbang selama proses Akhir proses, sistem pd kesetimbangan baru dg p, V, dan T baru Proses Irreversibel tidak dapat digambarkan dengan diagram p-V
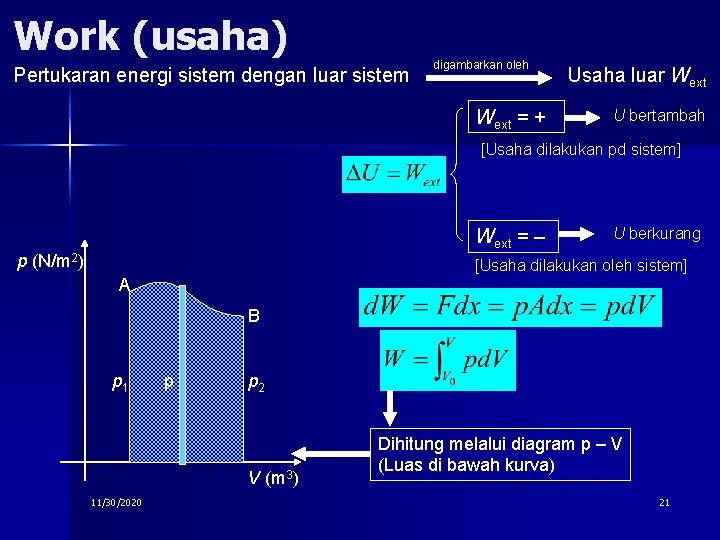
Work (usaha) Pertukaran energi sistem dengan luar sistem digambarkan oleh Wext = + Usaha luar Wext U bertambah [Usaha dilakukan pd sistem] Wext = – p (N/m 2) U berkurang [Usaha dilakukan oleh sistem] A B p 1 p p 2 V (m 3) 11/30/2020 Dihitung melalui diagram p – V (Luas di bawah kurva) 21

Kasus 1 Tekanan konstan Usaha yang dilakukan oleh sistem Karena maka Hukum Termodinamika I menjadi 11/30/2020 22

Kasus 2 Suhu konstan T konstan U=0 Q =W 11/30/2020 23

Kasus 3 volume konstan V konstan Usaha nol Kalor berbanding lurus dengan perubahan suhu, jumlah zat, dan kapasitas kalor volume tetap CV 11/30/2020 24

Ekspansi Adiabatik Kuasi Statik Gas Proses Adiabatik tidak ada kalor yang mengalir masuk atau keluar Lintasan Adiabatik Usaha Adiabatik : 25

Hukum Kedua Termodinamika Sadi Carnot (1796 – 1832) Dalam mesin kalor terjadi proses yang mana energi kalor diambil oleh sejumlah energi mekanik tetapi selang waktu tertentu jumlah kalor yang masuk mesin sama dengan yang hilang Lord Kelvin (1853) Batasan Hk 2 Termodinamika Tidak mungkin membuat mesin yang bekerja dalam suatu siklus, menerima kalor dari suatu reservoir dan mengubah kalor itu seluruhnya menjadi usaha Efisiensi Mesin Kalor = 1 - Q 1/Q 2 = 1 – T 1/T 2 Q 1 = Kalor pada suhu rendah T 1 Q 2 = Kalor pada suhu tinggi T 2 11/30/2020 26

Hukum Ketiga Termodinamika Terkait dengan ENTROPI sistem Ukuran penyimpangan/KETIDAKTERATURAN suatu sistem 11/30/2020 27

Entropi Penggambaran alam dalam mencapai kesetimbangan statistik/ keteraturan sistem k = konstanta Boltzmann P = probabilitas 11/30/2020 28

Hubungan Entropi dengan Kalor Contoh: Hitung perubahan entropi satu mole es untuk melebur pada 0 o. C jika selama proses es menyerap 1435 kalori/mol Jawab: 11/30/2020 29

Hukum ke Nol Termodinamika Dalam keadaan adiabatik, suatu gas ideal dalam ruangan terisolasi/tertutup, pemuaian sangat lambat, tidak ada kalor yang diterima maupun yang dilepas. Tercapai kesetimbangan termal suhu sama merata di setiap bagian 11/30/2020 30
- Slides: 30