Kafli 1 3 Tkn breytingar og uppbygging atms

Kafli 1. 3 Tákn, breytingar og uppbygging atóms KMS 1. lota 1

Táknun efnasambanda • Efnaformúla efnasambands inniheldur tákn allra frumefna sem það er sett saman úr, auk talna sem sýna fjölda atóma. Tölurnar eru í minna letri aftan við tákn frumefnisins. • Dæmi: Matarsalt = Na. Cl hér eru engar tölur því hver eining matarsalts inniheldur eitt natríumatóm og eitt klóratóm. • Gifs = Ca. SO 4 Talan 4 á bara við O. KMS - ÁI Hver eining af gifsi inniheldur eitt kalsíumatóm, eitt brennisteinsatóm og 4 súrefnisatóm. 2 1. lota

Efnabreyting er. . . . umröðun atóma eða breyting á ástandi þeirra. • Þrjár megingerðir efnabreytinga eru: – Ástandsbreytingar: Efni breytir um fasa. – Efnahvörf: Tvö eða fleiri atóm tengjast hvort öðru á nýjan hátt – Kjarnahvörf: Atómkjörnum sundrað eða þeir sameinaðir. Geislavirkir kjarnar sundrast í kjarnahvörfum !! KMS - ÁI 1. lota 3

Ástandsbreyting • Efni breytir um ástand, fer úr einum fasa í annan. – Dæmi : H 2 O(s) H 2 O(l) H 2 O(g) • Táknin fyrir ástand efna eru eftirfarandi: s = fast efni (solid) l = vökvi (liquid) g = lofttegund (gas) Bræðslumark : það hitastig er efni breytist úr föstu ástandi í fljótandi. Bræðslumark íss = 0°C Suðumark : það hitastig er efni breytist úr fljótandi ástandi í gas. Suðmark vatns = 100°C KMS - ÁI 1. lota 4

Efnahvörf. • Efnahvarf er ferli þar sem sameindir sundrast eða sameinast, og ný sameind eða jafnvel nýjar sameindir myndast. • Atóm hvorki eyðast né myndast, heldur raðast saman á annan hátt. • Efnajafna : Táknun fyrir efnahvarf. KMS - ÁI 1. lota 5

Efnajafna inniheldur : • • Efnaformúlur hvarfefna Ör sem sýnir stefnu hvarfsins Efnaformúlur myndefna Tölur sem sýna hlutföll efna sem eyðast eða myndast • Tákn fyrir ástand efnanna (s, l, g, aq) aq=uppleyst í vatni 2 H 2(g) + O 2(g) KMS - ÁI 1. lota 2 H 2 O(l) 6
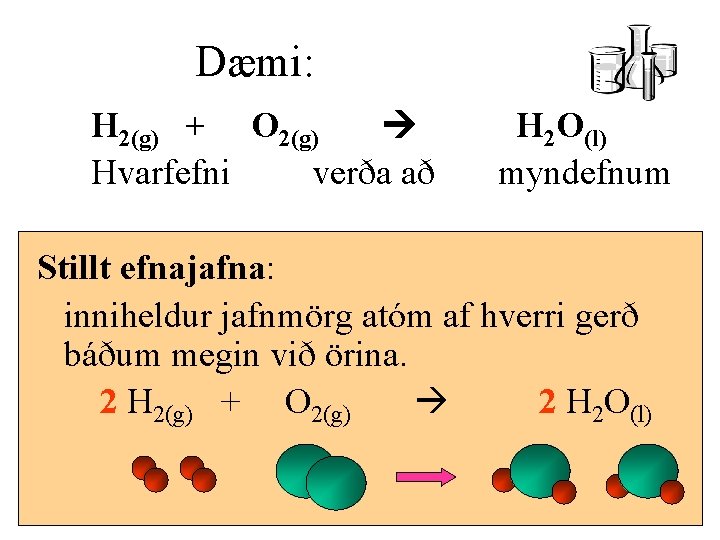
Dæmi: H 2(g) + O 2(g) Hvarfefni verða að H 2 O(l) myndefnum Stillt efnajafna: inniheldur jafnmörg atóm af hverri gerð báðum megin við örina. 2 H 2(g) + O 2(g) 2 H 2 O(l) KMS - ÁI 1. lota 7
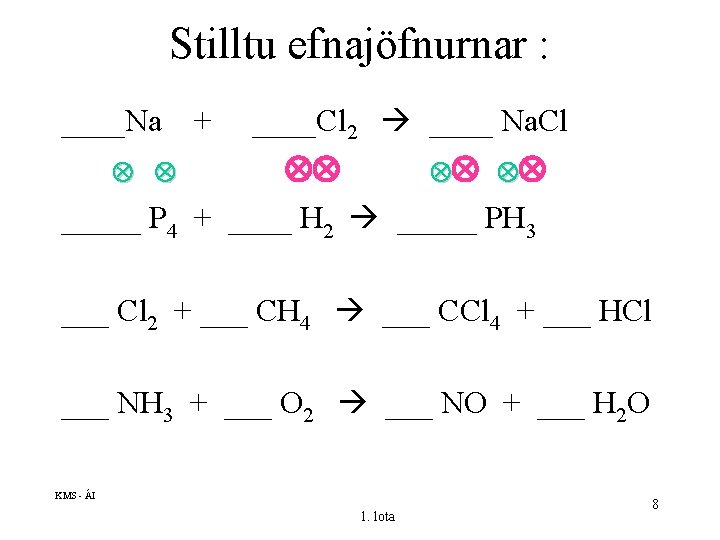
Stilltu efnajöfnurnar : ____Na + ____Cl 2 ____ Na. Cl _____ P 4 + ____ H 2 _____ PH 3 ___ Cl 2 + ___ CH 4 ___ CCl 4 + ___ HCl ___ NH 3 + ___ O 2 ___ NO + ___ H 2 O KMS - ÁI 1. lota 8
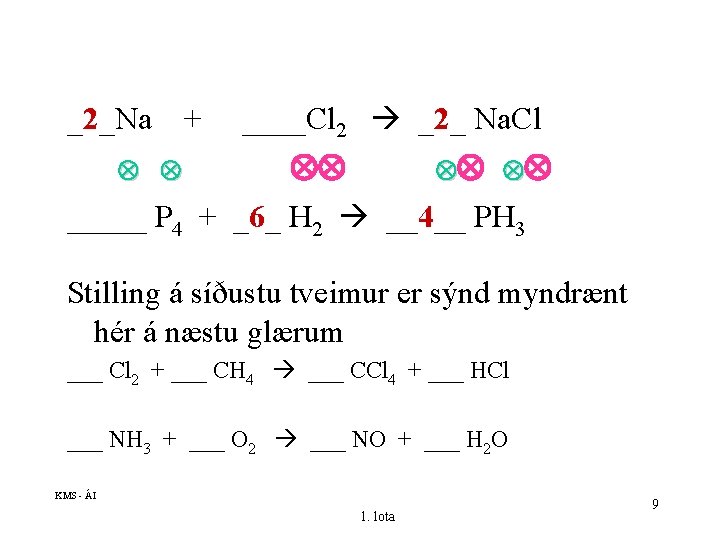
_2_Na + ____Cl 2 _2_ Na. Cl _____ P 4 + _6_ H 2 __4__ PH 3 Stilling á síðustu tveimur er sýnd myndrænt hér á næstu glærum ___ Cl 2 + ___ CH 4 ___ CCl 4 + ___ HCl ___ NH 3 + ___ O 2 ___ NO + ___ H 2 O KMS - ÁI 1. lota 9
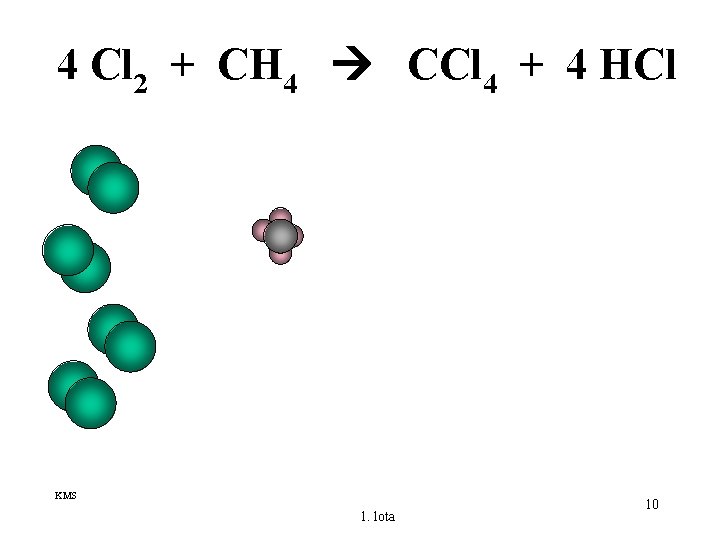
4 Cl 2 + CH 4 CCl 4 + 4 HCl KMS 1. lota 10
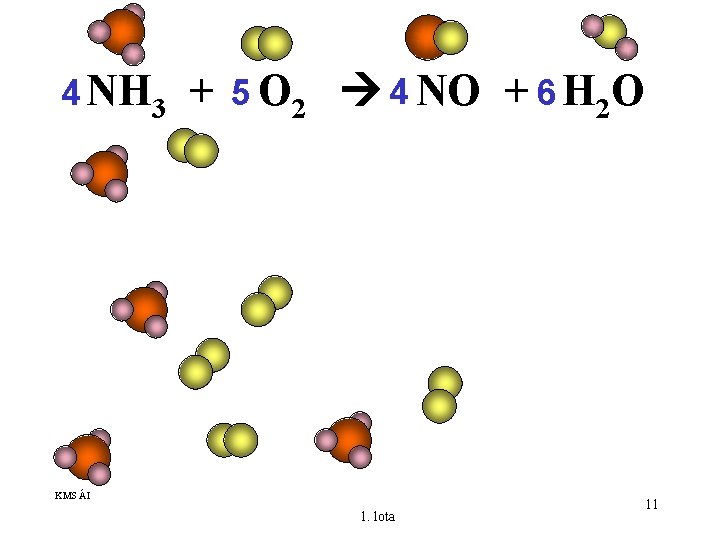
4 NH 3 + 5 O 2 4 NO + 6 H 2 O KMS ÁI 1. lota 11

Þróun hugmynda um atómið Hugmyndir manna um atómið hafa breyst í gegnum tíðina. • Dalton: Atómið óvirk kúla • Rutherford: (ca 1910) Atómið er innst kúlulaga þungur kjarni (plús hlaðinn) í kring eru örlitlar neikvæðar agnir á fleygiferð (rafeindir). • Bohr: (1922) Rafeindir ferðast eftir vissum brautum umhverfis kjarnann, brautir ráðast af mismunandi orku rafeindanna. KM - ÁI 1. lota 12

Hugmyndir okkar um atómið í dag • Atóm er að mestu leyti tómarúm. • Í miðju atóms er kjarni. – Kjarni vegur 99, 9% af massa atómsins – Rúmmál kjarna er 0, 001% af þvermáli atómsins. – Kjarninn er samsettur úr tvenns konar einingum : plúshlöðnum róteindum (p+) og óhlöðnum nifteindum (n 0) • Í kringum kjarnann sveima mínushlaðnar rafeindir (e-) eftir ákveðnum hvolfum (brautum). KMS - ÁI 1. lota 13

Rafeindir – elektrónur – e e- + • Eru mínushlaðnar agnir sem þeytast á miklum hraða umhverfis kjarna atóms. • Massi rafeinda er hverfandi (örlítill!) • Hleðsla hverrar rafeindar er – 1. • Fjöldi rafeinda er eitt af því sem einkennir hvert frumefni. • Eiginleikar efna ráðast einkum af þeim rafeindafjölda sem einkennir efnið. KMS 1. lota 14

Róteindir – prótónur – + p • Eru plúshlaðnar agnir í kjarna atóms. e • Massi róteindar er um það bil 1 u + (u = atómmassaeining) • Hleðsla róteindar er +1. • Atóm hvers frumefnis hafa alltaf jafnmargar róteindir í kjarna. • Hleðsla atóms ræðst af heildarfjölda róteinda og heildarfjölda rafeinda þess. Dæmi : Kolefnisatóm hefur 6 róteindir og 6 rafeindir. Hleðsla kolefnisatóms = + 6 – 6 = 0 KMS - ÁI 1. lota 15 -

Nifteindir – neftrónur – 0 n • Eru óhlaðnar agnir í kjarna atóms. • Massi nifteindar er um það bil sá sami og massi róteindar (1 u). • Hleðsla nifteindar = 0. • Atóm sama frumefnis geta haft mismunandi margar nifteindir í kjarna ! KMS - ÁI 1. lota 16

Tákn agna, hleðsla og massi : . Ögn Tákn Hleðsla Massi (grömm) Róteind p+ + 1, 673 · 10 -24 Rafeind e- - 9, 110 · 10 -28 Nifteind n 0 0 1, 675 · 10 -24 KMS - ÁI 1. lota 17
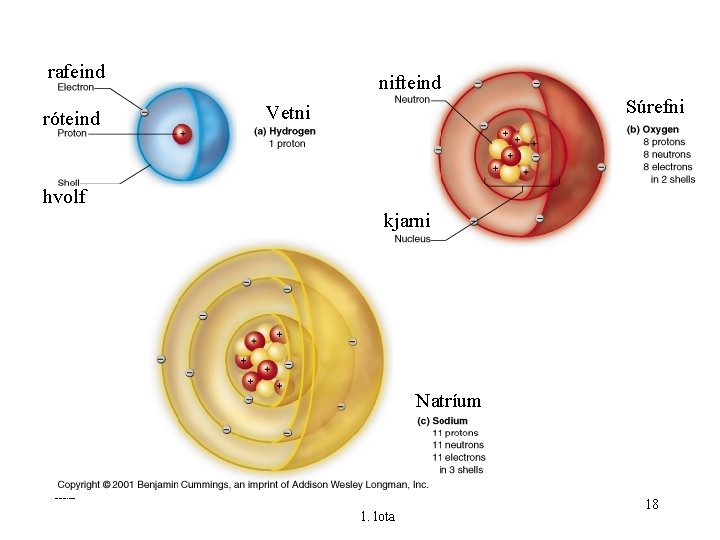
rafeind róteind nifteind Súrefni Vetni hvolf kjarni Natríum KMS 1. lota 18

Sætistala frumefnis. . . • . . . er eins konar kennitala frumefnisins. • . . . er númer frumefnisins í lotukerfinu. • . . . sýnir fjölda róteinda í kjarna atóma þess. • Öll atóm sama frumefnis hafa jafnmargar róteindir í kjarna sínum. KMS´-ÁI 1. lota 19

Samsætur • Atóm sama frumefnis hafa öll jafnmargar róteindir í kjarna. • Atóm sama frumefnis hafa hins vegar ekki öll sama massa, sum eru léttari önnur þyngri. • Munurinn liggur í fjölda nifteinda í kjarna ! • Samsætur eru misþung atóm sama frumefnis, vegna mismunandi fjölda nifteinda í kjarna. KMS - ÁI 1. lota 20
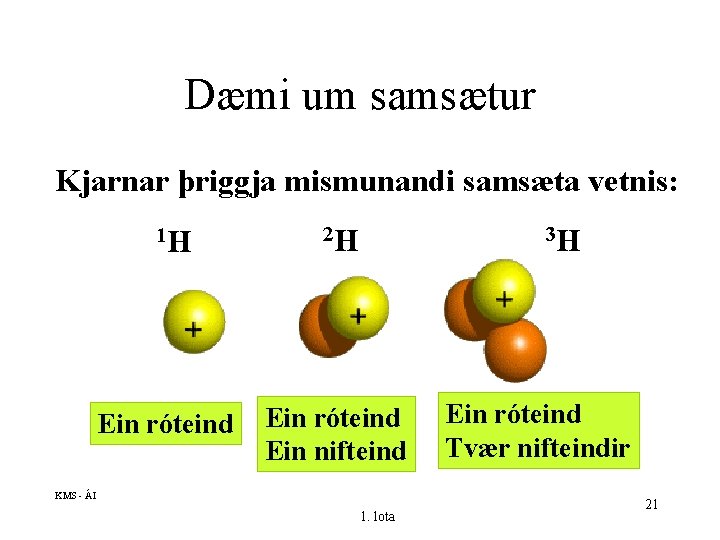
Dæmi um samsætur Kjarnar þriggja mismunandi samsæta vetnis: 1 H Ein róteind 2 H 3 H Ein róteind Ein nifteind KMS - ÁI 1. lota Ein róteind Tvær nifteindir 21
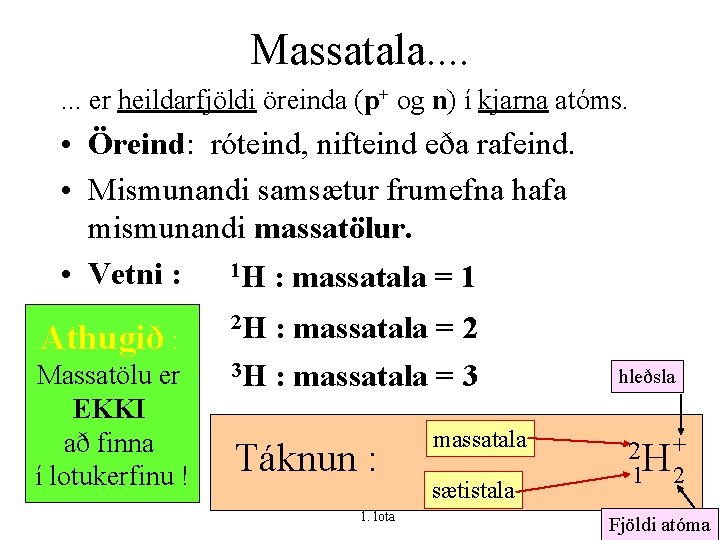
Massatala. . . . er heildarfjöldi öreinda (p+ og n) í kjarna atóms. • Öreind: róteind, nifteind eða rafeind. • Mismunandi samsætur frumefna hafa mismunandi massatölur. • Vetni : 1 H : massatala = 1 Athugið : Massatölu er EKKI að finna í lotukerfinu ! 2 H : massatala = 2 3 H : massatala = 3 Táknun : KMS - ÁI 1. lota massatala sætistala hleðsla 2 H + 1 2 22 Fjöldi atóma

Atómmassi : • Til hagræðis er massi öreinda skilgreindur í einingunni u (atom mass unit = amu) • 1 u er um það bil massi einnar róteindar eða einnar nifteindar. – Nánar : Róteind : 1, 0073 u 1 u Nifteind : 1, 0087 u 1 u Rafeind : 0, 00055 u 0 u KMS - ÁO 1. lota 23

• Hugtakið atómmassi er meðalmassi allra atóma sama frumefnis í náttúrunni. • Dæmi: Af frumefninu Iridíum (Ir) finnast tvær samsætur í náttúrunni. 37, 3% af Ir er samsætan 191 Ir og 62, 7% samsætan 193 Ir. • Atómmassi Ir er þá (37, 3 x 191 + 62, 7 x 193)/100 = 192, 25 • Atómmassi frumefna er gefinn upp í Sætistala lotukerfinu, þarf ekki að reikna. frumefnatákn KMS - ÁI 1. lota Atómmassi 1 H 24 1, 008

Fjöldi öreinda Óhlaðin atóm hafa jafnmargar róteindir og rafeindir. massatala 56 • 26 Fe : 26 róteindir og 26 rafeindir sætistala Massatala = fjöldi róteinda + fjöldi nifteinda • Massatala = 52 => 52 – 26 = 30 nifteindir KMS - ÁI 1. lota 25

Jónir eru plús- eða mínus-hlaðnar • Jón er atóm eða sameind þar sem fjöldi róteinda og rafeinda er ekki jafn. Það veldur hleðslu. . . Dæmi: • Na+ : 11 róteindir og 10 rafeindir : +11 – 10 = +1 (plúshleðsla) • Cl- : 17 róteindir og 18 rafeindir : + 17 – 18 = -1 (mínushleðsla) KMS - ÁI 1. lota 26

Útreikningar • Hægt er að nota upplýsingarnar í lotukerfinu til að reikna út fjölda öreinda. • Þannig er hægt að gera sér mynd af því hvernig atóm hvers einasta frumefnis lítur út. • Jafnvel hægt að teikna mynd • Yfirlit á næstu glæru. . . KMS - ÁI 1. lota 27

Massatala = fjöldi róteinda + fjöldi nifteinda Sætistala = fjöldi róteinda, númer frumefnis í lotukerfinu Hleðsla atóms = fjöldi róteinda - fjöldi rafeinda KMS - ÁI 1. lota 28
- Slides: 28