Jornada Cientfica Perioperatria Promoo Sociedade Brasileira de Enfermeiros

Jornada Científica Perioperatória Promoção: Sociedade Brasileira de Enfermeiros de Centro Cirúrgico, Recuperação Anestésica e Centro de Material e Esterilização “SEGURANÇA E BOAS PRÁTICAS EM MATERIAIS CONSIGNADOS” Enf. Ana Maria F. Miranda Apoio Administrativo – HSI SP. 09/11/2008

Agradecimento Débora S. Mello - Enf. SCIH IOT/HCFMUSP Riselda Moreno - Enf. Centro Cirúrgico HSI Vivian Amorim - Enf. CME Hospital Bandeirantes

Objetivo 1. Discutir a complexidade vivenciada pelas equipes de Central de Material e Esterilização e Centro Cirúrgico frente ao sistema de consignação; 2. Analisar criticamente as práticas atualmente desenvolvidas pela Central de Material e Esterilização e Centro Cirúrgico, identificando riscos no processamento e na utilização do material consignado; 3. Buscar ferramentas que assegurem a adoção de boas práticas com material consignado;

Definições 1) SEGURANÇA “Ausência de riscos inaceitáveis” (ISO 14971) 2) BOAS PRÁTICAS Conjunto de requisitos de planejamento, responsabilidades, práticas, procedimentos, processos e recursos para um determinado produto médico de forma a garantir a qualidade do produto e o controle dos fatores de risco à saúde do consumidor.

Consignar “enviar, em confiança mercadorias a outrem, para que as negocie”.

Material Consignado É o material enviado pelo fornecedor ao hospital sob sistema de consignação, para utilização e posterior faturamento.

OPME – Órtese, Prótese e Material Especial Órtese – peça ou aparelho de correção e/ou complementação de membros ou órgãos do corpo. Prótese – peça ou aparelho de substituição dos membros ou órgãos do corpo. Material Especial - Implante Ortopédico “Dispositivo implantado cirurgicamente no corpo, total ou parcialmente, temporária ou permanentemente, e usado como um auxílio no reparo de osso e/ou tecidos pertinentes ou como um substituto temporário ou permanente para estes tecidos” NBR ISO 8828 – 1997
Implante Ortopédico Classe de risco I baixo risco II médio risco III alto risco IV máximo risco

RDC nº 59 de 27 de junho de 2000 Parte F 1. Identificação e Rastreabilidade 2. Produtos de elevado risco (classe III e IV) – Rastreabilidade Cada fabricante deverá identificar cada unidade, lote ou partida de produtos de elevado risco (classe III e IV) com um número de controle. Essa identificação deverá ser registrada no registro histórico do produto. Parte L - Controle de embalagem e rotulagem 1. Embalagem de produtos 2. Rotulagem de produtos 3. Rotulagem de produtos de elevado risco (classe III e IV) • A rotulagem de produtos de elevado risco (classe III e IV) deverá conter um número de controle.

RDC nº 59 de 25 de agosto de 2008 Parte 3 - Definições Implante Permanente Produto implantável destinado à substituição definitiva de parte ou função das estruturas normais do corpo, como os implantes para artroplastia e coluna, não possuindo indicação de retirada devido à função que exerce Etiqueta de Rastreabilidade Documento complementar a ser fornecido com o produto ou sistema, contendo campo para inserção das seguintes informações: • Nome ou modelo comercial; • Identificação do fabricante ou importador • Código do produto ou do componente do sistema • Número de lote e número de registro na ANVISA
Risco – Produto para saúde Conceito engloba § probabilidade de ocorrência de dano; Cliente § conseqüência do dano. Fatores ISO 14971 de Risco Ambiente Profissional

ANVISA

MHRA

Material Consignado § Central de Material e Esterilização § Centro Cirúrgico § Setor Específico GEAPIO CME Média de empresas consignadas – 12 (doze)
Material Consignado

Fornecedor Documentação legal §Razão social da empresa fornecedora de implantes ortopédicos; §Código Nacional de Pessoa Jurídica; §Endereço para correspondência §Telefone; §Fax; §Correio Eletrônico; §Alvará de Funcionamento; §Autorização para comercialização; §Cópia do certificado de boas práticas de fabricação (ANVISA); §Licença de importação , no caso de implantes importados; §Responsável técnico e legal.

Fornecedor § § § Documentação legal; Qualificação; Visita técnica; Estabelecimento contrato; Membro de entidade representativa; § Instruções de uso: § Limpeza e desinfecção § Processamento e esterilização § Reações adversas e cuidados recomendados § Mercado nacional – ANVISA § 5000 empresas § 8% certificadas § Mercado nacional – ABRAIDI § 206 empresas filiadas § 94, 1% - selo – empresa BOA CIDADÃ


Implantes Ortopédicos CME § RECEBIMENTO § os implantes podem ser entregues a) estéreis b) não- estéreis Produto estéril § nome fabricante § marca § modelo § número do lote § número de registro do Min. Saúde § inviabilidade da embalagem

Implantes Ortopédicos Recebimento Estéril Não-Estéril

Implantes Ortopédicos Recebimento § Produto não –estéril § vale de consignação (dados de identificação do fornecedor e nº de controle) § avaliar se as marcações para medir as dimensões anatômicas estão nítidas e claras; § avaliar as indicações de Direito/Esquerdo.
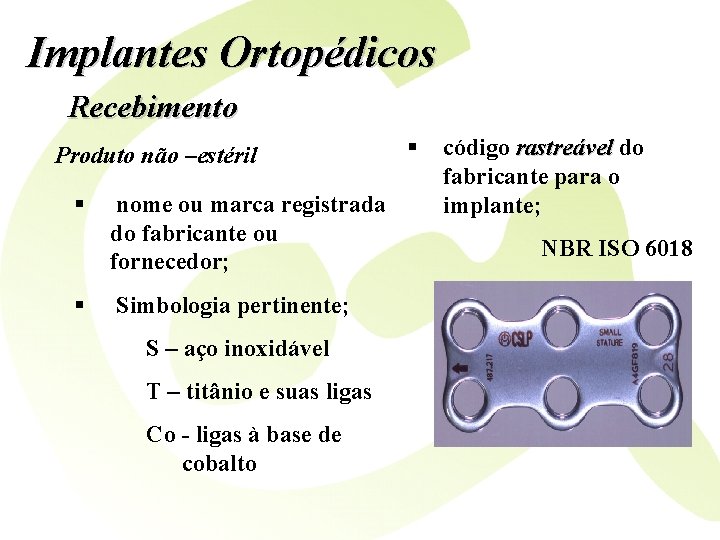
Implantes Ortopédicos Recebimento Produto não –estéril § § nome ou marca registrada do fabricante ou fornecedor; Simbologia pertinente; S – aço inoxidável T – titânio e suas ligas Co - ligas à base de cobalto § código rastreável do fabricante para o implante; NBR ISO 6018

Implantes Ortopédicos Inspeção Visual § acabamento § padrão de fabricação § rugosidades § trincas § ranhuras § zonas de debastação § danos pós-uso § condições de limpeza § implantes com a mesma logomarca § número de registro no Min. Saúde?
Limpeza Propósito §Redução de carga microbiana; §Redução dos contaminantes orgânicos e inorgânicos Finalidade Assegurar o processo de esterilização §Nível de endotoxina menor que 0, 25 IU/m Orientação AAMI 11737 ISO 11135 EN 1174

Limpeza Processo de limpeza: Validação AUTOMIZADA § reprodutibilidade § controlador lógico programável (CLP) § EN 15883, HTM 2030 § nível de segurança de desinfecção (DAL) § qualidade da água MANUAL § reprodutibilidade? § operador (treinamento, procedimento de limpeza bem definidos e descritos e análise visual.

Limpeza Água § água dura (sais de cálcio e magnésio) § água mole (desmineralizada) Métodos de tratamento da água §filtração §destilação §deionização §osmose reversa

Limpeza Secagem Enxágüe §Água tratada § Nível de atividade da água. Menor que 0. 6% UR Indústria Farmacêutica e Alimentícia Justificativa: O índice de atividade da água inferior a 0. 6% UR, impede a proliferação de microorganismos, embora os mesmos possam estar vivos sem que haja reprodução.

Journal of Clinical Microbiology, Oct. 2006 p. 3728 -3733 Comparative Study of Surgical Instruments from Sterile-Service Departaments for Presence of Residual Gram-Negative Endotoxin and Proteinaceous Deposits

Objetivos Avaliar a presença: • depósitos de resíduos, • microrganismos • endotoxinas Resultados Todos os instrumentais apresentaram contaminação por proteínas em pelo menos um dos locais da amostra. A análise estatística indicou diferença Metodologia • 9 caixas de instrumentais (350 itens) significativa nos níveis de contaminação, o que sugere que os procedimentos de limpeza em alguns serviços são melhores • Limpeza: lavadora desinfectadora do que em outros. Alguns instrumentos • Microscopia óptica e biofluorescência apresentaram locais com depósitos cristalinos (detergentes).


Preparo §Organização da caixa; §Evite acondicionar instrumental em espuma. Embalagem §Embalagem dupla; §Tamanho adequado; §Avalie a condutividade do produto(contâiner); §Campos de algodão “queimados” por super aquecimento não devem ser utilizados.

Esterilização §esterilização terminal; §esterilização no ponto de uso; §esterilização flash CICLO FLASH: “Flash sterilization should not be used for implantable devices” AORN, march 2006, vol. 83 nº 3 Propósito Processo que assegura a qualidade resultante da ausência de carga microbiana capaz de ocasionar infecção. Caixas gráficas Ciclo gravitacional - 22 min. ou 28 min. Ciclo pré-vácuo - 08 min ou 10 min Nota: instrução do fabricante do implante para esterilização
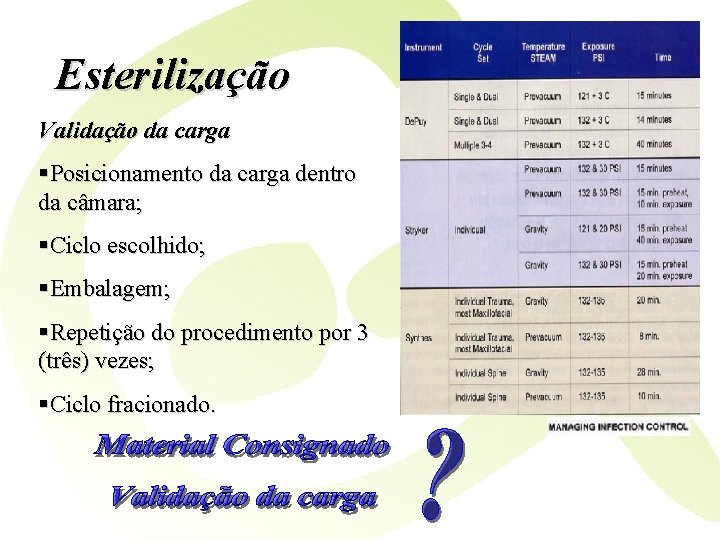
Esterilização Validação da carga §Posicionamento da carga dentro da câmara; §Ciclo escolhido; §Embalagem; §Repetição do procedimento por 3 (três) vezes; §Ciclo fracionado.

Esterilização Implantes poliméricos: polietileno de ultra-alto peso molecular e cimento ósseo acrílico NBR ISO 8828 – 1997 Sub-item 4. 1 Implantes silicone: contaminação (poeira, sujidade) desencadeia tecido fibrótico após implantação NBR ISO 8828 – 1997 Sub-item 4. 3 Componentes Cerâmicos: cabeça e acetábulo (cerâmicametal) - NBR ISO 8828 – 1997 Sub-item 5

Esterilização Monitorização do processo Indicador Biológico: deve ser incluído em todas as cargas que contenham implante e o implante deve permanecer em quarentena até que o resultado do IB seja conhecido. Indicador Químico : Integrador classe V AORN, march 2006, vol. 83, nº 3
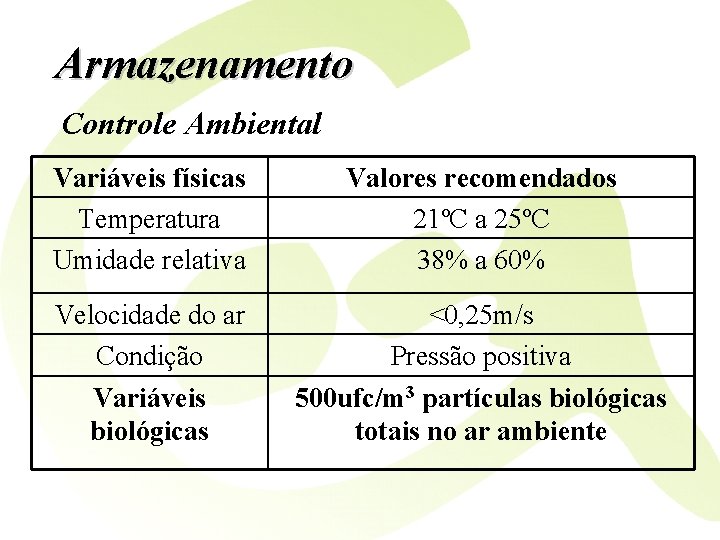
Armazenamento Controle Ambiental Variáveis físicas Temperatura Umidade relativa Valores recomendados 21ºC a 25ºC 38% a 60% Velocidade do ar Condição Variáveis biológicas <0, 25 m/s Pressão positiva 500 ufc/m 3 partículas biológicas totais no ar ambiente

Resolução CFM nº 1804 /2006 Estabelece normas para a utilização de materiais de implante Centro Cirúrgico §Verificar as informações rótulo §nome fabricante §nome do produto §técnico responsável precedido pela sigla do Conselho Profissional §Verificar dados §marca §modelo §número de lote §número do registro no Min. Saúde §prazo de validade do produto e da esterilização §indicador de temperatura §condições de inviolabilidade da embalagem interna e externa §inscrição “produto de uso único”

Centro Cirúrgico § Verificar a existência da bula em português; § Inutilizar as embalagens imediatamente após a utilização; § Registrar ocorrência formalmente, por escrito. § CME § setor de documentação fiscal da instituição § diretor técnico

Centro Cirúrgico Etiquetas de Identificação § Receber 5 (cinco) etiquetas, numeradas de 1 (um) a 5 (cinco) com o respectivo código de barras § Número CNPJ fabricante nacional ou do importador/distribuidor § Identificação do produto § Nome comercial § Número do registro do produto no Min. Saúde § Número do lote Etiquetas § Nº 1 prontuárioclinicodo paciente § Nº 2 laudo noentregue para o paciente § Nº 3 no documento fiscal que gera a cobrança na AIH ou na nota fiscal de venda § Nº 4 disponibilizadaparao controle do fornecedor § Nº 5 disponibilizada para o controle do cirurgião responsável

Centro Cirúrgico Enfermeiro do Centro Cirúrgico 1. 2. 3. Receber o material médico cirúrgico hospitalar solicitado com a respectiva nota fiscal de consignação ou vale de consignação; Checar os itens relacionados na nota fiscal de consignação com os itens entregues; Protocolar as notas fiscais recebidas, utilizando carimbo específico (data, horário e assinatura); 4. 5. Conferir o material médico cirúrgico hospitalar especial recebido comparando com o solicitado no agendamento e na nota fiscal de consignação ou vale de consignação; Checar os aparelhos, instrumentos e acessórios, com os dados da cirurgia (tipo de cirurgia, data e horário da cirurgia) e encaminhar oas aparelhos à sala de equipamentos e os instrumentais e acessórios para a CME.

Conclusão Os profissionais da saúde cada dia mais estão sendo desafiados, a prestar uma assistência eficiente, eficaz e segura aos seus clientes. É necessário adotar padrões de trabalho adequados e aplicáveis, onde todos os envolvidos na cadeia de fornecimento (material consignado) possam assumir a co-responsabilidade neste processo e assim, garantir a segurança do paciente.
- Slides: 41