JONSKA VEZA Jonska veza se javlja kada jedan







- Slides: 8

JONSKA VEZA!

Jonska veza se javlja kada jedan atom "preuzima" elektron od drugog atoma Primjeri molekula u kojima je ostvarena jonska veza su molekuli natrijum -hlorida Na. Cl i kalijum-hlorida KCl. Objašnjenje jonske veze dato je na primjeru Na. Cl. Prije formiranja molekula Na. Cl posmatraju se atomi Na i Cl u osnovnom stanju

§ Atom natrijuma u osnovnom stanju ima u jezgru 11 protona i u omotaču 11 elektrona. Raspodjela vjerovatnoće za 10 elektrona je sferno simetrična i oni se nalaze u sfernim ljuskama oko jezgra. Spoljašnji, jedanaesti elektron većinu vremena provodi izvan ovih ljuski. Jezgro elektrona natrijuma sa naelektrisanjem + 11 e zajedno sa 10 elektrona, u sfernim ljuskama oko jezgra, čije je naelektrisanje -10 e čine sistem čestica sa sa ukupnim naelektrisanjem +1 e.

§ U atomu hlorida 12 elektrona ima sferno Raspodjela bjerovatnoće za peti spoljašnji elektron simetričnu raspodjelu vjerovatnoće. od u atomu hlorida (na slici (a) to je predstavljeno preostalih 5 elektrona 4 imaju simetričnu isprekidanim linijama) raspodjelu u odnosu na Z osu

§ Izmedju nastalih suprotno naelektrisanih, Jona deluju privlacne sile I to privlacenje jeste JONSKA VEZA. § Kada atomi metala grade hemisku vezu sa atomima nemetala dolazi do primopredaje elektrona. § Atomi koi imaju visak elektrona(atomi metala) Predaju elektrone a atomi koima nedostaju elektroni (atomi nemetala ) primaju elektrone.

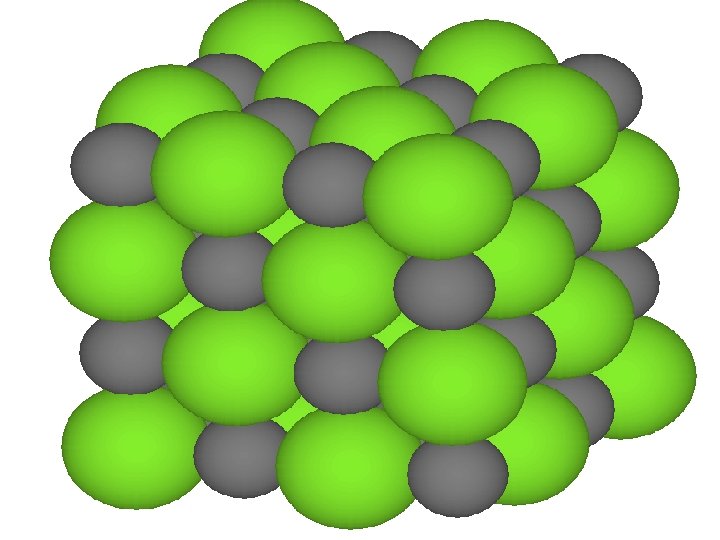
§ Joni natrrijuma I hlora ujedinjenju natrium-hlorid su pravilno rasporedjeni jedni oko drugih I grade kristalnu strukturu u kojoj se oko jednog jona natriuma nalazi 6 joan hlora I obrnuto. § Formulama jonskih jedinjenja prikazuje se samo odnos broja katijona I anjona u kristalnoj strukturi jedinjenja. § Kristalne supstance su supstance ciji delici imaju pravilan oblik. § Kristalne strukture izgradjene od jona nazivamo JONSKE KRISTALNE RESETKE!

