Jointly shaping the future of biosimilars Martin van

Jointly shaping the future of biosimilars Martin van der Graaff


Inhoud § § § Kernboodschappen Doel Uitwerking kernboodschappen Voorbeeld: EPO Farmacovigilantie Conclusies en aanbevelingen

Kernboodschappen § Biosimilars zijn geen generiek § Bijwerkingen correct toewijzen § Toepassing liefst onderbouwd met degelijk onderzoek per indicatie § Voorschrijver en patiënt hebben regie “If it ain’t broke, don’t fix it”

Doel § Informatie: – Veldpartijen maken gezamenlijk handleiding voor gebruik in het veld. – Bewustwording voorschrijvers, apothekers en patiënten nodig § Farmacovigilantie: – Signaal in de Eudravigilance databank moet direct éénduidig zijn! – Vigerende regels aanpassen op markt met veel originators en similars

Uitwerking kernboodschappen

Biosimilars zijn geen generiek § Tijdelijke verschillen(? ) – Aantal indicaties – Aantal toedieningsvormen cq sterktes – Kennis over lange termijn effecten § Permanente verschillen (naar verwachting) – Kweeksystemen – Relatieve doseringsverschillen (Dosing penalties) – Tendens tot genereren antilichamen – Profiel zeldzame ernstige bijwerkingen
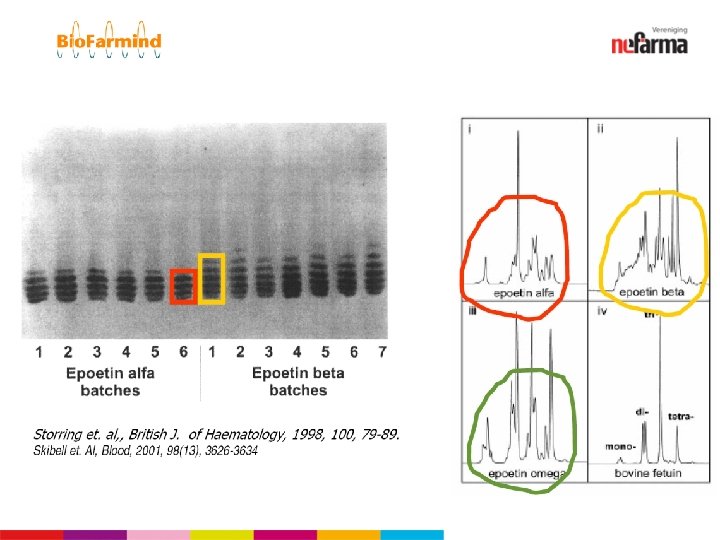

Verschil biosimilars onderling § Sommige biosimilars ontwikkeld vóórdat EMEA richtlijnen zijn vastgesteld: evolutie in soort dossier § Ieder biosimilar (&origineel) heeft zijn eigen set van indicaties, sterktes, dosing regime, (soms) INN; gevolg: anders kijken naar off-label! § Biosimilar kan alleen similar zijn naar een origineel, niet naar de hele klasse

Redenen voor terughoudendheid § § Belang patiënt EMEA garandeert geen interchangeability FDA Wet- en regelgeving in SE, ES, FR. Kortweg: geen substitutie zonder actief medisch toezicht § Verenigingen specialisten: eerste tijd geen switch tenzij op medische grond § Juridische argumenten (PW)

Praktijk moet meegroeien § § § Registratietechnisch Vigilantietechnisch Verzekeringstechnisch Vergoedingstechnisch Bewustwording veld

Dus vragen voor: § CBG: – Hoe gaan we samen het veld voorbereiden? – Waarom hebben biosimilars ‘gratis’ indicaties waar innovators voor moeten werken? – Welke stappen n. a. v. brief EU Comm. over farmacogivilantie? § VWS: – Wanneer advies aan CVZ vragen voor vergoedingsstatus van een biosimilar?

Vragen voor CVZ (1/2) § Hoe doorlopen biosimilars het vergoedingstraject : – Via een verkorte procedure zoals bij generiek? En leidend tot 1 A clustering? – Of via een andere route (waarom en hoe)? – Therapeutische waarde onderbouwen met gegevens? Zo ja, met welke?

Vragen voor CVZ (2/2) § In Kompas staat hier en daar: oppassen met therapeutische substitutie. Dus ook voor biosimilars? § Hoe wordt criterium “ervaring” hier ingekleurd? § Voorstel voor nieuwe categorie: de NBE (New Biosimilar Entity) § Aparte preparaattekst?

Kosten biosimilar producten lager § CVZ beheert pakket, maar: in hoeverre is kostenverschil leidend? § Ontwikkeling kosten product zal anders zijn dan ontwikkeling behandelkosten § Besparingen moeten inverdiend worden

Behandelkosten aandoening § Corrigeren voor confounding factors zoals bijvoorbeeld “dosing penalties” § Je gaat na een switch een periode in van monitoring op bereik stabiele situatie (bijv. Hb moet tussen 10 en 12 g/dl blijven). § Niet alle gevormde antilichamen hebben verwaarloosbaar effect

Voorbeeld EPO

Enige EPO vragen CBG: Geen klinische gegevens over subcutane toediening § Niettemin: Behandeling begint in predialysefase patiënt (sc noodzakelijk). § Hierover dus geen informatie in de bijsluiter van het biosimilar § Reden voor CBG communicatie?

Registraties EPO’s § Verschillen in registraties – CIA, anemie in premature kinderen, toepassing bij autologe bloedtransfusie – Verschillen in benodigde wekelijkse dosering (~15%), binnen marge klinische effectiviteit, maar wellicht wel gevolgen voor kosten – Subcutane indicatie soms zonder studies, hoewel bekend is dat dit problematisch kan zijn – Post Marketing Commitments (PMC’s) vergen nog heel wat werk

Biosimilar EPOs hebben § Niet alle indicaties (o. a. autologe bloeddonatie) § Niet alle doseringsvormen § Geen klinische gegevens over subcutane toediening § Mogelijk zelfs “dosing penalties”


Farmacovigilantie

Farmacovigilantie is uitdaging § Vigilanten weten wat ze nodig hebben, maar dokters en patiënten weten dat vaak niet. § Biosimilars zonder brand name maken het lastiger (Epoetin alfa …. . Hexal) § De kleine lettertjes: α, β, ω, of ζ? § In 2008 al 8 EPOs op de markt! § Gaat apotheker aandringen op unieke naam op recept?

Patiënten eenvoudig te volgen? § Output Eudravigilance is niet beter dan de input § AE rapporten vaak incompleet (bijv. lot number, iv of sc gedoseerd? ) § In NL geen indicatie op recept § Niet iedereen bij zelfde apotheek § Het kostte de originators jaren om de PCRA casus te ontleden. § Les: traceren kan in NL altijd, maar is daar de tijd voor?

Waarom samen? § Als bijwerking niet traceerbaar: verdenking van class effect waardoor originators ook terughoudend gebruikt worden § Gevolg is schade voor de patiënt en industrie. § Onbeheerste introductie brengt zowel veiligheid als kostenbesparing in gevaar § Uitdaging is om samen de weg te verkennen.

Conclusies en aanbevelingen

Conclusies § Inspanning nodig om verwarring te voorkomen § Er moet een goede (medische) reden zijn voor switch § Off-label liefst vermijden § Farmacovigilantie is kwestie van gezamenlijk belang en dus van gezamenlijke aanpak. § Communicatie naar het veld loont
- Slides: 27