Ivan ernuk Miroslav Urban Katedra fyziklnej a teoretickej

Ivan Černušák, Miroslav Urban Katedra fyzikálnej a teoretickej chémie Pri. F UK Teória chemickej väzby Bertrand Russell (1872 -1970): All exact science is dominated by the idea of approximation TCHV 1

Jednoduché otázky • Čo sú elementárne častice? • Čo sú atómy? • Čo sú molekuly? • Čo je ďalej. . . ? TCHV 2

Z histórie. . . • <10 -11 s Vesmír vypĺňa kvark/gluónová plazma (vznik/zánik elementárnych častíc) Baryogenéza (hmota dominuje nad antihmotou) • • 10 -6 s kvarky+gluóny Protóny/neutróny 1 s elektróny/pozitróny, T=1010 K 3 min atómy: vodík, deutérium, hélium. . . 3, 8 x 105 r ľahké atómy, svetlo a reliktné žiarenie 30 mil r hviezdy a ťažšie atómy 200 mil r galaxie, Mliečna cesta 9 mld r Slnečná sústava TCHV 3
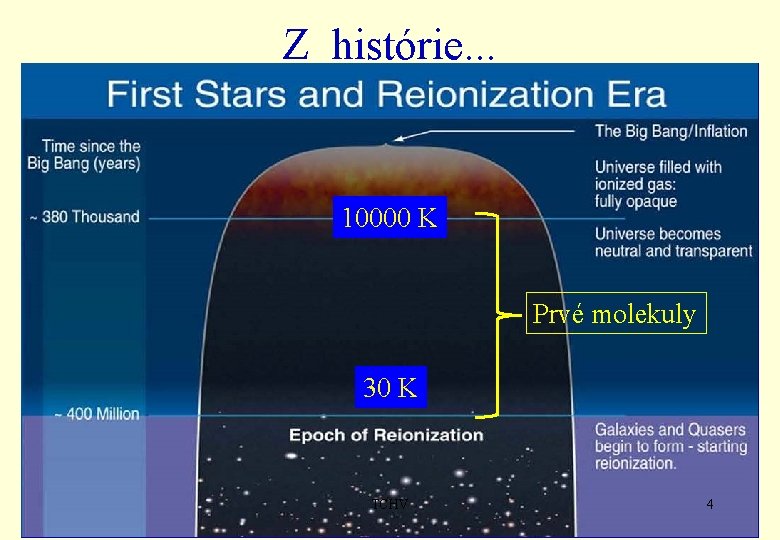
Z histórie. . . 10000 K Prvé molekuly 30 K TCHV 4

Astrofyzikálna časová os (úryvok z rozsiahlejšieho cyklu) TCHV 5
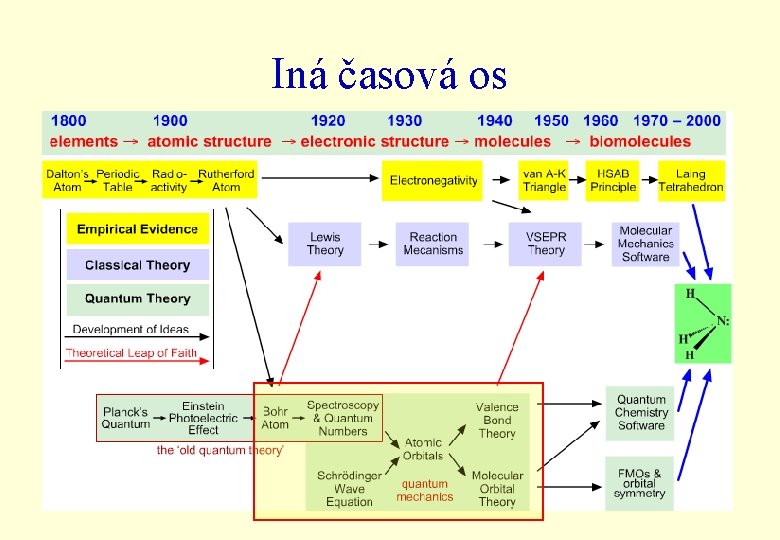
Iná časová os TCHV 6

Literatúra: 1. R. Zahradník, R. Polák: Základy kvantové chemie, SNTL Praha, 1985. motto: Fakta bez teorie je chaos. Teorie bez fakt je fantasie 2. R. Boča, S. Biskupič, Kvantová teória chemickej väzby a chemickej štruktúry, STU Bratislava, 2011 3. V. Lukeš a kol. , Počítačové modelovanie molekúl – metódy počítačovej chémie, STU Bratislava, 2011 4. R. L. de Kock, a H. B. Gray, Chemical Structure and Bonding. Benjamin/Cummings, Publishing Co. , 1980 http: //www. qch. fns. uniba. sk/TCHV/ TCHV 7

Pár hodín v knižnici Vám môže ušetriť mesiace práce v laboratóriu. * Kto je autorom tohto múdreho výroku , som už nenašiel. Ale dodávam pre chemikov (a nielen pre nich): d n í počítačového modelovania Pár týždňov Vám môže ušetriť mesiace zbytočnej práce v laboratóriu. * Existuje aj invertujúca glosa: Pár mesiacov driny v laboratóriu vás ušetrí od pár hodín v knižnici TCHV 8

Anotácia: 1. Minimórum z matematiky a fyziky (elementárne častice, vlnová funkcia, operátor, symetria, multiplicita. . . ) 2. Štruktúra atómu – vodík, spektrá, momenty hybnosti, term 3. Atómy a molekuly? N-časticová úloha nutnosť aproximácií – teórie MO a VV (N jednočasticových úloh) 4. ? ? Slaterov determinant, fermióny, antisymetria VF 5. (Skoro) všetko je v molekule vodíka! Ďalšie dvojatómové homo- a heteronukleárne molekuly, krivka pot. energie 6. Elektrónová konfigurácia ( , , d. . . väzby), orbitálne energie, korelačné diagramy, molekulové termy, excitované stavy, vlastnosti molekúl 7. Krok za 1 -časticový model: Fermiho a Coulombická diera, spinová a elektrónová korelácia, mnohočastičové efekty TCHV 9

7 - Krátka odbočka Two-body interactions Many-body interactions TCHV 10

F. A. Kekulé (von Stradonitz, sic!*), 1867: I rather expect that we shall someday find a mathematicomechanical explanation for what we now call atoms which will render an account of their properties. * Stará česká šľachtická rodina. Mimochodom, z prvých piatich Nobelových cien za chémiu boli tri udelené Kekulého žiakom. TCHV 11

Téza a Antitéza. . . While the various Lewis electron accountancy models work most of the time, they do not work all the time. Lewis theory cannot explain atomic or molecular spectroscopy or why oxygen, O 2, is paramagnetic. TCHV 12

Téza a Antitéza. . . Students tend to be introduced to chemistry through the various Lewis models. . . and are then surprised to learn that these models are not the whole story and can even be wrong. TCHV 13

Od interakcií k väzbám -E Van der Waals Multipól – multipól a i. Vodíková väzba, halogénová väzba, - stacking „neklasická“ väzba (2 e-3 c alebo ne-mc) Chemická väzba, elektrónová korelácia, relativistika? R TCHV 14

Príklady ión-dipól a relativistická väzba TCHV 15
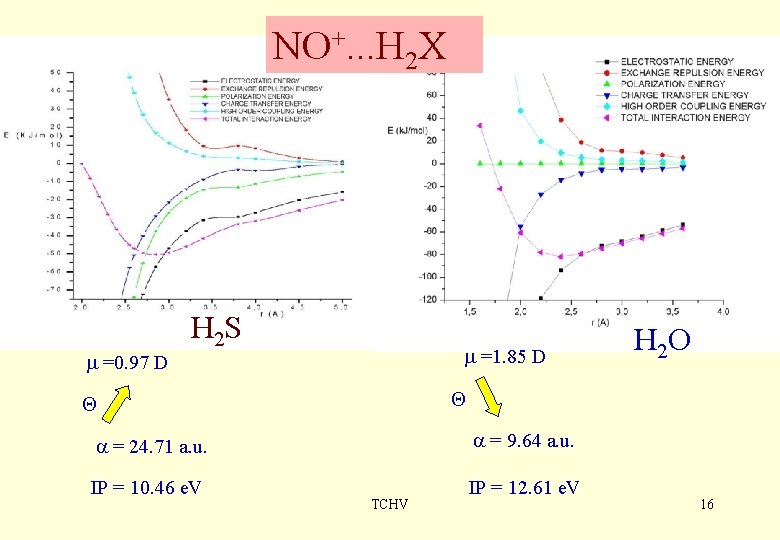
NO+. . . H 2 X m =0. 97 D H 2 S m =1. 85 D H 2 O Q Q a = 24. 71 a. u. a = 9. 64 a. u. IP = 10. 46 e. V IP = 12. 61 e. V TCHV 16

Mincové kovy + PH 3 Ag. PH 3 Cu. PH 3 M. . . PH 3 v nerelativistickej aproximácii – iba vd. W dimér! Au. PH 3 relativist. TCHV 17

Ťažisko tohto semestra - teória molekulových orbitalov - teória valenčných väzieb TCHV 18
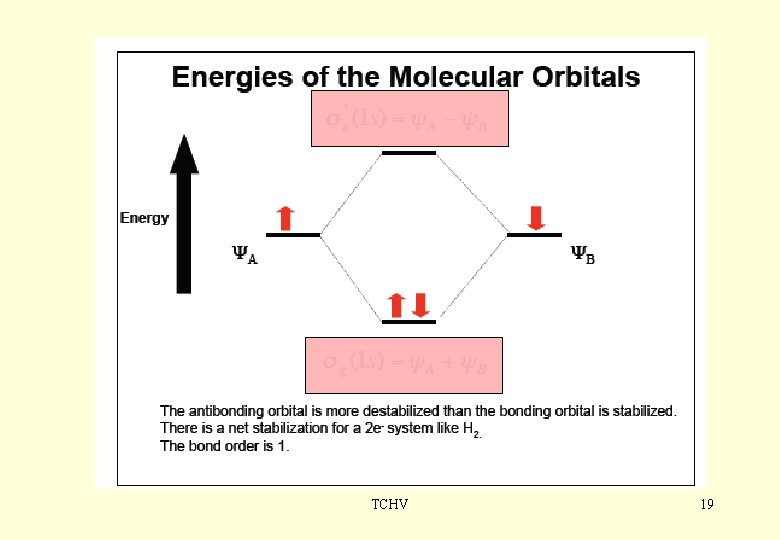
TCHV 19

TCHV 20
TCHV 21

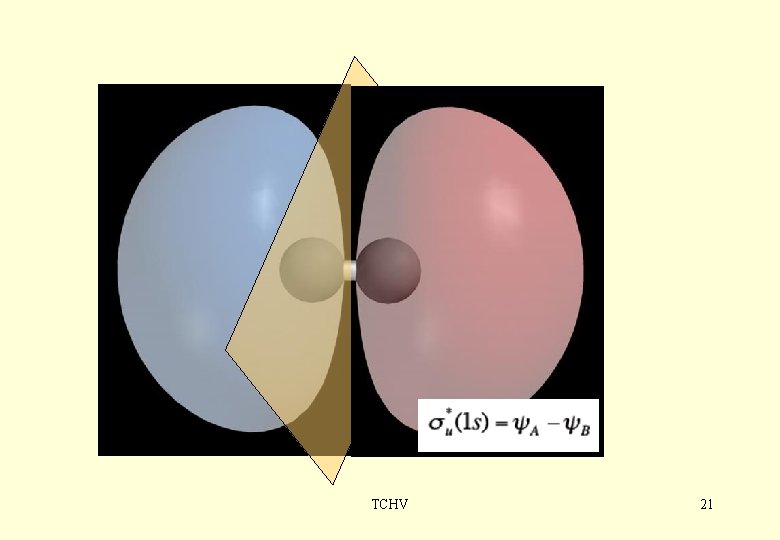
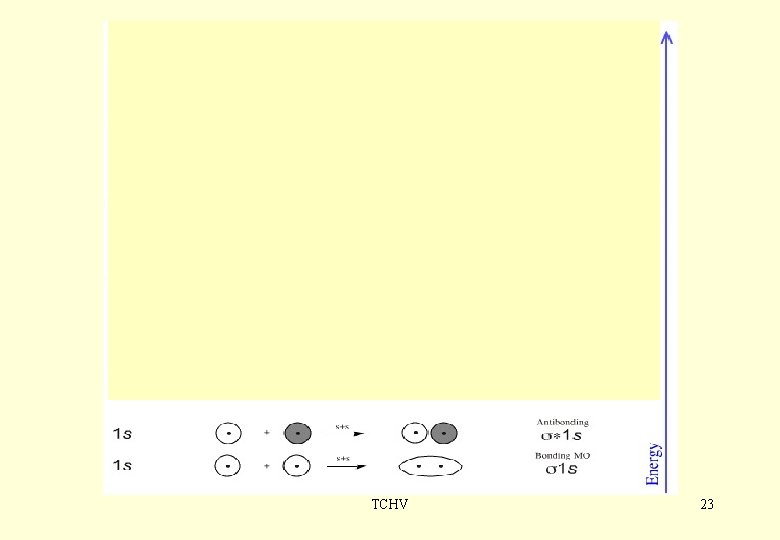
Pár príkladov MO s. A + s B → σ g ; s. A - s. B → σu*; ale: pz. A - pz. B → σg pz. A + pz. B → σu * px. A + px. B → πu; px. A - px. B → πg*; Podobne py atómové funkcie σg πu TCHV 22
TCHV 23
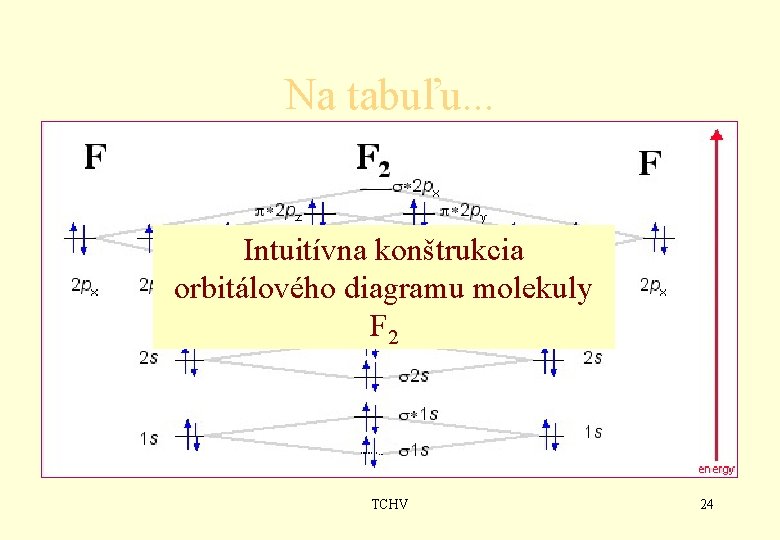
Na tabuľu. . . Intuitívna konštrukcia orbitálového diagramu molekuly F 2 TCHV 24
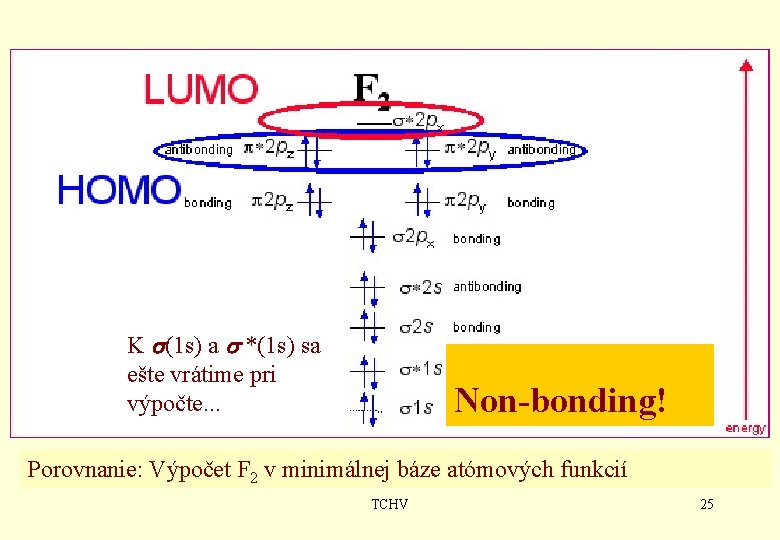
K s(1 s) a s *(1 s) sa ešte vrátime pri výpočte. . . ? Non-bonding! ? Porovnanie: Výpočet F 2 v minimálnej báze atómových funkcií TCHV 25

? Najprv analyzujeme všetky MO TCHV 26

Tzv. „core“ atómové funkcie (AO) nemajú prekryv nemá zmysel hovoriť o väzbových a antiväzbových MO, lebo sú neväzbové. Tento poznatok koreluje s výsledkami fotoelektrónovej spektroskopie. Also there is 2 s-2 p mixing, therefore 2 s-2 s is not more, but less, antibonding than 2 s+2 s is bonding: 2 s-2 s is nearly non-bonding, and Be 2 is a very weakly bound molecule. Similarly 2 p+2 p is only weakly bonding, and in N 2 it is just non-bonding. Spins are vectors in space, which are never vertical. The spin-z axis angle is the magic one, about 55 deg. , So there is an angle between socalled parallel spins of about 70 deg. Antiparallel spins are exactly antiparallel. alpha * beta for two electrons means both antiparallel or pseudo-parallel. V orbitálových diagramoch si treba uvedomiť aká je separácia elektrónových hladín: NIE ekvidistantná: 1 s < 2 p < 3 s < 3 p < 4 s <3 d < 4 p <5 s <4 d ALE: v súlade so spektroskopiou a kvantovou chémiou : 1 s << 2 s < 2 p << 3 s < 3 p << 3 d< 4 s < 4 p << 4 d <5 s Všimnite si: d < s poradie, čo je správne pre väčšinu prípadov, s výnimkou Li-Ne a Na-Ar periód. Poradie orbitálov vysvetľuje aj dĺžku riadkov v periodickej tabuľke: 1 s << 2 s, 2 p << 3 s, 3 p << 3 d, 4 p << 4 d, 5 p << 4 f, 5 d, 6 s etc. TCHV 27

Elektrónový a vibračný stav. . . ukážka výpočtu krivky potenciálnej energie. . . (ale najprv malé repetitórium) TCHV 28
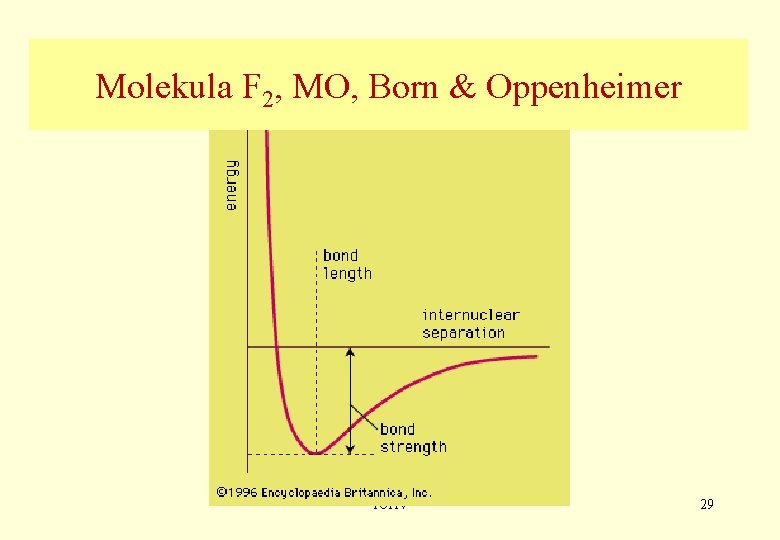
Molekula F 2, MO, Born & Oppenheimer TCHV 29
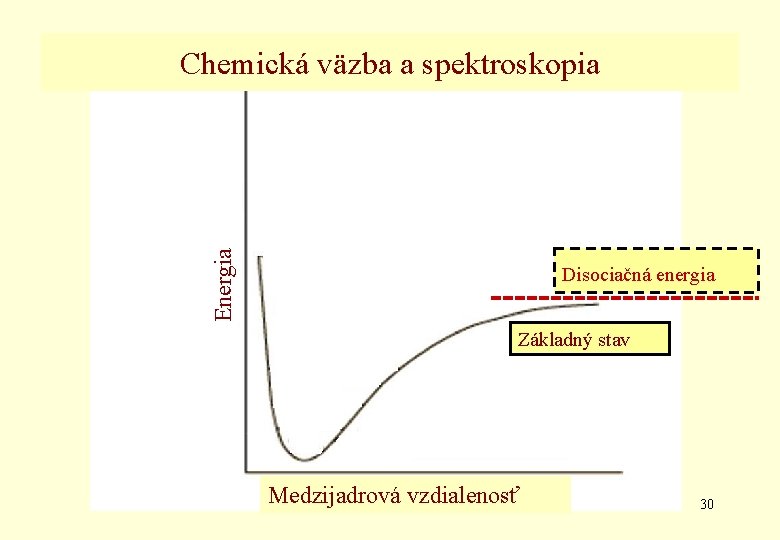
Energia Chemická väzba a spektroskopia Disociačná energia Základný stav Medzijadrová TCHVvzdialenosť 30
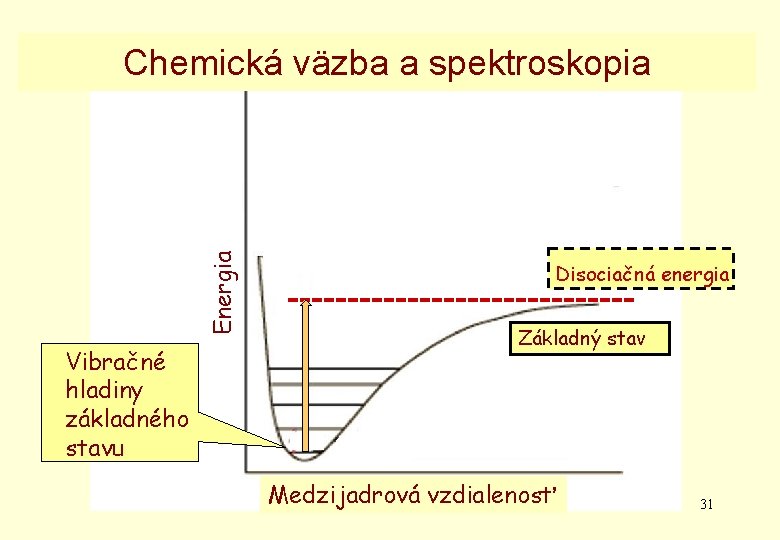
Energia Chemická väzba a spektroskopia Vibračné hladiny základného stavu Disociačná energia Základný stav Medzijadrová TCHV vzdialenosť 31
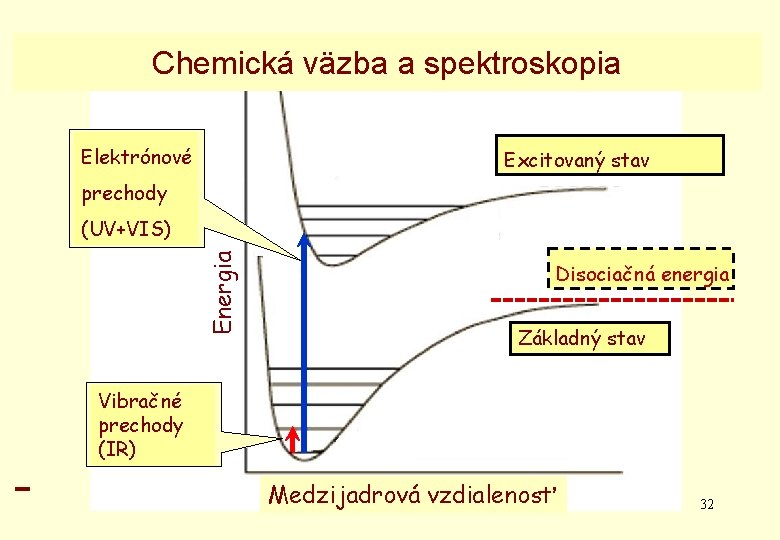
Chemická väzba a spektroskopia Elektrónové Excitovaný stav prechody Energia (UV+VIS) Disociačná energia Základný stav Vibračné prechody (IR) Medzijadrová TCHV vzdialenosť 32
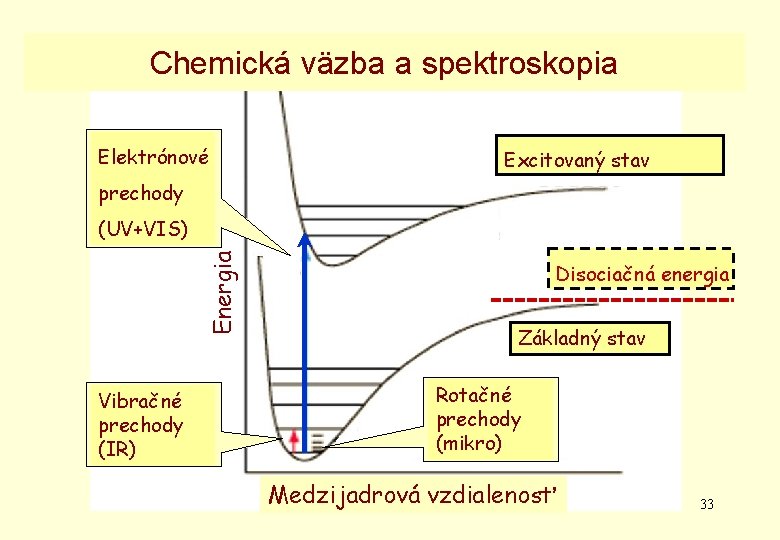
Chemická väzba a spektroskopia Elektrónové Excitovaný stav prechody Energia (UV+VIS) Vibračné prechody (IR) Disociačná energia Základný stav Rotačné prechody (mikro) Medzijadrová TCHV vzdialenosť 33
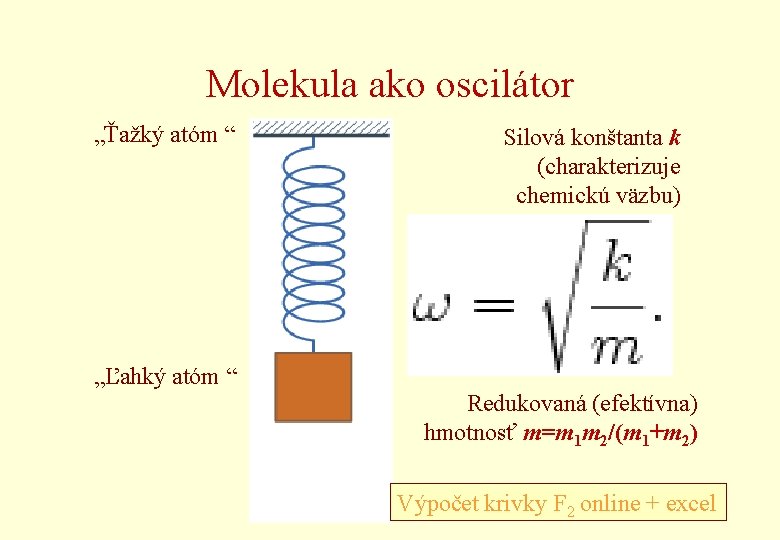
Molekula ako oscilátor „Ťažký atóm “ Silová konštanta k (charakterizuje chemickú väzbu) „Ľahký atóm “ Redukovaná (efektívna) hmotnosť m=m 1 m 2/(m 1+m 2) 34 Výpočet krivky F 2 online + excel TCHV
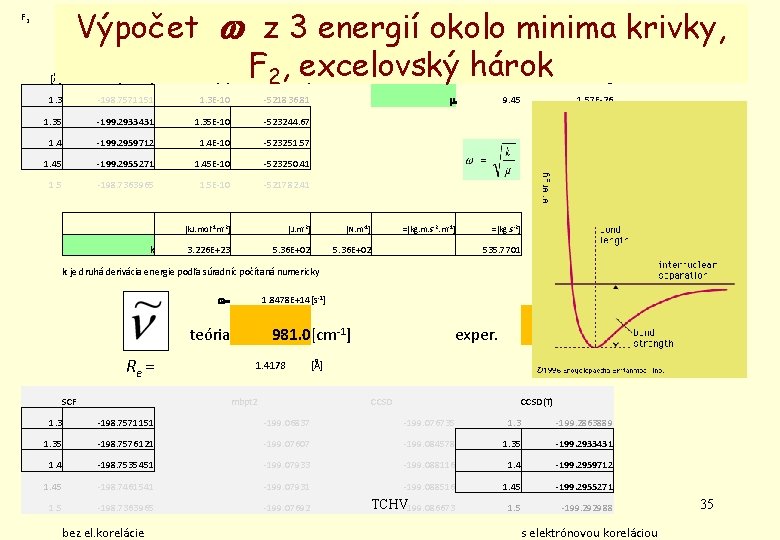
F 2 Výpočet w z 3 energií okolo minima krivky, F 2, excelovský hárok prevod R prevod E hm. jedn. NA c 1 E-10 2625. 5 1. 66 E-27 6. 02 E+23 3. 00 E+08 [hartree] [m] [k. J/mol] red. hmotn. au kg 1. 3 -198. 7571151 1. 3 E-10 -521836. 81 m 9. 45 1. 57 E-26 1. 35 -199. 2933431 1. 35 E-10 -523244. 67 1. 4 -199. 2959712 1. 4 E-10 -523251. 57 1. 45 -199. 2955271 1. 45 E-10 -523250. 41 1. 5 -198. 7363965 1. 5 E-10 -521782. 41 [k. J. mol-1 m-2] [J. m-2] [N. m-1] =[kg. m. s-2. m-1] =[kg. s-2] 3. 226 E+23 5. 36 E+02 [Å] k 3. 141593 2* 6. 2832 535. 7701 k je druhá derivácia energie podľa súradníc počítaná numericky w= 1. 8478 E+14[s-1] teória Re = SCF 981. 0[cm-1] 1. 4178 mbpt 2 exper. 916. 64[cm-1] 1. 41193[Å] CCSD(T) 1. 3 -198. 7571151 -199. 06837 -199. 076735 1. 3 -199. 2863889 1. 35 -198. 7576121 -199. 07607 -199. 084578 1. 35 -199. 2933431 1. 4 -198. 7535451 -199. 07933 -199. 088116 1. 4 -199. 2959712 1. 45 -198. 7461541 -199. 07931 -199. 088516 1. 45 -199. 2955271 1. 5 -198. 7363965 -199. 07692 TCHV-199. 086673 1. 5 -199. 292988 bez el. korelácie s elektrónovou koreláciou 35
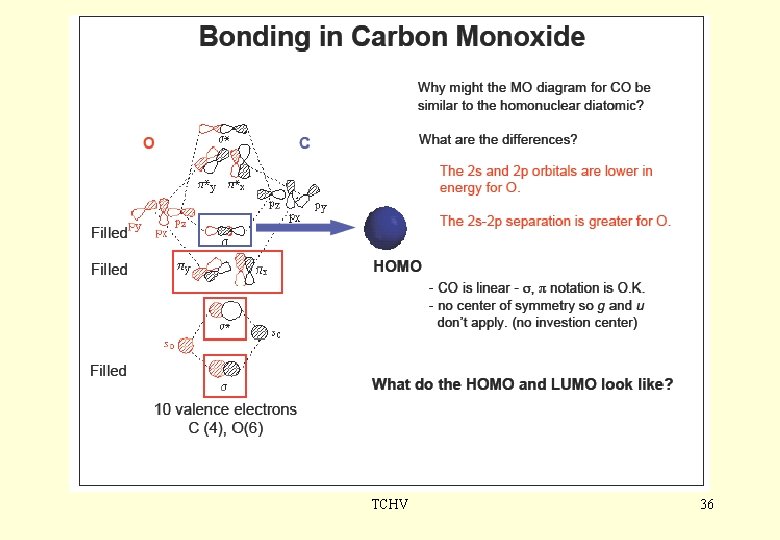
TCHV 36
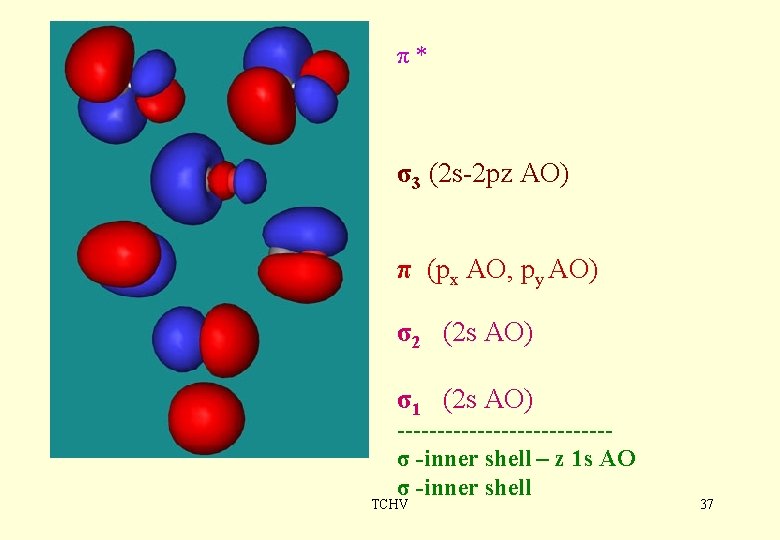
π* σ3 (2 s-2 pz AO) π (px AO, py AO) σ2 (2 s AO) σ1 (2 s AO) -------------σ -inner shell – z 1 s AO σ -inner shell TCHV 37
FIN Nasledujú nepoužité slajdy TCHV 38

TCHV 39

F. A. Kekulé (1867) "I fell into a reverie, and. . . - the atoms were gamboling before my eyes! Whenever, hitherto, these diminutive beings had appeared to me, they had always been in motion; but up to that time, I had never been able to discern the nature of their motion. Now, however, I saw how, frequently, two smaller atoms united to form a pair; how a larger one embraced the two smaller ones; how still larger ones kept hold of three or even four of the smaller; whilst the whole kept whirling in a giddy dance. I saw how the larger ones formed a chain, dragging the smaller ones after them, but only at the ends of the chain. . . The cry of the conductor: "Clapham Road, " awakened me from my dreaming; but I spent part of the night in putting on paper at least sketches of these dream forms. This was the origin of the Structural Theory. " TCHV 40

Z histórie. . . • ~500 p. K. – Leukippos a Demokritos – atómy a „prázdnota“ • 100 p. K. - Asclepiades z Prusy. . . o „klastroch atómov“ Titus Lucretius Carus: „De Rerum Natura“ Temný stredovek • 1803 – John Dalton - atómová teória (ale bez koncepcie väzieb) • 1811 - A. Avogadro – koncept molekuly • ~1858 – S. Cannizzaro – Sunto di un corso di filosofia chimica (rozdiel medzi at. a mol. hmostnosťami) TCHV 41

Téza a Antitéza. . . Chemistry sits right on the boundary between the quantum and classical worlds: the chemical bond is a quantum mechanical construct but the behaviour of molecular entities can often and conveniently be described in classical terms. As a result we have two entirely different types of model of chemical structure, bonding and reactivity. On one hand, we have theories that treat electrons as countable dots and stress the importance of electron accountancy. "Lewis" models recognise – but cannot explain – the magic numbers of electrons associated with the group 18 elements (He, Ne, Ar, Kr, Xe), aromatic π-systems, 18 -electron transition metal complexes, etc. Models include: Lewis octet theory, Lewis acids/base theory, electron accountancy, reactions mechanisms & curly arrows, VSEPR, etc. TCHV 42

Dve cesty k chemickej väzbe. . . On the other hand, we have quantum theory and models derived from the Schrödinger wave equation. These wave mechanical approaches lead to atomic orbitals, molecular orbital theory and valence bond theory. The MO approach has been developed into software such as Gaussian and Spartan. Quantum chemistry techniques give good numerical answers, but they are conceptually difficult. TCHV 43
- Slides: 43