IV rsz DNSRNSfehrje eukaritkban Tartalomjegyzk 6 Eukarita transzkripci

IV. rész DNS-RNS-fehérje eukariótákban

• Tartalomjegyzék • • 6. Eukarióta transzkripció 7. m. RNS érés, splicing 8. Riboszóma biogenezis 9. Eukarióta transzláció 10. Fehérjeszerkezet 11. Enzimkatalízis, Chaperonok 12. Sarlósejtes vérszegénység 13. Vezikuláris fehérjetranszport
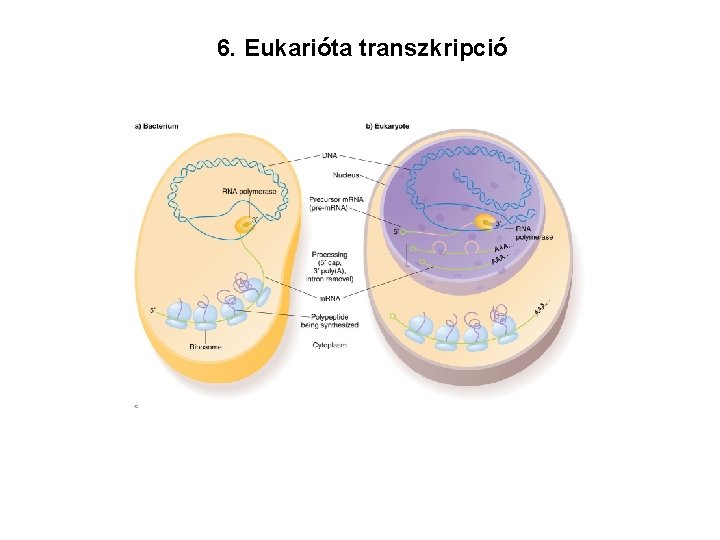
6. Eukarióta transzkripció
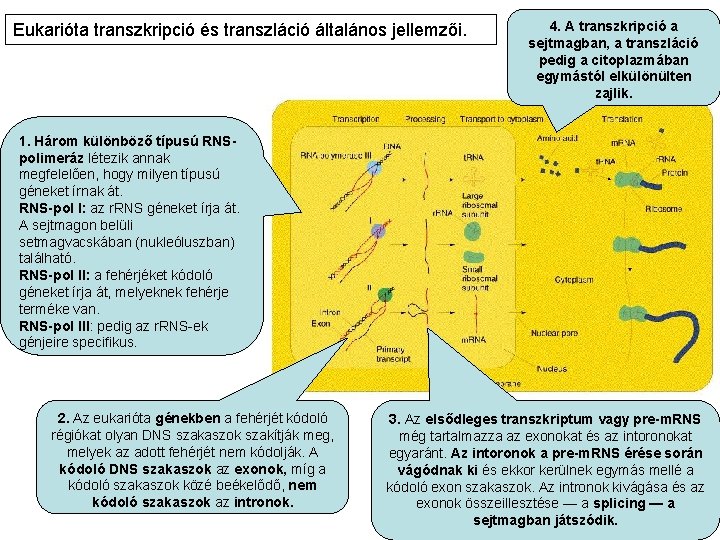
Eukarióta transzkripció és transzláció általános jellemzői. 4. A transzkripció a sejtmagban, a transzláció pedig a citoplazmában egymástól elkülönülten zajlik. 1. Három különböző típusú RNSpolimeráz létezik annak megfelelően, hogy milyen típusú géneket írnak át. RNS-pol I: az r. RNS géneket írja át. A sejtmagon belüli setmagvacskában (nukleóluszban) található. RNS-pol II: a fehérjéket kódoló géneket írja át, melyeknek fehérje terméke van. RNS-pol III: pedig az r. RNS-ek génjeire specifikus. 2. Az eukarióta génekben a fehérjét kódoló régiókat olyan DNS szakaszok szakítják meg, melyek az adott fehérjét nem kódolják. A kódoló DNS szakaszok az exonok, míg a kódoló szakaszok közé beékelődő, nem kódoló szakaszok az intronok. 3. Az elsődleges transzkriptum vagy pre-m. RNS még tartalmazza az exonokat és az intoronokat egyaránt. Az intoronok a pre-m. RNS érése során vágódnak ki és ekkor kerülnek egymás mellé a kódoló exon szakaszok. Az intronok kivágása és az exonok összeillesztése — a splicing — a sejtmagban játszódik.
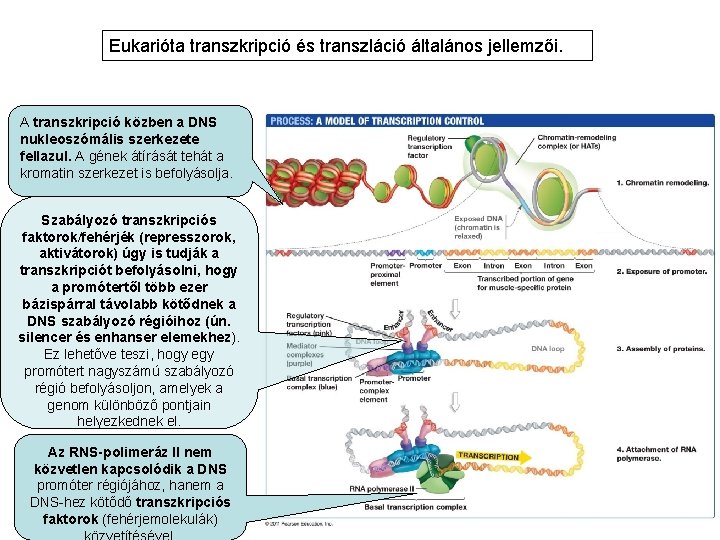
Eukarióta transzkripció és transzláció általános jellemzői. A transzkripció közben a DNS nukleoszómális szerkezete fellazul. A gének átírását tehát a kromatin szerkezet is befolyásolja. Szabályozó transzkripciós faktorok/fehérjék (represszorok, aktivátorok) úgy is tudják a transzkripciót befolyásolni, hogy a promótertől több ezer bázispárral távolabb kötődnek a DNS szabályozó régióihoz (ún. silencer és enhanser elemekhez). Ez lehetőve teszi, hogy egy promótert nagyszámú szabályozó régió befolyásoljon, amelyek a genom különböző pontjain helyezkednek el. Az RNS-polimeráz II nem közvetlen kapcsolódik a DNS promóter régiójához, hanem a DNS-hez kötődő transzkripciós faktorok (fehérjemolekulák)
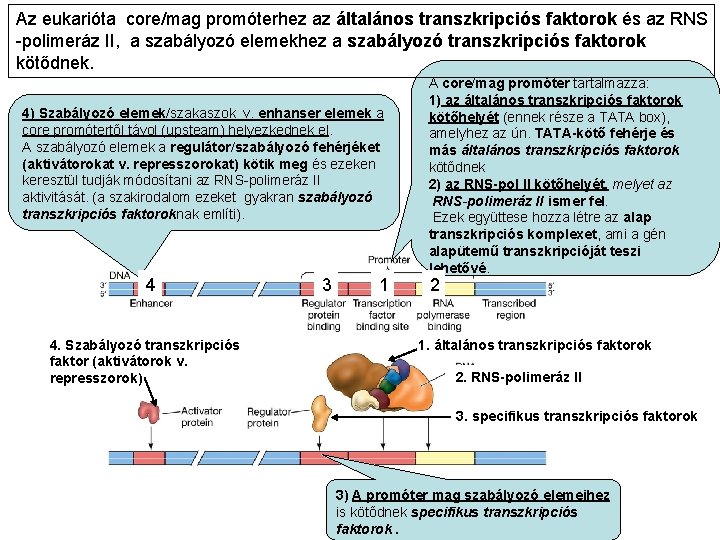
Az eukarióta core/mag promóterhez az általános transzkripciós faktorok és az RNS -polimeráz II, a szabályozó elemekhez a szabályozó transzkripciós faktorok kötődnek. 4) Szabályozó elemek/szakaszok v. enhanser elemek a core promótertől távol (upsteam) helyezkednek el. A szabályozó elemek a regulátor/szabályozó fehérjéket (aktivátorokat v. represszorokat) kötik meg és ezeken keresztül tudják módosítani az RNS-polimeráz II aktivitását. (a szakirodalom ezeket gyakran szabályozó transzkripciós faktoroknak említi). 4 4. Szabályozó transzkripciós faktor (aktivátorok v. represszorok) 3 1 A core/mag promóter tartalmazza: 1) az általános transzkripciós faktorok kötőhelyét (ennek része a TATA box), amelyhez az ún. TATA-kötő fehérje és más általános transzkripciós faktorok kötődnek 2) az RNS-pol II kötőhelyét, melyet az RNS-polimeráz II ismer fel. Ezek együttese hozza létre az alap transzkripciós komplexet, ami a gén alapütemű transzkripcióját teszi lehetővé. 2 1. általános transzkripciós faktorok 2. RNS-polimeráz II 3. specifikus transzkripciós faktorok 3) A promóter mag szabályozó elemeihez is kötődnek specifikus transzkripciós faktorok.
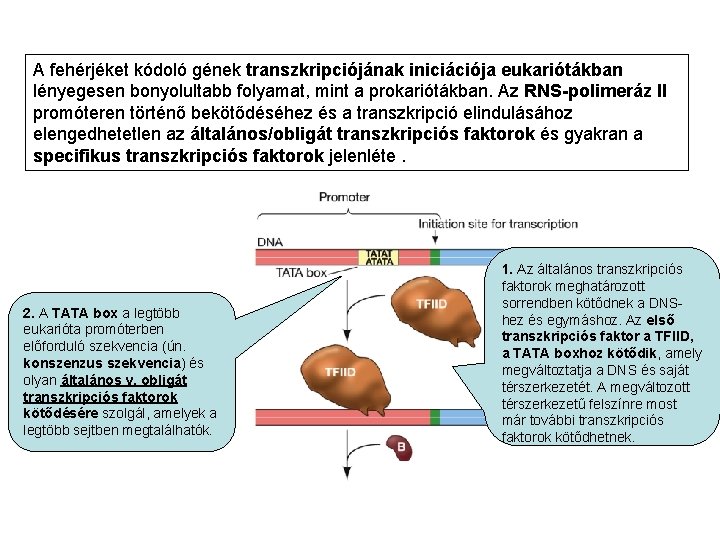
A fehérjéket kódoló gének transzkripciójának iniciációja eukariótákban lényegesen bonyolultabb folyamat, mint a prokariótákban. Az RNS-polimeráz II promóteren történő bekötődéséhez és a transzkripció elindulásához elengedhetetlen az általános/obligát transzkripciós faktorok és gyakran a specifikus transzkripciós faktorok jelenléte. 2. A TATA box a legtöbb eukarióta promóterben előforduló szekvencia (ún. konszenzus szekvencia) és olyan általános v. obligát transzkripciós faktorok kötődésére szolgál, amelyek a legtöbb sejtben megtalálhatók. 1. Az általános transzkripciós faktorok meghatározott sorrendben kötődnek a DNShez és egymáshoz. Az első transzkripciós faktor a TFIID, a TATA boxhoz kötődik, amely megváltoztatja a DNS és saját térszerkezetét. A megváltozott térszerkezetű felszínre most már további transzkripciós faktorok kötődhetnek.
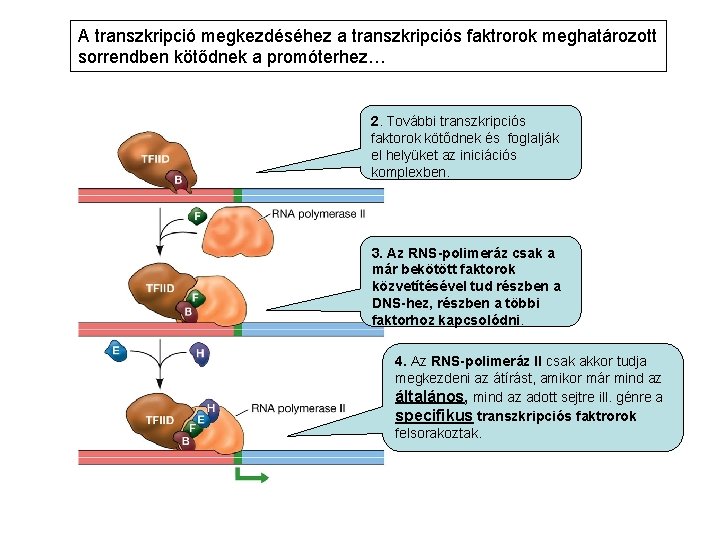
A transzkripció megkezdéséhez a transzkripciós faktrorok meghatározott sorrendben kötődnek a promóterhez… 2. További transzkripciós faktorok kötődnek és foglalják el helyüket az iniciációs komplexben. 3. Az RNS-polimeráz csak a már bekötött faktorok közvetítésével tud részben a DNS-hez, részben a többi faktorhoz kapcsolódni. 4. Az RNS-polimeráz II csak akkor tudja megkezdeni az átírást, amikor már mind az általános, mind az adott sejtre ill. génre a specifikus transzkripciós faktrorok felsorakoztak.
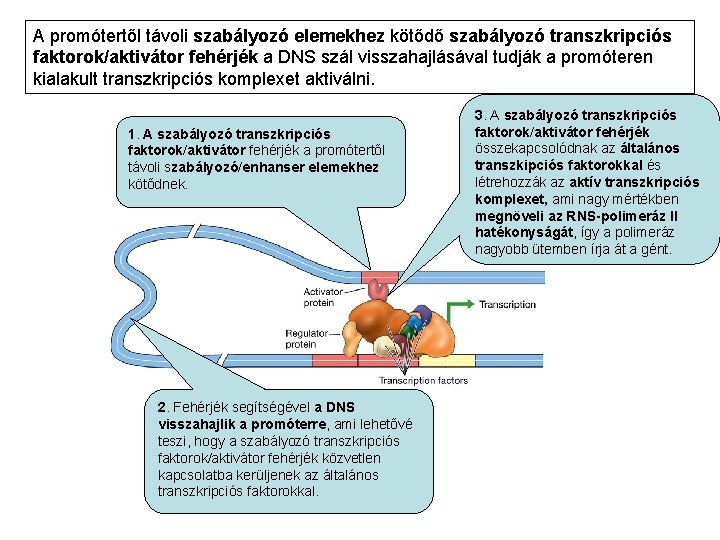
A promótertől távoli szabályozó elemekhez kötődő szabályozó transzkripciós faktorok/aktivátor fehérjék a DNS szál visszahajlásával tudják a promóteren kialakult transzkripciós komplexet aktiválni. 1. A szabályozó transzkripciós faktorok/aktivátor fehérjék a promótertől távoli szabályozó/enhanser elemekhez kötődnek. 2. Fehérjék segítségével a DNS visszahajlik a promóterre, ami lehetővé teszi, hogy a szabályozó transzkripciós faktorok/aktivátor fehérjék közvetlen kapcsolatba kerüljenek az általános transzkripciós faktorokkal. 3. A szabályozó transzkripciós faktorok/aktivátor fehérjék összekapcsolódnak az általános transzkipciós faktorokkal és létrehozzák az aktív transzkripciós komplexet, ami nagy mértékben megnöveli az RNS-polimeráz II hatékonyságát, így a polimeráz nagyobb ütemben írja át a gént.
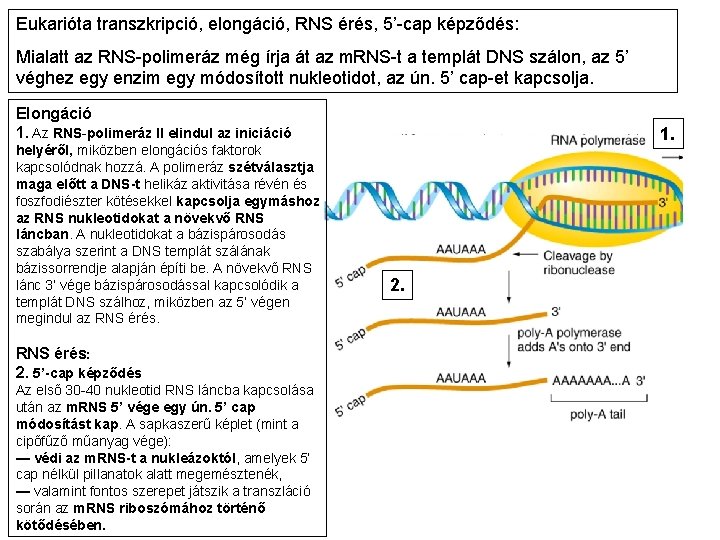
Eukarióta transzkripció, elongáció, RNS érés, 5’-cap képződés: Mialatt az RNS-polimeráz még írja át az m. RNS-t a templát DNS szálon, az 5’ véghez egy enzim egy módosított nukleotidot, az ún. 5’ cap-et kapcsolja. Elongáció 1. Az RNS-polimeráz II elindul az iniciáció helyéről, miközben elongációs faktorok kapcsolódnak hozzá. A polimeráz szétválasztja maga előtt a DNS-t helikáz aktivitása révén és foszfodiészter kötésekkel kapcsolja egymáshoz az RNS nukleotidokat a növekvő RNS láncban. A nukleotidokat a bázispárosodás szabálya szerint a DNS templát szálának bázissorrendje alapján építi be. A növekvő RNS lánc 3’ vége bázispárosodással kapcsolódik a templát DNS szálhoz, miközben az 5’ végen megindul az RNS érés: 2. 5’-cap képződés Az első 30 -40 nukleotid RNS láncba kapcsolása után az m. RNS 5’ vége egy ún. 5’ cap módosítást kap. A sapkaszerű képlet (mint a cipőfűző műanyag vége): — védi az m. RNS-t a nukleázoktól, amelyek 5’ cap nélkül pillanatok alatt megemésztenék, — valamint fontos szerepet játszik a transzláció során az m. RNS riboszómához történő kötődésében. 1. 2.
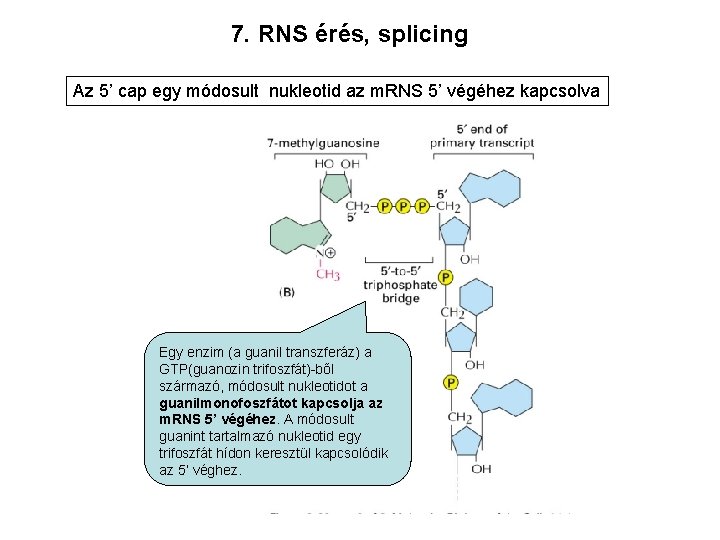
7. RNS érés, splicing Az 5’ cap egy módosult nukleotid az m. RNS 5’ végéhez kapcsolva Egy enzim (a guanil transzferáz) a GTP(guanozin trifoszfát)-ből származó, módosult nukleotidot a guanilmonofoszfátot kapcsolja az m. RNS 5’ végéhez. A módosult guanint tartalmazó nukleotid egy trifoszfát hídon keresztül kapcsolódik az 5’ véghez.
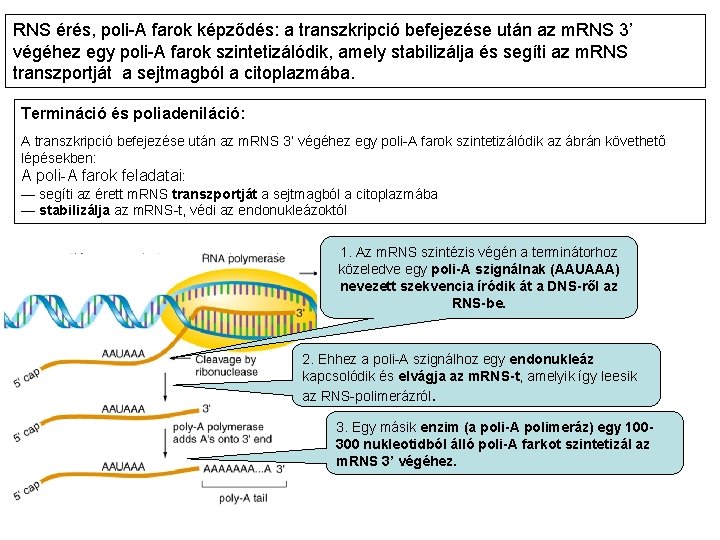
RNS érés, poli-A farok képződés: a transzkripció befejezése után az m. RNS 3’ végéhez egy poli-A farok szintetizálódik, amely stabilizálja és segíti az m. RNS transzportját a sejtmagból a citoplazmába. Termináció és poliadeniláció: A transzkripció befejezése után az m. RNS 3’ végéhez egy poli-A farok szintetizálódik az ábrán követhető lépésekben: A poli-A farok feladatai: — segíti az érett m. RNS transzportját a sejtmagból a citoplazmába — stabilizálja az m. RNS-t, védi az endonukleázoktól 1. Az m. RNS szintézis végén a terminátorhoz közeledve egy poli-A szignálnak (AAUAAA) nevezett szekvencia íródik át a DNS-ről az RNS-be. 2. Ehhez a poli-A szignálhoz egy endonukleáz kapcsolódik és elvágja az m. RNS-t, amelyik így leesik az RNS-polimerázról. 3. Egy másik enzim (a poli-A polimeráz) egy 100300 nukleotidból álló poli-A farkot szintetizál az m. RNS 3’ végéhez.
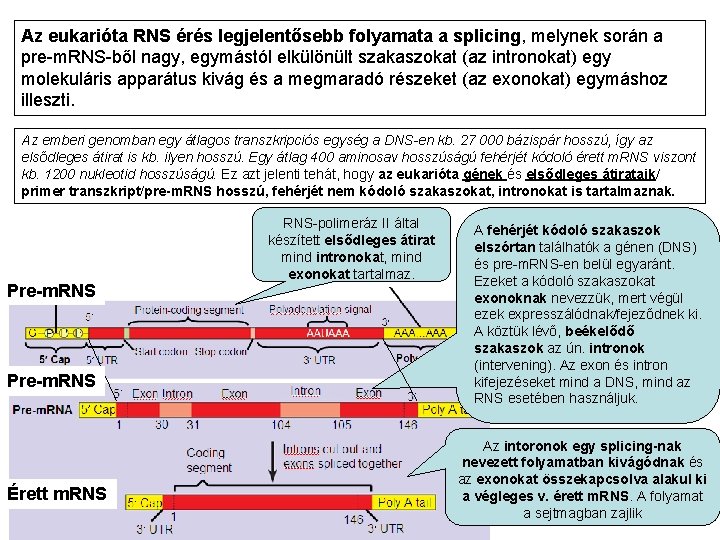
Az eukarióta RNS érés legjelentősebb folyamata a splicing, melynek során a pre-m. RNS-ből nagy, egymástól elkülönült szakaszokat (az intronokat) egy molekuláris apparátus kivág és a megmaradó részeket (az exonokat) egymáshoz illeszti. Az emberi genomban egy átlagos transzkripciós egység a DNS-en kb. 27 000 bázispár hosszú, így az elsődleges átirat is kb. ilyen hosszú. Egy átlag 400 aminosav hosszúságú fehérjét kódoló érett m. RNS viszont kb. 1200 nukleotid hosszúságú. Ez azt jelenti tehát, hogy az eukarióta gének és elsődleges átirataik/ primer transzkript/pre-m. RNS hosszú, fehérjét nem kódoló szakaszokat, intronokat is tartalmaznak. Pre-m. RNS Érett m. RNS-polimeráz II által készített elsődleges átirat mind intronokat, mind exonokat tartalmaz. A fehérjét kódoló szakaszok elszórtan találhatók a génen (DNS) és pre-m. RNS-en belül egyaránt. Ezeket a kódoló szakaszokat exonoknak nevezzük, mert végül ezek expresszálódnak/fejeződnek ki. A köztük lévő, beékelődő szakaszok az ún. intronok (intervening). Az exon és intron kifejezéseket mind a DNS, mind az RNS esetében használjuk. Az intoronok egy splicing-nak nevezett folyamatban kivágódnak és az exonokat összekapcsolva alakul ki a végleges v. érett m. RNS. A folyamat a sejtmagban zajlik
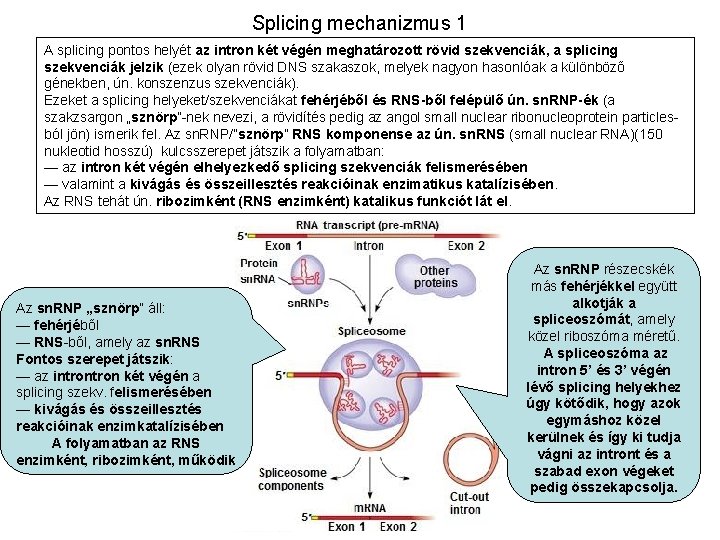
Splicing mechanizmus 1 A splicing pontos helyét az intron két végén meghatározott rövid szekvenciák, a splicing szekvenciák jelzik (ezek olyan rövid DNS szakaszok, melyek nagyon hasonlóak a különböző génekben, ún. konszenzus szekvenciák). Ezeket a splicing helyeket/szekvenciákat fehérjéből és RNS-ből felépülő ún. sn. RNP-ék (a szakzsargon „sznörp”-nek nevezi, a rövidítés pedig az angol small nuclear ribonucleoprotein particlesból jön) ismerik fel. Az sn. RNP/”sznörp” RNS komponense az ún. sn. RNS (small nuclear RNA)(150 nukleotid hosszú) kulcsszerepet játszik a folyamatban: — az intron két végén elhelyezkedő splicing szekvenciák felismerésében — valamint a kivágás és összeillesztés reakcióinak enzimatikus katalízisében. Az RNS tehát ún. ribozimként (RNS enzimként) katalikus funkciót lát el. Az sn. RNP „sznörp” áll: — fehérjéből — RNS-ből, amely az sn. RNS Fontos szerepet játszik: — az intron két végén a splicing szekv. felismerésében — kivágás és összeillesztés reakcióinak enzimkatalízisében A folyamatban az RNS enzimként, ribozimként, működik Az sn. RNP részecskék más fehérjékkel együtt alkotják a spliceoszómát, amely közel riboszóma méretű. A spliceoszóma az intron 5’ és 3’ végén lévő splicing helyekhez úgy kötődik, hogy azok egymáshoz közel kerülnek és így ki tudja vágni az intront és a szabad exon végeket pedig összekapcsolja.
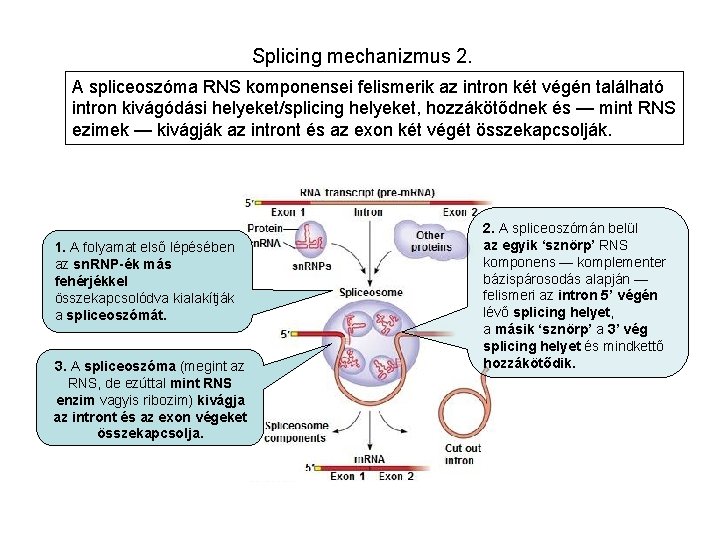
Splicing mechanizmus 2. A spliceoszóma RNS komponensei felismerik az intron két végén található intron kivágódási helyeket/splicing helyeket, hozzákötődnek és — mint RNS ezimek — kivágják az intront és az exon két végét összekapcsolják. 1. A folyamat első lépésében az sn. RNP-ék más fehérjékkel összekapcsolódva kialakítják a spliceoszómát. 3. A spliceoszóma (megint az RNS, de ezúttal mint RNS enzim vagyis ribozim) kivágja az intront és az exon végeket összekapcsolja. 2. A spliceoszómán belül az egyik ‘sznörp’ RNS komponens — komplementer bázispárosodás alapján — felismeri az intron 5’ végén lévő splicing helyet, a másik ‘sznörp’ a 3’ vég splicing helyet és mindkettő hozzákötődik.
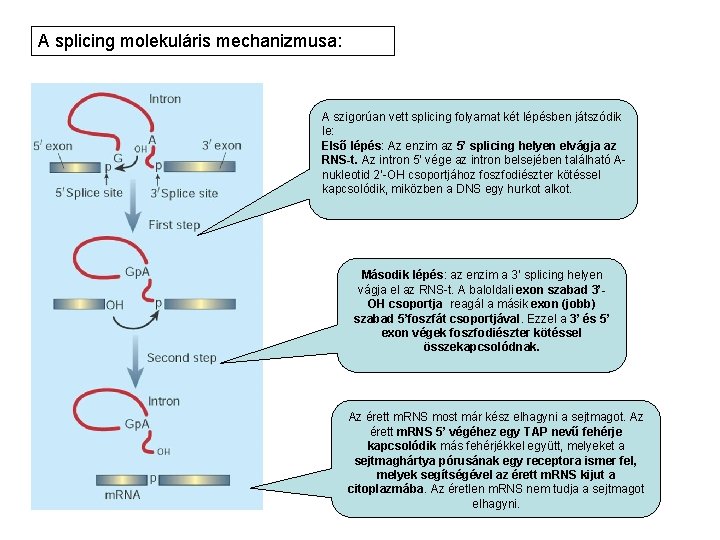
A splicing molekuláris mechanizmusa: A szigorúan vett splicing folyamat két lépésben játszódik le: Első lépés: Az enzim az 5’ splicing helyen elvágja az RNS-t. Az intron 5’ vége az intron belsejében található Anukleotid 2’-OH csoportjához foszfodiészter kötéssel kapcsolódik, miközben a DNS egy hurkot alkot. Második lépés: az enzim a 3’ splicing helyen vágja el az RNS-t. A baloldali exon szabad 3’OH csoportja reagál a másik exon (jobb) szabad 5’foszfát csoportjával. Ezzel a 3’ és 5’ exon végek foszfodiészter kötéssel összekapcsolódnak. Az érett m. RNS most már kész elhagyni a sejtmagot. Az érett m. RNS 5’ végéhez egy TAP nevű fehérje kapcsolódik más fehérjékkel együtt, melyeket a sejtmaghártya pórusának egy receptora ismer fel, melyek segítségével az érett m. RNS kijut a citoplazmába. Az éretlen m. RNS nem tudja a sejtmagot elhagyni.
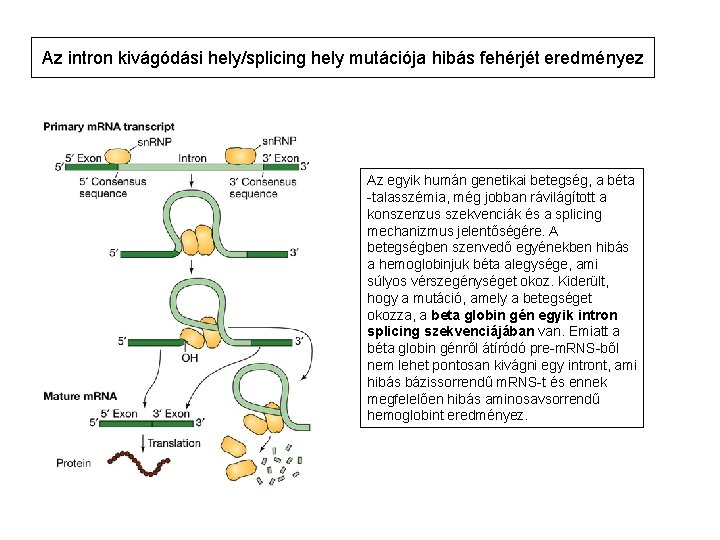
Az intron kivágódási hely/splicing hely mutációja hibás fehérjét eredményez Az egyik humán genetikai betegség, a béta -talasszémia, még jobban rávilágított a konszenzus szekvenciák és a splicing mechanizmus jelentőségére. A betegségben szenvedő egyénekben hibás a hemoglobinjuk béta alegysége, ami súlyos vérszegénységet okoz. Kiderült, hogy a mutáció, amely a betegséget okozza, a beta globin gén egyik intron splicing szekvenciájában van. Emiatt a béta globin génről átíródó pre-m. RNS-ből nem lehet pontosan kivágni egy intront, ami hibás bázissorrendű m. RNS-t és ennek megfelelően hibás aminosavsorrendű hemoglobint eredményez.
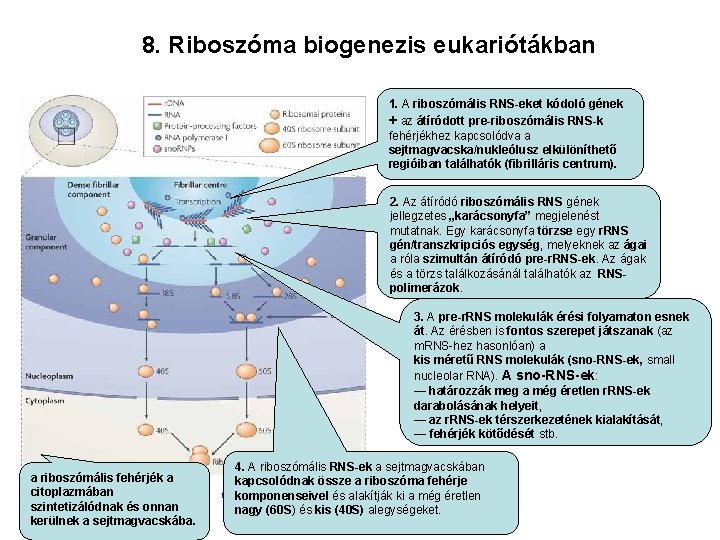
8. Riboszóma biogenezis eukariótákban 1. A riboszómális RNS-eket kódoló gének + az átíródott pre-riboszómális RNS-k fehérjékhez kapcsolódva a sejtmagvacska/nukleólusz elkülöníthető regióiban találhatók (fibrilláris centrum). 2. Az átíródó riboszómális RNS gének jellegzetes „karácsonyfa” megjelenést mutatnak. Egy karácsonyfa törzse egy r. RNS gén/transzkripciós egység, melyeknek az ágai a róla szimultán átíródó pre-r. RNS-ek. Az ágak és a törzs találkozásánál találhatók az RNSpolimerázok. 3. A pre-r. RNS molekulák érési folyamaton esnek át. Az érésben is fontos szerepet játszanak (az m. RNS-hez hasonlóan) a kis méretű RNS molekulák (sno-RNS-ek, small nucleolar RNA). A sno-RNS-ek: — határozzák meg a még éretlen r. RNS-ek darabolásának helyeit, — az r. RNS-ek térszerkezetének kialakítását, — fehérjék kötődését stb. a riboszómális fehérjék a citoplazmában szintetizálódnak és onnan kerülnek a sejtmagvacskába. 4. A riboszómális RNS-ek a sejtmagvacskában kapcsolódnak össze a riboszóma fehérje komponenseivel és alakítják ki a még éretlen nagy (60 S) és kis (40 S) alegységeket.
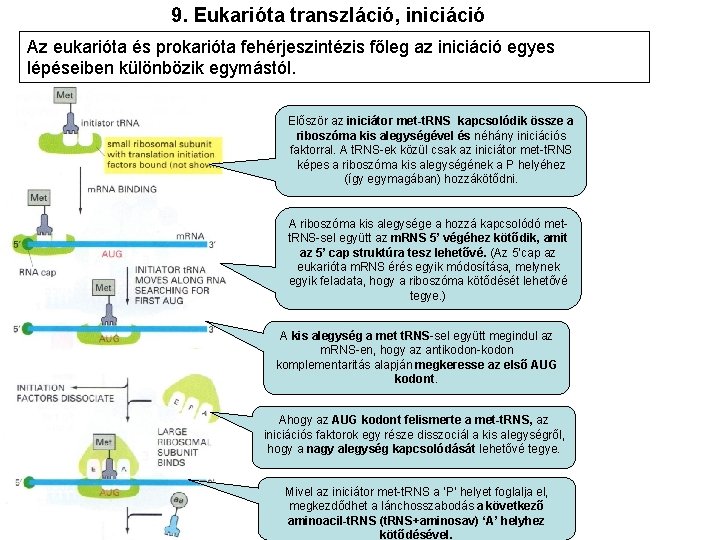
9. Eukarióta transzláció, iniciáció Az eukarióta és prokarióta fehérjeszintézis főleg az iniciáció egyes lépéseiben különbözik egymástól. Először az iniciátor met-t. RNS kapcsolódik össze a riboszóma kis alegységével és néhány iniciációs faktorral. A t. RNS-ek közül csak az iniciátor met-t. RNS képes a riboszóma kis alegységének a P helyéhez (így egymagában) hozzákötődni. A riboszóma kis alegysége a hozzá kapcsolódó mett. RNS-sel együtt az m. RNS 5’ végéhez kötődik, amit az 5’ cap struktúra tesz lehetővé. (Az 5’cap az eukarióta m. RNS érés egyik módosítása, melynek egyik feladata, hogy a riboszóma kötődését lehetővé tegye. ) A kis alegység a met t. RNS-sel együtt megindul az m. RNS-en, hogy az antikodon-kodon komplementaritás alapján megkeresse az első AUG kodont. Ahogy az AUG kodont felismerte a met-t. RNS, az iniciációs faktorok egy része disszociál a kis alegységről, hogy a nagy alegység kapcsolódását lehetővé tegye. Mivel az iniciátor met-t. RNS a ‘P’ helyet foglalja el, megkezdődhet a lánchosszabodás a következő aminoacil-t. RNS (t. RNS+aminosav) ‘A’ helyhez kötődésével.
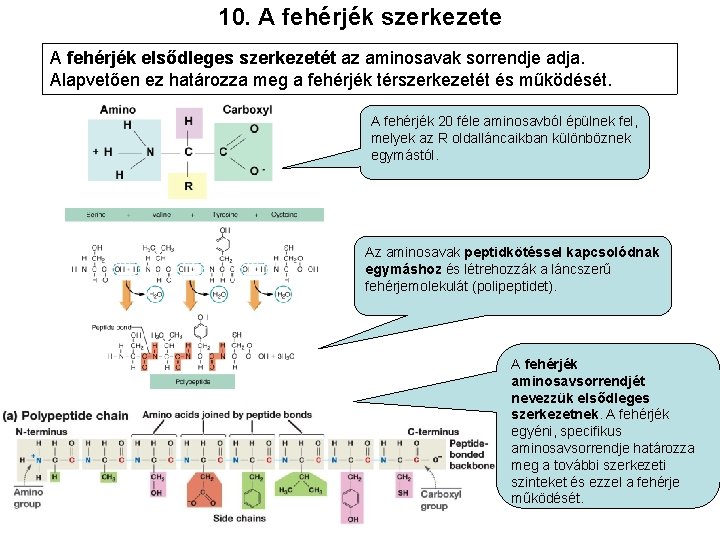
10. A fehérjék szerkezete A fehérjék elsődleges szerkezetét az aminosavak sorrendje adja. Alapvetően ez határozza meg a fehérjék térszerkezetét és működését. A fehérjék 20 féle aminosavból épülnek fel, melyek az R oldalláncaikban különböznek egymástól. Az aminosavak peptidkötéssel kapcsolódnak egymáshoz és létrehozzák a láncszerű fehérjemolekulát (polipeptidet). A fehérjék aminosavsorrendjét nevezzük elsődleges szerkezetnek. A fehérjék egyéni, specifikus aminosavsorrendje határozza meg a további szerkezeti szinteket és ezzel a fehérje működését.
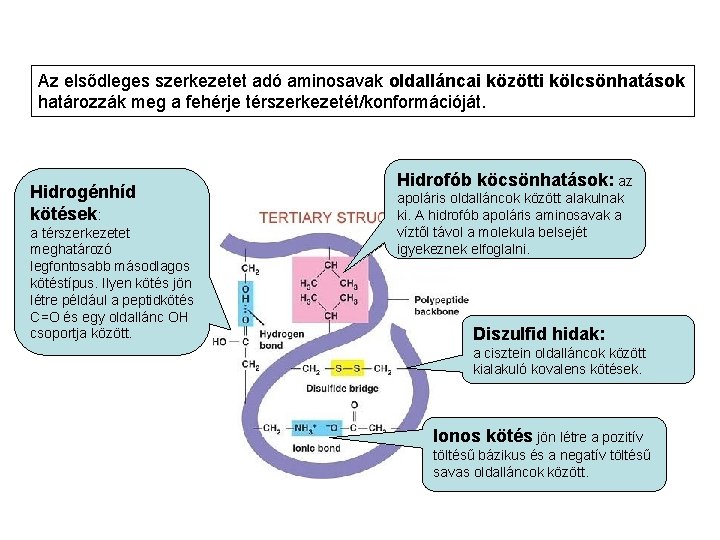
Az elsődleges szerkezetet adó aminosavak oldalláncai közötti kölcsönhatások határozzák meg a fehérje térszerkezetét/konformációját. Hidrogénhíd kötések: a térszerkezetet meghatározó legfontosabb másodlagos kötéstípus. Ilyen kötés jön létre például a peptidkötés C=O és egy oldallánc OH csoportja között. Hidrofób köcsönhatások: az apoláris oldalláncok között alakulnak ki. A hidrofób apoláris aminosavak a víztől távol a molekula belsejét igyekeznek elfoglalni. Diszulfid hidak: a cisztein oldalláncok között kialakuló kovalens kötések. Ionos kötés jön létre a pozitív töltésű bázikus és a negatív töltésű savas oldalláncok között.
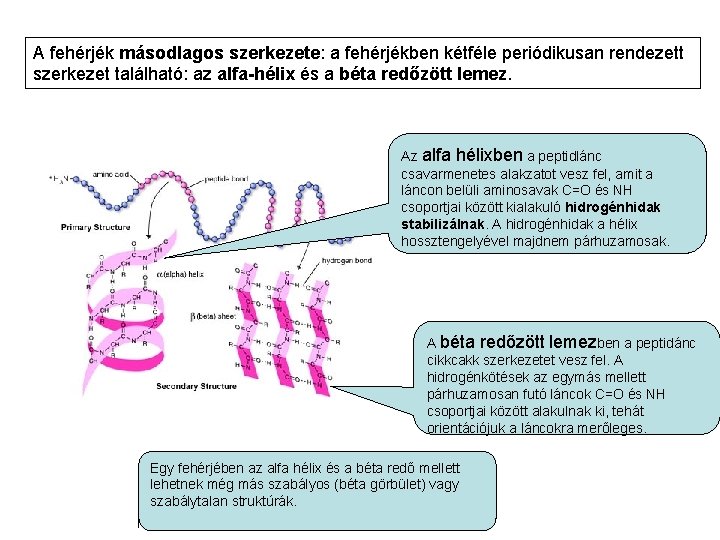
A fehérjék másodlagos szerkezete: a fehérjékben kétféle periódikusan rendezett szerkezet található: az alfa-hélix és a béta redőzött lemez. Az alfa hélixben a peptidlánc csavarmenetes alakzatot vesz fel, amit a láncon belüli aminosavak C=O és NH csoportjai között kialakuló hidrogénhidak stabilizálnak. A hidrogénhidak a hélix hossztengelyével majdnem párhuzamosak. A béta redőzött lemezben a peptidánc cikkcakk szerkezetet vesz fel. A hidrogénkötések az egymás mellett párhuzamosan futó láncok C=O és NH csoportjai között alakulnak ki, tehát orientációjuk a láncokra merőleges. Egy fehérjében az alfa hélix és a béta redő mellett lehetnek még más szabályos (béta görbület) vagy szabálytalan struktúrák.
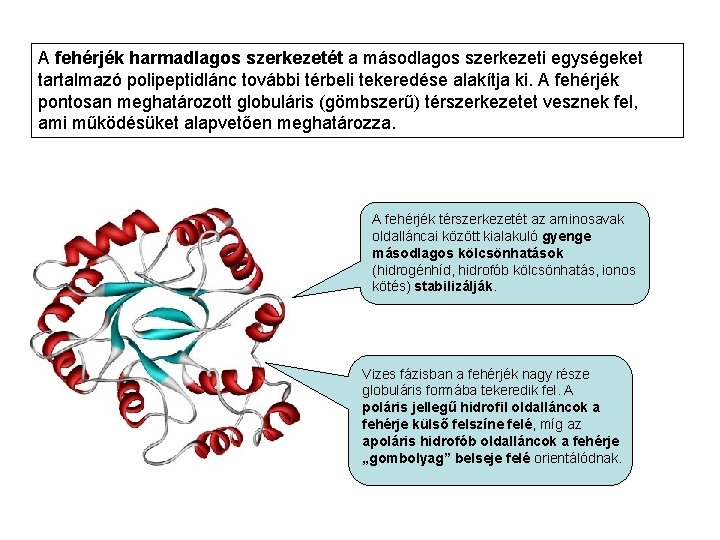
A fehérjék harmadlagos szerkezetét a másodlagos szerkezeti egységeket tartalmazó polipeptidlánc további térbeli tekeredése alakítja ki. A fehérjék pontosan meghatározott globuláris (gömbszerű) térszerkezetet vesznek fel, ami működésüket alapvetően meghatározza. A fehérjék térszerkezetét az aminosavak oldalláncai között kialakuló gyenge másodlagos kölcsönhatások (hidrogénhíd, hidrofób kölcsönhatás, ionos kötés) stabilizálják. Vizes fázisban a fehérjék nagy része globuláris formába tekeredik fel. A poláris jellegű hidrofil oldalláncok a fehérje külső felszíne felé, míg az apoláris hidrofób oldalláncok a fehérje „gombolyag” belseje felé orientálódnak.
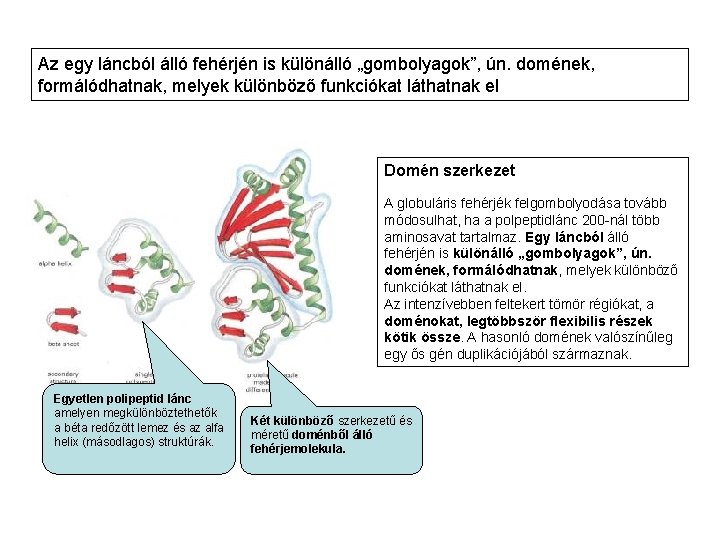
Az egy láncból álló fehérjén is különálló „gombolyagok”, ún. domének, formálódhatnak, melyek különböző funkciókat láthatnak el Domén szerkezet A globuláris fehérjék felgombolyodása tovább módosulhat, ha a polpeptidlánc 200 -nál több aminosavat tartalmaz. Egy láncból álló fehérjén is különálló „gombolyagok”, ún. domének, formálódhatnak, melyek különböző funkciókat láthatnak el. Az intenzívebben feltekert tömör régiókat, a doménokat, legtöbbször flexibilis részek kötik össze. A hasonló domének valószínűleg egy ős gén duplikációjából származnak. Egyetlen polipeptid lánc amelyen megkülönböztethetők a béta redőzött lemez és az alfa helix (másodlagos) struktúrák. Két különböző szerkezetű és méretű doménből álló fehérjemolekula.
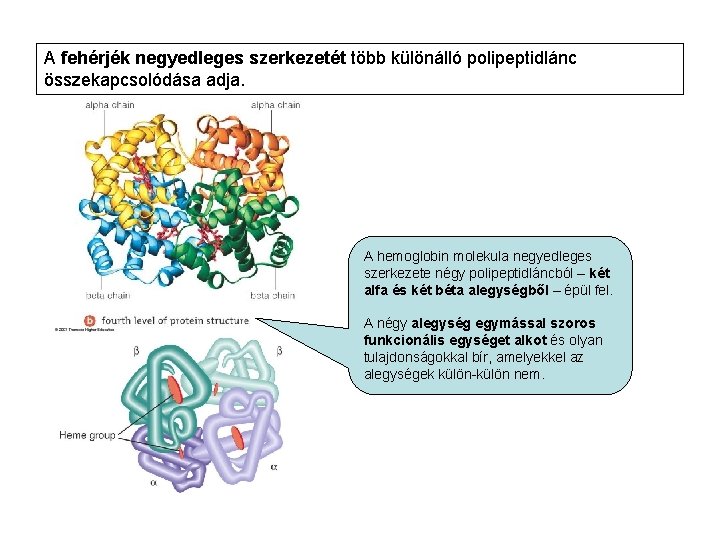
A fehérjék negyedleges szerkezetét több különálló polipeptidlánc összekapcsolódása adja. A hemoglobin molekula negyedleges szerkezete négy polipeptidláncból – két alfa és két béta alegységből – épül fel. A négy alegység egymással szoros funkcionális egységet alkot és olyan tulajdonságokkal bír, amelyekkel az alegységek külön-külön nem.
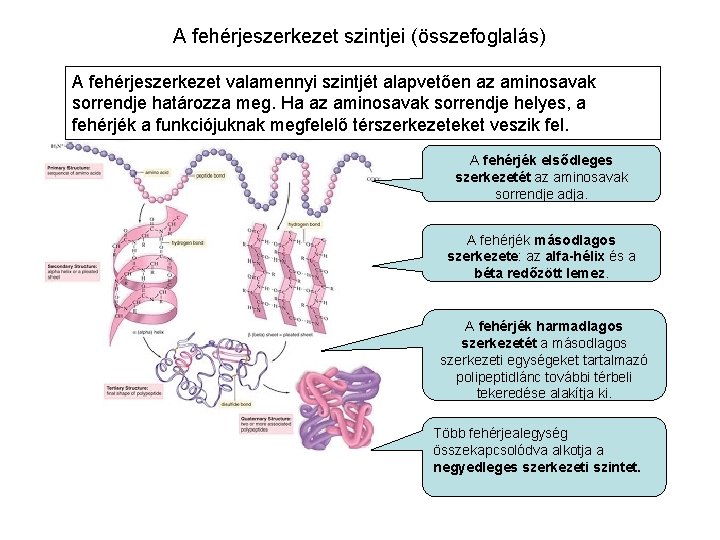
A fehérjeszerkezet szintjei (összefoglalás) A fehérjeszerkezet valamennyi szintjét alapvetően az aminosavak sorrendje határozza meg. Ha az aminosavak sorrendje helyes, a fehérjék a funkciójuknak megfelelő térszerkezeteket veszik fel. A fehérjék elsődleges szerkezetét az aminosavak sorrendje adja. A fehérjék másodlagos szerkezete: az alfa-hélix és a béta redőzött lemez. A fehérjék harmadlagos szerkezetét a másodlagos szerkezeti egységeket tartalmazó polipeptidlánc további térbeli tekeredése alakítja ki. Több fehérjealegység összekapcsolódva alkotja a negyedleges szerkezeti szintet.
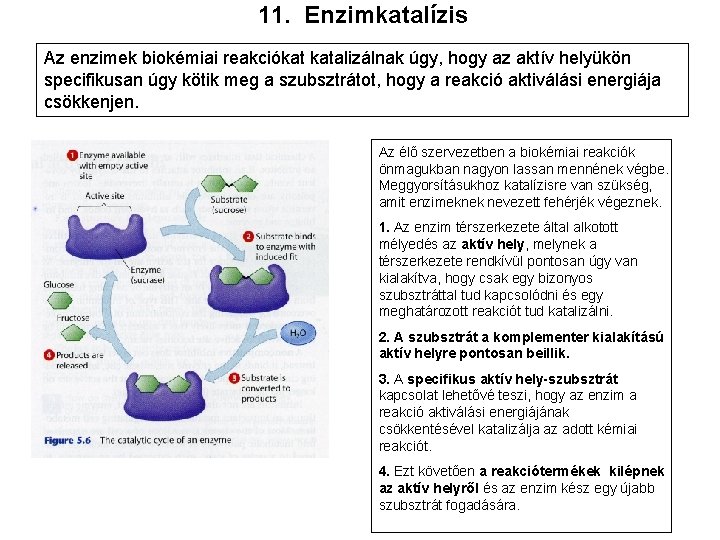
11. Enzimkatalízis Az enzimek biokémiai reakciókat katalizálnak úgy, hogy az aktív helyükön specifikusan úgy kötik meg a szubsztrátot, hogy a reakció aktiválási energiája csökkenjen. Az élő szervezetben a biokémiai reakciók önmagukban nagyon lassan mennének végbe. Meggyorsításukhoz katalízisre van szükség, amit enzimeknek nevezett fehérjék végeznek. 1. Az enzim térszerkezete által alkotott mélyedés az aktív hely, melynek a térszerkezete rendkívül pontosan úgy van kialakítva, hogy csak egy bizonyos szubsztráttal tud kapcsolódni és egy meghatározott reakciót tud katalizálni. 2. A szubsztrát a komplementer kialakítású aktív helyre pontosan beillik. 3. A specifikus aktív hely-szubsztrát kapcsolat lehetővé teszi, hogy az enzim a reakció aktiválási energiájának csökkentésével katalizálja az adott kémiai reakciót. 4. Ezt követően a reakciótermékek kilépnek az aktív helyről és az enzim kész egy újabb szubsztrát fogadására.
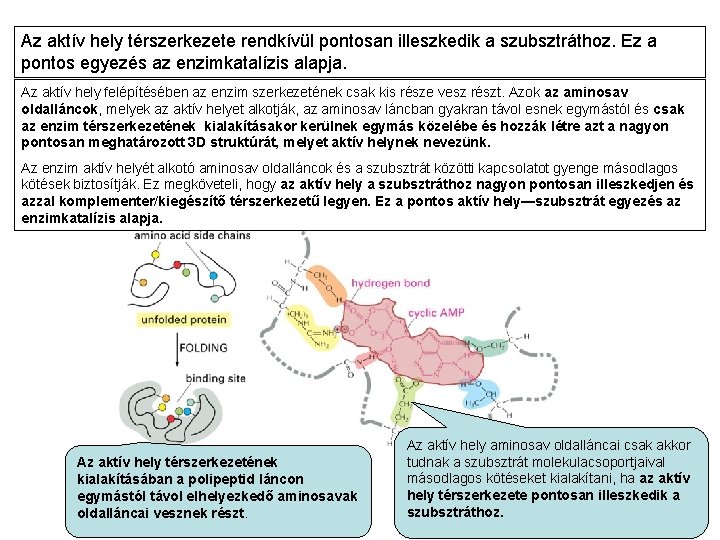
Az aktív hely térszerkezete rendkívül pontosan illeszkedik a szubsztráthoz. Ez a pontos egyezés az enzimkatalízis alapja. Az aktív hely felépítésében az enzim szerkezetének csak kis része vesz részt. Azok az aminosav oldalláncok, melyek az aktív helyet alkotják, az aminosav láncban gyakran távol esnek egymástól és csak az enzim térszerkezetének kialakításakor kerülnek egymás közelébe és hozzák létre azt a nagyon pontosan meghatározott 3 D struktúrát, melyet aktív helynek nevezünk. Az enzim aktív helyét alkotó aminosav oldalláncok és a szubsztrát közötti kapcsolatot gyenge másodlagos kötések biztosítják. Ez megköveteli, hogy az aktív hely a szubsztráthoz nagyon pontosan illeszkedjen és azzal komplementer/kiegészítő térszerkezetű legyen. Ez a pontos aktív hely—szubsztrát egyezés az enzimkatalízis alapja. Az aktív hely térszerkezetének kialakításában a polipeptid láncon egymástól távol elhelyezkedő aminosavak oldalláncai vesznek részt. Az aktív hely aminosav oldalláncai csak akkor tudnak a szubsztrát molekulacsoportjaival másodlagos kötéseket kialakítani, ha az aktív hely térszerkezete pontosan illeszkedik a szubsztráthoz.
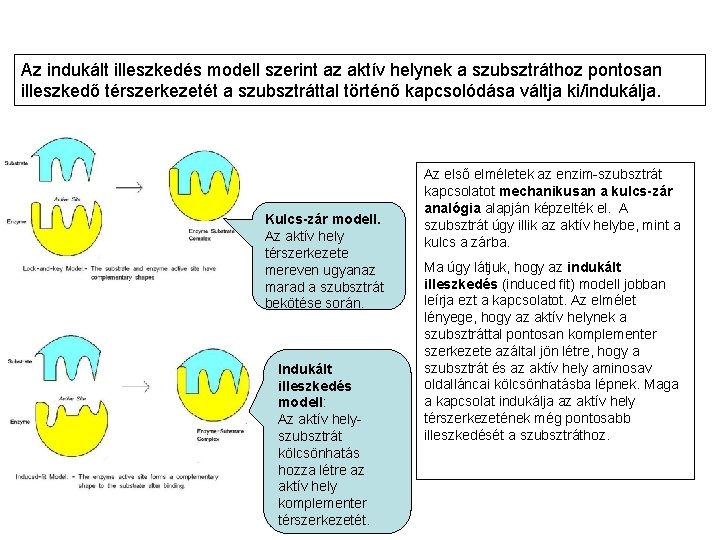
Az indukált illeszkedés modell szerint az aktív helynek a szubsztráthoz pontosan illeszkedő térszerkezetét a szubsztráttal történő kapcsolódása váltja ki/indukálja. Kulcs-zár modell. Az aktív hely térszerkezete mereven ugyanaz marad a szubsztrát bekötése során. Indukált illeszkedés modell: Az aktív helyszubsztrát kölcsönhatás hozza létre az aktív hely komplementer térszerkezetét. Az első elméletek az enzim-szubsztrát kapcsolatot mechanikusan a kulcs-zár analógia alapján képzelték el. A szubsztrát úgy illik az aktív helybe, mint a kulcs a zárba. Ma úgy látjuk, hogy az indukált illeszkedés (induced fit) modell jobban leírja ezt a kapcsolatot. Az elmélet lényege, hogy az aktív helynek a szubsztráttal pontosan komplementer szerkezete azáltal jön létre, hogy a szubsztrát és az aktív hely aminosav oldalláncai kölcsönhatásba lépnek. Maga a kapcsolat indukálja az aktív hely térszerkezetének még pontosabb illeszkedését a szubsztráthoz.
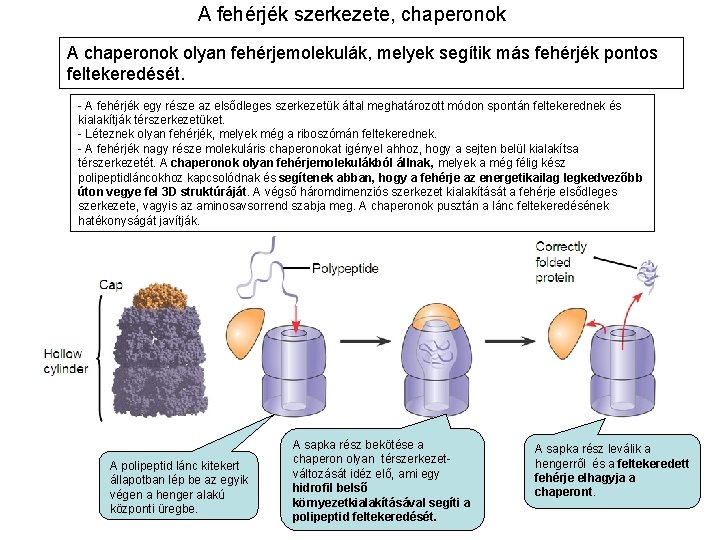
A fehérjék szerkezete, chaperonok A chaperonok olyan fehérjemolekulák, melyek segítik más fehérjék pontos feltekeredését. - A fehérjék egy része az elsődleges szerkezetük által meghatározott módon spontán feltekerednek és kialakítják térszerkezetüket. - Léteznek olyan fehérjék, melyek még a riboszómán feltekerednek. - A fehérjék nagy része molekuláris chaperonokat igényel ahhoz, hogy a sejten belül kialakítsa térszerkezetét. A chaperonok olyan fehérjemolekulákból állnak, melyek a még félig kész polipeptidláncokhoz kapcsolódnak és segítenek abban, hogy a fehérje az energetikailag legkedvezőbb úton vegye fel 3 D struktúráját. A végső háromdimenziós szerkezet kialakítását a fehérje elsődleges szerkezete, vagyis az aminosavsorrend szabja meg. A chaperonok pusztán a lánc feltekeredésének hatékonyságát javítják. A polipeptid lánc kitekert állapotban lép be az egyik végen a henger alakú központi üregbe. A sapka rész bekötése a chaperon olyan térszerkezetváltozását idéz elő, ami egy hidrofil belső környezetkialakításával segíti a polipeptid feltekeredését. A sapka rész leválik a hengerről és a feltekeredett fehérje elhagyja a chaperont.
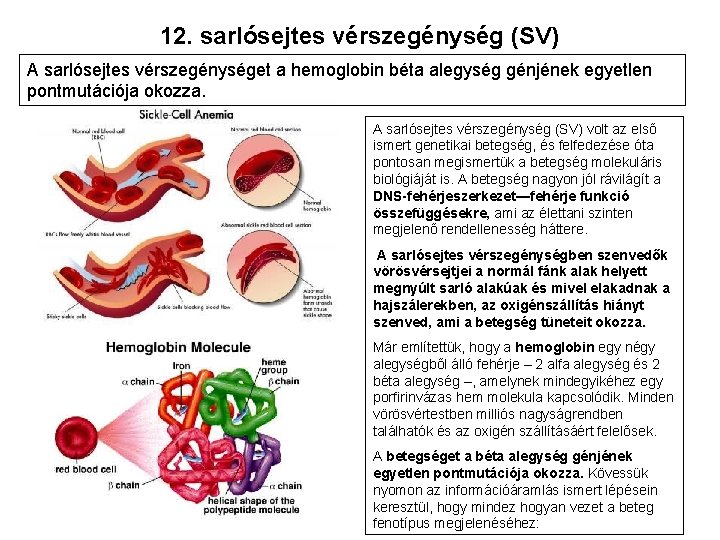
12. sarlósejtes vérszegénység (SV) A sarlósejtes vérszegénységet a hemoglobin béta alegység génjének egyetlen pontmutációja okozza. A sarlósejtes vérszegénység (SV) volt az első ismert genetikai betegség, és felfedezése óta pontosan megismertük a betegség molekuláris biológiáját is. A betegség nagyon jól rávilágít a DNS-fehérjeszerkezet—fehérje funkció összefüggésekre, ami az élettani szinten megjelenő rendellenesség háttere. A sarlósejtes vérszegénységben szenvedők vörösvérsejtjei a normál fánk alak helyett megnyúlt sarló alakúak és mivel elakadnak a hajszálerekben, az oxigénszállítás hiányt szenved, ami a betegség tüneteit okozza. Már említettük, hogy a hemoglobin egy négy alegységből álló fehérje – 2 alfa alegység és 2 béta alegység –, amelynek mindegyikéhez egy porfirinvázas hem molekula kapcsolódik. Minden vörösvértestben milliós nagyságrendben találhatók és az oxigén szállításáért felelősek. A betegséget a béta alegység génjének egyetlen pontmutációja okozza. Kövessük nyomon az információáramlás ismert lépésein keresztül, hogy mindez hogyan vezet a beteg fenotípus megjelenéséhez:
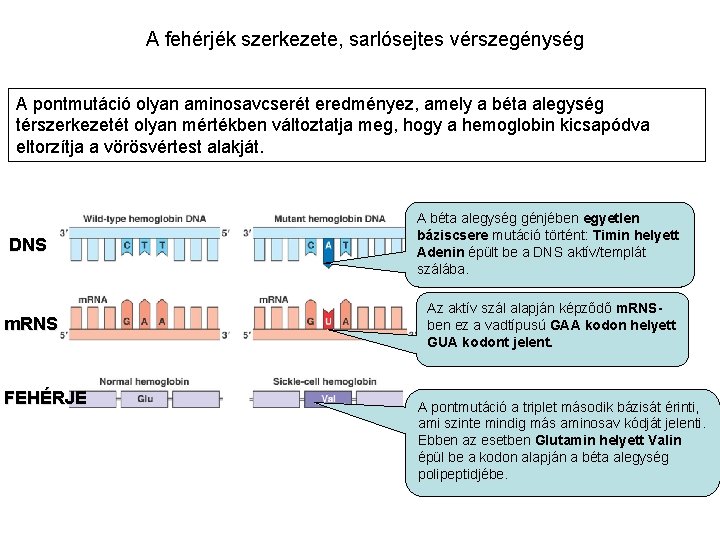
A fehérjék szerkezete, sarlósejtes vérszegénység A pontmutáció olyan aminosavcserét eredményez, amely a béta alegység térszerkezetét olyan mértékben változtatja meg, hogy a hemoglobin kicsapódva eltorzítja a vörösvértest alakját. DNS A béta alegység génjében egyetlen báziscsere mutáció történt: Timin helyett Adenin épült be a DNS aktív/templát szálába. m. RNS Az aktív szál alapján képződő m. RNSben ez a vadtípusú GAA kodon helyett GUA kodont jelent. FEHÉRJE A pontmutáció a triplet második bázisát érinti, ami szinte mindig más aminosav kódját jelenti. Ebben az esetben Glutamin helyett Valin épül be a kodon alapján a béta alegység polipeptidjébe.
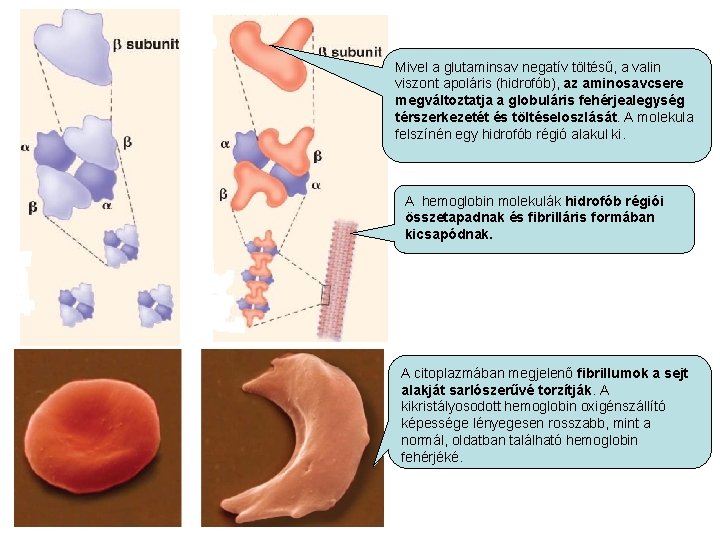
Mivel a glutaminsav negatív töltésű, a valin viszont apoláris (hidrofób), az aminosavcsere megváltoztatja a globuláris fehérjealegység térszerkezetét és töltéseloszlását. A molekula felszínén egy hidrofób régió alakul ki. A hemoglobin molekulák hidrofób régiói összetapadnak és fibrilláris formában kicsapódnak. A citoplazmában megjelenő fibrillumok a sejt alakját sarlószerűvé torzítják. A kikristályosodott hemoglobin oxigénszállító képessége lényegesen rosszabb, mint a normál, oldatban található hemoglobin fehérjéké.
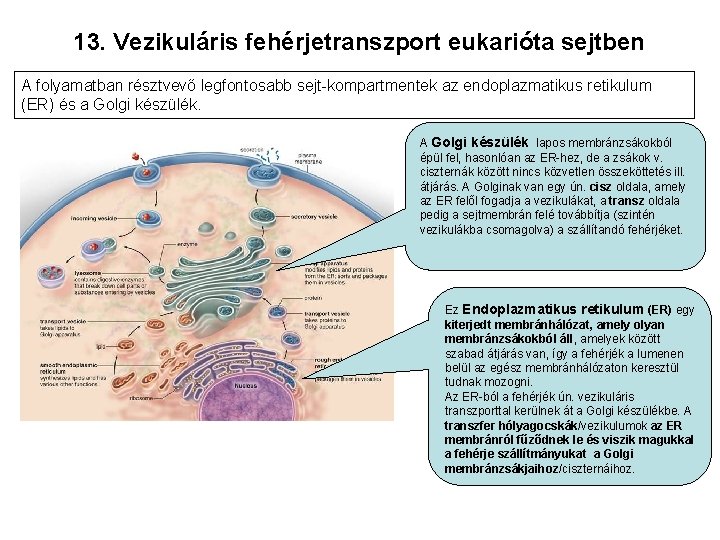
13. Vezikuláris fehérjetranszport eukarióta sejtben A folyamatban résztvevő legfontosabb sejt-kompartmentek az endoplazmatikus retikulum (ER) és a Golgi készülék. A Golgi készülék lapos membránzsákokból épül fel, hasonlóan az ER-hez, de a zsákok v. ciszternák között nincs közvetlen összeköttetés ill. átjárás. A Golginak van egy ún. cisz oldala, amely az ER felől fogadja a vezikulákat, a transz oldala pedig a sejtmembrán felé továbbítja (szintén vezikulákba csomagolva) a szállítandó fehérjéket. Ez Endoplazmatikus retikulum (ER) egy kiterjedt membránhálózat, amely olyan membránzsákokból áll, amelyek között szabad átjárás van, így a fehérjék a lumenen belül az egész membránhálózaton keresztül tudnak mozogni. Az ER-ból a fehérjék ún. vezikuláris transzporttal kerülnek át a Golgi készülékbe. A transzfer hólyagocskák/vezikulumok az ER membránról fűződnek le és viszik magukkal a fehérje szállítmányukat a Golgi membránzsákjaihoz/ciszternáihoz.
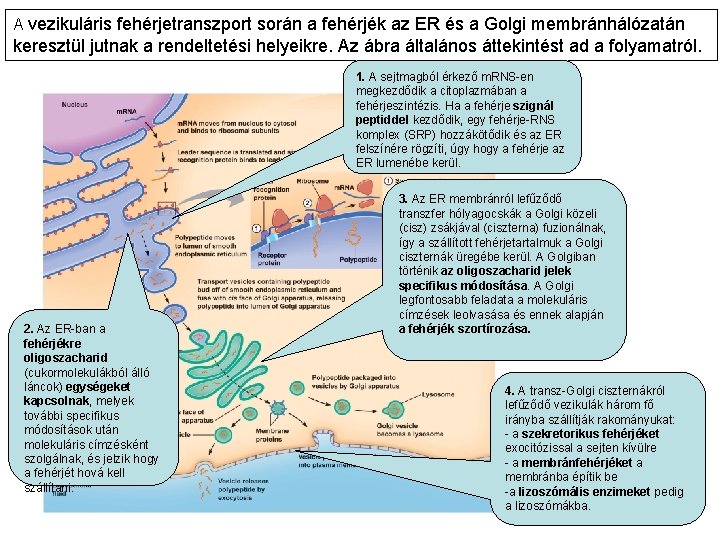
A vezikuláris fehérjetranszport során a fehérjék az ER és a Golgi membránhálózatán keresztül jutnak a rendeltetési helyeikre. Az ábra általános áttekintést ad a folyamatról. 1. A sejtmagból érkező m. RNS-en megkezdődik a citoplazmában a fehérjeszintézis. Ha a fehérje szignál peptiddel kezdődik, egy fehérje-RNS komplex (SRP) hozzákötődik és az ER felszínére rögzíti, úgy hogy a fehérje az ER lumenébe kerül. 2. Az ER-ban a fehérjékre oligoszacharid (cukormolekulákból álló láncok) egységeket kapcsolnak, melyek további specifikus módosítások után molekuláris címzésként szolgálnak, és jelzik hogy a fehérjét hová kell szállítani. 3. Az ER membránról lefűződő transzfer hólyagocskák a Golgi közeli (cisz) zsákjával (ciszterna) fuzionálnak, így a szállított fehérjetartalmuk a Golgi ciszternák üregébe kerül. A Golgiban történik az oligoszacharid jelek specifikus módosítása. A Golgi legfontosabb feladata a molekuláris címzések leolvasása és ennek alapján a fehérjék szortírozása. 4. A transz-Golgi ciszternákról lefűződő vezikulák három fő irányba szállítják rakományukat: - a szekretorikus fehérjéket exocitózissal a sejten kívülre - a membránfehérjéket a membránba építik be -a lizoszómális enzimeket pedig a lizoszómákba.
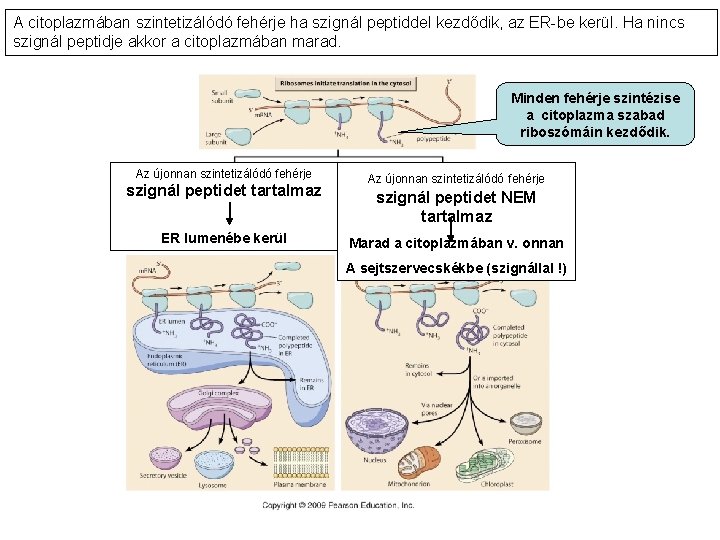
A citoplazmában szintetizálódó fehérje ha szignál peptiddel kezdődik, az ER-be kerül. Ha nincs szignál peptidje akkor a citoplazmában marad. Minden fehérje szintézise a citoplazma szabad riboszómáin kezdődik. Az újonnan szintetizálódó fehérje szignál peptidet tartalmaz ER lumenébe kerül Az újonnan szintetizálódó fehérje szignál peptidet NEM tartalmaz Marad a citoplazmában v. onnan A sejtszervecskékbe (szignállal !)
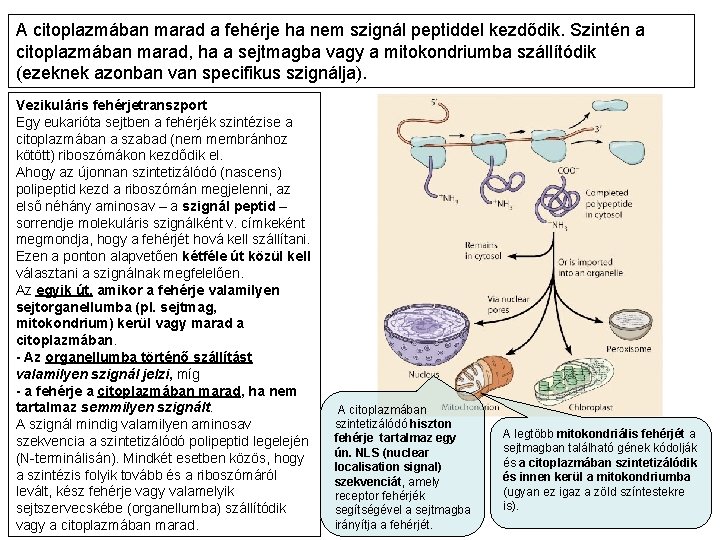
A citoplazmában marad a fehérje ha nem szignál peptiddel kezdődik. Szintén a citoplazmában marad, ha a sejtmagba vagy a mitokondriumba szállítódik (ezeknek azonban van specifikus szignálja). Vezikuláris fehérjetranszport Egy eukarióta sejtben a fehérjék szintézise a citoplazmában a szabad (nem membránhoz kötött) riboszómákon kezdődik el. Ahogy az újonnan szintetizálódó (nascens) polipeptid kezd a riboszómán megjelenni, az első néhány aminosav – a szignál peptid – sorrendje molekuláris szignálként v. címkeként megmondja, hogy a fehérjét hová kell szállítani. Ezen a ponton alapvetően kétféle út közül kell választani a szignálnak megfelelően. Az egyik út, amikor a fehérje valamilyen sejtorganellumba (pl. sejtmag, mitokondrium) kerül vagy marad a citoplazmában. - Az organellumba történő szállítást valamilyen szignál jelzi, míg - a fehérje a citoplazmában marad, ha nem tartalmaz semmilyen szignált. A szignál mindig valamilyen aminosav szekvencia a szintetizálódó polipeptid legelején (N-terminálisán). Mindkét esetben közös, hogy a szintézis folyik tovább és a riboszómáról levált, kész fehérje vagy valamelyik sejtszervecskébe (organellumba) szállítódik vagy a citoplazmában marad. A citoplazmában szintetizálódó hiszton fehérje tartalmaz egy ún. NLS (nuclear localisation signal) szekvenciát, amely receptor fehérjék segítségével a sejtmagba irányítja a fehérjét. A legtöbb mitokondriális fehérjét a sejtmagban található gének kódolják és a citoplazmában szintetizálódik és innen kerül a mitokondriumba (ugyan ez igaz a zöld színtestekre is).
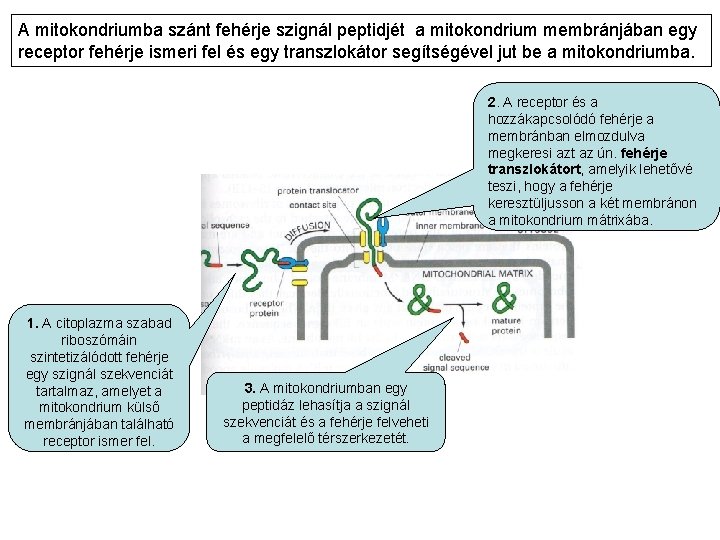
A mitokondriumba szánt fehérje szignál peptidjét a mitokondrium membránjában egy receptor fehérje ismeri fel és egy transzlokátor segítségével jut be a mitokondriumba. 2. A receptor és a hozzákapcsolódó fehérje a membránban elmozdulva megkeresi azt az ún. fehérje transzlokátort, amelyik lehetővé teszi, hogy a fehérje keresztüljusson a két membránon a mitokondrium mátrixába. 1. A citoplazma szabad riboszómáin szintetizálódott fehérje egy szignál szekvenciát tartalmaz, amelyet a mitokondrium külső membránjában található receptor ismer fel. 3. A mitokondriumban egy peptidáz lehasítja a szignál szekvenciát és a fehérje felveheti a megfelelő térszerkezetét.
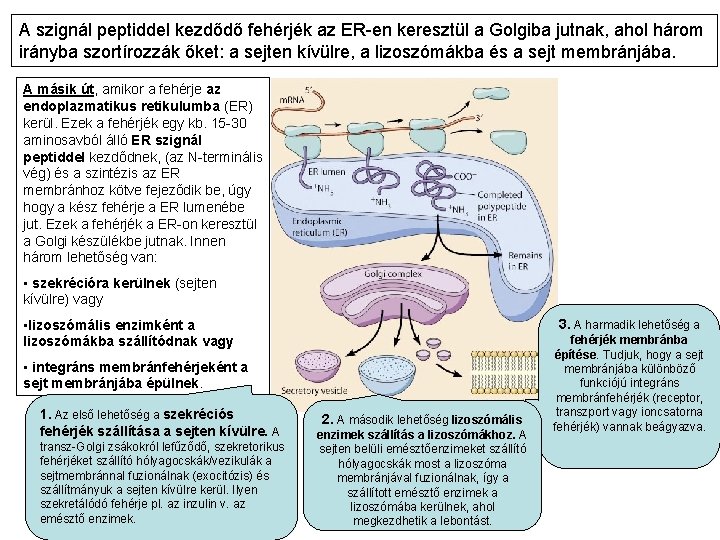
A szignál peptiddel kezdődő fehérjék az ER-en keresztül a Golgiba jutnak, ahol három irányba szortírozzák őket: a sejten kívülre, a lizoszómákba és a sejt membránjába. A másik út, amikor a fehérje az endoplazmatikus retikulumba (ER) kerül. Ezek a fehérjék egy kb. 15 -30 aminosavból álló ER szignál peptiddel kezdődnek, (az N-terminális vég) és a szintézis az ER membránhoz kötve fejeződik be, úgy hogy a kész fehérje a ER lumenébe jut. Ezek a fehérjék a ER-on keresztül a Golgi készülékbe jutnak. Innen három lehetőség van: • szekrécióra kerülnek (sejten kívülre) vagy • lizoszómális enzimként a lizoszómákba szállítódnak vagy 3. A harmadik lehetőség a • integráns membránfehérjeként a sejt membránjába épülnek. 1. Az első lehetőség a szekréciós fehérjék szállítása a sejten kívülre. A transz-Golgi zsákokról lefűződő, szekretorikus fehérjéket szállító hólyagocskák/vezikulák a sejtmembránnal fuzionálnak (exocitózis) és szállítmányuk a sejten kívülre kerül. Ilyen szekretálódó fehérje pl. az inzulin v. az emésztő enzimek. 2. A második lehetőség lizoszómális enzimek szállítás a lizoszómákhoz. A sejten belüli emésztőenzimeket szállító hólyagocskák most a lizoszóma membránjával fuzionálnak, így a szállított emésztő enzimek a lizoszómába kerülnek, ahol megkezdhetik a lebontást. fehérjék membránba építése. Tudjuk, hogy a sejt membránjába különböző funkciójú integráns membránfehérjék (receptor, transzport vagy ioncsatorna fehérjék) vannak beágyazva.
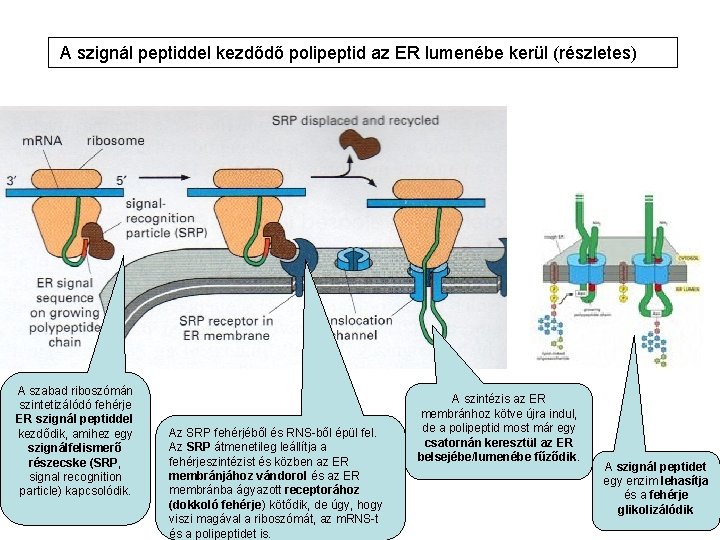
A szignál peptiddel kezdődő polipeptid az ER lumenébe kerül (részletes) A szabad riboszómán szintetizálódó fehérje ER szignál peptiddel kezdődik, amihez egy szignálfelismerő részecske (SRP, signal recognition particle) kapcsolódik. Az SRP fehérjéből és RNS-ből épül fel. Az SRP átmenetileg leállítja a fehérjeszintézist és közben az ER membránjához vándorol és az ER membránba ágyazott receptorához (dokkoló fehérje) kötődik, de úgy, hogy viszi magával a riboszómát, az m. RNS-t és a polipeptidet is. A szintézis az ER membránhoz kötve újra indul, de a polipeptid most már egy csatornán keresztül az ER belsejébe/lumenébe fűződik. A szignál peptidet egy enzim lehasítja és a fehérje glikolizálódik
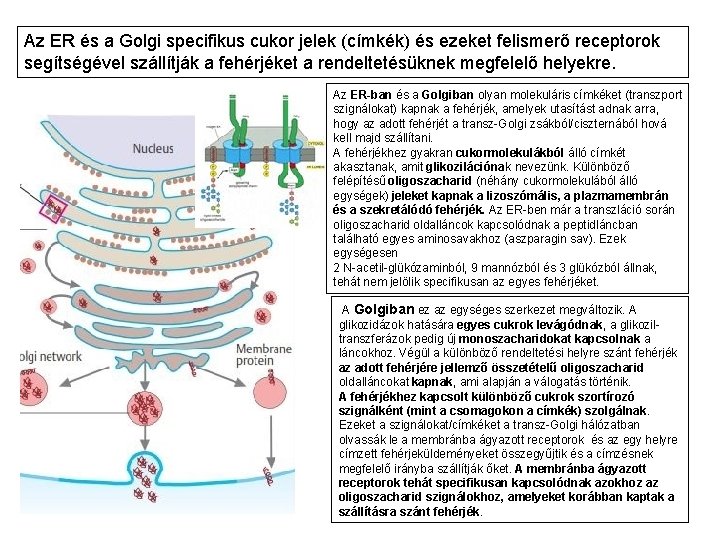
Az ER és a Golgi specifikus cukor jelek (címkék) és ezeket felismerő receptorok segítségével szállítják a fehérjéket a rendeltetésüknek megfelelő helyekre. Az ER-ban és a Golgiban olyan molekuláris címkéket (transzport szignálokat) kapnak a fehérjék, amelyek utasítást adnak arra, hogy az adott fehérjét a transz-Golgi zsákból/ciszternából hová kell majd szállítani. A fehérjékhez gyakran cukormolekulákból álló címkét akasztanak, amit glikozilációnak nevezünk. Különböző felépítésű oligoszacharid (néhány cukormolekulából álló egységek) jeleket kapnak a lizoszómális, a plazmamembrán és a szekretálódó fehérjék. Az ER-ben már a transzláció során oligoszacharid oldalláncok kapcsolódnak a peptidláncban található egyes aminosavakhoz (aszparagin sav). Ezek egységesen 2 N-acetil-glükózaminból, 9 mannózból és 3 glükózból állnak, tehát nem jelölik specifikusan az egyes fehérjéket. A Golgiban ez az egységes szerkezet megváltozik. A glikozidázok hatására egyes cukrok levágódnak, a glikoziltranszferázok pedig új monoszacharidokat kapcsolnak a láncokhoz. Végül a különböző rendeltetési helyre szánt fehérjék az adott fehérjére jellemző összetételű oligoszacharid oldalláncokat kapnak, ami alapján a válogatás történik. A fehérjékhez kapcsolt különböző cukrok szortírozó szignálként (mint a csomagokon a címkék) szolgálnak. Ezeket a szignálokat/címkéket a transz-Golgi hálózatban olvassák le a membránba ágyazott receptorok és az egy helyre címzett fehérjeküldeményeket összegyűjtik és a címzésnek megfelelő irányba szállítják őket. A membránba ágyazott receptorok tehát specifikusan kapcsolódnak azokhoz az oligoszacharid szignálokhoz, amelyeket korábban kaptak a szállításra szánt fehérjék.
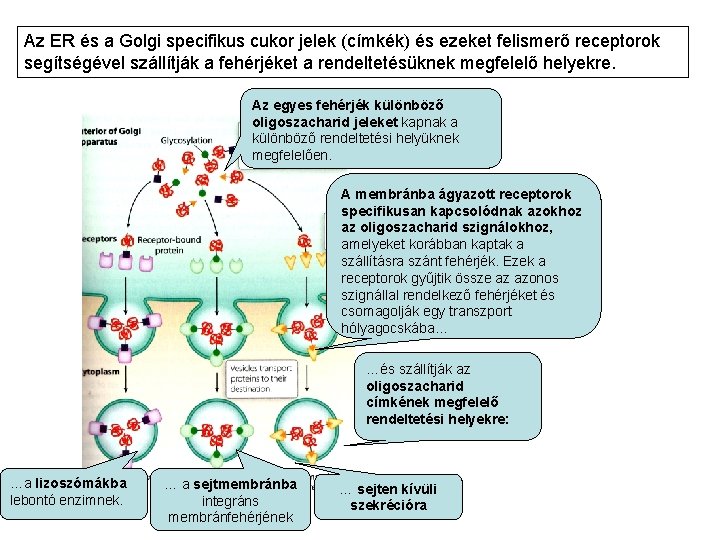
Az ER és a Golgi specifikus cukor jelek (címkék) és ezeket felismerő receptorok segítségével szállítják a fehérjéket a rendeltetésüknek megfelelő helyekre. Az egyes fehérjék különböző oligoszacharid jeleket kapnak a különböző rendeltetési helyüknek megfelelően. A membránba ágyazott receptorok specifikusan kapcsolódnak azokhoz az oligoszacharid szignálokhoz, amelyeket korábban kaptak a szállításra szánt fehérjék. Ezek a receptorok gyűjtik össze az azonos szignállal rendelkező fehérjéket és csomagolják egy transzport hólyagocskába… …és szállítják az oligoszacharid címkének megfelelő rendeltetési helyekre: …a lizoszómákba lebontó enzimnek. … a sejtmembránba integráns membránfehérjének … sejten kívüli szekrécióra
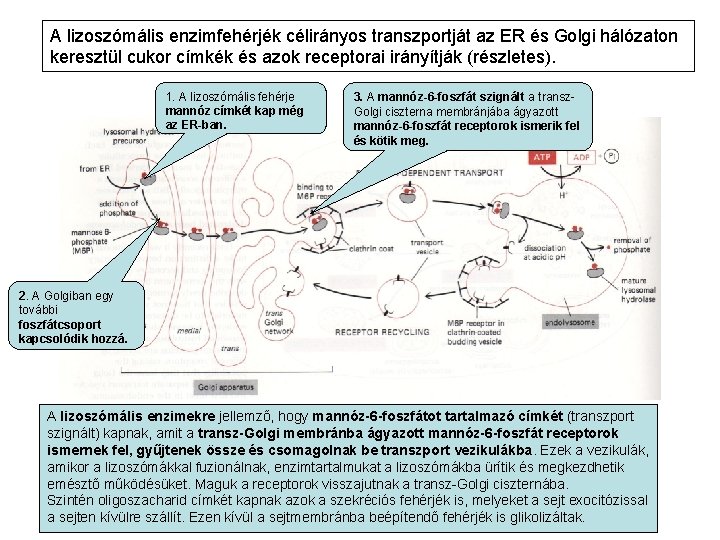
A lizoszómális enzimfehérjék célirányos transzportját az ER és Golgi hálózaton keresztül cukor címkék és azok receptorai irányítják (részletes). 1. A lizoszómális fehérje mannóz címkét kap még az ER-ban. 3. A mannóz-6 -foszfát szignált a transz. Golgi ciszterna membránjába ágyazott mannóz-6 -foszfát receptorok ismerik fel és kötik meg. 2. A Golgiban egy további foszfátcsoport kapcsolódik hozzá. A lizoszómális enzimekre jellemző, hogy mannóz-6 -foszfátot tartalmazó címkét (transzport szignált) kapnak, amit a transz-Golgi membránba ágyazott mannóz-6 -foszfát receptorok ismernek fel, gyűjtenek össze és csomagolnak be transzport vezikulákba. Ezek a vezikulák, amikor a lizoszómákkal fuzionálnak, enzimtartalmukat a lizoszómákba ürítik és megkezdhetik emésztő működésüket. Maguk a receptorok visszajutnak a transz-Golgi ciszternába. Szintén oligoszacharid címkét kapnak azok a szekréciós fehérjék is, melyeket a sejt exocitózissal a sejten kívülre szállít. Ezen kívül a sejtmembránba beépítendő fehérjék is glikolizáltak.
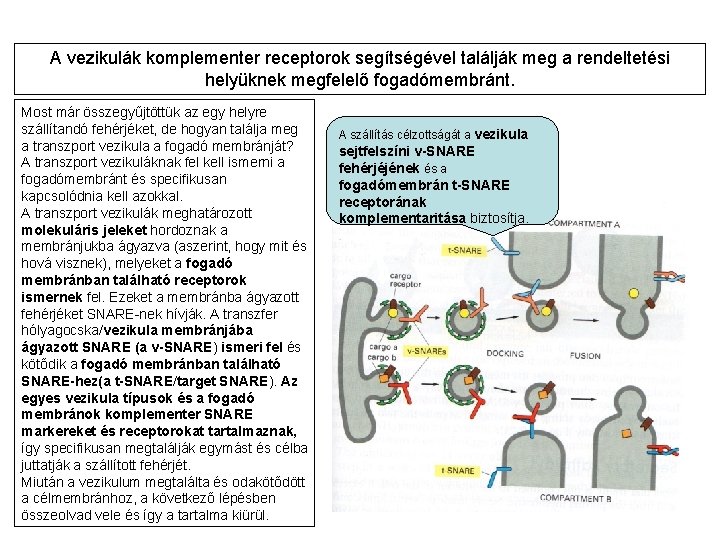
A vezikulák komplementer receptorok segítségével találják meg a rendeltetési helyüknek megfelelő fogadómembránt. Most már összegyűjtöttük az egy helyre szállítandó fehérjéket, de hogyan találja meg a transzport vezikula a fogadó membránját? A transzport vezikuláknak fel kell ismerni a fogadómembránt és specifikusan kapcsolódnia kell azokkal. A transzport vezikulák meghatározott molekuláris jeleket hordoznak a membránjukba ágyazva (aszerint, hogy mit és hová visznek), melyeket a fogadó membránban található receptorok ismernek fel. Ezeket a membránba ágyazott fehérjéket SNARE-nek hívják. A transzfer hólyagocska/vezikula membránjába ágyazott SNARE (a v-SNARE) ismeri fel és kötődik a fogadó membránban található SNARE-hez(a t-SNARE/target SNARE). Az egyes vezikula típusok és a fogadó membránok komplementer SNARE markereket és receptorokat tartalmaznak, így specifikusan megtalálják egymást és célba juttatják a szállított fehérjét. Miután a vezikulum megtalálta és odakötődött a célmembránhoz, a következő lépésben összeolvad vele és így a tartalma kiürül. A szállítás célzottságát a vezikula sejtfelszíni v-SNARE fehérjéjének és a fogadómembrán t-SNARE receptorának komplementaritása biztosítja.
- Slides: 44