IUPAC Polyaddition polycondensation Mise en oeuvre de monomres







![Réaction stœchiométrique avec catalyseur IUPAC Polyestérification, catalyse H+ Disparition alcool : [alcool] = (acide] Réaction stœchiométrique avec catalyseur IUPAC Polyestérification, catalyse H+ Disparition alcool : [alcool] = (acide]](https://slidetodoc.com/presentation_image_h/876115d254e58440c61b97581b44ca45/image-31.jpg)













- Slides: 63

IUPAC Polyaddition - polycondensation Mise en oeuvre de monomères fonctionnels (alcool, acide, amine, isocyanate …) C'est une chimie de fonctions : la conversion s'exprime en fonction du nombre de fonctions ayant réagies en général, les polymères portent le nom des fonctions créées (polyester …) Quelques exemples Acide + alcool Acide + amine Ester 1 + alcool 1 → → → Isocyanate + alcool → Isocyanate + amine → Ester + eau Amide + eau Ester 2 + alcool 2 (estérification) polyester (amidification) polyamide (transestérification) polyester uréthane urée polyuréthane polyurée La formation de la chaîne nécessite des monomères au moins difonctionnels diol + diacide, diamine + diacide, amino acide … Chimie Macromoléculaire/ Polycondensation - Polyaddition 1

IUPAC Polyaddition - polycondensation Mi + M j M i+j (+ L) Il y a toujours deux extrémités réactives en fin de chaîne Chimie Macromoléculaire/ Polycondensation - Polyaddition 2

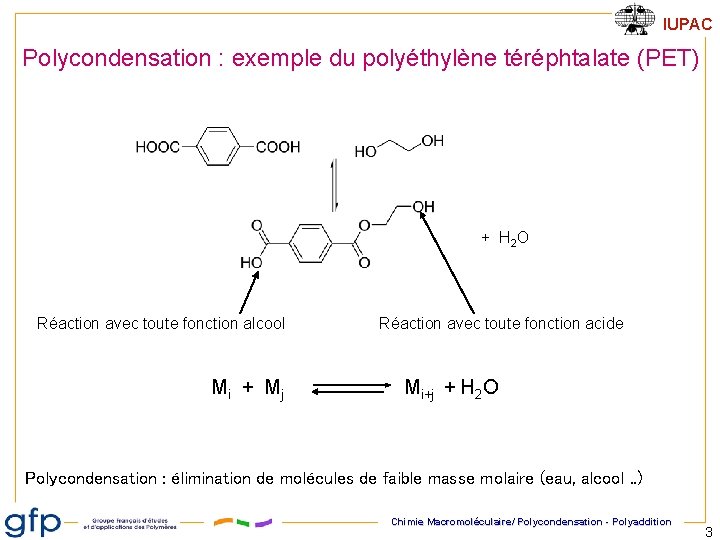
IUPAC Polycondensation : exemple du polyéthylène téréphtalate (PET) + H 2 O Réaction avec toute fonction alcool Mi + Mj Réaction avec toute fonction acide Mi+j + H 2 O Polycondensation : élimination de molécules de faible masse molaire (eau, alcool. . ) Chimie Macromoléculaire/ Polycondensation - Polyaddition 3

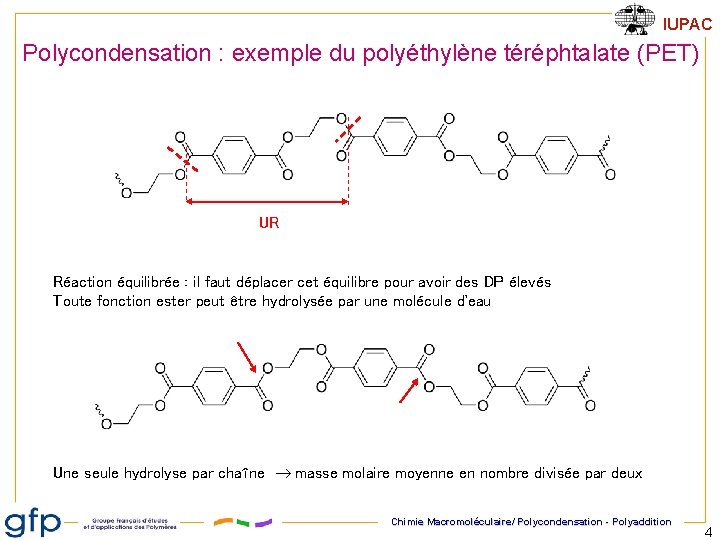
IUPAC Polycondensation : exemple du polyéthylène téréphtalate (PET) UR Réaction équilibrée : il faut déplacer cet équilibre pour avoir des DP élevés Toute fonction ester peut être hydrolysée par une molécule d'eau Une seule hydrolyse par chaîne masse molaire moyenne en nombre divisée par deux Chimie Macromoléculaire/ Polycondensation - Polyaddition 4

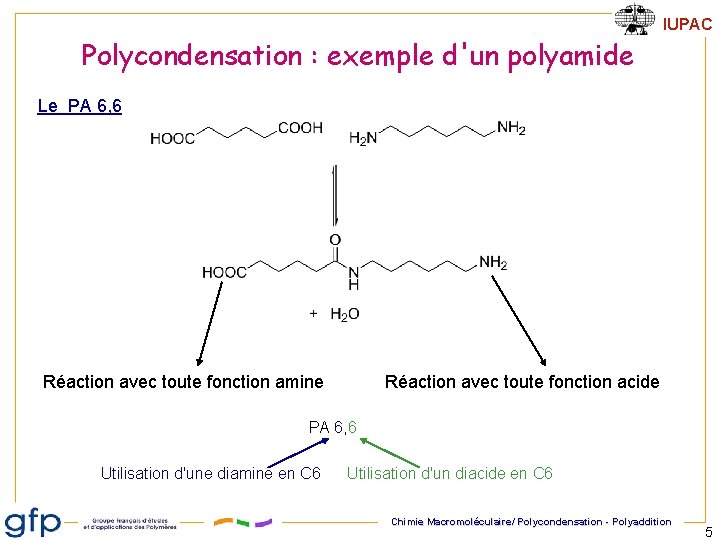
IUPAC Polycondensation : exemple d'un polyamide Le PA 6, 6 Réaction avec toute fonction amine Réaction avec toute fonction acide PA 6, 6 Utilisation d'une diamine en C 6 Utilisation d'un diacide en C 6 Chimie Macromoléculaire/ Polycondensation - Polyaddition 5

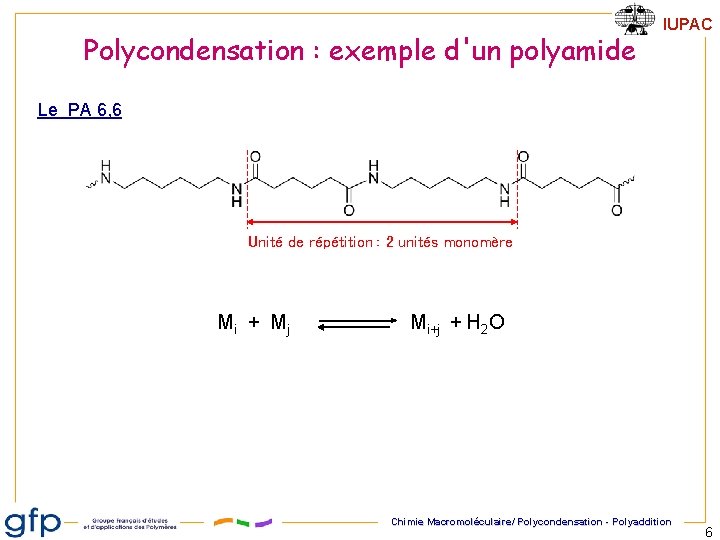
Polycondensation : exemple d'un polyamide IUPAC Le PA 6, 6 Unité de répétition : 2 unités monomère Mi + Mj Mi+j + H 2 O Chimie Macromoléculaire/ Polycondensation - Polyaddition 6

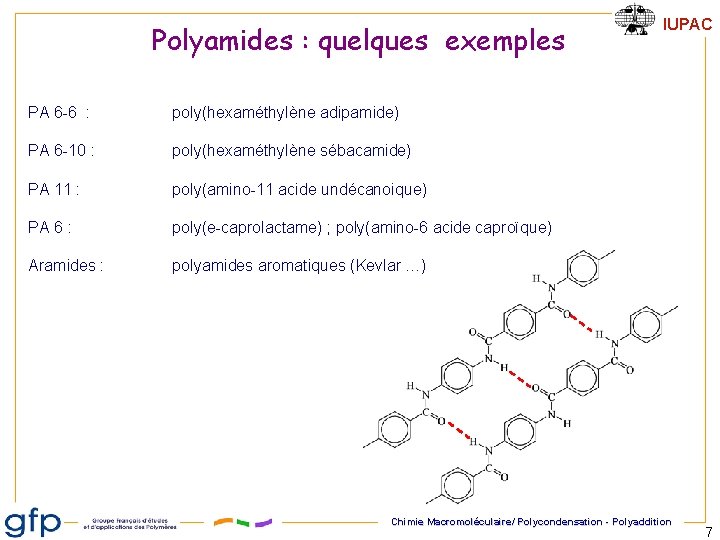
Polyamides : quelques exemples PA 6 -6 : poly(hexaméthylène adipamide) PA 6 -10 : poly(hexaméthylène sébacamide) PA 11 : poly(amino-11 acide undécanoique) PA 6 : poly(e-caprolactame) ; poly(amino-6 acide caproïque) Aramides : polyamides aromatiques (Kevlar …) IUPAC Chimie Macromoléculaire/ Polycondensation - Polyaddition 7

IUPAC Utilisation d'un chlorure d'acide Application : PA par polymérisation interfaciale Expérience Verser dans un bécher, 10 ml d'hexaméthylène diamine en solution dans l'eau dans un bécher. Ajouter 10 ml de chlorure de sébacyle en solution dans de l'heptane. On observe la formation de 2 phases (l'eau et l'heptane ne sont pas miscibles). A l'interface des 2 solutions, un film s'est formé. On peut étirer ce film avec un crochet pour obtenir un fil de PA 6 -10. http: //www. masc. ulg. ac. be/fiches/FR/polymeres. pdf Chimie Macromoléculaire/ Polycondensation - Polyaddition 8

polycondensation interfaciale en milieu dispersé IUPAC Dispersion d'un monomère organosoluble dans une phase aqueuse (avec un tensioactif) contenant le second monomère hydrosoluble hexaméthylène diamine en solution aqueuse Addition de chlorure d'adipoyle goutte à goutte. Formation de nanocapsules polyamides en dispersion dans l'eau Ce principe de polymérisation interfaciale en milieu dispersé est aussi utilisé avec les polyuréthanes. Chimie Macromoléculaire/ Polycondensation - Polyaddition 9

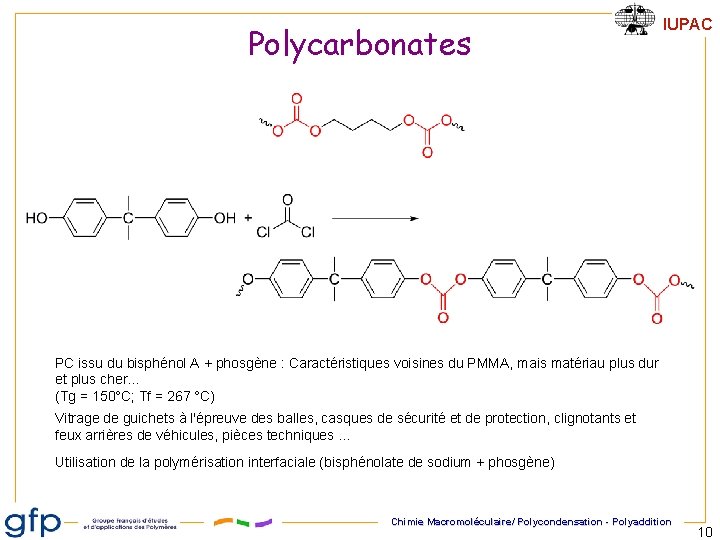
Polycarbonates IUPAC PC issu du bisphénol A + phosgène : Caractéristiques voisines du PMMA, mais matériau plus dur et plus cher… (Tg = 150°C; Tf = 267 °C) Vitrage de guichets à l'épreuve des balles, casques de sécurité et de protection, clignotants et feux arrières de véhicules, pièces techniques. . . Utilisation de la polymérisation interfaciale (bisphénolate de sodium + phosgène) Chimie Macromoléculaire/ Polycondensation - Polyaddition 10

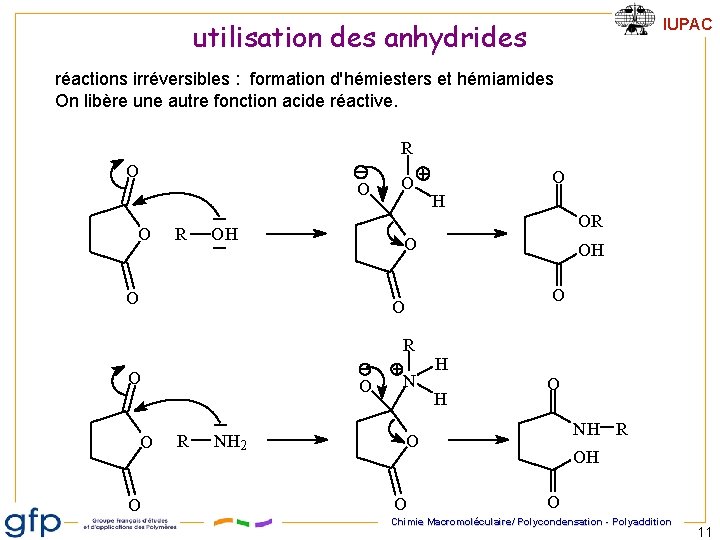
IUPAC utilisation des anhydrides réactions irréversibles : formation d'hémiesters et hémiamides On libère une autre fonction acide réactive. R O O O R O O H OR OH O O R NH 2 N H H O NH R O O OH O Chimie Macromoléculaire/ Polycondensation - Polyaddition 11

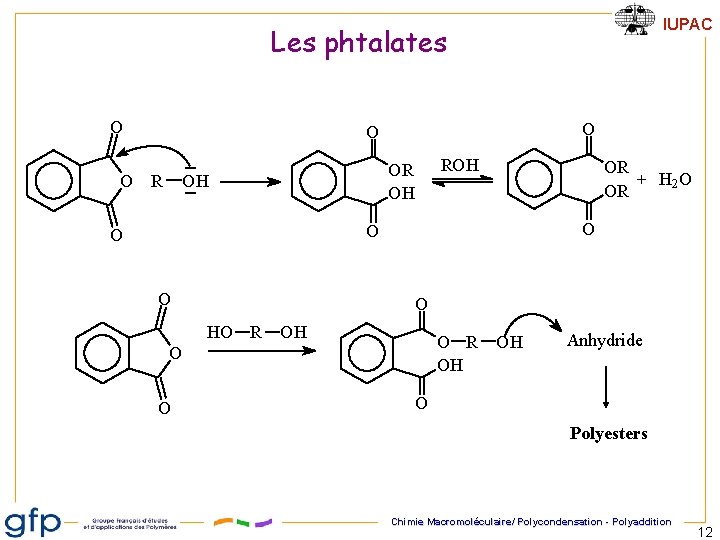
IUPAC Les phtalates O O R ROH OR OH OH OR + H 2 O OR O O O HO R OH O O OH Anhydride O Polyesters Chimie Macromoléculaire/ Polycondensation - Polyaddition 12

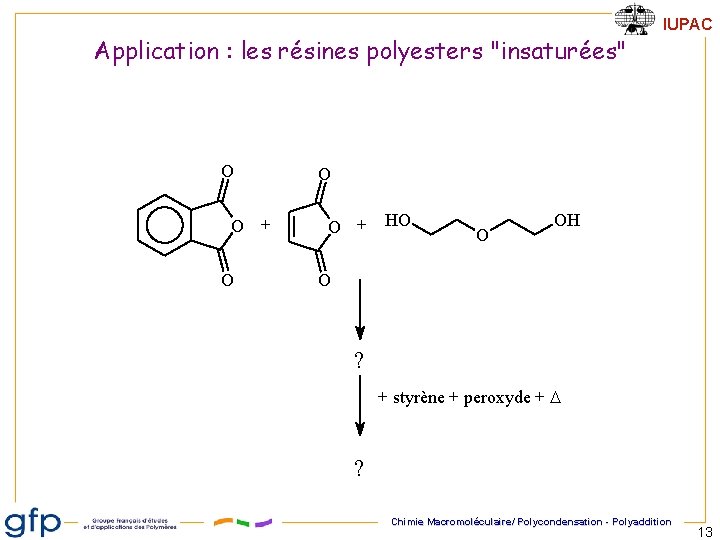
Application : les résines polyesters "insaturées" O O + O IUPAC O O + HO O OH O ? + styrène + peroxyde + ? Chimie Macromoléculaire/ Polycondensation - Polyaddition 13

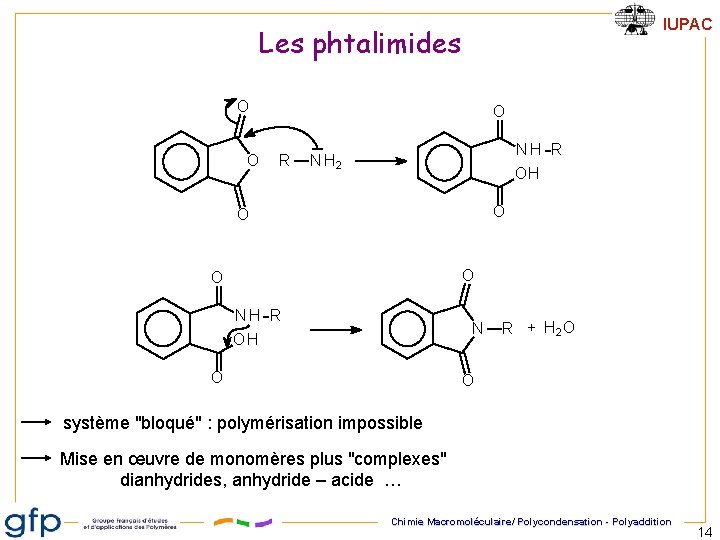
IUPAC Les phtalimides O O O R NH R N H 2 OH O O NH R OH N O R + H 2 O O système "bloqué" : polymérisation impossible Mise en œuvre de monomères plus "complexes" dianhydrides, anhydride – acide … Chimie Macromoléculaire/ Polycondensation - Polyaddition 14

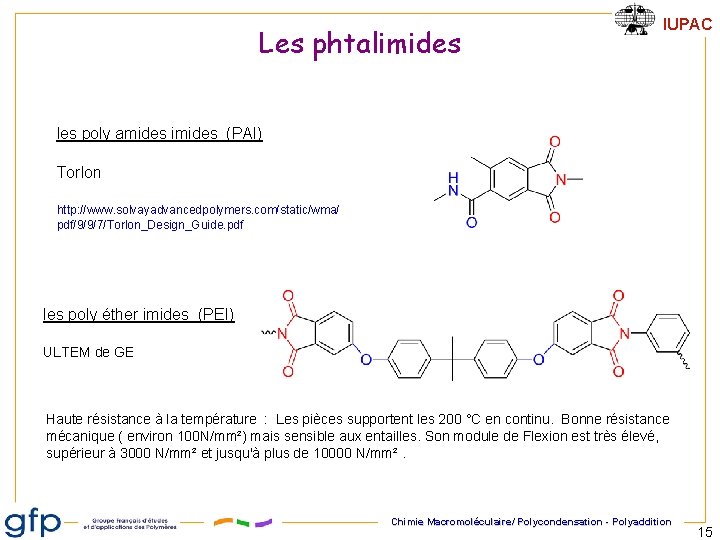
Les phtalimides IUPAC les poly amides imides (PAI) Torlon http: //www. solvayadvancedpolymers. com/static/wma/ pdf/9/9/7/Torlon_Design_Guide. pdf les poly éther imides (PEI) ULTEM de GE Haute résistance à la température : Les pièces supportent les 200 °C en continu. Bonne résistance mécanique ( environ 100 N/mm²) mais sensible aux entailles. Son module de Flexion est très élevé, supérieur à 3000 N/mm² et jusqu'à plus de 10000 N/mm². Chimie Macromoléculaire/ Polycondensation - Polyaddition 15

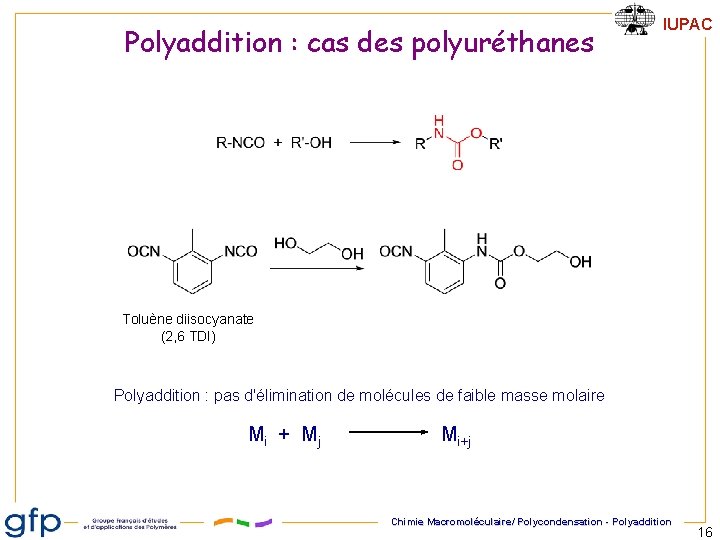
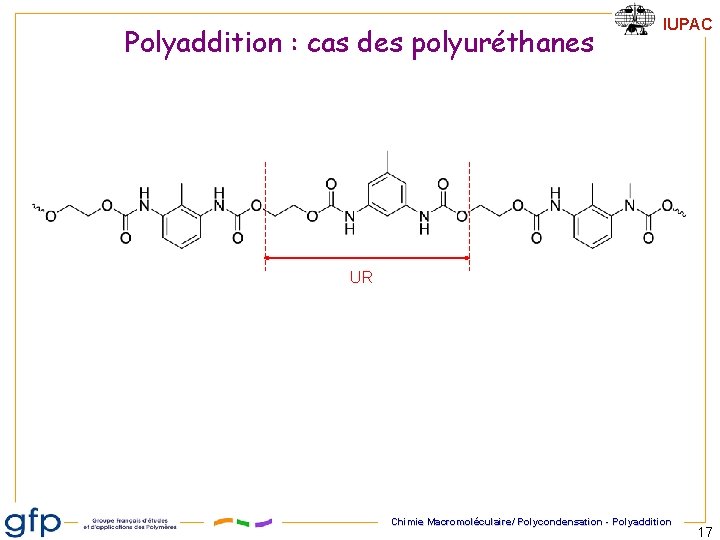
Polyaddition : cas des polyuréthanes IUPAC Toluène diisocyanate (2, 6 TDI) Polyaddition : pas d'élimination de molécules de faible masse molaire Mi + Mj Mi+j Chimie Macromoléculaire/ Polycondensation - Polyaddition 16

Polyaddition : cas des polyuréthanes IUPAC UR Chimie Macromoléculaire/ Polycondensation - Polyaddition 17

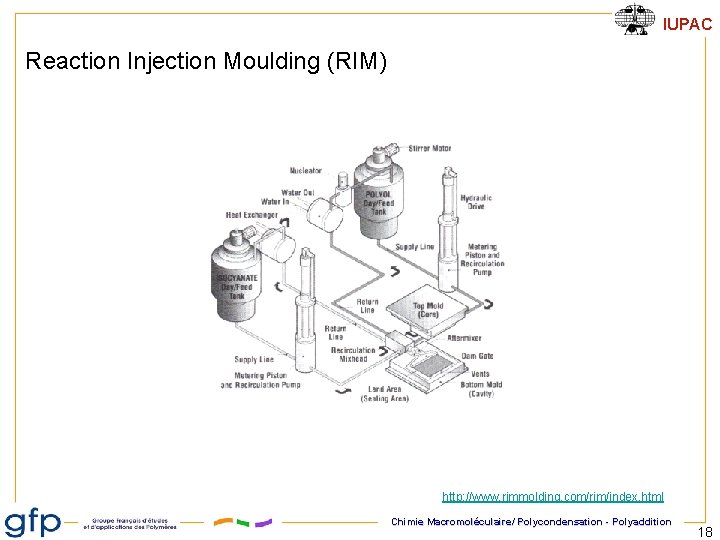
IUPAC Reaction Injection Moulding (RIM) http: //www. rimmolding. com/rim/index. html Chimie Macromoléculaire/ Polycondensation - Polyaddition 18

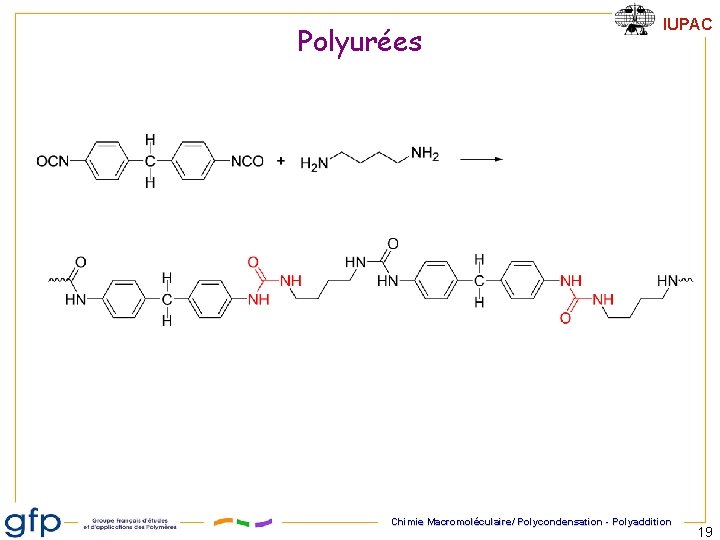
Polyurées IUPAC Chimie Macromoléculaire/ Polycondensation - Polyaddition 19

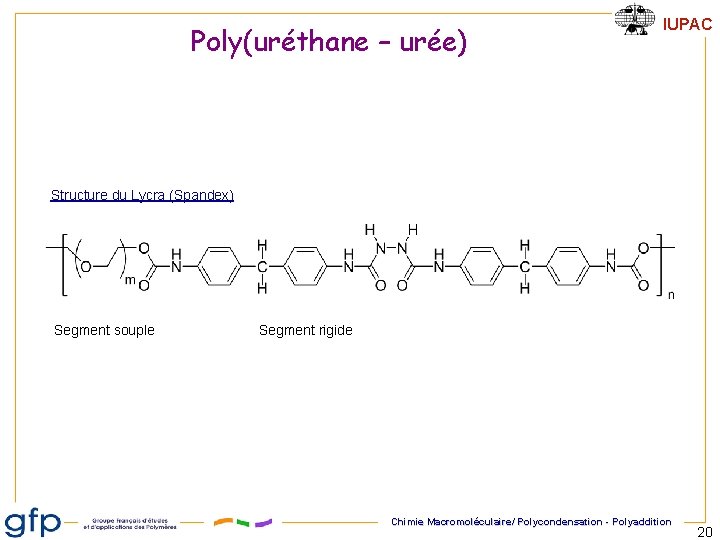
Poly(uréthane – urée) IUPAC Structure du Lycra (Spandex) Segment souple Segment rigide Chimie Macromoléculaire/ Polycondensation - Polyaddition 20

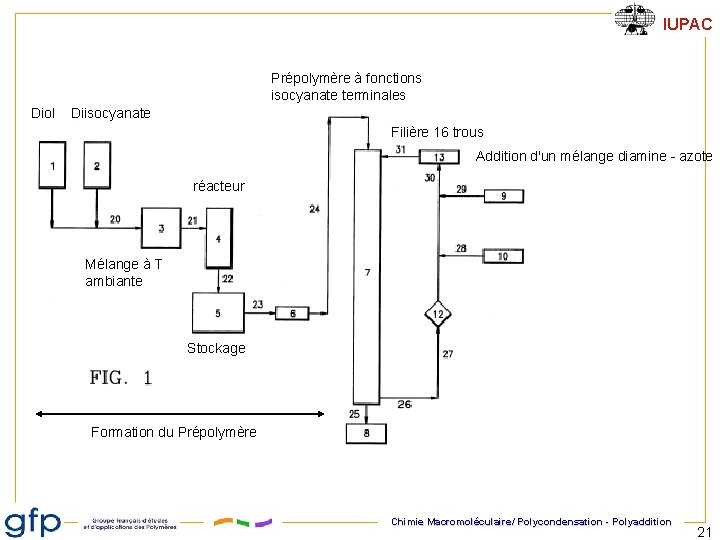
IUPAC Prépolymère à fonctions isocyanate terminales Diol Diisocyanate Filière 16 trous Addition d'un mélange diamine - azote réacteur Mélange à T ambiante Stockage Formation du Prépolymère Chimie Macromoléculaire/ Polycondensation - Polyaddition 21

Stœchiométrie et non–stœchiométrie IUPAC Stœchiométrie même nombre de fonctions chimiques antagonistes Par ex : n moles de diacide + n moles de diamine. Les fonctions réagissent toujours 2 à 2. On reste toujours en stœchiométrie de fonctions. théoriquement parlant, on pourrait arriver à une macromolécule de DP infini Non-stœchiométrie écart à la stœchiométrie. Par ex : m moles de diacide + n moles de diamine. Les fonctions réagissent toujours 2 à 2. Il arrive un moment où les fonctions en défaut ont disparu on arrive à des macromolécules de DP fini. Chimie Macromoléculaire/ Polycondensation - Polyaddition 22

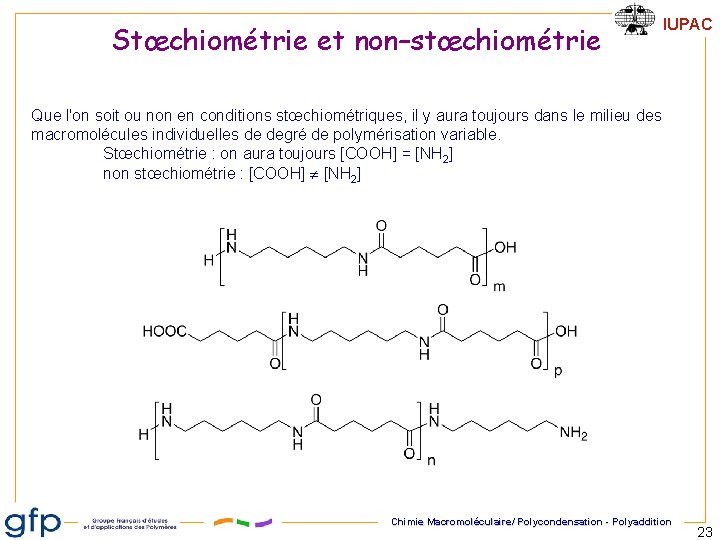
Stœchiométrie et non–stœchiométrie IUPAC Que l'on soit ou non en conditions stœchiométriques, il y aura toujours dans le milieu des macromolécules individuelles de degré de polymérisation variable. Stœchiométrie : on aura toujours [COOH] = [NH 2] non stœchiométrie : [COOH] [NH 2] Chimie Macromoléculaire/ Polycondensation - Polyaddition 23

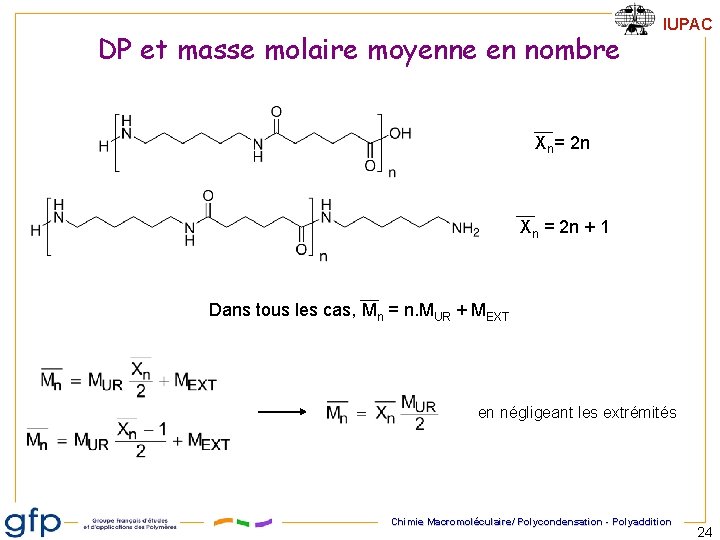
DP et masse molaire moyenne en nombre IUPAC Xn= 2 n Xn = 2 n + 1 Dans tous les cas, Mn = n. MUR + MEXT en négligeant les extrémités Chimie Macromoléculaire/ Polycondensation - Polyaddition 24

DP moyen en nombre Xn = IUPAC Nombre d'unités dans les chaînes Nombre de chaînes De façon générale, nombre d'unités polymérisées = nombre de molécules initiales même les monomères n'ayant pas réagi participent au décompte (X = 1) Monomères bifonctionnels molécules linéaires nombre de fonctions = 2 nombre de chaînes Xn = Nombre de monomères à t = 0 Moitié des fonctions résiduelles au temps t Il faut toujours raisonner en termes de fonctions chimiques Chimie Macromoléculaire/ Polycondensation - Polyaddition 25

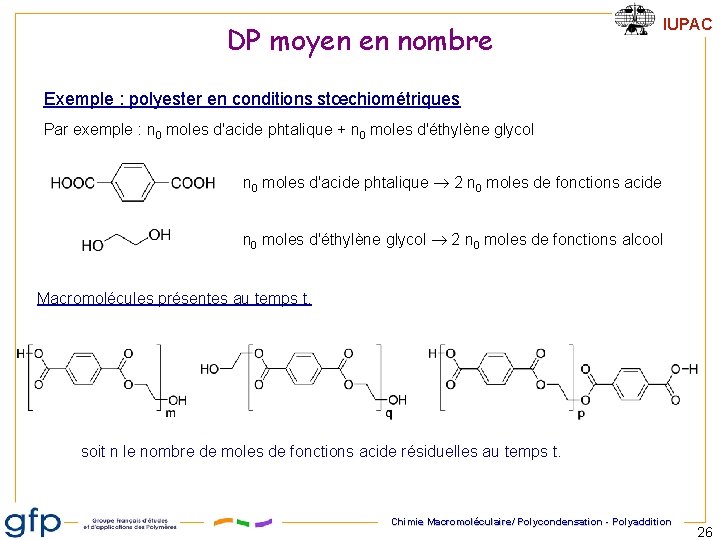
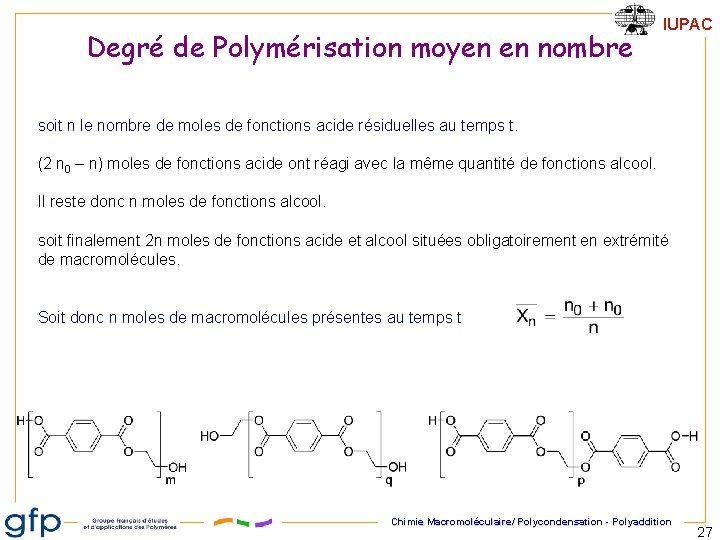
DP moyen en nombre IUPAC Exemple : polyester en conditions stœchiométriques Par exemple : n 0 moles d'acide phtalique + n 0 moles d'éthylène glycol n 0 moles d'acide phtalique 2 n 0 moles de fonctions acide n 0 moles d'éthylène glycol 2 n 0 moles de fonctions alcool Macromolécules présentes au temps t. soit n le nombre de moles de fonctions acide résiduelles au temps t. Chimie Macromoléculaire/ Polycondensation - Polyaddition 26

Degré de Polymérisation moyen en nombre IUPAC soit n le nombre de moles de fonctions acide résiduelles au temps t. (2 n 0 – n) moles de fonctions acide ont réagi avec la même quantité de fonctions alcool. Il reste donc n moles de fonctions alcool. soit finalement 2 n moles de fonctions acide et alcool situées obligatoirement en extrémité de macromolécules. Soit donc n moles de macromolécules présentes au temps t Chimie Macromoléculaire/ Polycondensation - Polyaddition 27

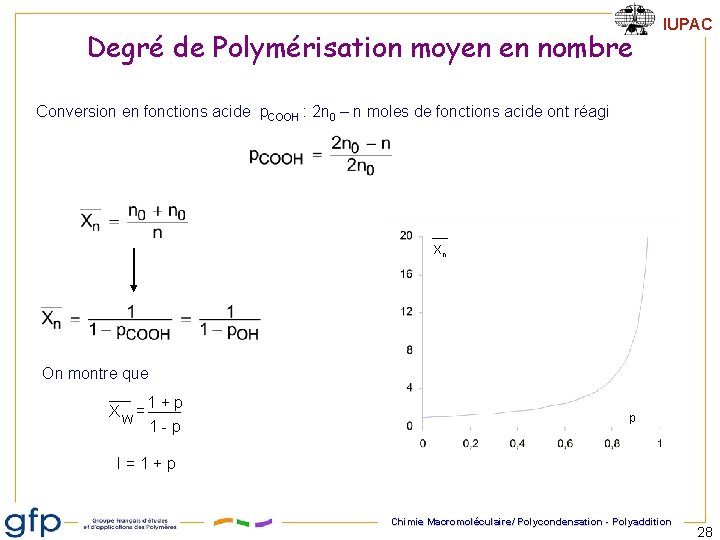
Degré de Polymérisation moyen en nombre IUPAC Conversion en fonctions acide p. COOH : 2 n 0 – n moles de fonctions acide ont réagi Xn On montre que Xw= 1+p 1 -p p I=1+p Chimie Macromoléculaire/ Polycondensation - Polyaddition 28

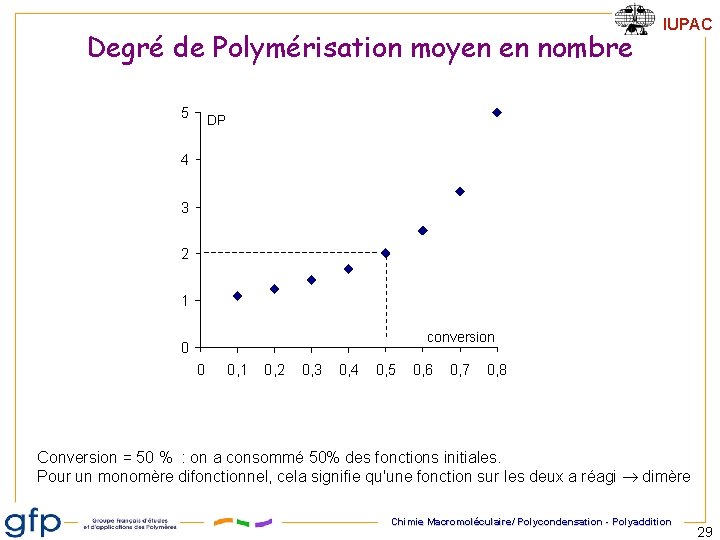
Degré de Polymérisation moyen en nombre 5 IUPAC DP 4 3 2 1 conversion 0 0 0, 1 0, 2 0, 3 0, 4 0, 5 0, 6 0, 7 0, 8 Conversion = 50 % : on a consommé 50% des fonctions initiales. Pour un monomère difonctionnel, cela signifie qu'une fonction sur les deux a réagi dimère Chimie Macromoléculaire/ Polycondensation - Polyaddition 29

Calcul de Xn en non stœchiométrie IUPAC Soient m 0 le nombre de diol et n 0 le nombre de diacide avec un excès de diol On définit r = n 0 / m 0 < 1 On montre que Xn = 1+r 1 + r - 2 rp avec p la conversion en acide (composé en défaut) p 1 Xn = 1+r 1 -r exemple : pour un degré de polymérisation de 100, r = 0, 98 Chimie Macromoléculaire/ Polycondensation - Polyaddition 30
![Réaction stœchiométrique avec catalyseur IUPAC Polyestérification catalyse H Disparition alcool alcool acide Réaction stœchiométrique avec catalyseur IUPAC Polyestérification, catalyse H+ Disparition alcool : [alcool] = (acide]](https://slidetodoc.com/presentation_image_h/876115d254e58440c61b97581b44ca45/image-31.jpg)
Réaction stœchiométrique avec catalyseur IUPAC Polyestérification, catalyse H+ Disparition alcool : [alcool] = (acide] = C k[H+] = K Intégration : En fonction de la conversion DP = f(t) linéaire Chimie Macromoléculaire/ Polycondensation - Polyaddition 31

Réaction stœchiométrique sans catalyseur IUPAC Réaction du troisième ordre Chimie Macromoléculaire/ Polycondensation - Polyaddition 32

Cinétique : limitations IUPAC La linéarité entre Xn ou Xn 2 et le temps n'est en fait observée que dans un domaine étroit de conversion. Cette déviation peut s'expliquer par : - à basse conversion : grands changements du milieu réactionnel : acide + alcool ester par exemple : associations alcool + acide à basse conversion qui diminuent les concentrations en espèces actives. - à plus haute conversion : perte de réactifs par évaporation (travail à haute température) pas d'élimination des sous-produits car la viscosité augmente fortement dégradation des réactifs (déshydratation, decarboxylation. . . ) Chimie Macromoléculaire/ Polycondensation - Polyaddition 33

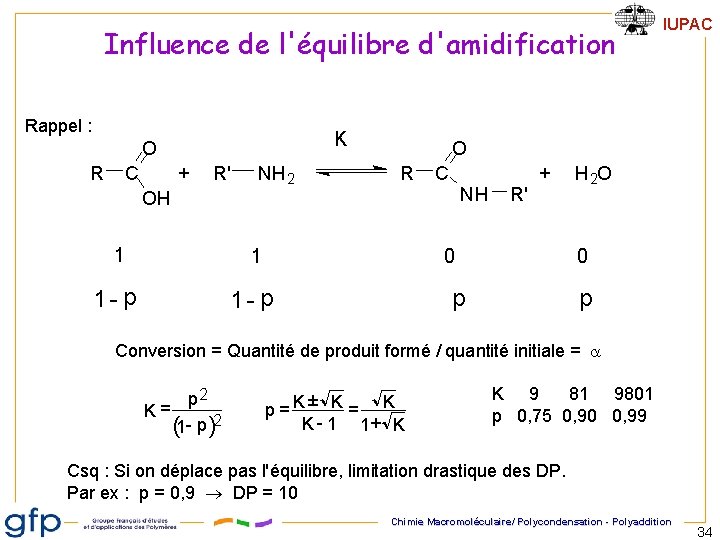
Influence de l'équilibre d'amidification Rappel : K O R + C R' NH 2 O R + C NH OH 1 1 1 - p IUPAC R' 0 H 2 O 0 p p Conversion = Quantité de produit formé / quantité initiale = a p 2 K= (1 - p )2 ± p =K K = K K - 1 1+ K K 9 81 9801 p 0, 75 0, 90 0, 99 Csq : Si on déplace pas l'équilibre, limitation drastique des DP. Par ex : p = 0, 9 DP = 10 Chimie Macromoléculaire/ Polycondensation - Polyaddition 34

IUPAC Déplacement de l'équilibre K O R + C R' O NH 2 R NH OH 1 - p + C 1 - p R' p K = H 2 O e p. e (1 - p )2 Il reste toujours de l'eau résiduelle. K garde la même valeur. On veut p = 0, 99 ( DP = 100) e= 2 K (1 - p ) p = 81. 0 , 01 0 , 99 2 = 8 , 18. 10 3 Chimie Macromoléculaire/ Polycondensation - Polyaddition 35

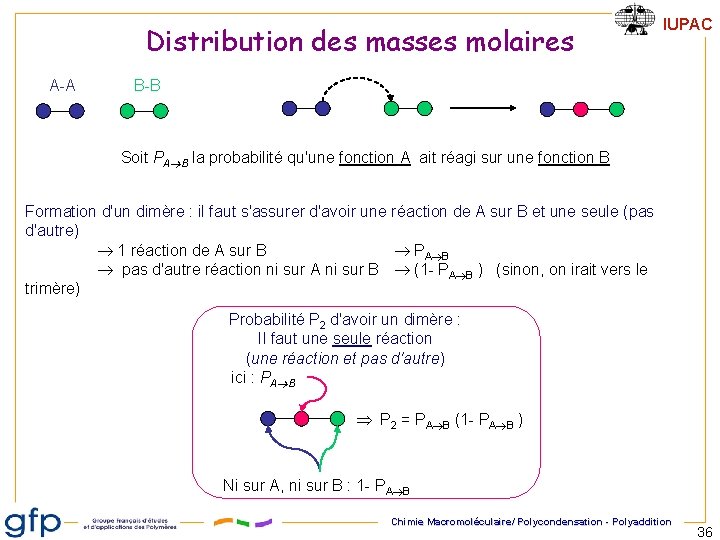
Distribution des masses molaires A-A IUPAC B-B Soit PA B la probabilité qu'une fonction A ait réagi sur une fonction B Formation d'un dimère : il faut s'assurer d'avoir une réaction de A sur B et une seule (pas d'autre) 1 réaction de A sur B PA B pas d'autre réaction ni sur A ni sur B (1 - PA B ) (sinon, on irait vers le trimère) Probabilité P 2 d'avoir un dimère : Il faut une seule réaction (une réaction et pas d'autre) ici : PA B P 2 = PA B (1 - PA B ) Ni sur A, ni sur B : 1 - PA B Chimie Macromoléculaire/ Polycondensation - Polyaddition 36

Distribution des masses molaires P 3 = (PA B)2(1 - PA B ) IUPAC P 4 = (PA B)3(1 - PA B ) Probabilité d'avoir un i-mère : Pi= (PA B)i-1(1 - PA B ) Cette probabilité Pi est aussi égale à Ni / N Ni nombre de chaînes de DP = i N nombre total de macromolécules Il est donc possible de connaître Ni connaissant Pi, donc de connaître la distribution des masses molaires …. Chimie Macromoléculaire/ Polycondensation - Polyaddition 37

Distribution des masses molaires IUPAC On a Ni = N. Pi = N. (PA B)i-1(1 - PA B ) Calcul de N : Pour un système stœchiométrique : n. A(0) fonctions A = n. B(0) fonctions B initialement Pour une conversion p. A en fonctions A = p. B : p. A = [n. A(0) – n. A(t)] / n. A(0) n. A(t) : nombre de fonctions A résiduelles = n. B(t) puisque stœchiométrie Il reste donc 2 n. A(t) fonctions résiduelles, soit n. A(t) chaînes N = n. A(t) = n. A(0) (1 -p. A) Ni = n. A(0)(1 -p. A). (PA B)i-1(1 - PA B ) Il reste à déterminer PA B …. Chimie Macromoléculaire/ Polycondensation - Polyaddition 38

Distribution des masses molaires IUPAC Ni = n. A(0)(1 -p. A). (PA B)i-1(1 - PA B ) Détermination de PA B On a [n. A(0) – n. A(t)] = n. A(0). p. A = nombre de fonctions A ayant réagi sur B Ce nombre de fonctions A ayant réagi sur B est aussi égal à n. A(0). PA B avec PA B probabilité qu'une fonction A ait réagi sur B on a donc p. A = PA B Ni = n. A(0)(1 -p. A). (p. A)i-1(1 - p. A ) = n. A(0)(1 -p. A)2. (p. A)i-1 Chimie Macromoléculaire/ Polycondensation - Polyaddition 39

Distribution des masses molaires IUPAC Ni = n. A(0)(1 -p. A). (p. A)i-1(1 - p. A ) = n. A(0)(1 -p. A)2. (p. A)i-1 Pour une conversion p. A = 90 % , n. A(0) = 1 eq * Xn = 10 monomère N 1 = (1 -P)2 = 0, 01 (il reste 1% de monomère résiduel) dimère N 2 = (1 -p. A)2(p. A) = 0, 009 trimère N 3 = (1 -p. A)2(p. A)2 = 0, 0081 etc … * soit 0, 5 mole de AA et 0, 5 mole de BB, donc 1 mole de monomères Chimie Macromoléculaire/ Polycondensation - Polyaddition 40

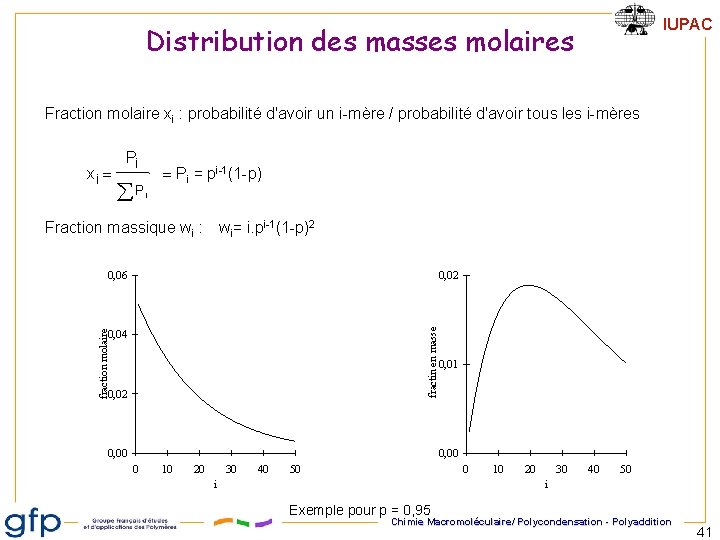
IUPAC Distribution des masses molaires Fraction molaire xi : probabilité d'avoir un i-mère / probabilité d'avoir tous les i-mères xi = Pi åP = Pi = pi-1(1 -p) i Fraction massique wi : wi= i. pi-1(1 -p)2 0, 02 fraction molaire fractin en masse 0, 06 0, 04 0, 01 0, 02 0, 00 0 10 20 30 40 50 0 i 10 20 30 40 50 i Exemple pour p = 0, 95 Chimie Macromoléculaire/ Polycondensation - Polyaddition 41

Distribution des masses molaires IUPAC Xn = xi. i xi = Pi = pi-1 (1 -p) Retrouver Xn = f(conversion) Chimie Macromoléculaire/ Polycondensation - Polyaddition 42

Distribution des masses molaires Mn = å x i Mi Mw = åw i. Mi Mn = Mw = IUPAC å (1 - p)pi -1 i. M 0 å (1 -p)2 pi-1 i 2. M 0 Chimie Macromoléculaire/ Polycondensation - Polyaddition 43

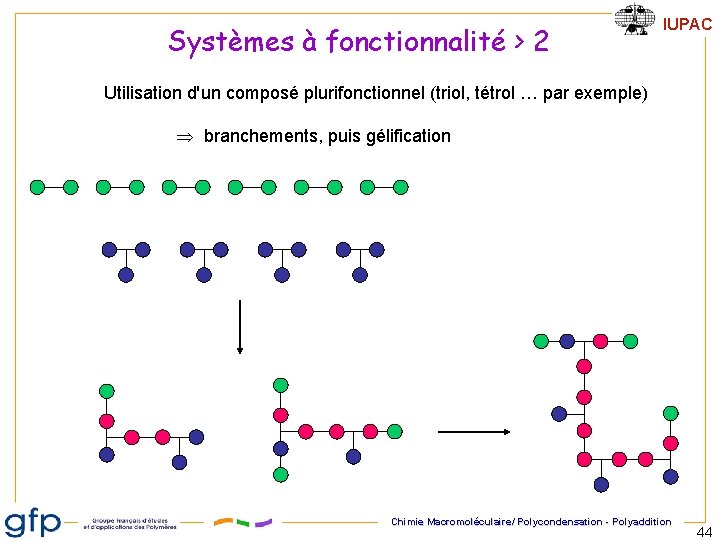
Systèmes à fonctionnalité > 2 IUPAC Utilisation d'un composé plurifonctionnel (triol, tétrol … par exemple) branchements, puis gélification Chimie Macromoléculaire/ Polycondensation - Polyaddition 44

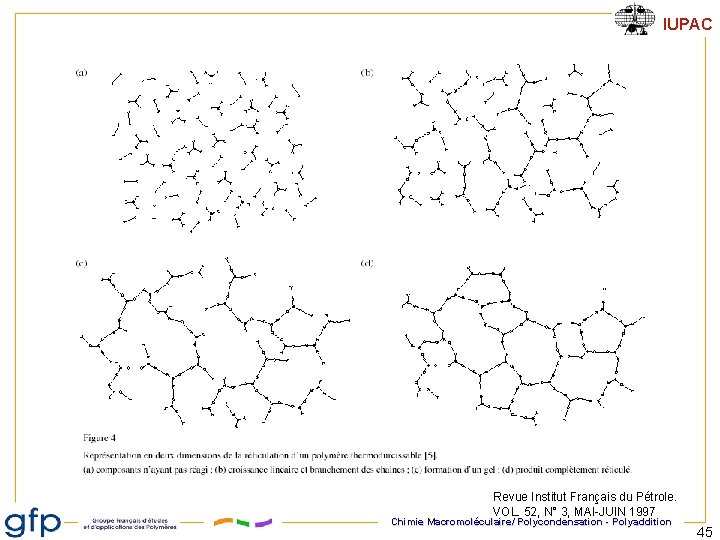
IUPAC Revue Institut Français du Pétrole. VOL. 52, N° 3, MAI-JUIN 1997 Chimie Macromoléculaire/ Polycondensation - Polyaddition 45

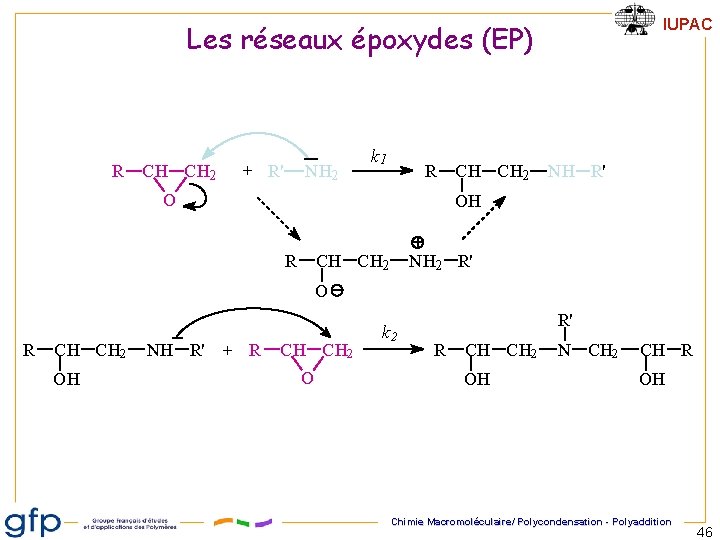
IUPAC Les réseaux époxydes (EP) R CH CH 2 + R' NH 2 k 1 R O CH CH 2 NH R' OH R CH CH 2 NH 2 R' O R CH CH 2 OH NH R' + R CH CH 2 O k 2 R' R CH CH 2 OH N CH 2 CH R OH Chimie Macromoléculaire/ Polycondensation - Polyaddition 46

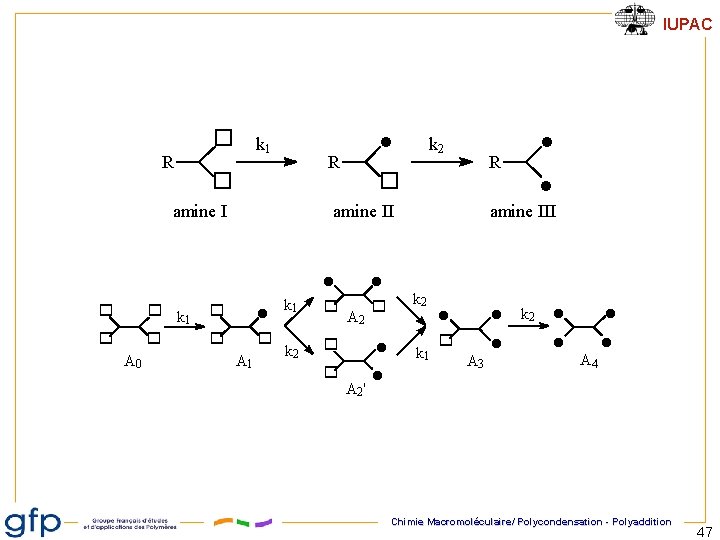
IUPAC o R l k 1 R o amine I o o k 1 o o A 0 l k 2 R o l amine III amine II o l o o A 1 l l k 1 o o k 2 o l k 1 o A 2' l l l o l A 3 k 2 l l A 4 Chimie Macromoléculaire/ Polycondensation - Polyaddition 47

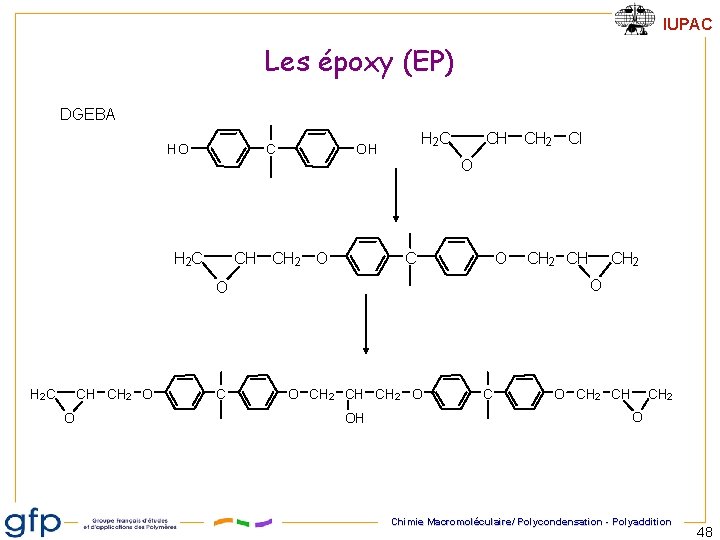
IUPAC Les époxy (EP) DGEBA HO C H 2 C OH CH CH 2 O CH CH 2 Cl O CH CH 2 O O C CH 2 O O H 2 C CH 2 CH O CH 2 CH CH 2 O OH C O CH 2 CH CH 2 O Chimie Macromoléculaire/ Polycondensation - Polyaddition 48

IUPAC Les réseaux époxydes H 2 C CH CH 2 O CH 2 CH CH 2 O O OH C O CH 2 CH n CH 2 O Réactions sur les sites réactifs - cycles époxyde en fin de structure - fonction alcool sur la chaîne Avec - Amines - anhydrides d'acide, en présence d'accélérateurs (amines tertiaires …) - bases de Lewis Chimie Macromoléculaire/ Polycondensation - Polyaddition 49

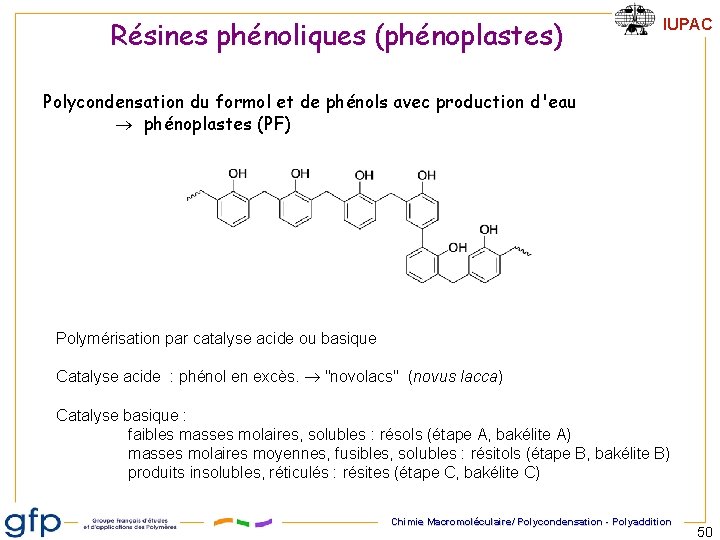
Résines phénoliques (phénoplastes) IUPAC Polycondensation du formol et de phénols avec production d'eau phénoplastes (PF) Polymérisation par catalyse acide ou basique Catalyse acide : phénol en excès. "novolacs" (novus lacca) Catalyse basique : faibles masses molaires, solubles : résols (étape A, bakélite A) masses molaires moyennes, fusibles, solubles : résitols (étape B, bakélite B) produits insolubles, réticulés : résites (étape C, bakélite C) Chimie Macromoléculaire/ Polycondensation - Polyaddition 50

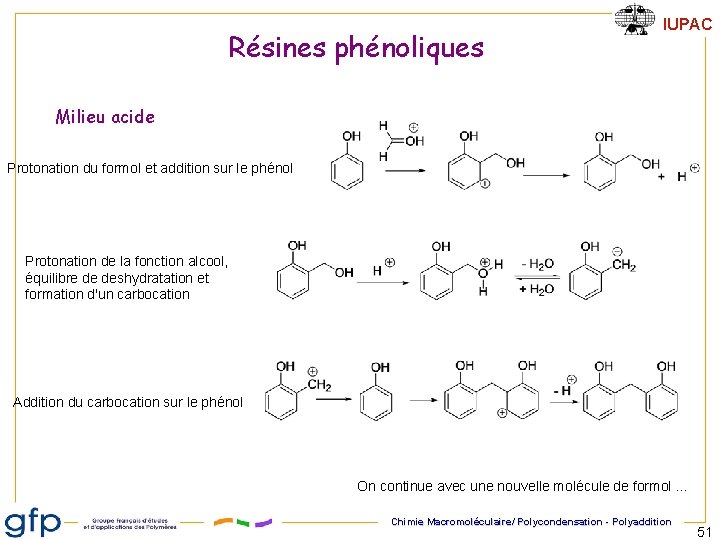
Résines phénoliques IUPAC Milieu acide Protonation du formol et addition sur le phénol Protonation de la fonction alcool, équilibre de deshydratation et formation d'un carbocation Addition du carbocation sur le phénol On continue avec une nouvelle molécule de formol … Chimie Macromoléculaire/ Polycondensation - Polyaddition 51

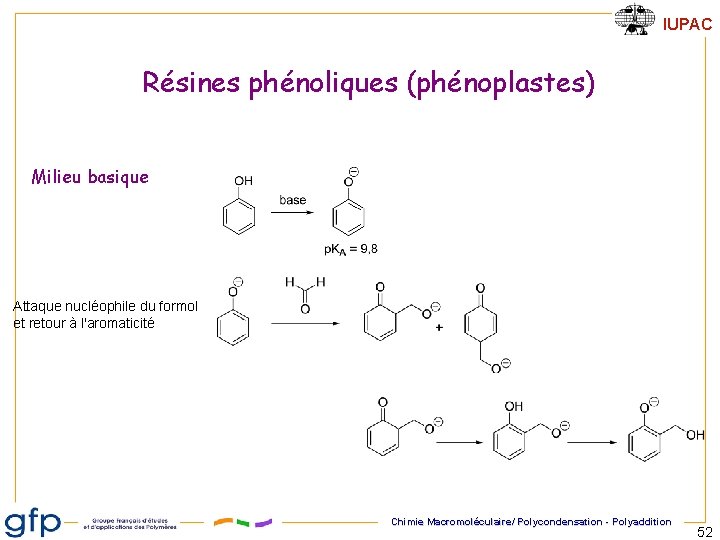
IUPAC Résines phénoliques (phénoplastes) Milieu basique Attaque nucléophile du formol et retour à l'aromaticité Chimie Macromoléculaire/ Polycondensation - Polyaddition 52

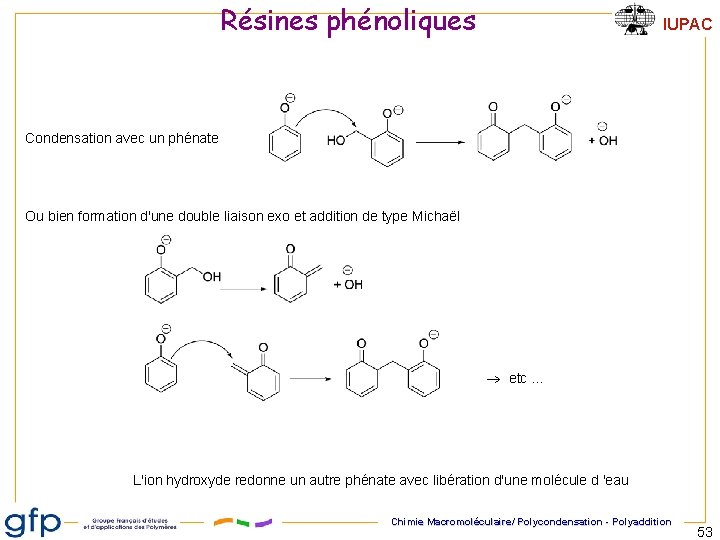
Résines phénoliques IUPAC Condensation avec un phénate Ou bien formation d'une double liaison exo et addition de type Michaël etc … L'ion hydroxyde redonne un autre phénate avec libération d'une molécule d 'eau Chimie Macromoléculaire/ Polycondensation - Polyaddition 53

IUPAC Résines phénoliques Autres résines formo-phénoliques à base de Furfural Résorcinol m-crésol Xylénol … Chimie Macromoléculaire/ Polycondensation - Polyaddition 54

Résines aminoplastes IUPAC Polycondensation entre l'urée ou la mélamine et le formol urée – formaldéhyde (UF) mélamine – formaldéhyde (MF) 1 - Réaction urée – formol p. H 7 - 8 2 – formation d'un carbocation 3 – polycondensation Chimie Macromoléculaire/ Polycondensation - Polyaddition 55

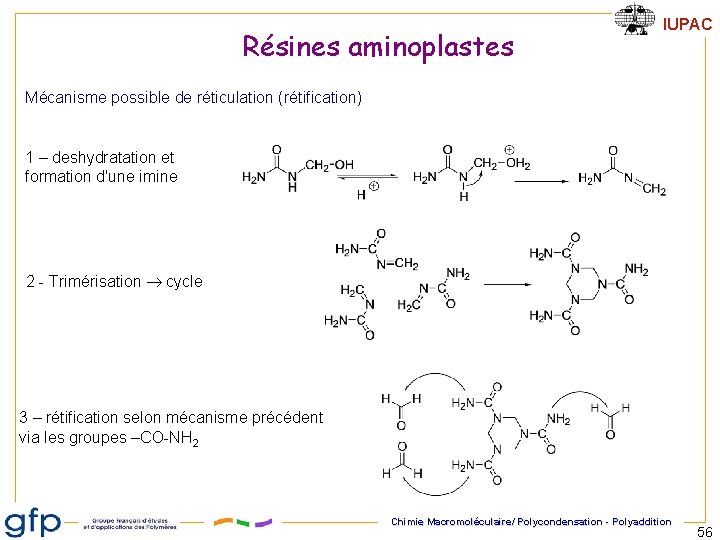
Résines aminoplastes IUPAC Mécanisme possible de réticulation (rétification) 1 – deshydratation et formation d'une imine 2 - Trimérisation cycle 3 – rétification selon mécanisme précédent via les groupes –CO-NH 2 Chimie Macromoléculaire/ Polycondensation - Polyaddition 56

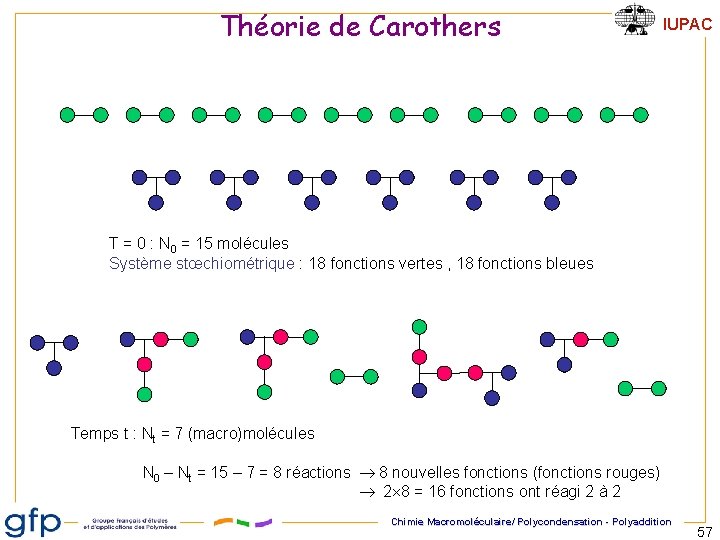
Théorie de Carothers IUPAC T = 0 : N 0 = 15 molécules Système stœchiométrique : 18 fonctions vertes , 18 fonctions bleues Temps t : Nt = 7 (macro)molécules N 0 – Nt = 15 – 7 = 8 réactions 8 nouvelles fonctions (fonctions rouges) 2 8 = 16 fonctions ont réagi 2 à 2 Chimie Macromoléculaire/ Polycondensation - Polyaddition 57

IUPAC Théorie de Carothers Fonctionnalité moyenne f = nombre de fonctions disponibles nombre de molécules nombre de fonctions disponibles = N 0. f Q= 40 2. (N 0 -Nt) Xn = 35 N 0. f f = 2, 4 f=2 30 N 0 25 20 Nt 15 10 2æ ç 1 Q = f çè 1 ö ÷ Xn ÷ø Qgel = 2 5 f 0 0 0, 1 0, 2 0, 3 0, 4 0, 5 0, 6 0, 7 0, 8 0, 9 1 Cette théorie ne s'applique pour des systèmes "stœchiométriques" (équimolaires en fonctions réactives); dans le cas contraire : théorie de Flory - Stockmayer Chimie Macromoléculaire/ Polycondensation - Polyaddition 58

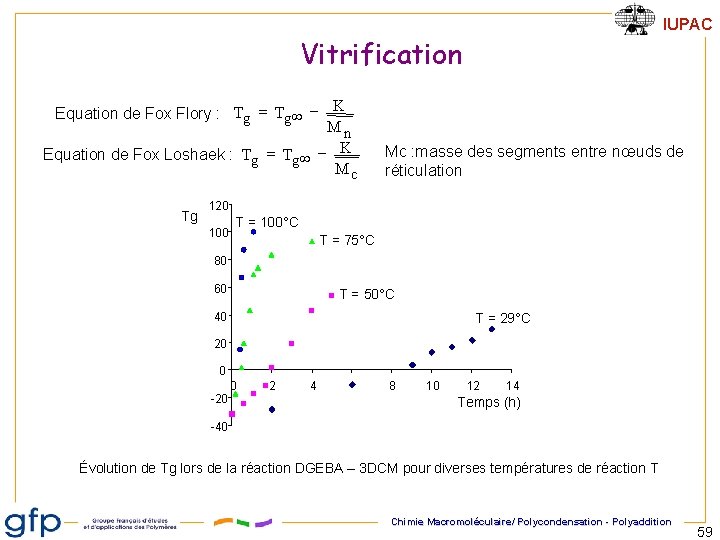
IUPAC Vitrification Equation de Fox Flory : Tg = Tg ¥ - K Mn Equation de Fox Loshaek : Tg = Tg ¥ - K Mc Tg Mc : masse des segments entre nœuds de réticulation 120 100 T = 100°C T = 75°C 80 60 T = 50°C 40 T = 29°C 20 0 0 -20 2 4 8 10 12 14 Temps (h) -40 Évolution de Tg lors de la réaction DGEBA – 3 DCM pour diverses températures de réaction T Chimie Macromoléculaire/ Polycondensation - Polyaddition 59

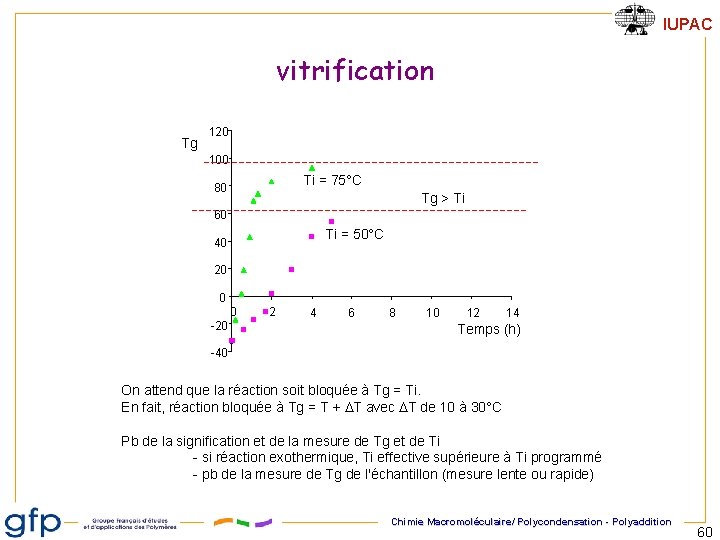
IUPAC vitrification Tg 120 100 Ti = 75°C 80 Tg > Ti 60 Ti = 50°C 40 20 0 0 -20 2 4 6 8 10 12 14 Temps (h) -40 On attend que la réaction soit bloquée à Tg = Ti. En fait, réaction bloquée à Tg = T + T avec T de 10 à 30°C Pb de la signification et de la mesure de Tg et de Ti - si réaction exothermique, Ti effective supérieure à Ti programmé - pb de la mesure de Tg de l'échantillon (mesure lente ou rapide) Chimie Macromoléculaire/ Polycondensation - Polyaddition 60

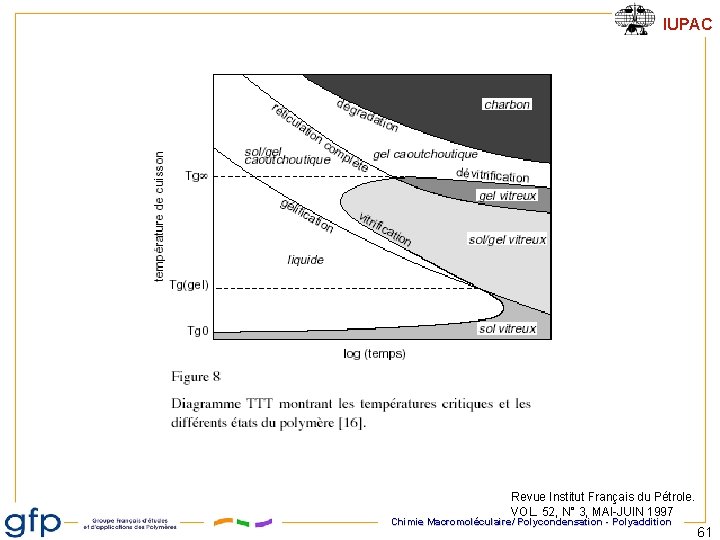
IUPAC Revue Institut Français du Pétrole. VOL. 52, N° 3, MAI-JUIN 1997 Chimie Macromoléculaire/ Polycondensation - Polyaddition 61

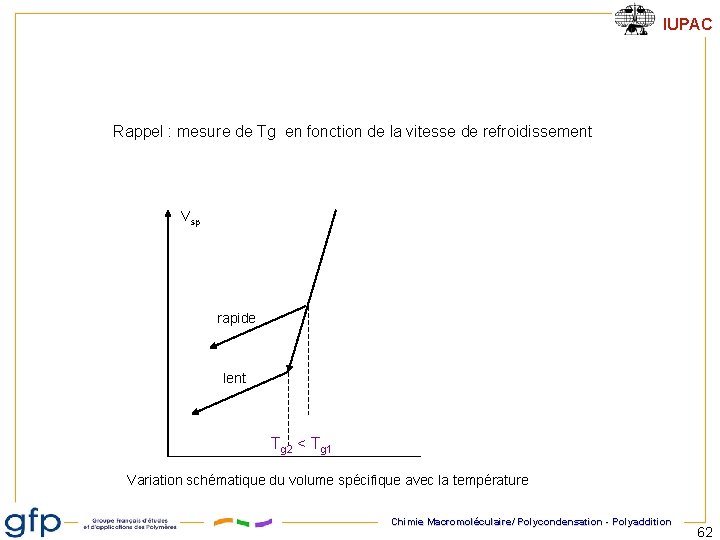
IUPAC Rappel : mesure de Tg en fonction de la vitesse de refroidissement Vsp rapide lent Tg 2 < Tg 1 Variation schématique du volume spécifique avec la température Chimie Macromoléculaire/ Polycondensation - Polyaddition 62

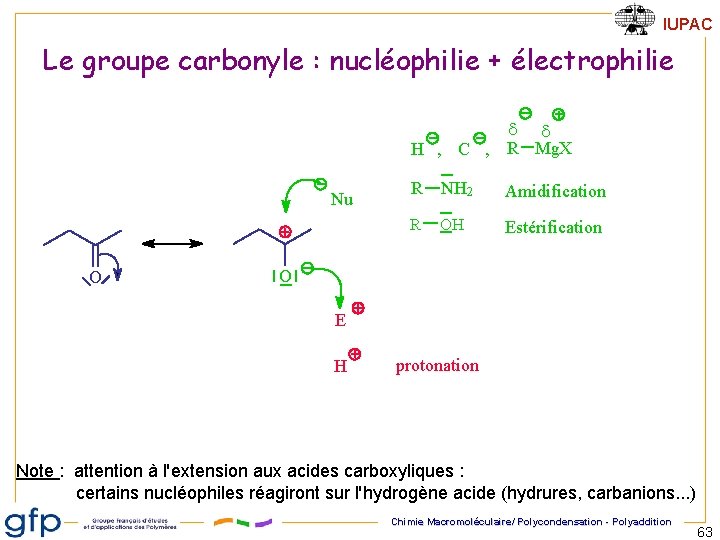
IUPAC Le groupe carbonyle : nucléophilie + électrophilie d d H , C , R Mg. X Nu O R NH 2 Amidification R OH Estérification O E H protonation Note : attention à l'extension aux acides carboxyliques : certains nucléophiles réagiront sur l'hydrogène acide (hydrures, carbanions. . . ) Chimie Macromoléculaire/ Polycondensation - Polyaddition 63