istopos estveis Fbio R D de Andrade Instituto
isótopos estáveis Fábio R. D. de Andrade, Instituto de Geociências
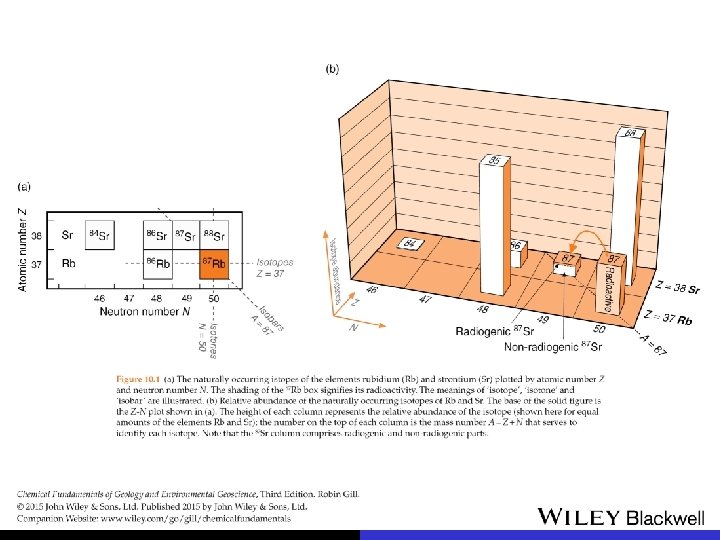
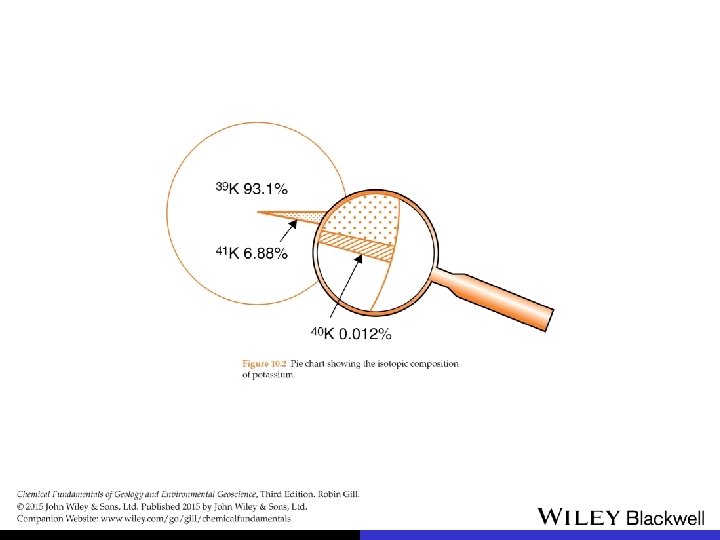
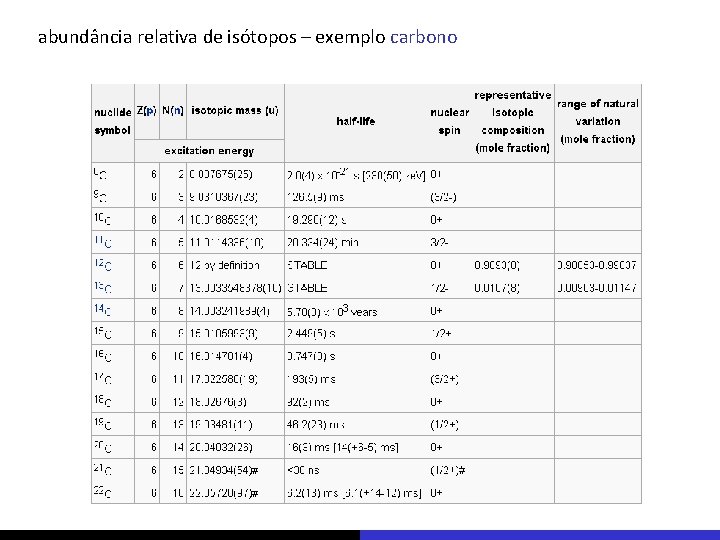
abundância relativa de isótopos – exemplo carbono

roteiro isótopos estáveis: notações gráficas e padrões internacionais mecanismos de fracionamento sistemas isotópicos mais usados hidrogênio carbono oxigênio enxofre geotermômetros isotópicos e paleoclimatologia
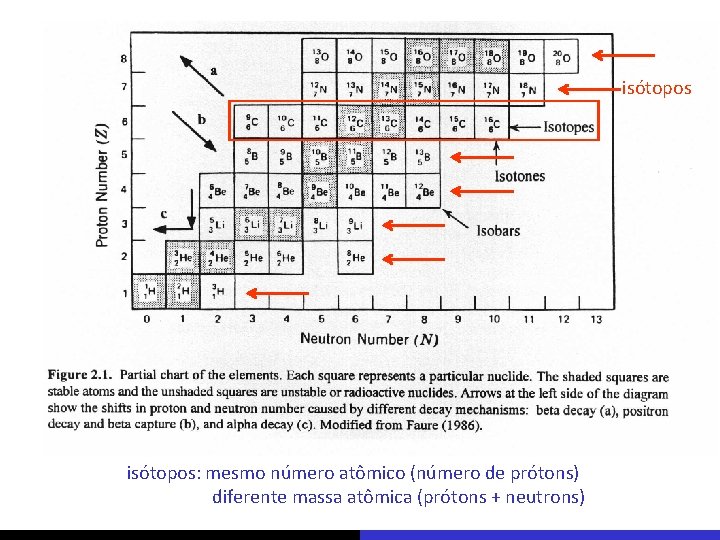
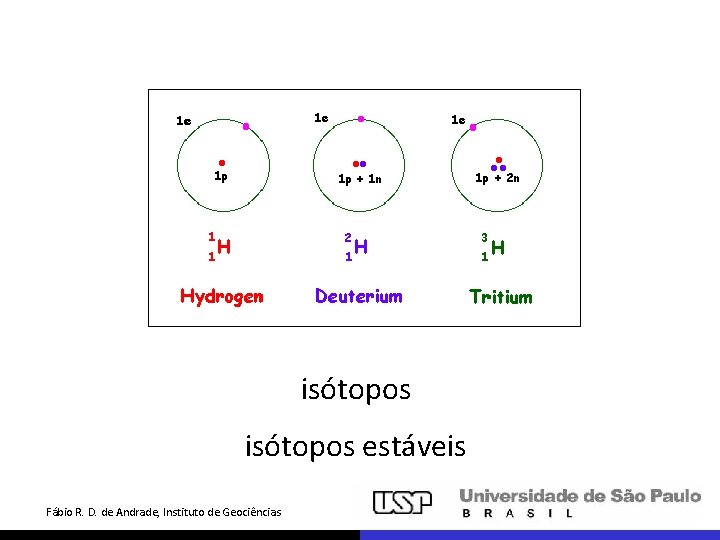
isótopos: mesmo número atômico (número de prótons) diferente massa atômica (prótons + neutrons)

isótopos estáveis principais aplicações paleoclimatologia reconstituições paleoambientais geologia econômica, gênese de jazidas petrologia, processos petrogenéticos isótopos estáveis mais usados para fins geológicos 1 H – 2 H (2 H = D, deutério) 12 C – 13 C 16 O – 18 O 32 S – 34 S
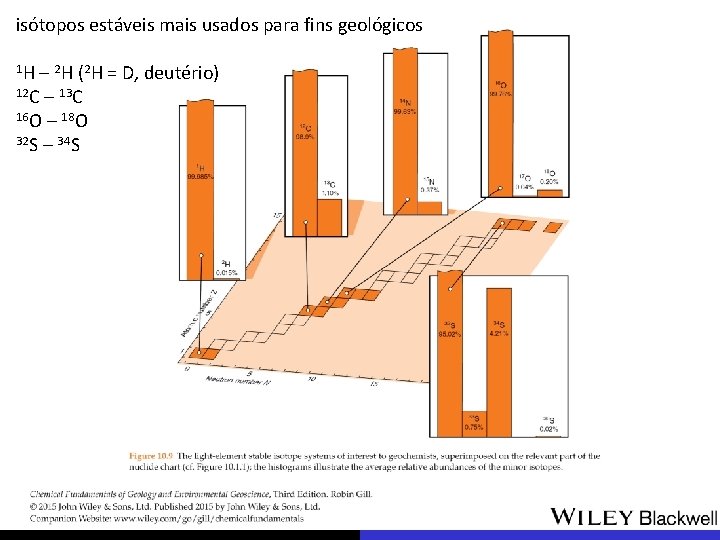
isótopos estáveis mais usados para fins geológicos 1 H – 2 H (2 H = D, deutério) 12 C – 13 C 16 O – 18 O 32 S – 34 S
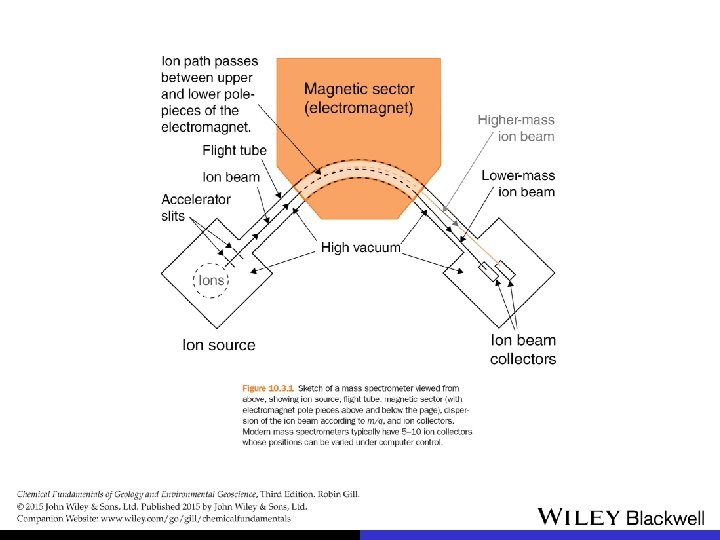
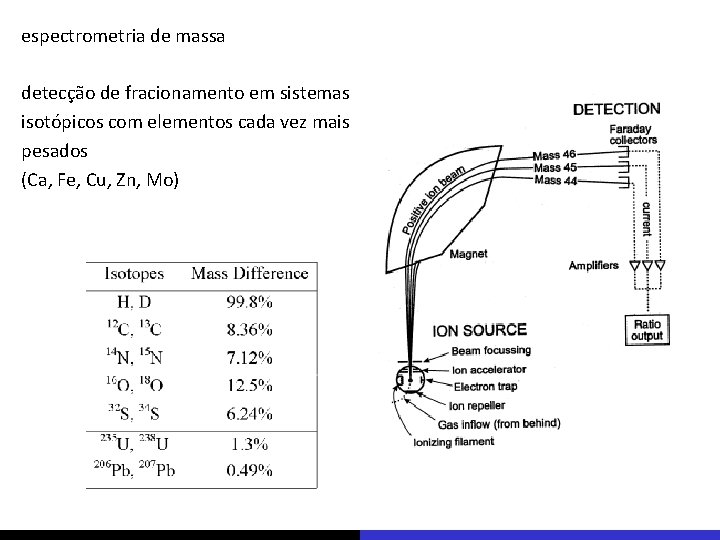
espectrometria de massa detecção de fracionamento em sistemas isotópicos com elementos cada vez mais pesados (Ca, Fe, Cu, Zn, Mo)
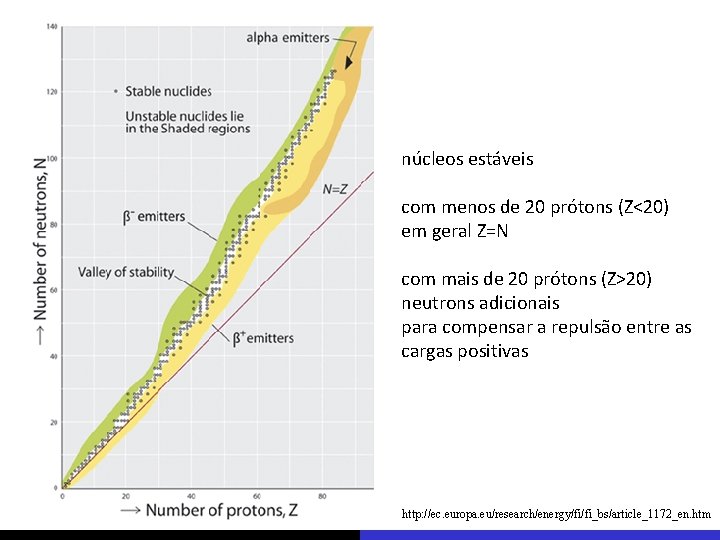
núcleos estáveis com menos de 20 prótons (Z<20) em geral Z=N com mais de 20 prótons (Z>20) neutrons adicionais para compensar a repulsão entre as cargas positivas http: //ec. europa. eu/research/energy/fi/fi_bs/article_1172_en. htm
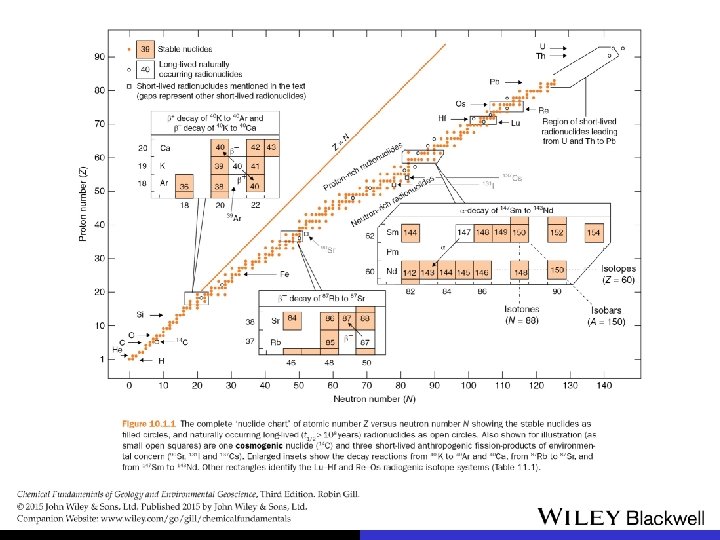
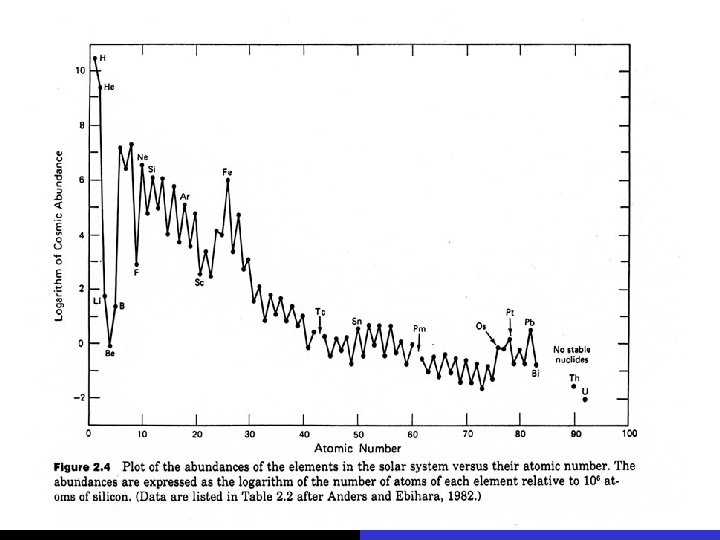
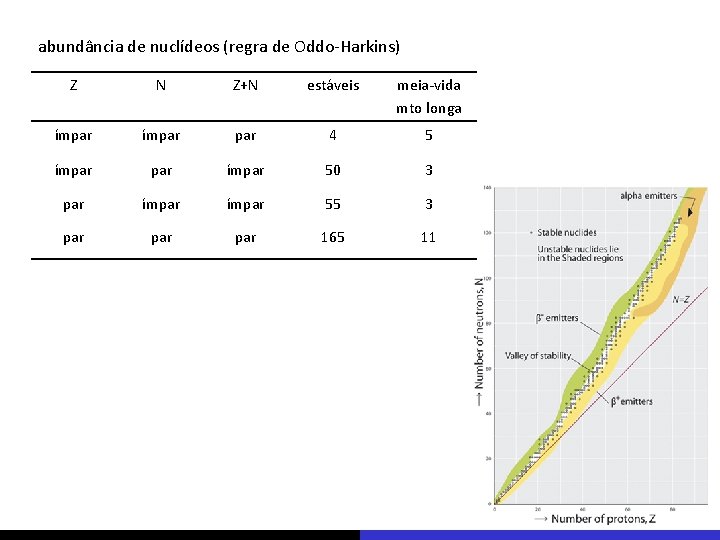
abundância de nuclídeos (regra de Oddo-Harkins) Z N Z+N estáveis meia-vida mto longa ímpar par 4 5 ímpar 50 3 par ímpar 55 3 par par 165 11

características (desejáveis) dos isótopos estáveis usados em geologia 1. baixa massa atômica 2. grande diferença relativa entre a massa dos isotópos 3. existência em mais de um estado de oxidação (C, N, S), formando diversos tipos de compostos – são componentes comuns em sólidos e fluidos naturais 4. abundância do isótopo mais raro suficiente para permitir análises de rotina

fracionamento de isótopos estáveis do mesmo elementos têm quase as mesmas características químicas, já que possuem as mesmas configurações eletrônicas fracionamento: processo de separação ou concentração parcial de isótopos de um mesmo elemento fracionamento dependente da massa fracionamento em equilíbrio fracionamento cinético fracionamento independente da massa

fracionamento de isótopos estáveis isótopos mais pesados tendem a se concentrar em substâncias com maior energia de ligação o fracionamento é mais intenso a baixas temperaturas é a base dos geotermomêtros isotópicos D/H e 18 O/16 O em sondagens em geleiras 18 O/16 O em materiais carbonáticos (calcários, espeleotemas, carapaças)

fracionamento de isótopos estáveis isótopos mais pesados têm frequência vibracional menor White, Geochemistry vibração rotação translação
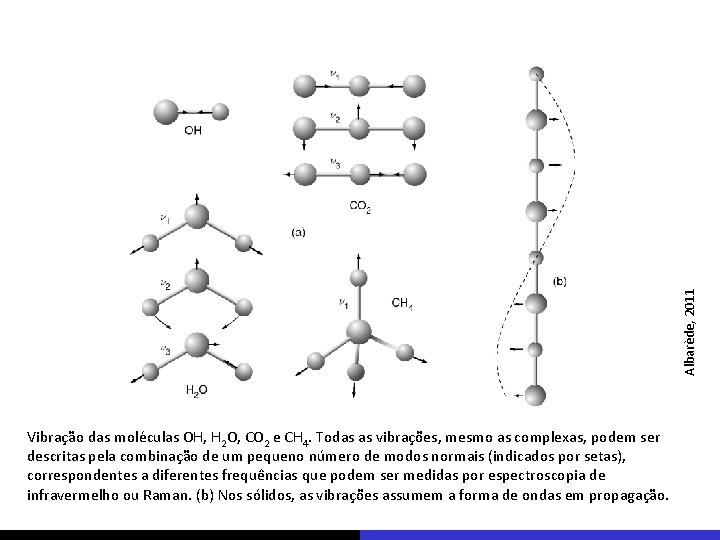
Albarède, 2011 Vibração das moléculas OH, H 2 O, CO 2 e CH 4. Todas as vibrações, mesmo as complexas, podem ser descritas pela combinação de um pequeno número de modos normais (indicados por setas), correspondentes a diferentes frequências que podem ser medidas por espectroscopia de infravermelho ou Raman. (b) Nos sólidos, as vibrações assumem a forma de ondas em propagação.
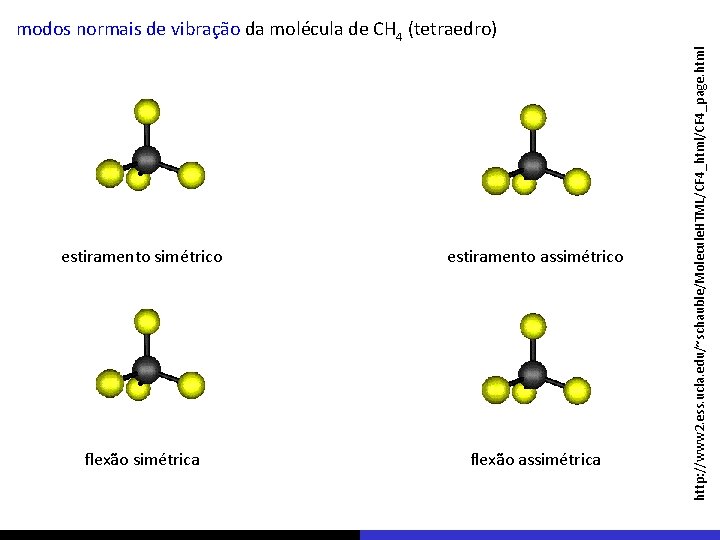
estiramento simétrico estiramento assimétrico flexão simétrica flexão assimétrica http: //www 2. ess. ucla. edu/~schauble/Molecule. HTML/CF 4_html/CF 4_page. html modos normais de vibração da molécula de CH 4 (tetraedro)
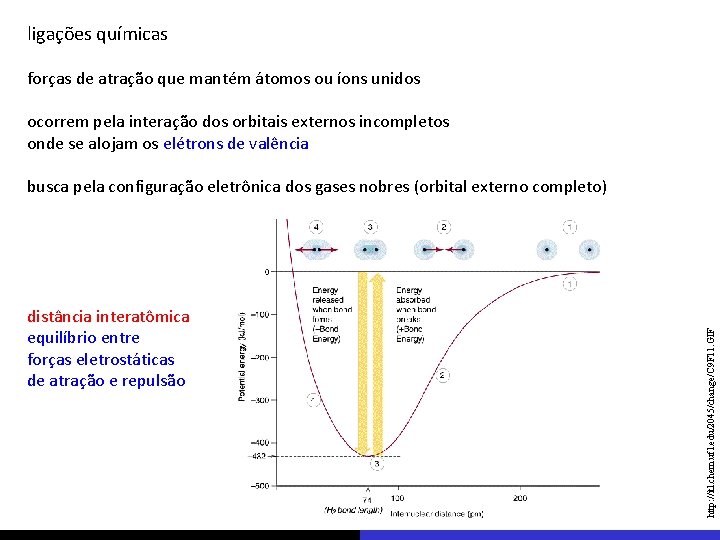
ligações químicas forças de atração que mantém átomos ou íons unidos ocorrem pela interação dos orbitais externos incompletos onde se alojam os elétrons de valência distância interatômica equilíbrio entre forças eletrostáticas de atração e repulsão http: //itl. chem. ufl. edu/2045/change/C 9 F 11. GIF busca pela configuração eletrônica dos gases nobres (orbital externo completo)
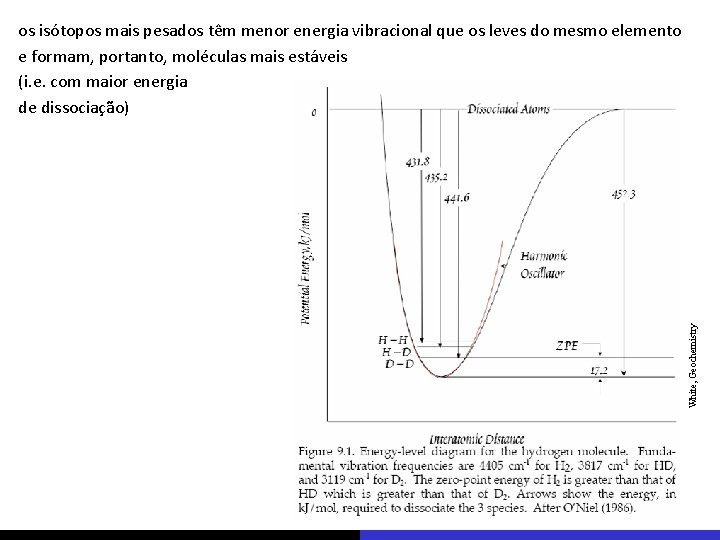
White, Geochemistry os isótopos mais pesados têm menor energia vibracional que os leves do mesmo elemento e formam, portanto, moléculas mais estáveis (i. e. com maior energia de dissociação)
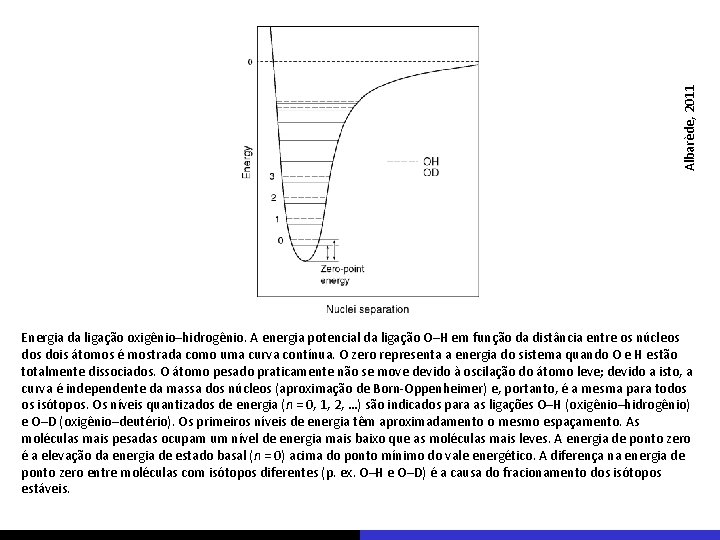
Albarède, 2011 Energia da ligação oxigênio–hidrogênio. A energia potencial da ligação O–H em função da distância entre os núcleos dois átomos é mostrada como uma curva contínua. O zero representa a energia do sistema quando O e H estão totalmente dissociados. O átomo pesado praticamente não se move devido à oscilação do átomo leve; devido a isto, a curva é independente da massa dos núcleos (aproximação de Born-Oppenheimer) e, portanto, é a mesma para todos os isótopos. Os níveis quantizados de energia (n = 0, 1, 2, …) são indicados para as ligações O–H (oxigênio–hidrogênio) e O–D (oxigênio–deutério). Os primeiros níveis de energia têm aproximadamento o mesmo espaçamento. As moléculas mais pesadas ocupam um nível de energia mais baixo que as moléculas mais leves. A energia de ponto zero é a elevação da energia de estado basal (n = 0) acima do ponto mínimo do vale energético. A diferença na energia de ponto zero entre moléculas com isótopos diferentes (p. ex. O–H e O–D) é a causa do fracionamento dos isótopos estáveis.

notação isotópica isótopo especificado pelo número de massa sobrescrito antes do símbolo 13 C 18 O 32 S … a composição isotópica de qualquer substância é dada em termos da variação das razões entre os isótopos em comparação com uma substância padrão de composição conhecida SMOW – standard mean ocean water NIST – National Inst. for Standards and Technology PDB – Pee Dee belemnite CDT – Canyon Diablo Troilite

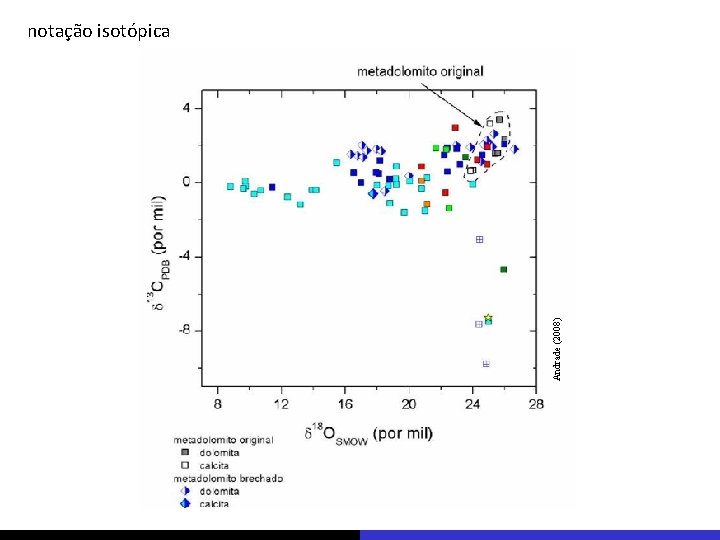
Andrade (2008) notação isotópica
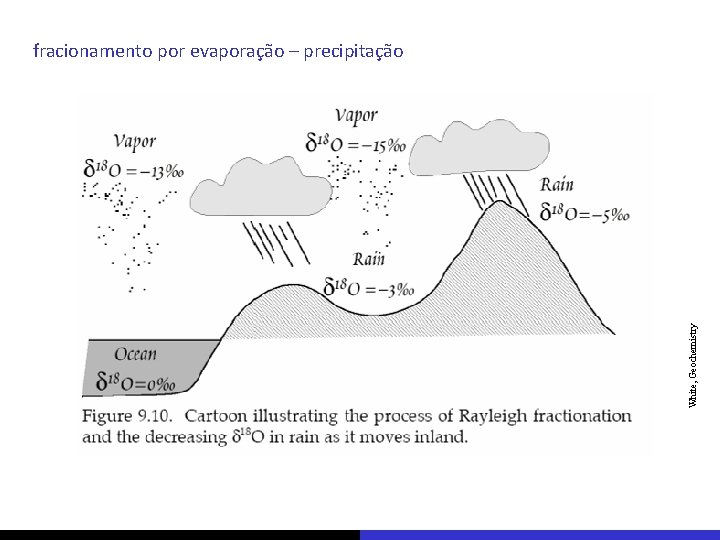
White, Geochemistry fracionamento por evaporação – precipitação
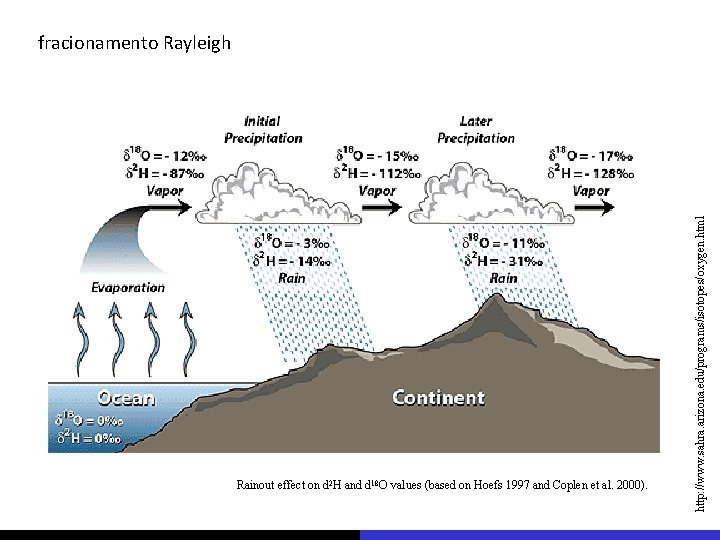
Rainout effect on d 2 H and d 18 O values (based on Hoefs 1997 and Coplen et al. 2000). http: //www. sahra. arizona. edu/programs/isotopes/oxygen. html fracionamento Rayleigh
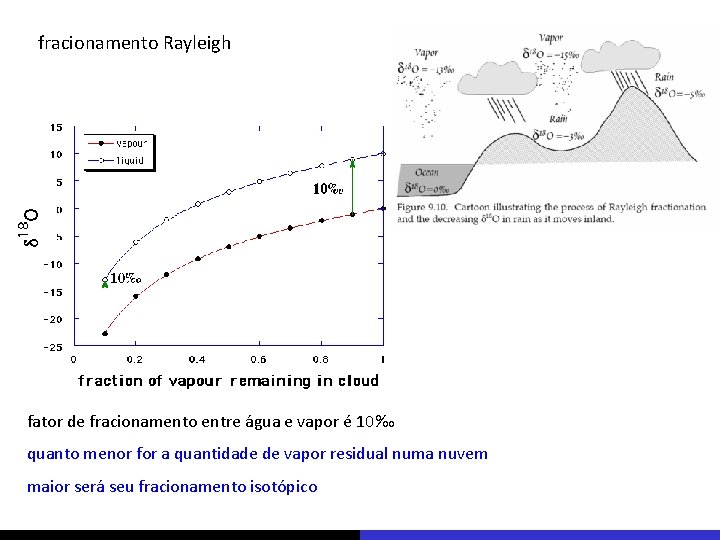
fracionamento Rayleigh fator de fracionamento entre água e vapor é 10‰ quanto menor for a quantidade de vapor residual numa nuvem maior será seu fracionamento isotópico
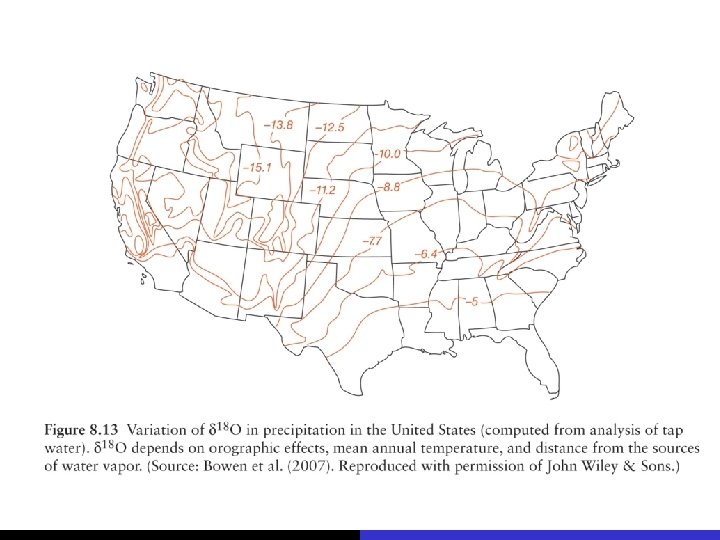
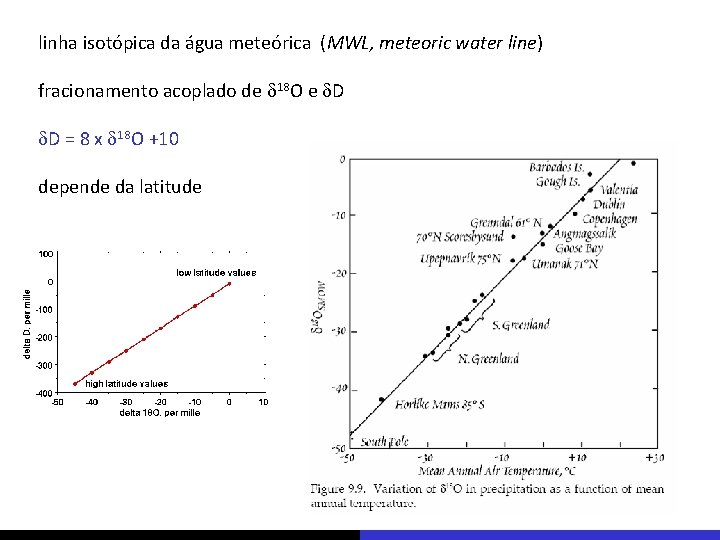
linha isotópica da água meteórica (MWL, meteoric water line) fracionamento acoplado de d 18 O e d. D = 8 x d 18 O +10 depende da latitude
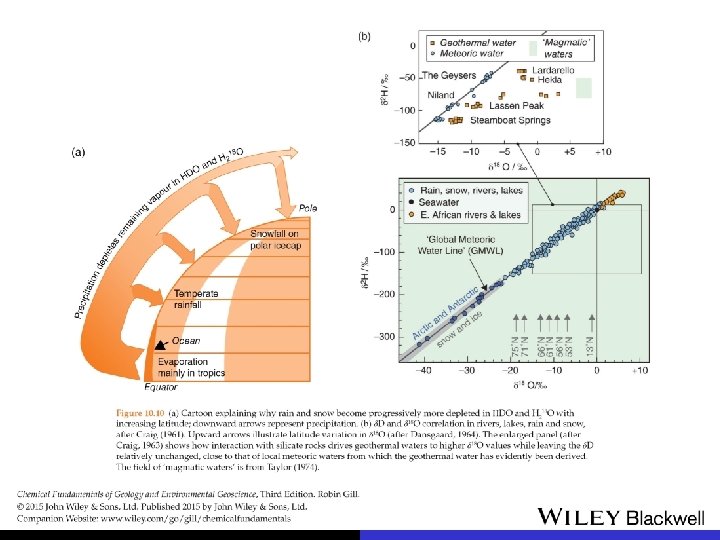
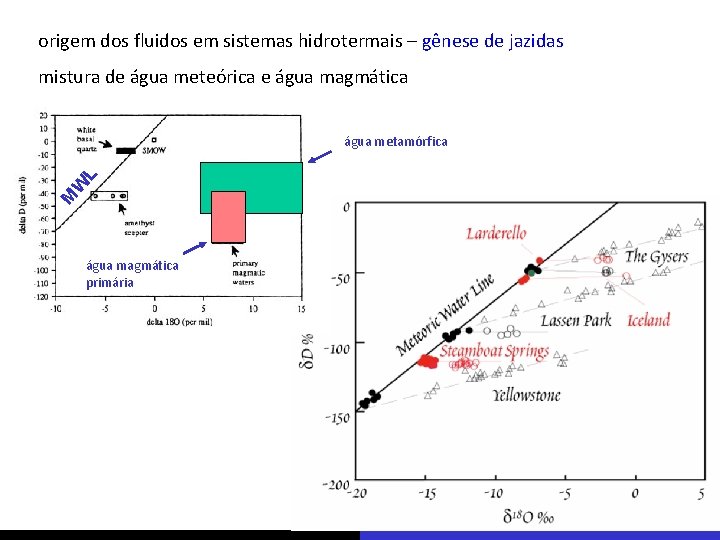
origem dos fluidos em sistemas hidrotermais – gênese de jazidas mistura de água meteórica e água magmática M W L água metamórfica água magmática primária
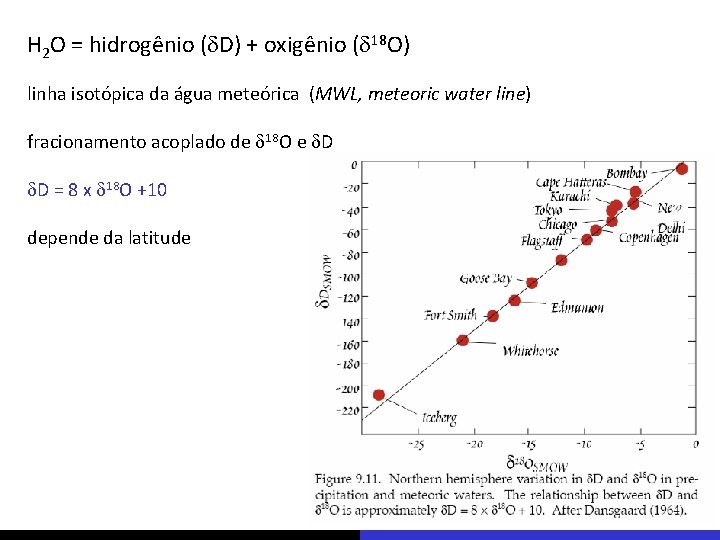
H 2 O = hidrogênio (d. D) + oxigênio (d 18 O) linha isotópica da água meteórica (MWL, meteoric water line) fracionamento acoplado de d 18 O e d. D = 8 x d 18 O +10 depende da latitude
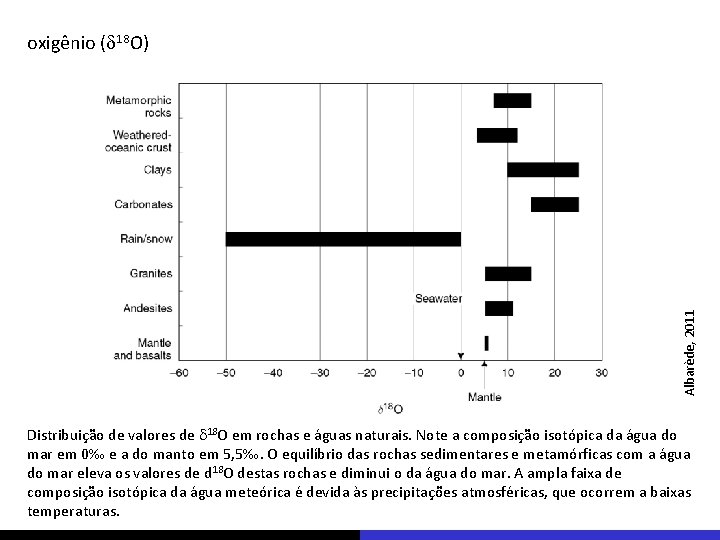
Albarède, 2011 oxigênio (d 18 O) Distribuição de valores de d 18 O em rochas e águas naturais. Note a composição isotópica da água do mar em 0‰ e a do manto em 5, 5‰. O equilíbrio das rochas sedimentares e metamórficas com a água do mar eleva os valores de d 18 O destas rochas e diminui o da água do mar. A ampla faixa de composição isotópica da água meteórica é devida às precipitações atmosféricas, que ocorrem a baixas temperaturas.
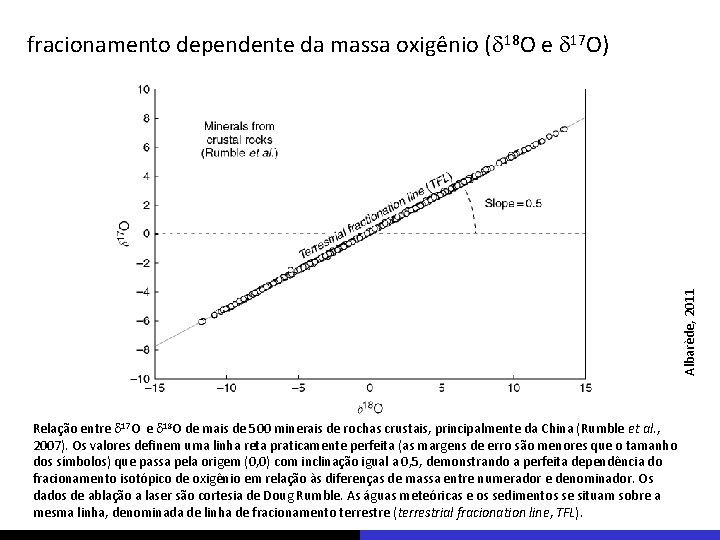
Albarède, 2011 fracionamento dependente da massa oxigênio (d 18 O e d 17 O) Relação entre d 17 O e d 18 O de mais de 500 minerais de rochas crustais, principalmente da China (Rumble et al. , 2007). Os valores definem uma linha reta praticamente perfeita (as margens de erro são menores que o tamanho dos símbolos) que passa pela origem (0, 0) com inclinação igual a 0, 5, demonstrando a perfeita dependência do fracionamento isotópico de oxigênio em relação às diferenças de massa entre numerador e denominador. Os dados de ablação a laser são cortesia de Doug Rumble. As águas meteóricas e os sedimentos se situam sobre a mesma linha, denominada de linha de fracionamento terrestre (terrestrial fracionation line, TFL).
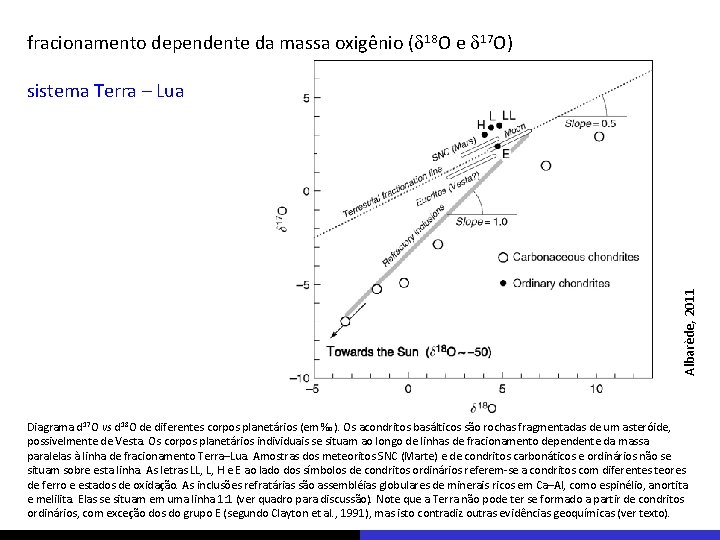
fracionamento dependente da massa oxigênio (d 18 O e d 17 O) Albarède, 2011 sistema Terra – Lua Diagrama d 17 O vs d 18 O de diferentes corpos planetários (em ‰). Os acondritos basálticos são rochas fragmentadas de um asteróide, possivelmente de Vesta. Os corpos planetários individuais se situam ao longo de linhas de fracionamento dependente da massa paralelas à linha de fracionamento Terra–Lua. Amostras dos meteoritos SNC (Marte) e de condritos carbonáticos e ordinários não se situam sobre esta linha. As letras LL, L, H e E ao lado dos símbolos de condritos ordinários referem-se a condritos com diferentes teores de ferro e estados de oxidação. As inclusões refratárias são assembléias globulares de minerais ricos em Ca–Al, como espinélio, anortita e melilita. Elas se situam em uma linha 1: 1 (ver quadro para discussão). Note que a Terra não pode ter se formado a partir de condritos ordinários, com exceção dos do grupo E (segundo Clayton et al. , 1991), mas isto contradiz outras evidências geoquímicas (ver texto).
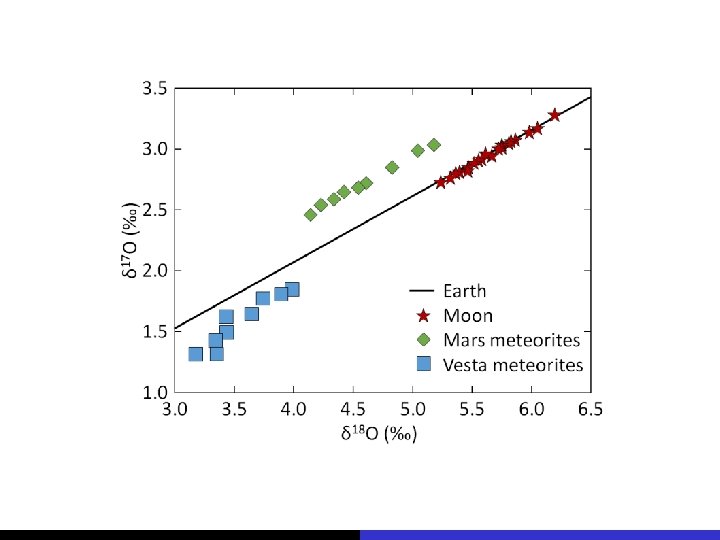
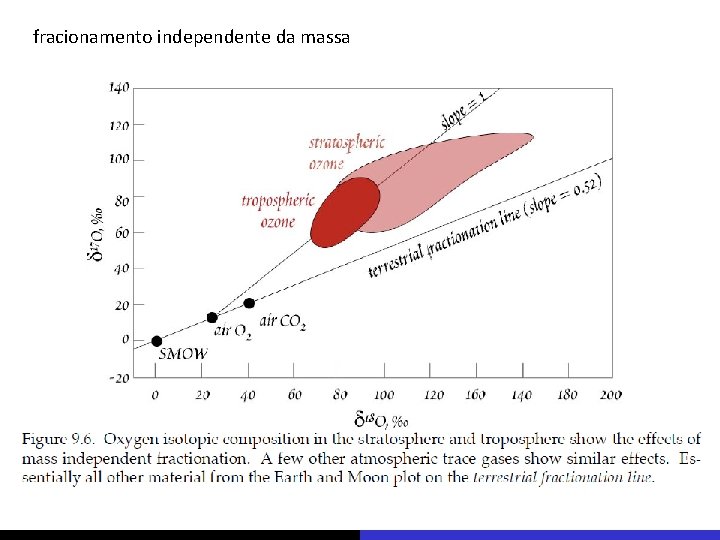
fracionamento independente da massa

enxofre (d 34 S) padrão CDT (Canyon Diablo Troilite – meteorito, Fe. S) d 34 S entre -30‰ em carvão e +60‰ em sulfatos 32 S prefere compostos com enxofre reduzido 34 S prefere compostos com enxofre oxidado principal mecanismo de fracionamento metabolismo de bactérias anaeróbicas
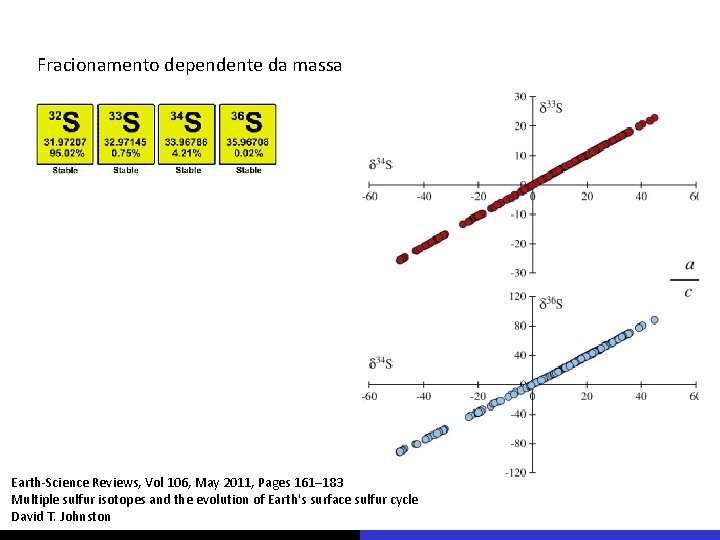
Fracionamento dependente da massa Earth-Science Reviews, Vol 106, May 2011, Pages 161– 183 Multiple sulfur isotopes and the evolution of Earth's surface sulfur cycle David T. Johnston
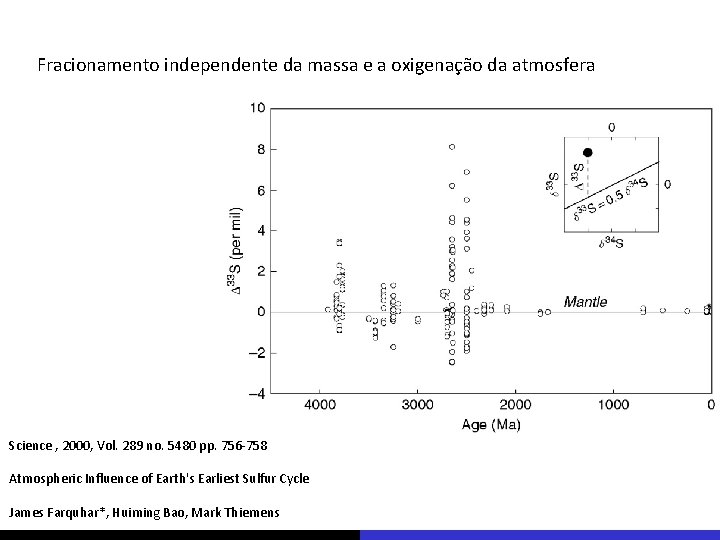
Fracionamento independente da massa e a oxigenação da atmosfera Science , 2000, Vol. 289 no. 5480 pp. 756 -758 Atmospheric Influence of Earth's Earliest Sulfur Cycle James Farquhar*, Huiming Bao, Mark Thiemens
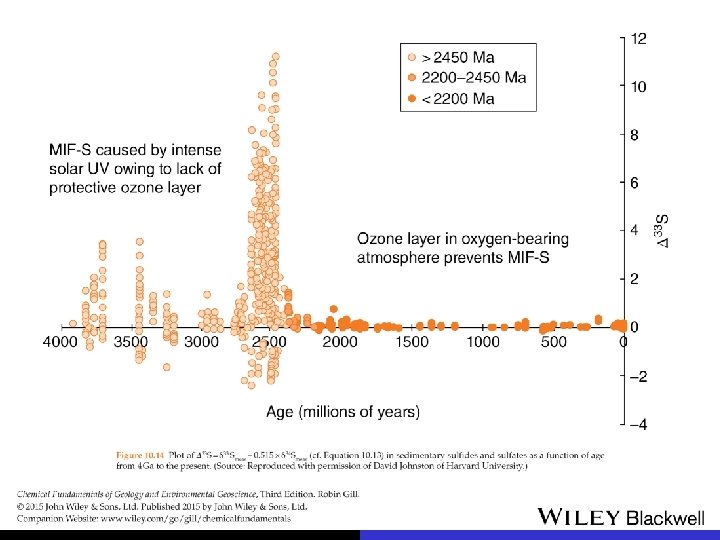

paleoclimatologia isotópica Urey (1947) estimar paleotemperatura dos oceanos a partir do fracionamento isotópico de oxigênio entre Ca. CO 3 e a água do mar D calcita-H 2 O fórmula empírica T (o. C) = 16, 9 – 4, 2 Dcal-H 2 O + 0, 13 D 2 cal-H 2 O reconstituição climática com base em carbonatos marinhos
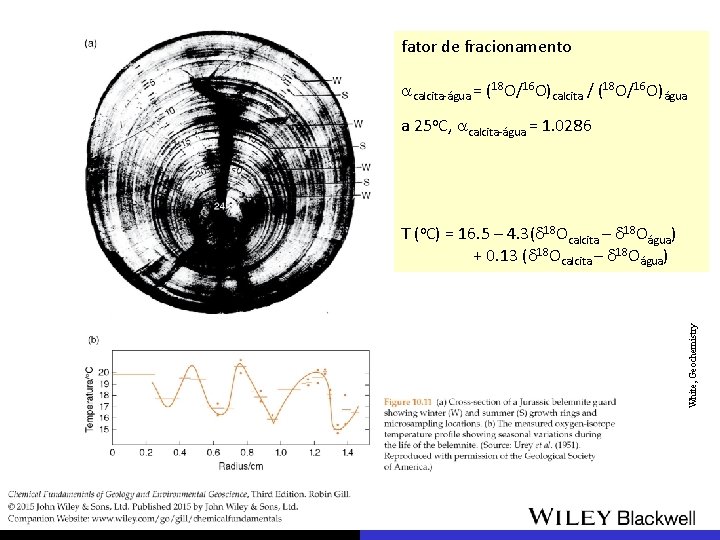
fator de fracionamento acalcita-água = (18 O/16 O)calcita / (18 O/16 O)água a 25 o. C, acalcita-água = 1. 0286 White, Geochemistry T (o. C) = 16. 5 – 4. 3(d 18 Ocalcita – d 18 Oágua) + 0. 13 (d 18 Ocalcita – d 18 Oágua)
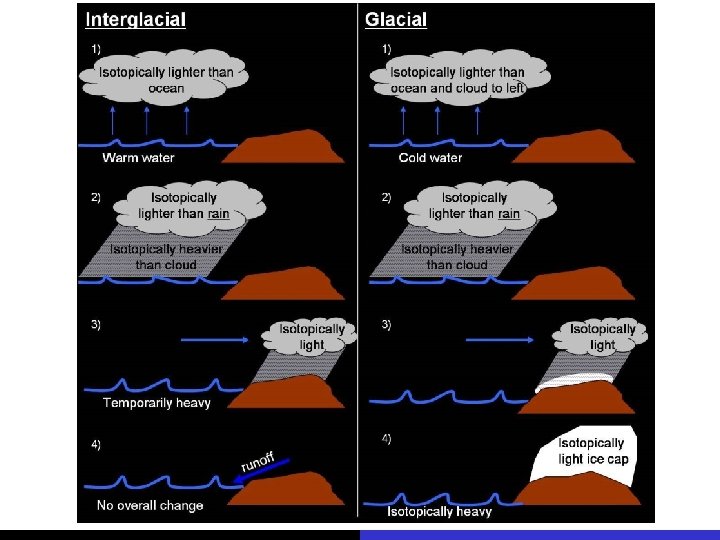
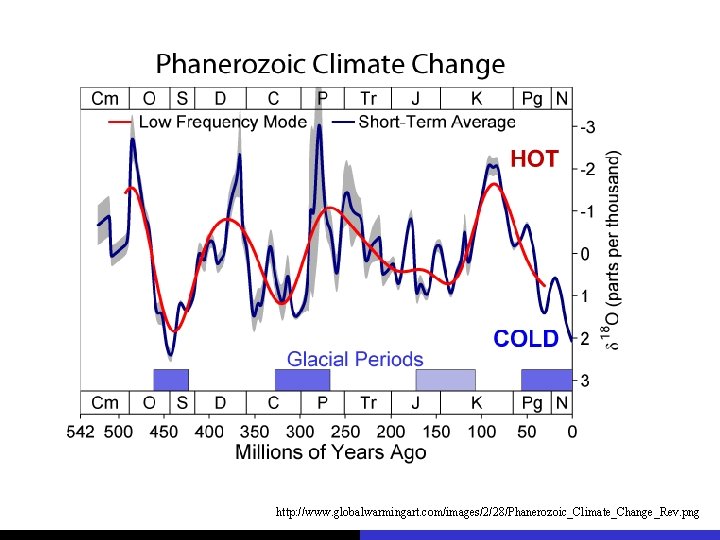
http: //www. globalwarmingart. com/images/2/28/Phanerozoic_Climate_Change_Rev. png
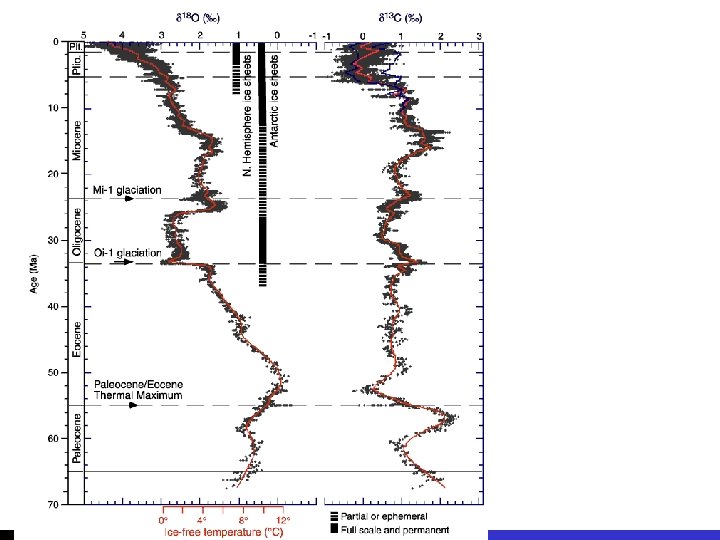

efeito vital: os seres vivos concentram 12 C em seus tecidos rastreamento das mais antigas evidências de vida http: //www. carleton. edu/departments/GEOL/Dave. STELLA/Carbon/c_isotope_models. htm isótopos de carbono e atividade biológica
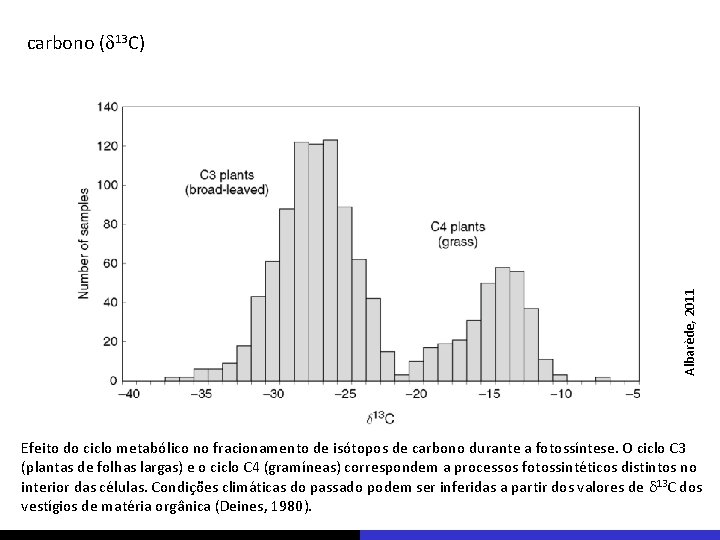
Albarède, 2011 carbono (d 13 C) Efeito do ciclo metabólico no fracionamento de isótopos de carbono durante a fotossíntese. O ciclo C 3 (plantas de folhas largas) e o ciclo C 4 (gramíneas) correspondem a processos fotossintéticos distintos no interior das células. Condições climáticas do passado podem ser inferidas a partir dos valores de d 13 C dos vestígios de matéria orgânica (Deines, 1980).
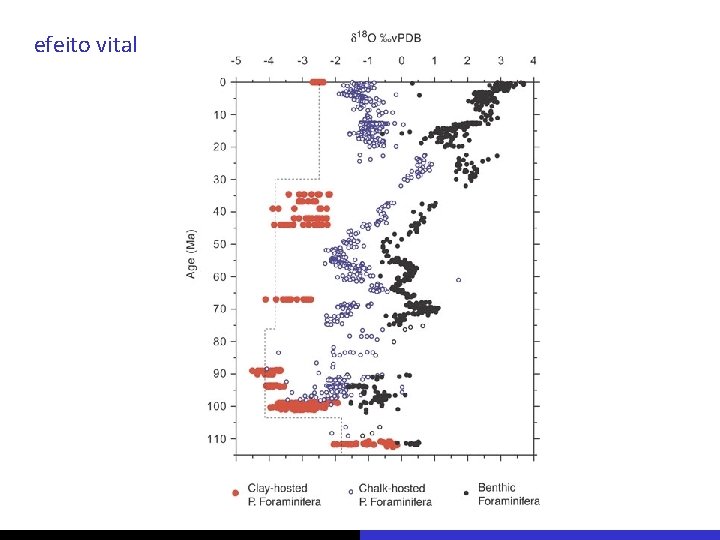
efeito vital
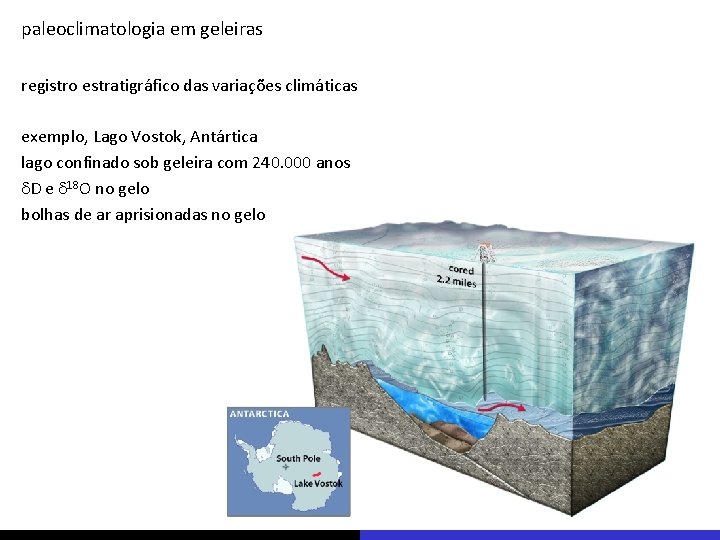
paleoclimatologia em geleiras registro estratigráfico das variações climáticas exemplo, Lago Vostok, Antártica lago confinado sob geleira com 240. 000 anos d. D e d 18 O no gelo bolhas de ar aprisionadas no gelo
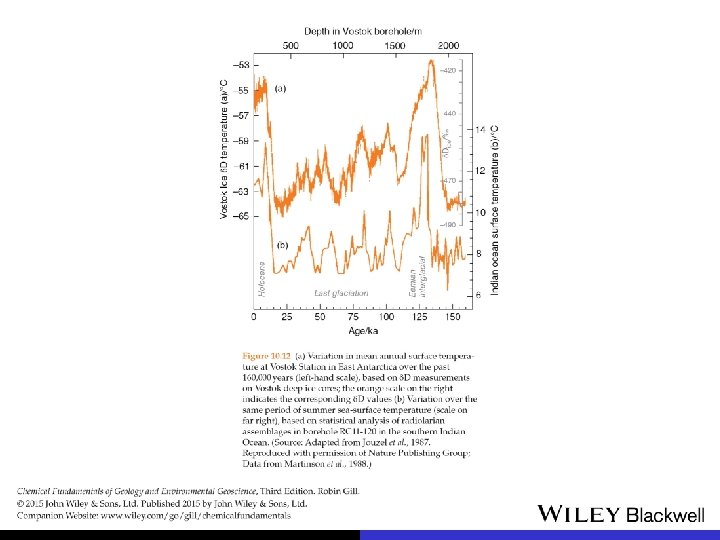
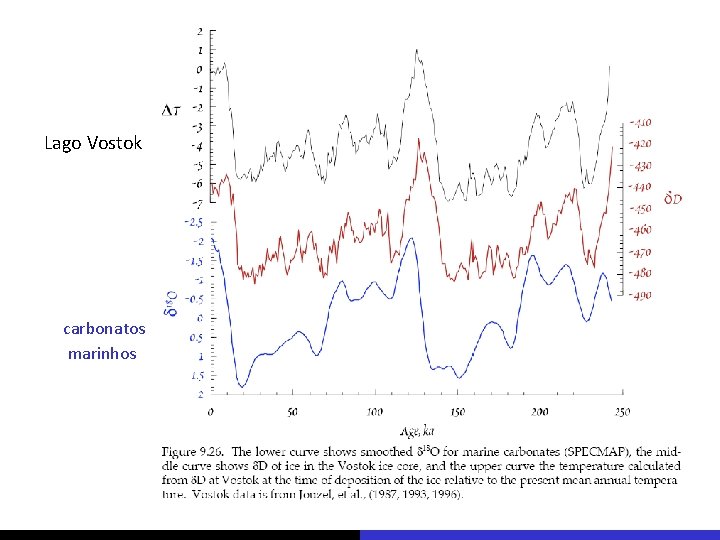
Lago Vostok carbonatos marinhos
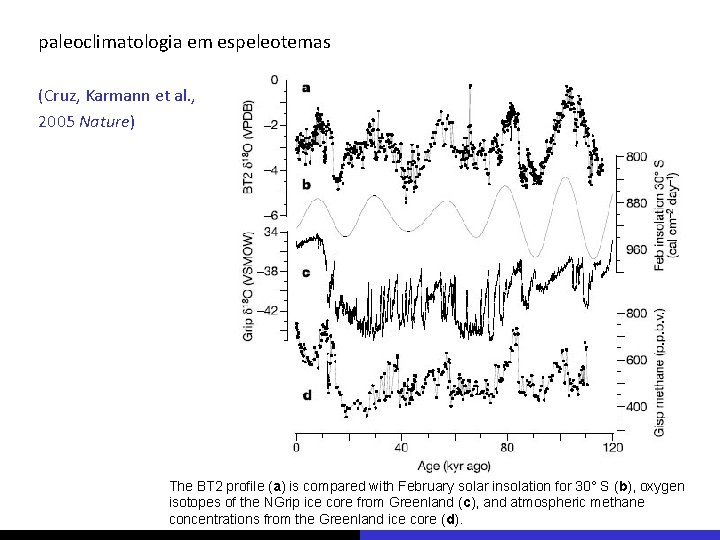
paleoclimatologia em espeleotemas (Cruz, Karmann et al. , 2005 Nature) The BT 2 profile (a) is compared with February solar insolation for 30° S (b), oxygen isotopes of the NGrip ice core from Greenland (c), and atmospheric methane concentrations from the Greenland ice core (d).
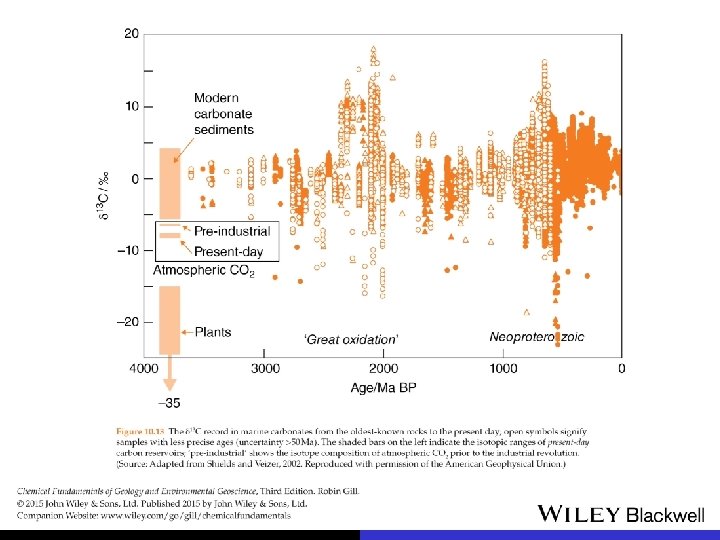

geotermômetros isotópicos – alta temperatura exemplos pares quartzo - mineral
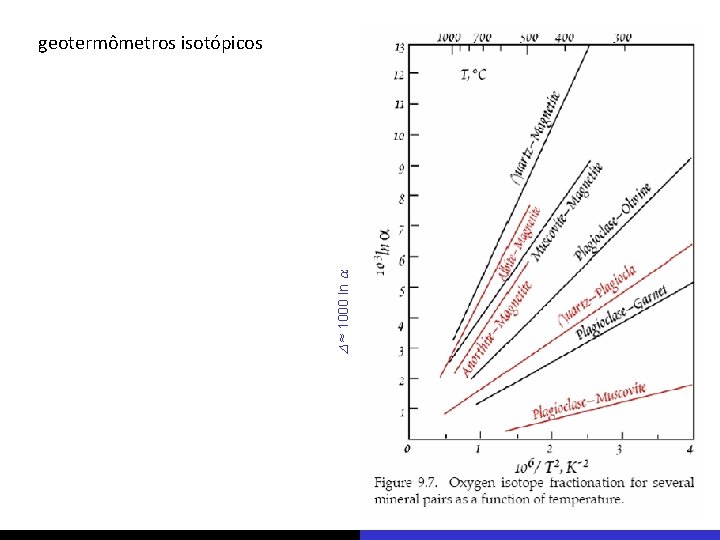
D ≈ 1000 ln a geotermômetros isotópicos
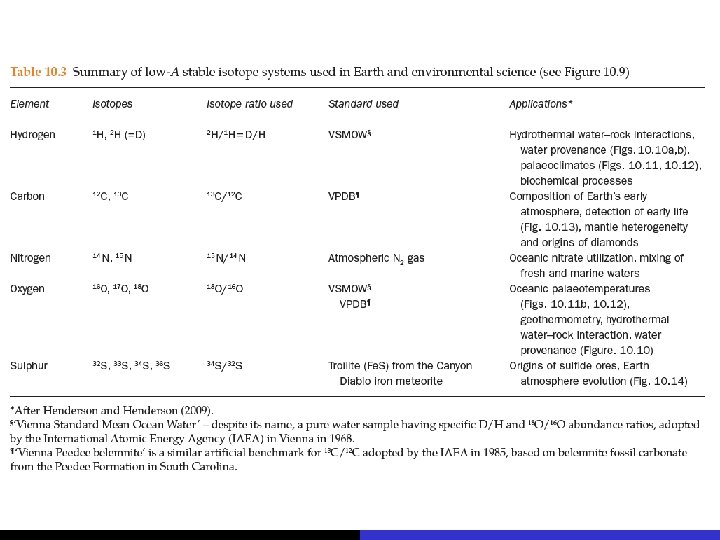

Referências Gill, Chemical Fundamentals of Geology, 2015, Capítulo 10 Hoefs, 2004. Stable isotope geochemistry, 6ª. edição Capítulo 1 Albarède, 2011. Geoquímica. Caps. 3 e 9 White, Geochemistry, Capítulo 9 White, Isotope Geochemistry, 2016
- Slides: 60