ISOMERIA Prof Ren Machado Isomeria Este fenmeno ocorre




























- Slides: 40

ISOMERIA Prof. : Renê Machado

Isomeria Este fenômeno ocorre com duas ou mais substâncias orgânicas diferentes que apresentam a mesma fórmula molecular. Ex. com a fórmula C 3 H 6 O, tem-se os compostos: CH 3 – CH 3 e CH 3 – CH 2 – C – H | | O (propanona) (propanal) que pertencem a funções diferentes.

Existem vários isômeros, que se dividem em dois tipos: Isomeria plana: compostos que apresentam diferença na fórmula estrutural plana. Ø Ø Isomeria espacial: composto que apresentam igual fórmula estrutural plana e diferentes fórmulas estruturais espaciais.

1) Isomeria plana Existem varias formas de isomeria plana: De cadeia De posição De função ou funcional De compensação ou metameria De tautomerização ou tautomeria

a) Isomeria de cadeia Ocorre em compostos, que pertencem a mesma função orgânica e diferem na cadeia principal. Ex. C 4 H 10 CH 3 – CH 2 – CH 3 (butano) CH 3 – CH 3 (metil - propano) | CH 3 Ambos são hidrocarbonetos, porém diferem na cadeia principal, onde uma tem 4 carbonos (sendo normal) e a outra tem 3 carbonos (sendo ramificada).

Ex. C 4 H 8 CH 3 – CH 2 – CH = CH 2 ( 1 -buteno) CH 2 – CH 2 | ( ciclo butano ) CH 2 – CH 2 Ambos são hidrocarbonetos, porém diferem na cadeia principal, onde uma tem 4 carbonos (sendo fechada e insaturada) e a outra também tem 4 carbonos (sendo aberta e saturada).

Ex. C 2 H 7 N CH 3 – CH 2 – NH 2 (etilamina) CH 3 – N – CH 3 (N - metilamina) | H Ambos são aminas, porém diferem na cadeia principal, onde uma é homogênea e a outra é heterogênea.

Ex. C 7 H 16 CH 3 – CH 2 – CH 3 | (3 -metil-hexano) CH 3 CH 2 – CH 2 – CH 3 | (3 -etil-pentano) CH 2– CH 3 Ambos são hidrocarbonetos, porém diferem na cadeia principal, onde uma tem 6 carbonos (sendo um ramificação com 2 carbonos) e a outra tem 5 carbonos (sendo um ramificação com 1 carbono).

b) Isomeria de posição Ocorre em compostos, que pertencem a mesma função orgânica, com igual cadeia principal que diferem na posição de uma ramificação, ou de uma insaturação (dupla ou tripla ligação), ou de um grupo funcional.

Ex. C 6 H 14 2 CH 3 – CH 2– CH 3 | (2 -metil-pentano ) CH 3 3 CH 3 – CH 2– CH 3 | ( 3 -metil-pentano ) CH 3 Ambos são hidrocarbonetos, porém diferem na posição da ramificação. Uma está no carbono número 2 e outra no carbono 3 da cadeia principal.

Ex. C 5 H 10 CH 3 – C = CH – CH 3 | ( 2 -metil – but - 2 - eno ) CH 3 CH 2 = C – CH 2 – CH 3 | ( 2 -metil – but - 1 -eno ) CH 3 Ambos são hidrocarbonetos com ramificações em igual posição, porém diferem na posição da insaturação. Uma está no carbono número 1 e outra no carbono 2 da cadeia principal.

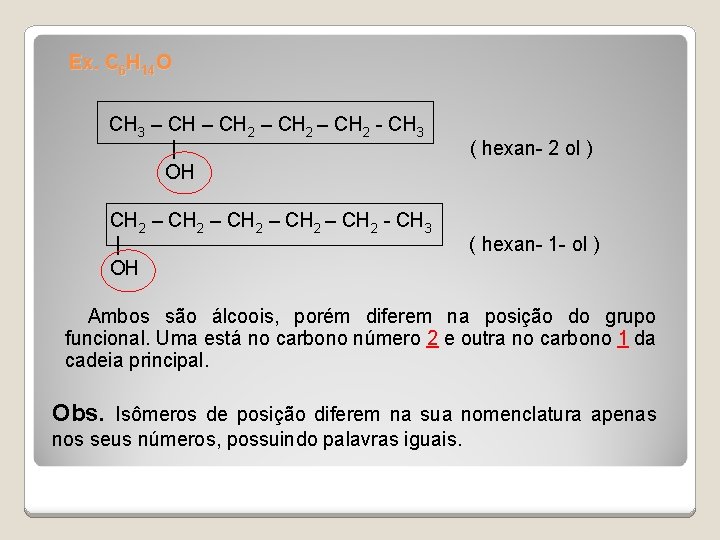
Ex. C 6 H 14 O CH 3 – CH 2 - CH 3 | ( hexan- 2 ol ) OH CH 2 – CH 2 - CH 3 | ( hexan- 1 - ol ) OH Ambos são álcoois, porém diferem na posição do grupo funcional. Uma está no carbono número 2 e outra no carbono 1 da cadeia principal. Obs. Isômeros de posição diferem na sua nomenclatura apenas nos seus números, possuindo palavras iguais.

c) isomeria de função ou funcional Ocorre em compostos, que pertencem a funções orgânicas e diferentes, independente de sua cadeia principal. Ø álcool e éter (Cn. H 2 n+2 O) Ex. C 4 H 10 O CH 3 – CH 2 – CH 3 | ( 2 -butanol ) OH CH 3 – CH 2 – O – CH 2 – CH 3 ( etoxi-etano )

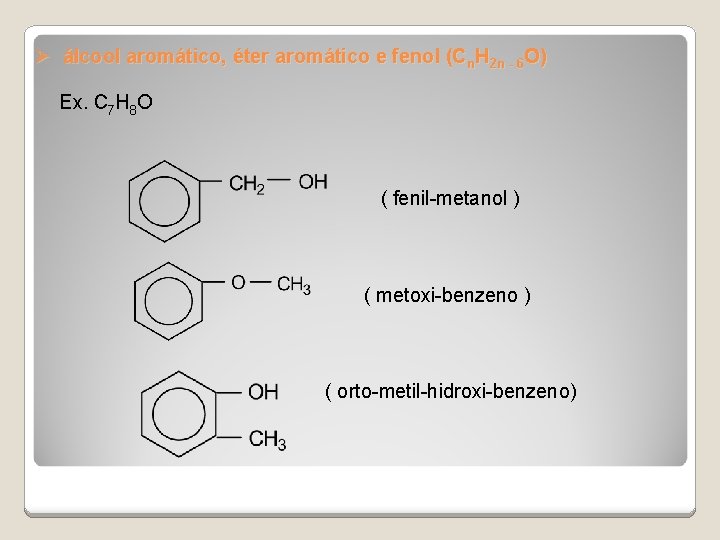
Ø álcool aromático, éter aromático e fenol (Cn. H 2 n - 6 O) Ex. C 7 H 8 O ( fenil-metanol ) ( metoxi-benzeno ) ( orto-metil-hidroxi-benzeno)

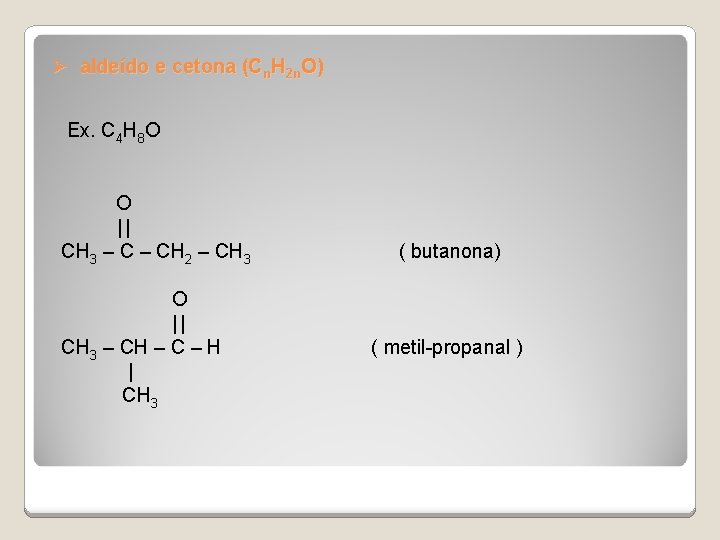
Ø aldeído e cetona (Cn. H 2 n. O) Ex. C 4 H 8 O O | | CH 3 – CH 2 – CH 3 ( butanona) O | | CH 3 – CH – C – H ( metil-propanal ) | CH 3

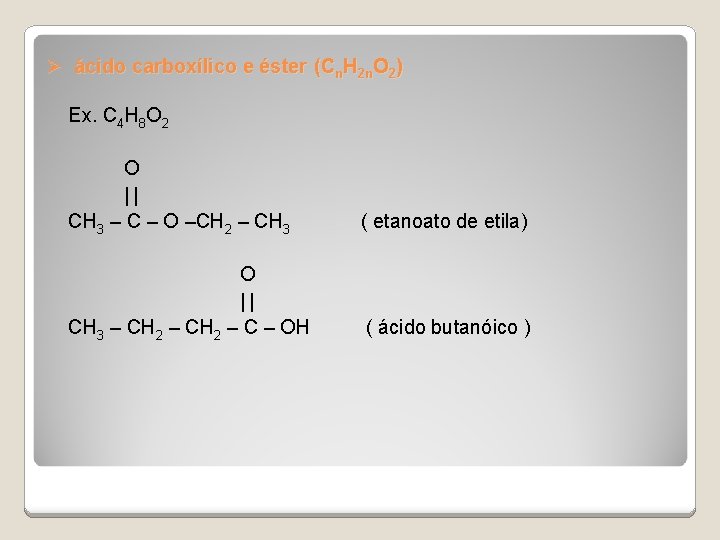
Ø ácido carboxílico e éster (Cn. H 2 n. O 2) Ex. C 4 H 8 O 2 O | | CH 3 – C – O –CH 2 – CH 3 ( etanoato de etila) O | | CH 3 – CH 2 – C – OH ( ácido butanóico )

d) isomeria de compensação ou metameria É um tipo especial de isomeria de posição que corre em compostos, que pertencem a mesma função orgânica, diferem na posição de um heteroátomo. Lembrete: Um heteroátomo é um elemento organógeno ligado entre dois carbonos.

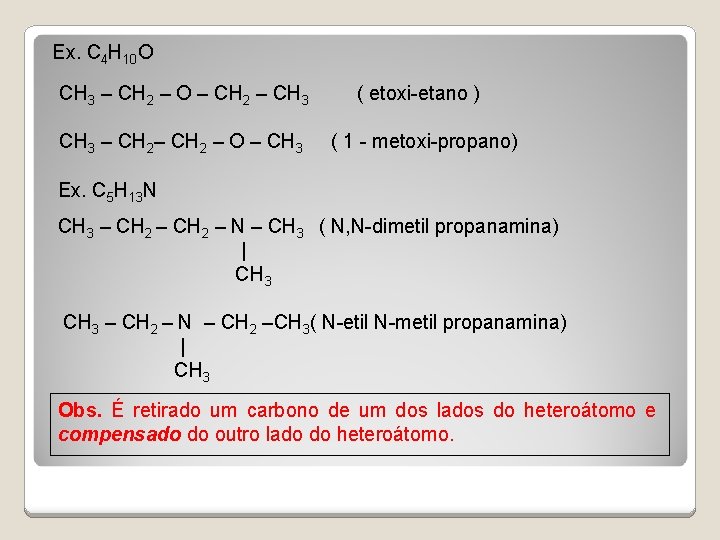
Ex. C 4 H 10 O CH 3 – CH 2 – O – CH 2 – CH 3 ( etoxi-etano ) CH 3 – CH 2 – O – CH 3 ( 1 - metoxi-propano) Ex. C 5 H 13 N CH 3 – CH 2 – N – CH 3 ( N, N-dimetil propanamina) | CH 3 – CH 2 – N – CH 2 –CH 3( N-etil N-metil propanamina) | CH 3 Obs. É retirado um carbono de um dos lados do heteroátomo e compensado do outro lado do heteroátomo.

e) tautomeria ou tautomerização É um caso particular de isomeria de função, em que os compostos estabelecem um equilíbrio químico. Esse tipo também é chamado de isomeria dinâmica, que possui duas formas: ü aldoenólica: entre aldeído e enol ü cetoenólica: entre cetona e enol

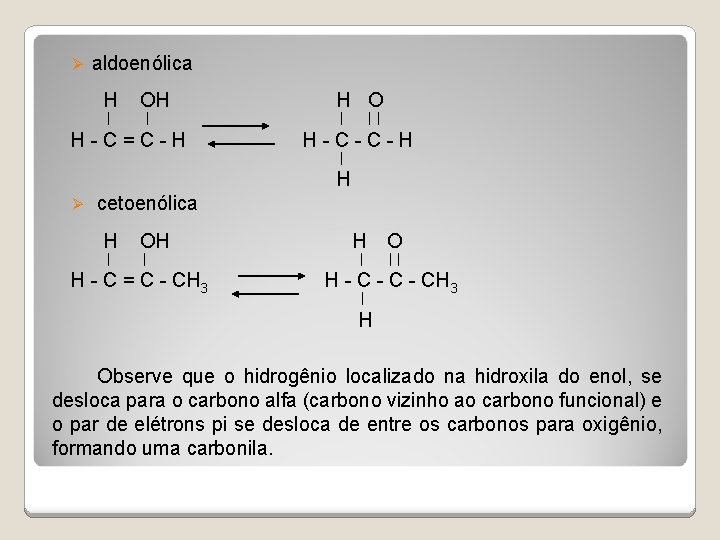
Ø aldoenólica H OH H O H - C = C - H H - C - H H Ø cetoenólica H OH H O H - C = C - CH 3 H - C - CH 3 H Observe que o hidrogênio localizado na hidroxila do enol, se desloca para o carbono alfa (carbono vizinho ao carbono funcional) e o par de elétrons pi se desloca de entre os carbonos para oxigênio, formando uma carbonila.

Alguns aldeídos e cetonas não irão realizar tautomeria, pois não possuem hidrogênio alfa (átomo de hidrogênio ligado a carbono alfa). CH 3 O CH 3 -C - H CH 3

2) Isomeria espacial Divide-se em geométrica e ótica e também é chamada de estereoisomeria.

Isomeria Geométrica ou Cis-Trans.

isomeria geométrica em composto de cadeia alifática. Para que ocorra isomeria geométrica é necessário que o composto seja derivado de um alceno, ou seja, apresente um dupla ligação na cadeia e ligantes diferentes em cada um dos carbonos insaturados da dupla (R 1 R 2 e R 3 R 4) Obs. : pode haver ligantes iguais em carbonos diferentes da dupla. R 1 R 3 C = C R 2 R 4

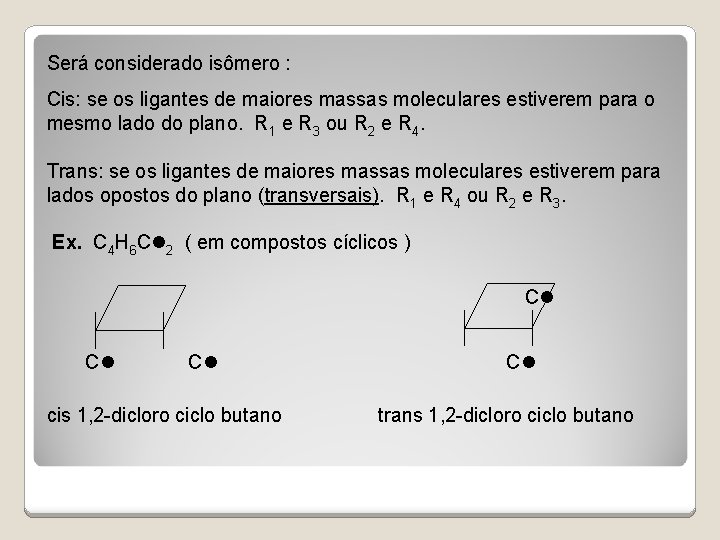
Será considerado isômero : Cis: se os ligantes de maiores massas moleculares estiverem para o mesmo lado do plano. R 1 e R 3 ou R 2 e R 4. Trans: se os ligantes de maiores massas moleculares estiverem para lados opostos do plano (transversais). R 1 e R 4 ou R 2 e R 3.

Ex. : 2 -bromo-but -2 - eno CH 3 – CH = CH – CH 3 Br Através da fórmula estrutural plana não é possível identificar o tipo de isomeria geométrica, mostrando, somente, que o composto forma isomeria geométrica. Dadas as massa moleculares: Br = 80, CH 3 = 15 e H = 1 Observe que no primeiro carbono insaturado o grupo formado pelo metil apresenta maior massa molecular e no segundo carbono insaturado o grupo formado pelo bromo tem massa molecular maior .

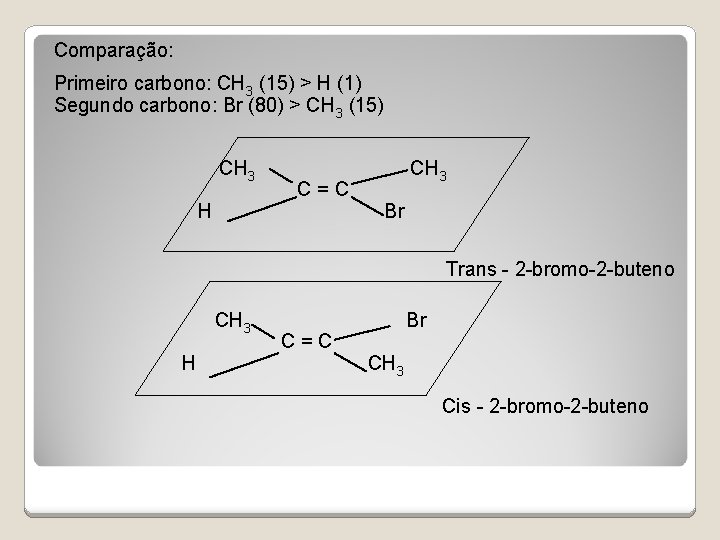
Comparação: Primeiro carbono: CH 3 (15) > H (1) Segundo carbono: Br (80) > CH 3 (15) CH 3 C = C H Br Trans - 2 -bromo-2 -buteno CH 3 Br C = C H CH 3 Cis - 2 -bromo-2 -buteno

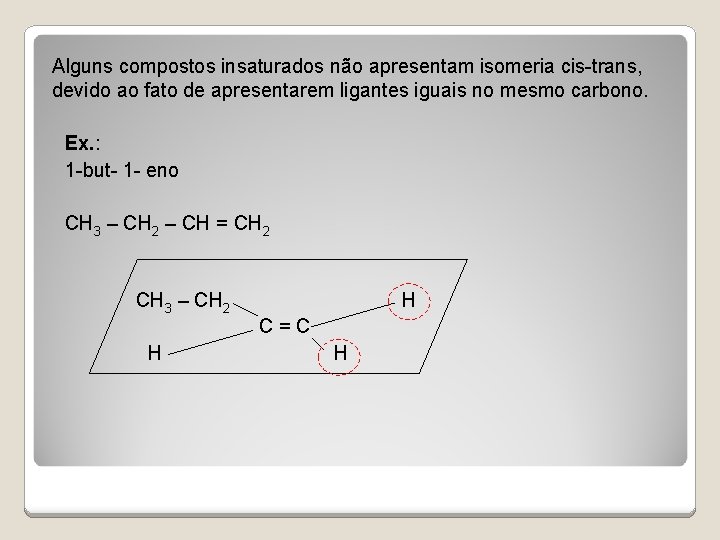
Alguns compostos insaturados não apresentam isomeria cis-trans, devido ao fato de apresentarem ligantes iguais no mesmo carbono. Ex. : 1 -but- 1 - eno CH 3 – CH 2 – CH = CH 2 CH 3 – CH 2 H C = C H H

isomeria geométrica em composto de cadeia fechada. Para que ocorra isomeria geométrica é necessário que o composto seja derivado de um cicloalcano, e ligantes diferentes em cada um dos carbonos vizinhos (R 1 R 2 e R 3 R 4) R 1 R 3 R 2 R 4

Será considerado isômero : Cis: se os ligantes de maiores massas moleculares estiverem para o mesmo lado do plano. R 1 e R 3 ou R 2 e R 4. Trans: se os ligantes de maiores massas moleculares estiverem para lados opostos do plano (transversais). R 1 e R 4 ou R 2 e R 3. Ex. C 4 H 6 C 2 ( em compostos cíclicos ) C C C cis 1, 2 -dicloro ciclo butano trans 1, 2 -dicloro ciclo butano

Isomeria óptica.

Isomeria óptica. Os estereoisômeros ópticos desviam o plano da luz polarizada para lados opostos. Luz natural : como toda luz, possui um campo magnético e um campo elétrico perpendiculares entre si e que giram em torno do eixo de propagação. Luz polarizada: é proveniente de uma luz natural que atravessou um prisma polarizador e tem seu campo elétrico e seu campo magnético ainda perpendiculares entre si, porém agora, não giram mais em torno do eixo de propagação. Essa diferença não é possível de ser distinguida a olho nu.

Um composto para ser opticamente ativo precisa conter um carbono quiral (assimétrico). Carbono quiral: carbono saturado que apresenta 4 grupos ligantes diferentes entre si. R 2 R 1 – C – R 3 R 4 onde R 1 R 2 R 3 R 4

Ex. 1 2 -butanol (álcool com menor massa molecular que apresenta carbono quiral). Grupos ligantes: H CH 3 OH C 2 H 5 CH 3 – CH 2 – CH 3 OH O 2 -butanol apresenta dois estereoisômeros, chamados de enantiômeros ou antípodas ópticas.

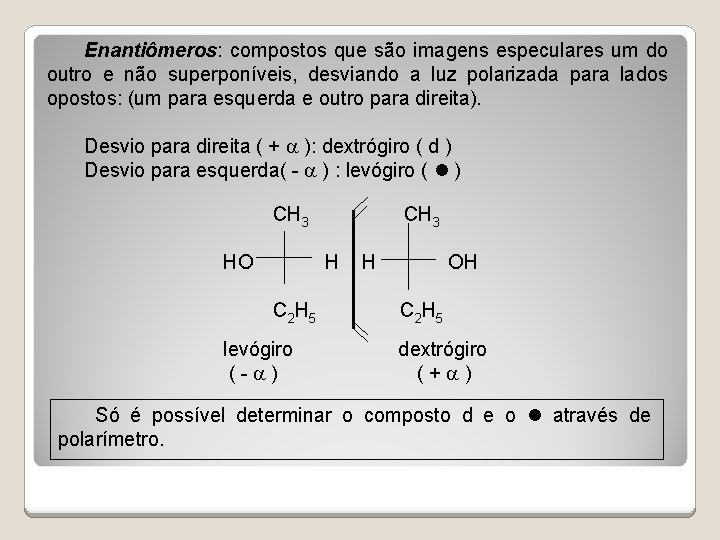
Enantiômeros: compostos que são imagens especulares um do outro e não superponíveis, desviando a luz polarizada para lados opostos: (um para esquerda e outro para direita). Desvio para direita ( + ): dextrógiro ( d ) Desvio para esquerda( - ) : levógiro ( ) CH 3 HO H H OH C 2 H 5 levógiro dextrógiro ( - ) ( + ) Só é possível determinar o composto d e o através de polarímetro.

ESTRUTURAS DE FISCHER Trabalhar com fórmulas espaciais como o fizemos para o d-2 -butanol e -2 -butanol fica muito difícil. Para facilitar o estudo e compreensão das substâncias que apresentam carbono quiral (assimétrico) e conseqüentemente isomeria óptica, passaremos a utilizar as Fórmulas de Projeção de Fischer. As convenções de Fischer são as seguintes: 1º) A molécula é representada em forma de cruz. 2º) Fica subentendido que cada carbono quiral (assimétrico) está localizada na intercessão das hastes que formam a cruz. 3º) Na linha vertical ficará a cadeia carbônica principal.

Exemplo : Consideremos a estrutura do ácido 2 - hidroxipropanóico (ácido lático): CH 3 – CH – COOH | CH 3

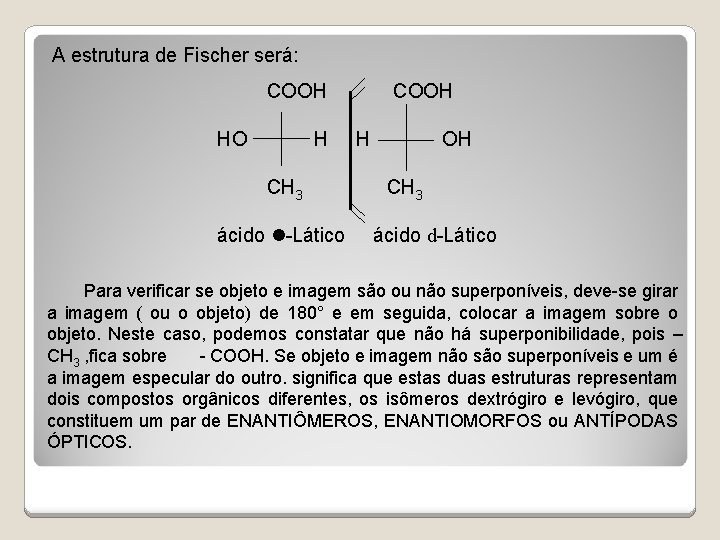
A estrutura de Fischer será: COOH HO H H OH CH 3 ácido -Lático ácido d-Lático Para verificar se objeto e imagem são ou não superponíveis, deve-se girar a imagem ( ou o objeto) de 180° e em seguida, colocar a imagem sobre o objeto. Neste caso, podemos constatar que não há superponibilidade, pois – CH 3 , fica sobre - COOH. Se objeto e imagem não superponíveis e um é a imagem especular do outro. significa que estas duas estruturas representam dois compostos orgânicos diferentes, os isômeros dextrógiro e levógiro, que constituem um par de ENANTIÔMEROS, ENANTIOMORFOS ou ANTÍPODAS ÓPTICOS.

Podemos calcular o número de isômeros opticamente ativos através da fórmula: n 2 onde: n = número de carbonos quirais diferentes na molécula.

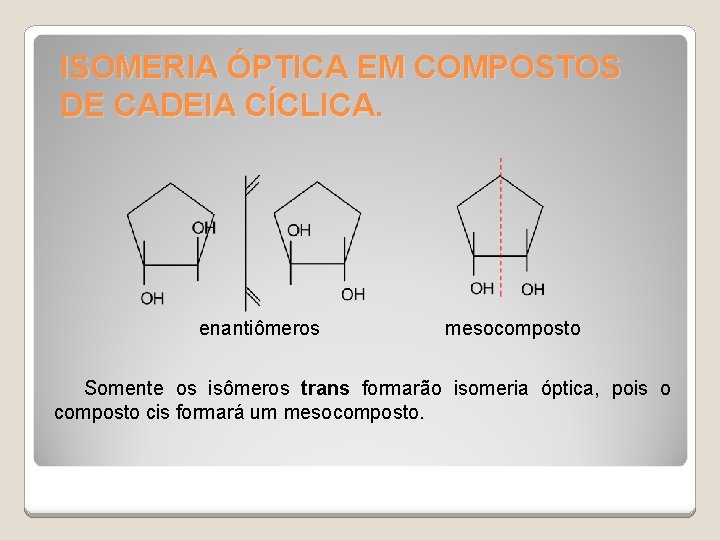
ISOMERIA ÓPTICA EM COMPOSTOS DE CADEIA CÍCLICA. enantiômeros mesocomposto Somente os isômeros trans formarão isomeria óptica, pois o composto cis formará um mesocomposto.