ISOMERIA Prof Agamenon Roberto carbonos H H H

ISOMERIA Prof. Agamenon Roberto
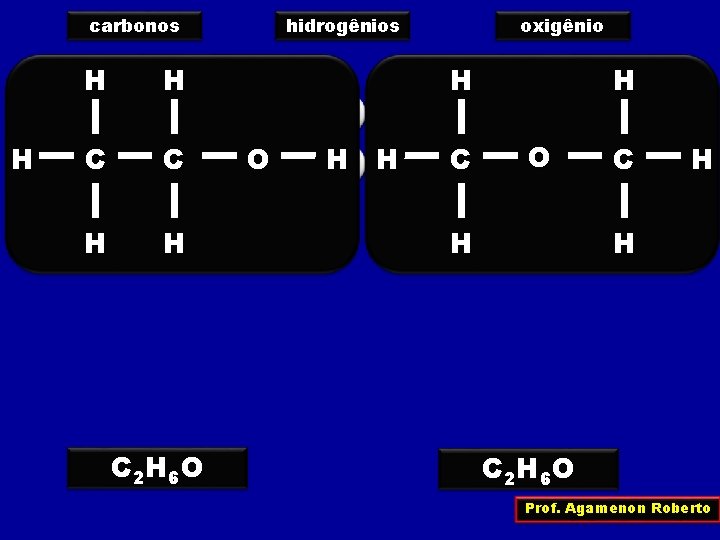
carbonos H H H C C H H C 2 H 6 O hidrogênios oxigênio H O H H C H O H C H H C 2 H 6 O Prof. Agamenon Roberto

Os compostos H 3 C – CH 2 – OH e H 3 C – O – CH 3 são ISÔMEROS são compostos diferentes que possuem a mesma fórmula molecular A este fenômeno damos o nome de ISOMERIA Prof. Agamenon Roberto

ISOMERIA pode ser Plana ou Constitucional Espacial ou estereoisomeria Ø Isomeria de cadeia. Ø Geométrica. Ø Isomeria de posição. Ø Óptica. Ø Isomeria de compensação. Ø Isomeria de função. Ø Isomeria de tautomeria Prof. Agamenon Roberto
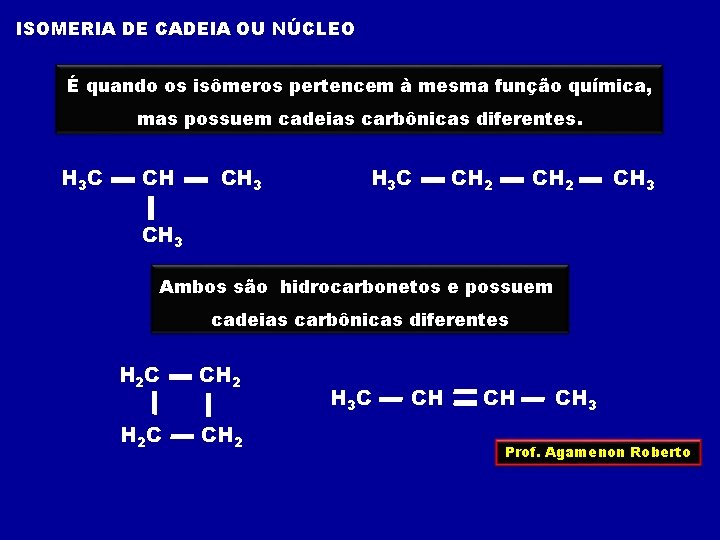
ISOMERIA DE CADEIA OU NÚCLEO É quando os isômeros pertencem à mesma função química, mas possuem cadeias carbônicas diferentes. H 3 C CH CH 3 H 3 C CH 2 CH 3 Ambos são hidrocarbonetos e possuem cadeias carbônicas diferentes H 2 C CH 2 H 3 C CH CH CH 3 Prof. Agamenon Roberto

ISOMERIA DE POSIÇÃO É quando os isômeros pertencem à mesma função química, mas diferem na posição de um substituinte ou insaturação H 2 C CH CH 2 CH 3 H 3 C CH CH CH 3 Ambos são hidrocarbonetos e diferem na posição da dupla ligação H 3 C CH OH CH 2 CH 3 H 2 C CH 2 CH 3 OH Ambos são alcoóis e diferem na posição da oxidrila Prof. Agamenon Roberto
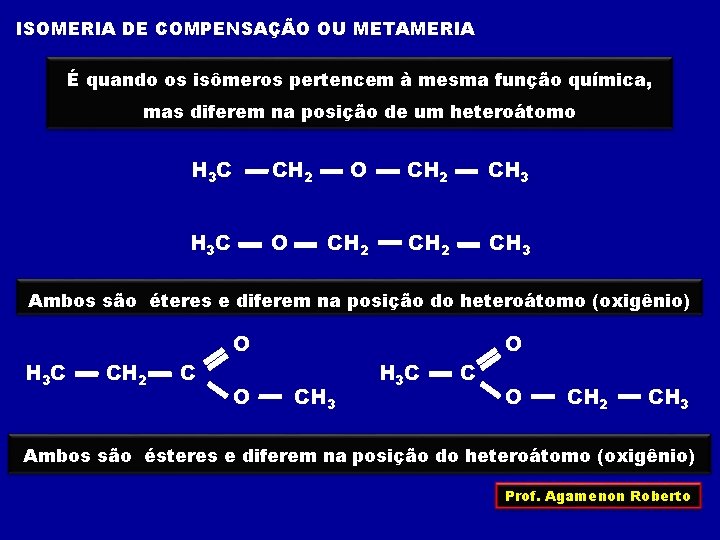
ISOMERIA DE COMPENSAÇÃO OU METAMERIA É quando os isômeros pertencem à mesma função química, mas diferem na posição de um heteroátomo H 3 C CH 2 H 3 C O O CH 2 CH 3 Ambos são éteres e diferem na posição do heteroátomo (oxigênio) H 3 C CH 2 C O O CH 3 H 3 C C O O CH 2 CH 3 Ambos são ésteres e diferem na posição do heteroátomo (oxigênio) Prof. Agamenon Roberto
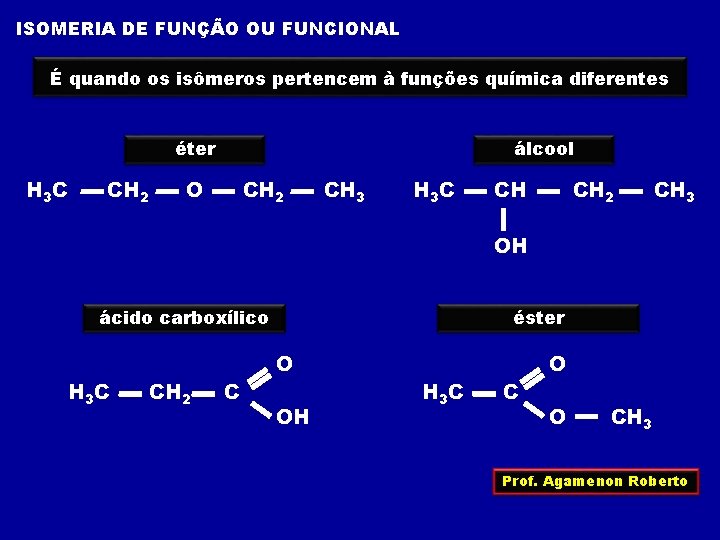
ISOMERIA DE FUNÇÃO OU FUNCIONAL É quando os isômeros pertencem à funções química diferentes éter H 3 C CH 2 álcool O CH 2 CH 3 H 3 C CH CH 2 CH 3 OH ácido carboxílico H 3 C CH 2 C éster O OH H 3 C C O O CH 3 Prof. Agamenon Roberto
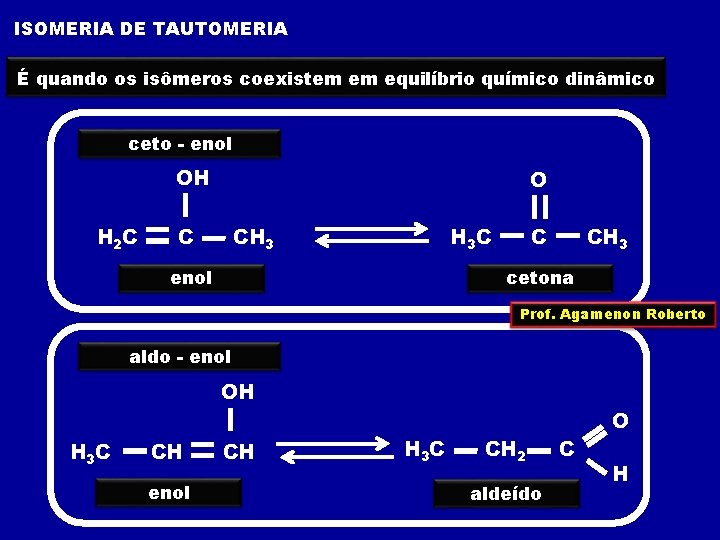
ISOMERIA DE TAUTOMERIA É quando os isômeros coexistem em equilíbrio químico dinâmico ceto - enol OH H 2 C O C CH 3 H 3 C enol C CH 3 cetona Prof. Agamenon Roberto aldo - enol OH H 3 C CH enol CH H 3 C CH 2 aldeído C O H
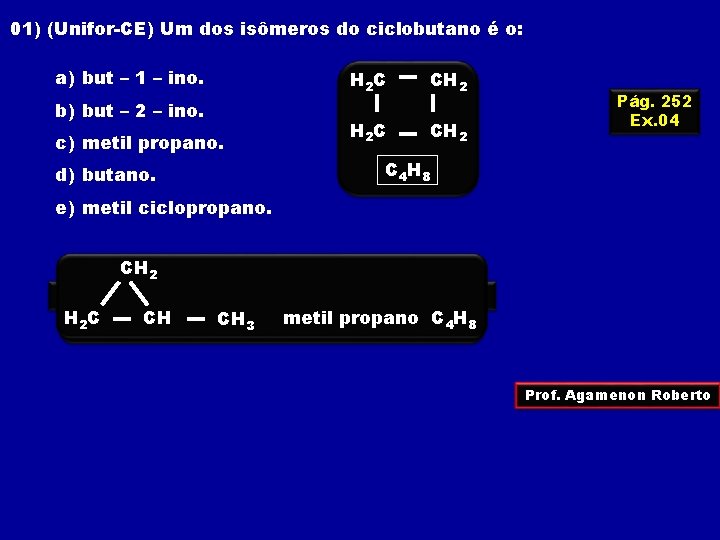
01) (Unifor-CE) Um dos isômeros do ciclobutano é o: a) but – 1 – ino. b) but – 2 – ino. c) metil propano. H 2 C CH 2 Pág. 252 Ex. 04 C 4 H 8 d) butano. e) metil ciclopropano. CH 2 metil propano : H 3 C – CH 3 C 4 H 10 1 – butino HC –CH CH butano 2 : H 3: C H – 3 CH CΞ– 2 C C – –CH ΞCH C 2 – 2– CH C C 444 H H 6610 33 3 H 2 C CH metil CH 3 CH propano C 4 H 8 3 Prof. Agamenon Roberto
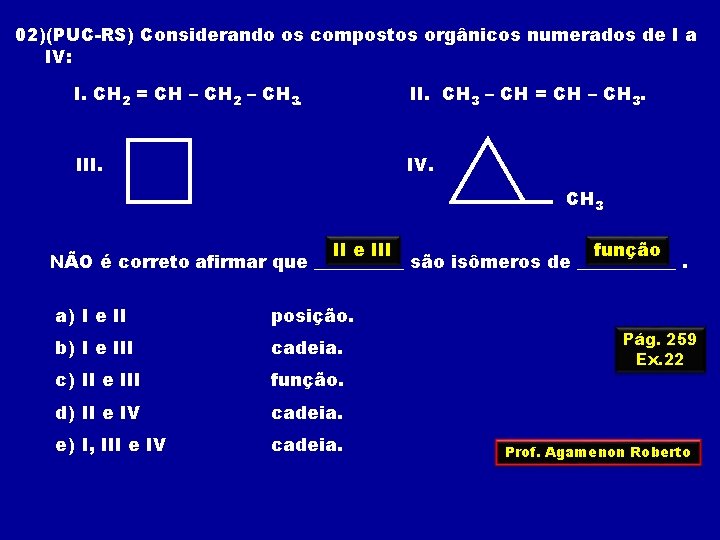
02)(PUC-RS) Considerando os compostos orgânicos numerados de I a IV: I. CH 2 = CH – CH 2 – CH 3. II. CH 3 – CH = CH – CH 3. III. IV. CH 3 II e III função NÃO é correto afirmar que _____ são isômeros de ______. a) I e II posição. b) I e III cadeia. c) II e III função. d) II e IV cadeia. e) I, III e IV cadeia. Pág. 259 Ex. 22 Prof. Agamenon Roberto
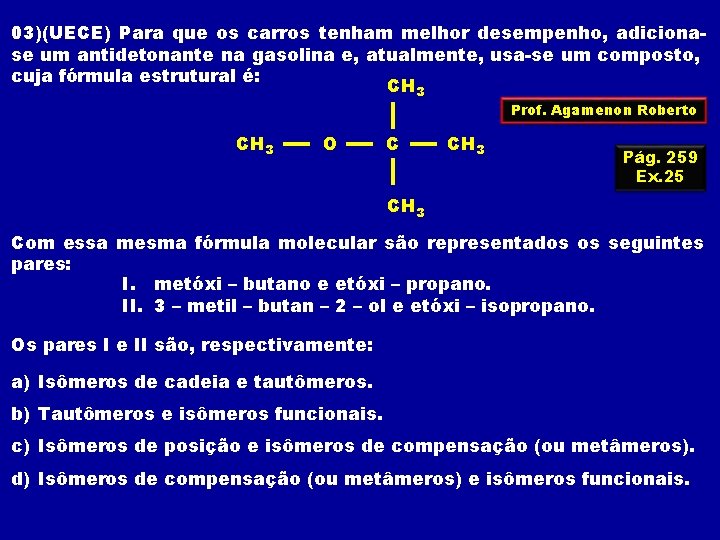
03)(UECE) Para que os carros tenham melhor desempenho, adicionase um antidetonante na gasolina e, atualmente, usa-se um composto, cuja fórmula estrutural é: CH 3 Prof. Agamenon Roberto CH 3 O C CH 3 Pág. 259 Ex. 25 CH 3 Com essa mesma fórmula molecular são representados os seguintes pares: I. metóxi – butano e etóxi – propano. II. 3 – metil – butan – 2 – ol e etóxi – isopropano. Os pares I e II são, respectivamente: a) Isômeros de cadeia e tautômeros. b) Tautômeros e isômeros funcionais. c) Isômeros de posição e isômeros de compensação (ou metâmeros). d) Isômeros de compensação (ou metâmeros) e isômeros funcionais.

É quando os isômeros apresentam as ligações entre seus átomos dispostas de maneira diferente no espaço Existem dois tipos de isomeria espacial Isomeria geométrica ou cis-trans. Isomeria óptica. Prof. Agamenon Roberto
Pode ocorrer em dois casos principais: Em compostos com duplas ligações. Em compostos cíclicos. Prof. Agamenon Roberto

Nos compostos com duplas ligações deveremos ter a seguinte estrutura: R 1 C=C R 2 R 1 R 3 R 2 e R 4 R 3 R 4 Prof. Agamenon Roberto
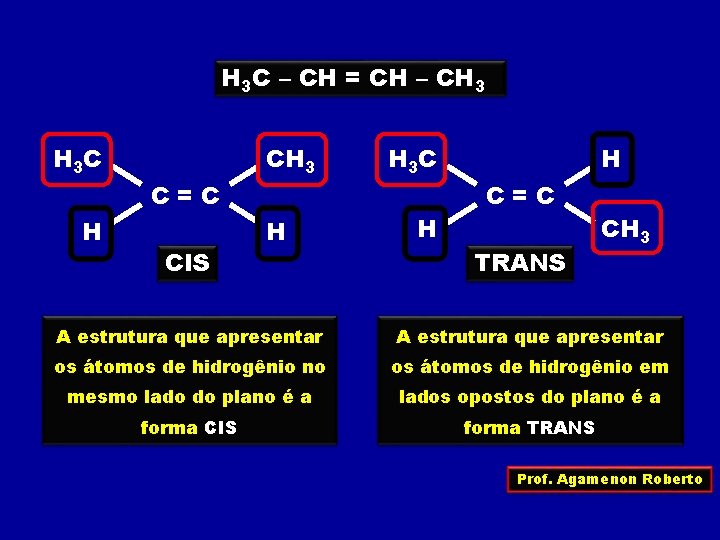
H 3 C – CH = CH – CH 3 C H C=C CIS CH 3 H H 3 C H H C=C TRANS CH 3 A estrutura que apresentar os átomos de hidrogênio no os átomos de hidrogênio em mesmo lado do plano é a lados opostos do plano é a forma CIS forma TRANS Prof. Agamenon Roberto
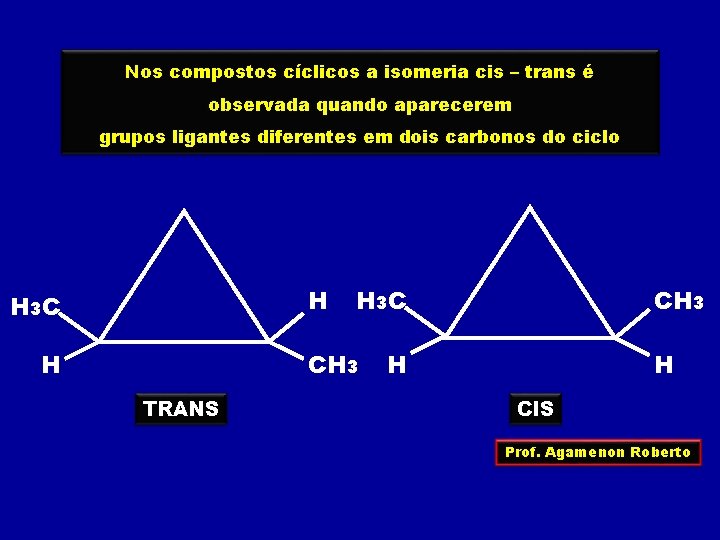
Nos compostos cíclicos a isomeria cis – trans é observada quando aparecerem grupos ligantes diferentes em dois carbonos do ciclo H H 3 C CH 3 TRANS CH 3 H H CIS Prof. Agamenon Roberto

No caso de não existirem dois átomos de hidrogênio nos carbonos da dupla ligação A IUPAC recomenda a utilização dos prefixos Z e E Z: zusammen (juntos) E: entgegen (opostos) Prof. Agamenon Roberto
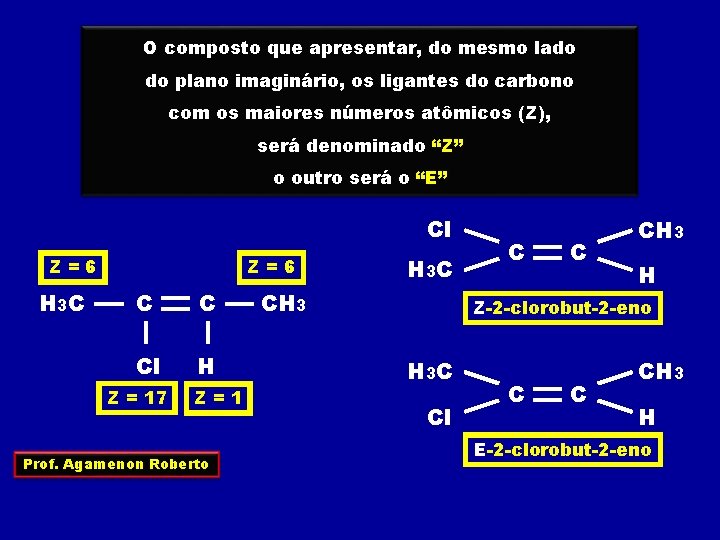
O composto que apresentar, do mesmo lado do plano imaginário, os ligantes do carbono com os maiores números atômicos (Z), será denominado “Z” o outro será o “E” Cl Z=6 H 3 C Z=6 C C Cl H Z = 17 Z=1 Prof. Agamenon Roberto H 3 C C CH 3 H Z-2 -clorobut-2 -eno H 3 C Cl C C CH 3 H E-2 -clorobut-2 -eno
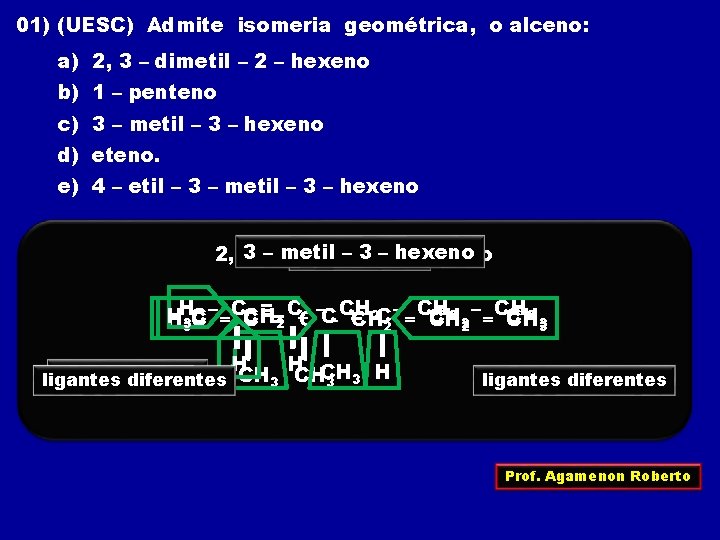
01) (UESC) Admite isomeria geométrica, o alceno: a) 2, 3 – dimetil – 2 – hexeno b) 1 – penteno c) 3 – metil – 3 – hexeno d) eteno. e) 4 – etil – 3 – metil – 3 – hexeno 2, 3 – dimetil – 2 – hexeno 1 – penteno – – CCH = C– –C CH 2 C – – CH 2 – – CH 3 HH C = CH CH C = C – CH 3 2 2 3 H H CH H ligantes iguais CH ligantes iguais diferentes 3 CH 3 3 ligantes diferentes Prof. Agamenon Roberto
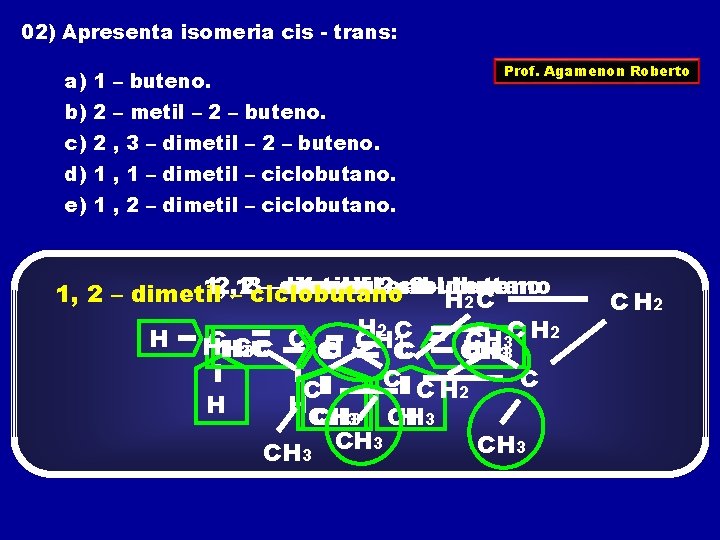
02) Apresenta isomeria cis - trans: a) 1 – buteno. Prof. Agamenon Roberto b) 2 – metil – 2 – buteno. c) 2 , 3 – dimetil – 2 – buteno. d) 1 , 1 – dimetil – ciclobutano. e) 1 , 2 – dimetil – ciclobutano. 1, 2, – 123 –––dimetil 1 – buteno – – 2–ciclobutano – 2 buteno – buteno 1, 2 – dimetil ciclobutano H 2 C C H 2 H H C CH CH 2 CH 3 3 H H HC 33 C C C CH CH 33 C C H 2 C C H HCH CH 33 CH H 3 CH 3 C H 2

Prof. Agamenon Roberto
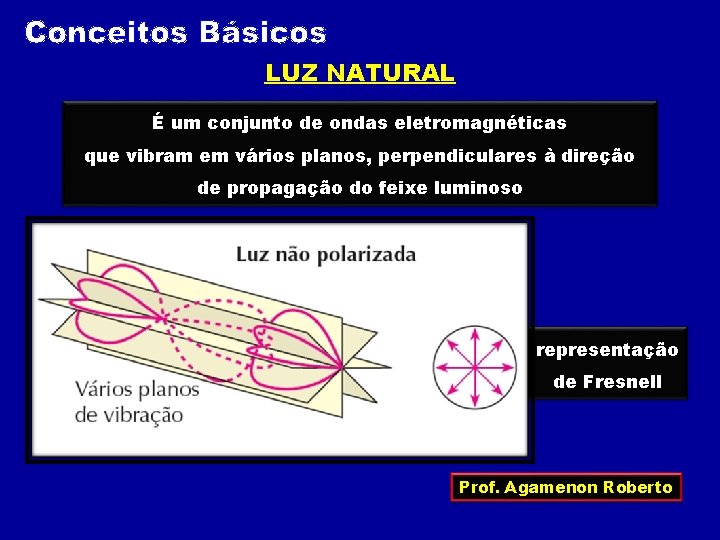
LUZ NATURAL É um conjunto de ondas eletromagnéticas que vibram em vários planos, perpendiculares à direção de propagação do feixe luminoso representação de Fresnell Prof. Agamenon Roberto
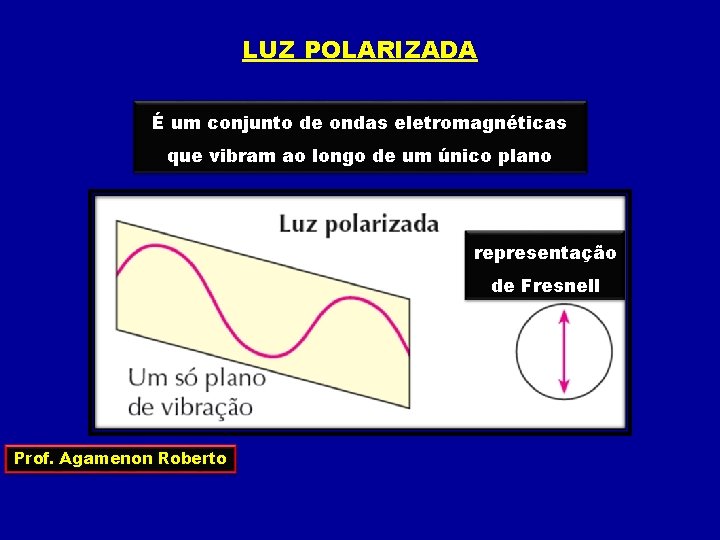
LUZ POLARIZADA É um conjunto de ondas eletromagnéticas que vibram ao longo de um único plano representação de Fresnell Prof. Agamenon Roberto
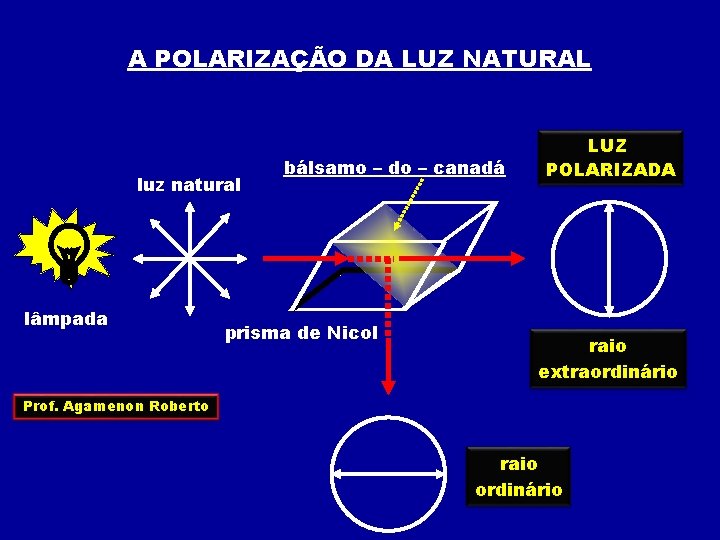
A POLARIZAÇÃO DA LUZ NATURAL luz natural lâmpada bálsamo – do – canadá prisma de Nicol LUZ POLARIZADA raio extraordinário Prof. Agamenon Roberto raio ordinário
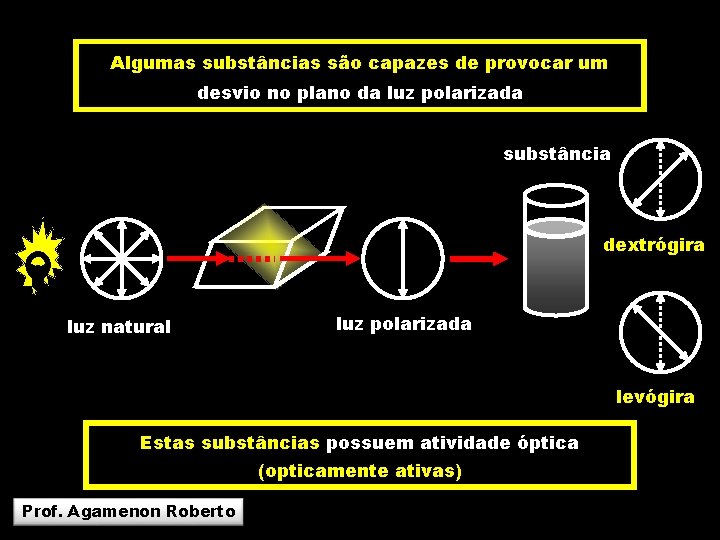
Algumas substâncias são capazes de provocar um desvio no plano da luz polarizada substância dextrógira luz natural luz polarizada levógira Estas substâncias possuem atividade óptica (opticamente ativas) Prof. Agamenon Roberto

Algumas substâncias são capazes de provocar um desvio no plano da luz polarizada Prof. Agamenon Roberto
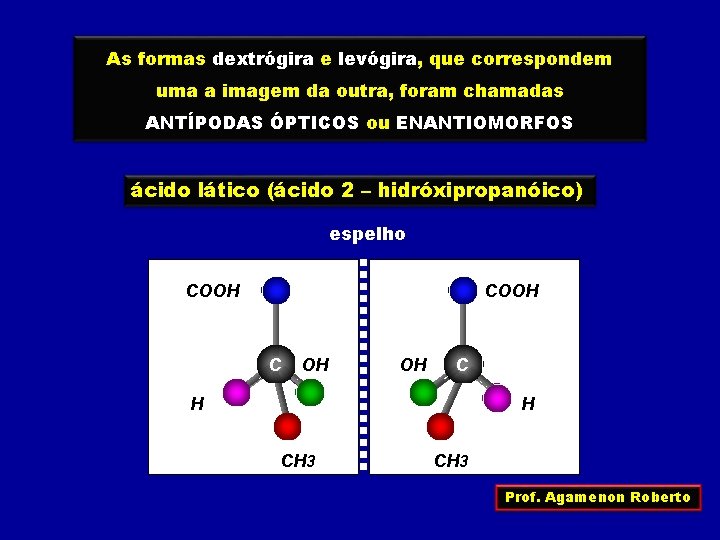
As formas dextrógira e levógira, que correspondem uma a imagem da outra, foram chamadas ANTÍPODAS ÓPTICOS ou ENANTIOMORFOS ácido lático (ácido 2 – hidróxipropanóico) espelho COOH C OH OH C H H CH 3 Prof. Agamenon Roberto

A mistura em partes iguais dos antípodas ópticos fornece por compensação dos efeitos contrários um conjunto OPTICAMENTE INATIVO, que foi chamado MISTURA RACÊMICA As substâncias assimétricas possuem atividade óptica A estrutura orgânica que tem CARBONO ASSIMÉTRICO possuirá atividade óptica (opticamente ativa) Prof. Agamenon Roberto
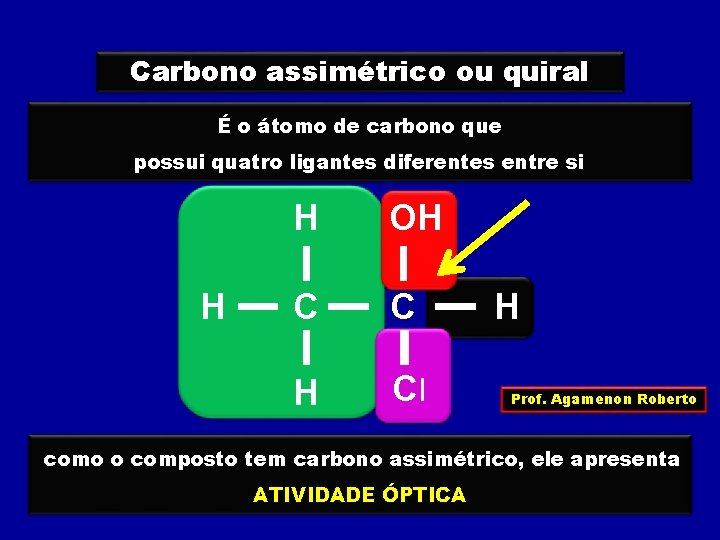
Carbono assimétrico ou quiral É o átomo de carbono que possui quatro ligantes diferentes entre si H H OH C C H Cl H Prof. Agamenon Roberto como o composto tem carbono assimétrico, ele apresenta ATIVIDADE ÓPTICA
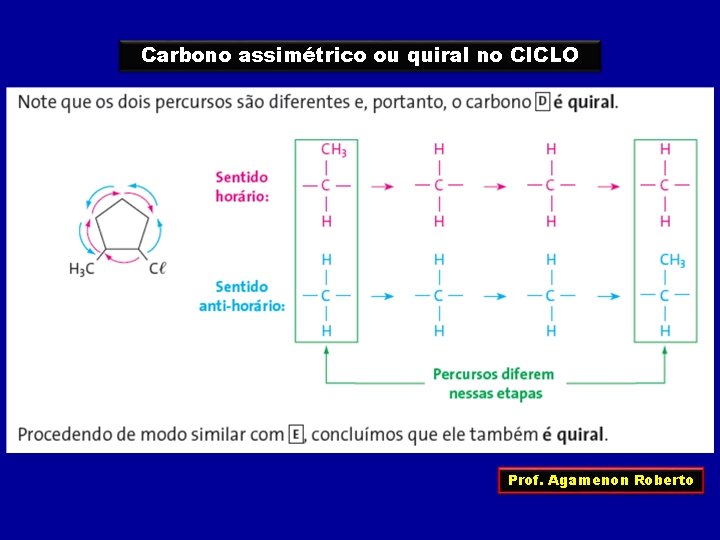
Carbono assimétrico ou quiral no CICLO Prof. Agamenon Roberto
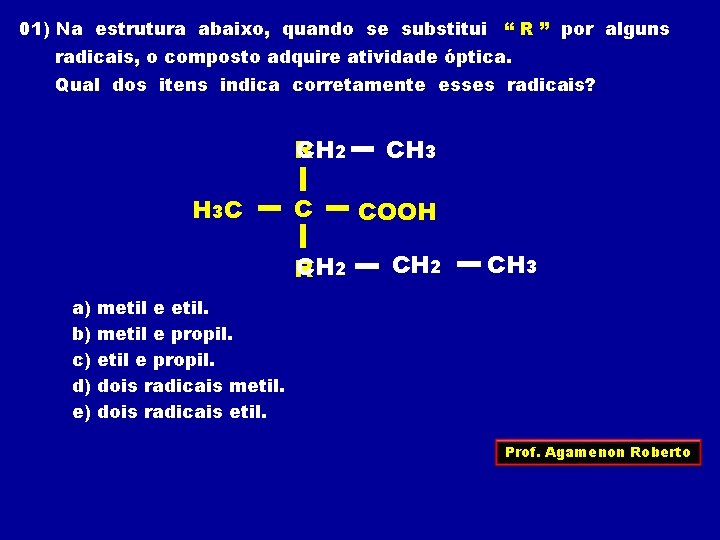
01) Na estrutura abaixo, quando se substitui “ R ” por alguns radicais, o composto adquire atividade óptica. Qual dos itens indica corretamente esses radicais? R CH 2 H 3 C C CH 2 R a) b) c) d) e) CH 3 COOH CH 2 CH 3 metil e etil. metil e propil. dois radicais metil. dois radicais etil. Prof. Agamenon Roberto
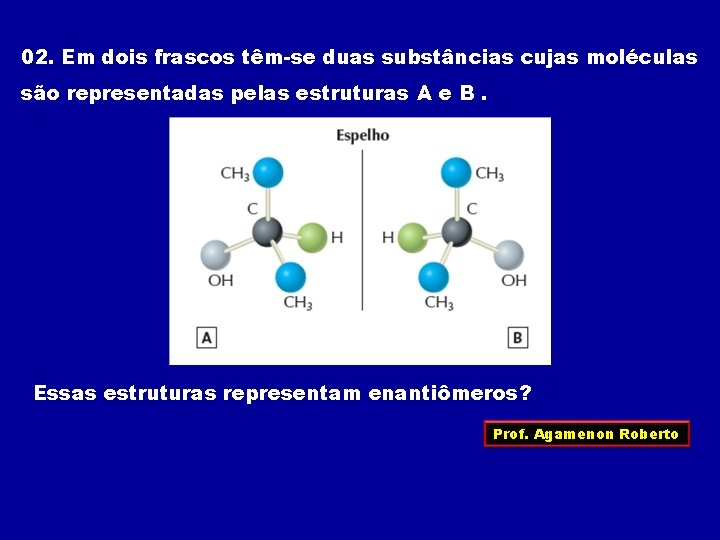
02. Em dois frascos têm-se duas substâncias cujas moléculas são representadas pelas estruturas A e B. Essas estruturas representam enantiômeros? Prof. Agamenon Roberto
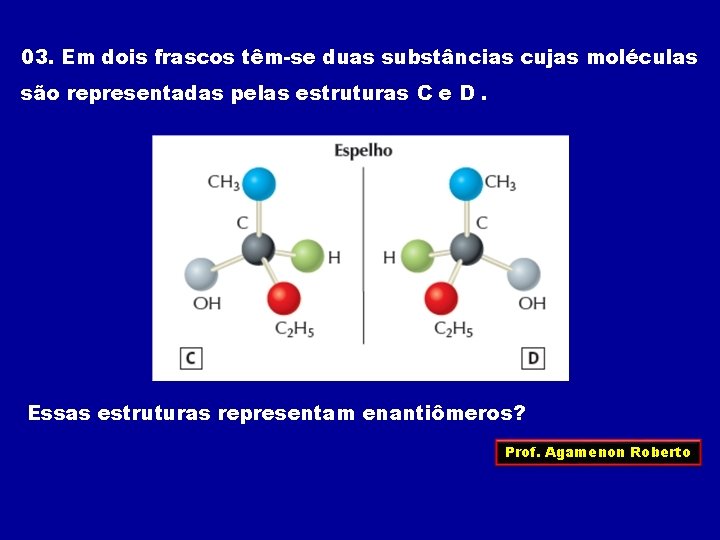
03. Em dois frascos têm-se duas substâncias cujas moléculas são representadas pelas estruturas C e D. Essas estruturas representam enantiômeros? Prof. Agamenon Roberto

04. (Ufes) A utilização de novas técnicas no controle de pragas, como os feromônios, visa minimizar os efeitos nocivos à natureza causados pelo uso indiscriminado de agrotóxicos. Abaixo está descrita a estrutura química do feromônio sexual da mariposa Cydia pomonella, a traça da maçã, que vem sendo utilizado em armadilhas do tipo atrai-mata nos pomares do sul do Brasil. Sobre a estrutura desse feromônio, é CORRETO afirmar que a) possui carbono quiral. b) é um álcool secundário. c) apresenta a fórmula C 12 H 20 O. d) possui o nome sistemático de dodeca-8, 10 -en--1 -ol. e) possui duas isomeria trans. ligações duplas carbono-carbono com Prof. Agamenon Roberto
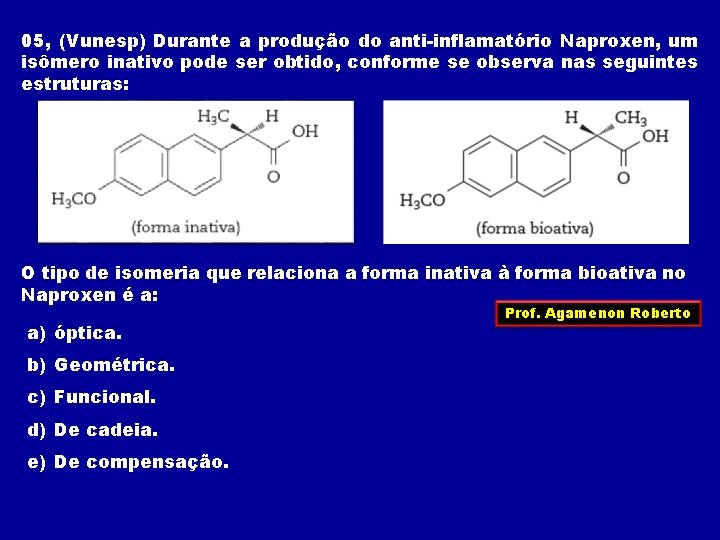
05, (Vunesp) Durante a produção do anti-inflamatório Naproxen, um isômero inativo pode ser obtido, conforme se observa nas seguintes estruturas: O tipo de isomeria que relaciona a forma inativa à forma bioativa no Naproxen é a: a) óptica. b) Geométrica. c) Funcional. d) De cadeia. e) De compensação. Prof. Agamenon Roberto

06)(Unifor-CE) Uma estrutura molecular “quiral” contém carbono assimétrico, ou seja, admite enantiômeros. Analise os compostos representados a seguir quanto à existência de enantiômeros. Possibilitam a existência de enantiômeros SOMENTE as estruturas: a) I e II. b) II e IV. c) I, III e V. d) II, III e IV. e) III, IV e V. Prof. Agamenon Roberto
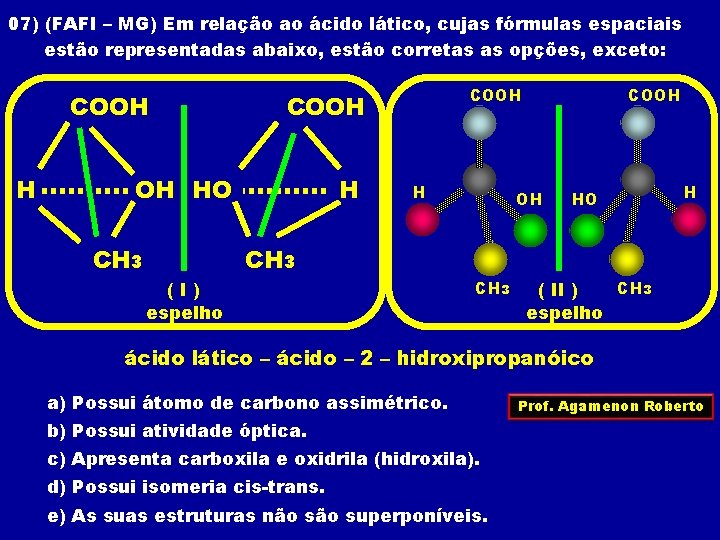
07) (FAFI – MG) Em relação ao ácido lático, cujas fórmulas espaciais estão representadas abaixo, estão corretas as opções, exceto: COOH HO CH 3 COOH H H COOH OH HO H CH 3 (I) espelho CH 3 ( II ) espelho ácido lático – ácido – 2 – hidroxipropanóico a) Possui átomo de carbono assimétrico. b) Possui atividade óptica. c) Apresenta carboxila e oxidrila (hidroxila). d) Possui isomeria cis-trans. e) As suas estruturas não superponíveis. Prof. Agamenon Roberto
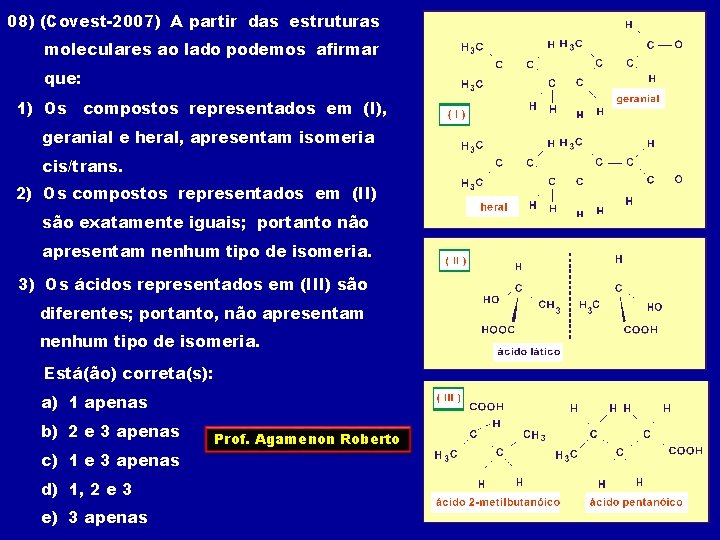
08) (Covest-2007) A partir das estruturas moleculares ao lado podemos afirmar que: 1) Os compostos representados em (I), geranial e heral, apresentam isomeria cis/trans. 2) Os compostos representados em (II) são exatamente iguais; portanto não apresentam nenhum tipo de isomeria. 3) Os ácidos representados em (III) são diferentes; portanto, não apresentam nenhum tipo de isomeria. Está(ão) correta(s): a) 1 apenas b) 2 e 3 apenas c) 1 e 3 apenas d) 1, 2 e 3 e) 3 apenas Prof. Agamenon Roberto

Para uma substância orgânica, com carbono assimétrico, o número de isômeros ativos e inativos é dado pelas expressões: número de isômeros ativos número de isômeros inativos 2 2 n n– 1 “n” é o número de carbonos assimétricos Prof. Agamenon Roberto
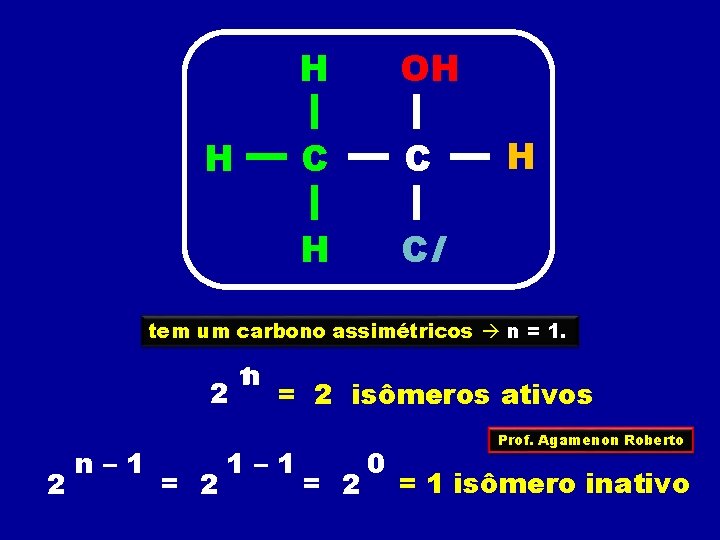
H H OH C C H Cl H tem um carbono assimétricos n = 1. 2 2 n– 1 = 2 1 n = 2 isômeros ativos 1– 1 = 2 0 Prof. Agamenon Roberto = 1 isômero inativo

01) O número total de isômeros (ativos e inativos) da molécula abaixo é: H I H 3 C – I Cl a) 2. b) 4. c) 6. d) 8. e) 10. Prof. Agamenon Roberto H I C – NH 2 I Cl Este composto possui dois átomos de carbono assimétricos diferentes, portanto n = 2 2 n = 2 n – 1 2 2 = 4 isômeros ativos 2 – 1 total de isômeros: = 1 2 = 2 isômero inativo 4 ativos + 2 inativos = 6 isômeros

02) (FESP-PE) Considere o composto: ácido 2, 3 – dicloro – 3 – fenilpropanóico Ele apresenta: a) 4 isômeros sem atividade óptica. b) um total de 6 isômeros, sendo 2 sem atividade óptica. c) um total de 4 isômeros, sendo 2 sem atividade óptica. d) não apresenta isomeria óptica. Prof. Agamenon Roberto e) só 2 isômeros ativos e um meso composto. Tem dois carbonos assimétricos n = 2 n 2 2 = 4 isômeros ativos 2 n– 1 = 2 2– 1 = 2 isômeros inativos Total de isômeros = 4 + 2 = 6 isõmeros
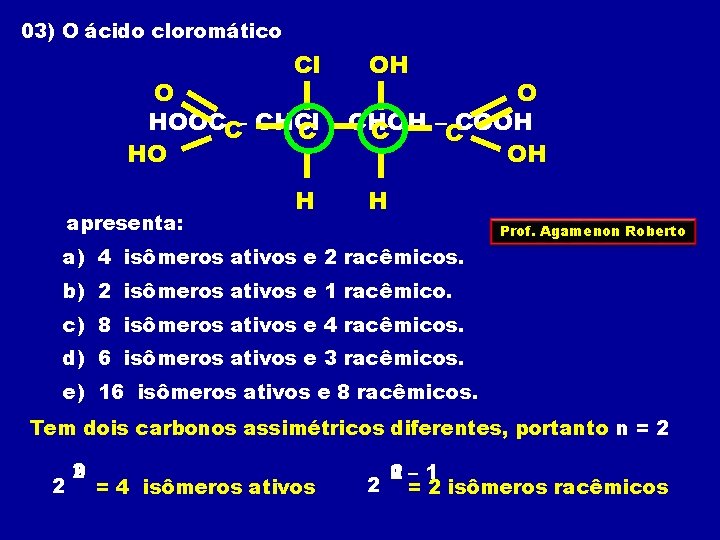
03) O ácido cloromático Cl OH H H O O HOOCC– CHCl –CCOOH C – CHOH C HO OH apresenta: Prof. Agamenon Roberto a) 4 isômeros ativos e 2 racêmicos. b) 2 isômeros ativos e 1 racêmico. c) 8 isômeros ativos e 4 racêmicos. d) 6 isômeros ativos e 3 racêmicos. e) 16 isômeros ativos e 8 racêmicos. Tem dois carbonos assimétricos diferentes, portanto n = 2 2 n 2 = 4 isômeros ativos n– 1 1 2 2 = 2 isômeros racêmicos
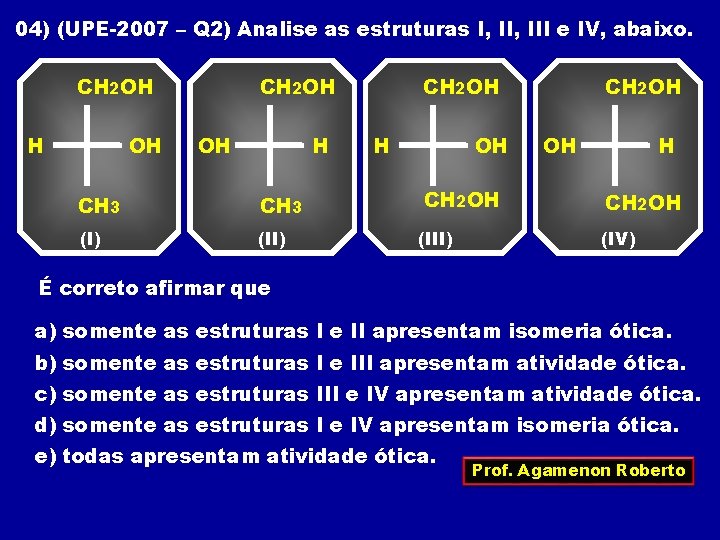
04) (UPE-2007 – Q 2) Analise as estruturas I, III e IV, abaixo. CH 2 OH H OH CH 2 OH OH H CH 3 (I) (II) CH 2 OH H OH CH 2 OH (III) CH 2 OH OH H CH 2 OH (IV) É correto afirmar que a) somente as estruturas I e II apresentam isomeria ótica. b) somente as estruturas I e III apresentam atividade ótica. c) somente as estruturas III e IV apresentam atividade ótica. d) somente as estruturas I e IV apresentam isomeria ótica. e) todas apresentam atividade ótica. Prof. Agamenon Roberto
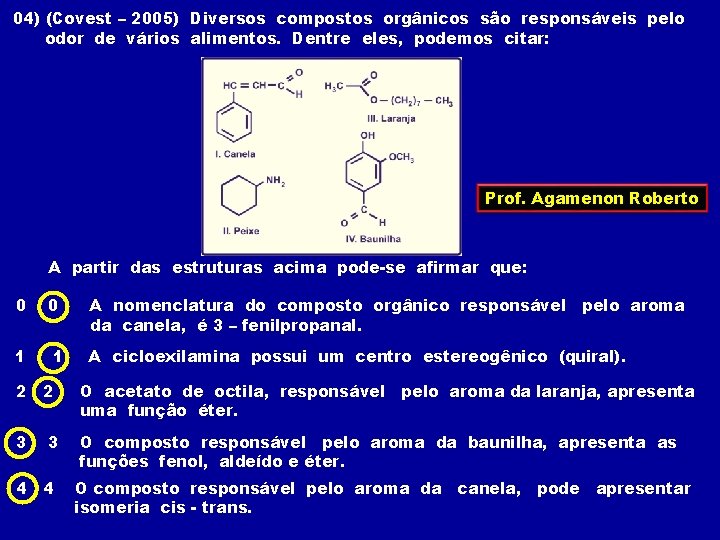
04) (Covest – 2005) Diversos compostos orgânicos são responsáveis pelo odor de vários alimentos. Dentre eles, podemos citar: Prof. Agamenon Roberto A partir das estruturas acima pode-se afirmar que: 0 0 A nomenclatura do composto orgânico responsável pelo aroma da canela, é 3 – fenilpropanal. 1 1 A cicloexilamina possui um centro estereogênico (quiral). 2 2 O acetato de octila, responsável pelo aroma da laranja, apresenta uma função éter. 3 O composto responsável pelo aroma da baunilha, apresenta as funções fenol, aldeído e éter. 3 4 4 O composto responsável pelo aroma da canela, pode apresentar isomeria cis - trans.

06) (UPE-2006 -Q 2) Analise as afirmativas acerca dos diversos compostos orgânicos e suas propriedades e assinale-as devidamente. Prof. Agamenon Roberto F 0 0 Os compostos butanal e metilpropanal exemplificam um caso de isomeria espacial O F 1 1 Os isômeros de posição Opertencem à mesma função possuem diferem H 3 Corgânica H 3 C mas. CH C a mesma cadeia, C entre CH 2 si apenas quanto à posição do heteroátomo H H V 2 2 Um hidrocarboneto cíclico pode ser isômero de um CH 3 ORG NICA ISÔMEROS DE POSIÇÃO PERTENCEM À MESMA FUNÇÃO hidrocarboneto alifático insaturado SÃO ISÔMEROS DE CADEIA E TÊM A MESMA CADEIA, MAS DIFEREM ENTRE SI PELA POSIÇÃO RADICAL OU UMA INSATURAÇÃO cresóis, C 7 DE H 8 UM O, são conhecidos quimicamente como V 3 3 Os hidroximetilbenzenos e podem apresentar isomeria plana, tanto de função de posição H 2 C e como CH CH 3 SÃO ISÔMEROS F 4 4 A atividade ótica de uma substância está relacionada com a C 3 H 6 OH C 3 H 6 OH simetria cristalina ou molecular das substâncias É UM CRESOL ISÔMERO DE É ISÔMERO DE ESTÁÉ RELACIONADA COM A ASSIMETRIA FUNÇÃO DO POSIÇÃO DO CH 3 CH 2 OH CH 3

EXERCÍCIOS Prof. Agamenon Roberto

01. Sobre os compostos orgânicos abaixo afirma-se: I. São hidrocarbonetos alifáticos e insaturados. II. O propino possui duas ligações “pi” e 6 ligações sigma. III. O propano é um alcano com um átomo de carbono secundário e dois átomos de carbono primários. O propino reagindo com um mol de H 2 produz o propeno São corretas, apenas as afirmações: a) b) c) d) e) I, II e III. II, III e IV. . II e III. I, III e IV. Prof. Agamenon Roberto
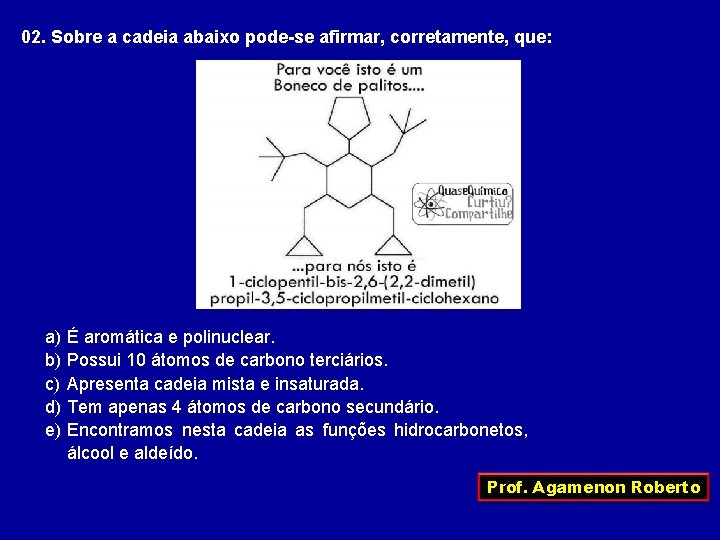
02. Sobre a cadeia abaixo pode-se afirmar, corretamente, que: a) b) c) d) e) É aromática e polinuclear. Possui 10 átomos de carbono terciários. Apresenta cadeia mista e insaturada. Tem apenas 4 átomos de carbono secundário. Encontramos nesta cadeia as funções hidrocarbonetos, álcool e aldeído. Prof. Agamenon Roberto

03. Observando a imagem abaixo, assinale a afirmação verdadeira: a) O composto de fórmula CH 4 é o metano e apresenta geometria piramidal. b) O metanol pertence à função aldeído. c) No metanol o oxigênio da oxidrila é um heteroátomo. d) Todo composto que possui o elemento químico carbono é orgânico. e) No metano a hibridização do carbono é sp 3. . Prof. Agamenon Roberto
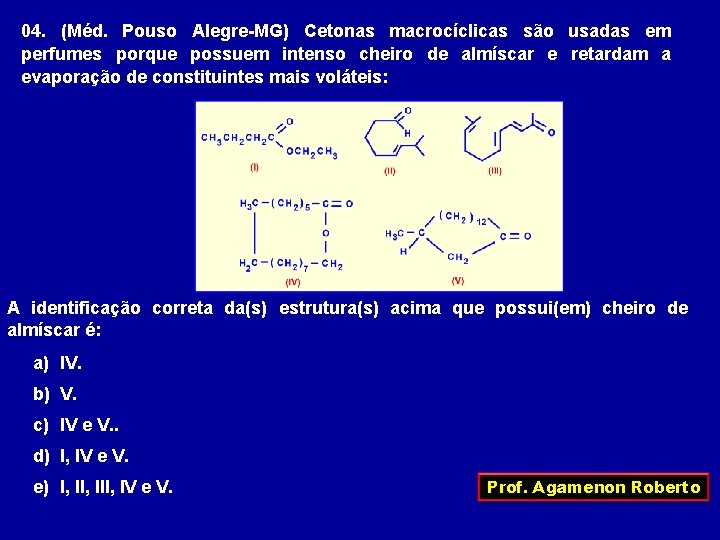
04. (Méd. Pouso Alegre-MG) Cetonas macrocíclicas são usadas em perfumes porque possuem intenso cheiro de almíscar e retardam a evaporação de constituintes mais voláteis: A identificação correta da(s) estrutura(s) acima que possui(em) cheiro de almíscar é: a) IV. b) V. c) IV e V. . d) I, IV e V. e) I, III, IV e V. Prof. Agamenon Roberto

05. (UDESC) Analise o composto representado na figura abaixo: Sobre o composto, é FALSO afirmar que: a) o seu nome é 2, 2, 4 – trimetil – 4 – penteno. b)apresenta dois carbonos com hibridização sp 2. c) é um alceno ramificado de cadeia aberta. d)é um hidrocarboneto ramificado de cadeia aberta. e) apresenta seis carbonos com hibridização sp 3. . Prof. Agamenon Roberto
06. (UNAMA-AM) O nylon-66 é um co-polímero do ácido adípico ou hexanodióico com a hexametileno diamina, usado na fabricação de paraquedas e roupas. A estrutura plana do ácido adípico está corretamente representada na alternativa, a) HOOC – CH = CH – CH 2 – COOH. b) HOOC – CH = CH – CH 2 – CH 3. c) HOOC – CH 2 – COOH. d) HOOC – CH 2 – COOH. . e) HOOC – CH 2 – CH 2 – COOH. Prof. Agamenon Roberto

07. (ACR-2007) Abaixo se encontra uma reação química, onde vários compostos participam. A respeito das substâncias participantes desta reação assinale a alternativa falsa: a) O composto (I) propanal. . b) O composto (II) é um álcool primário. c) A substância (III) é um éster chamado propanoato de etila. d) Segundo a IUPAC, o composto (II) chama-se etanol. e) O ácido propanóico possui um átomo de carbono híbrido sp 2. Prof. Agamenon Roberto

08. A transformação do propan – 1 – ol em propileno (propeno), como esquematizado a seguir, constitui reação de: a) hidratação. b) hidrogenação. c) halogenação. d) descarboxilação. e) desidratação. . Prof. Agamenon Roberto
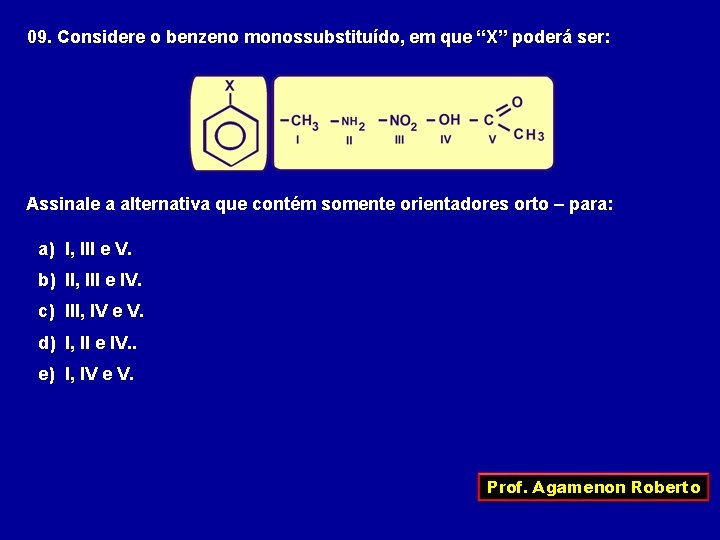
09. Considere o benzeno monossubstituído, em que “X” poderá ser: Assinale a alternativa que contém somente orientadores orto – para: a) I, III e V. b) II, III e IV. c) III, IV e V. d) I, II e IV. . e) I, IV e V. Prof. Agamenon Roberto

10. O produto principal da reação abaixo é um: a) álcool primário. b) álcool secundário. . c) aldeído. d) ácido carboxílico. e) cetona. Prof. Agamenon Roberto

11) Sobre os compostos: éter metil fenílico e meta hidroxi-tolueno. 0 0 São isômeros. 1 1 Pertencem à mesma função química. 2 2 Ambos possuem fórmula molecular C 7 H 8 O. 3 3 Ambos são aromáticos. 4 4 Ambos são isômeros do álcool benzílico. Prof. Agamenon Roberto
12)(Ufersa-RN) A substituição de um hidrogênio por uma etila no carbono secundário do butano resulta em um isômero do: a) b) c) d) e) pentano. 2 – metil – pentano. 3 – metil – pentano. 2 – etil – butano. hexano. Prof. Agamenon Roberto
13) (Unemat-MT) O composto ácido pentanóico é isômero de cadeia do composto: a) Ácido 2, 2 – dimetil – pentanóico. b)Ácido 2 – metil – butanoico. c) Ácido fenil – metanoico. d)Ácido 4 – metil – pentanóico. e) Ácido 3 -metil-benzoico. Prof. Agamenon Roberto

14) O éter sulfúrico (etóxi-etano), também chamado éter etílico, foi muito empregado como anestésico. Entretanto, em virtude da sua toxidade, ele não é mais utilizado para esse fim. Marque a opção que apresenta um isômero plano de função do éter sulfúrico. a) etanoato de etila. b) 1 butanol. c) butanóico. d) butanona. e) butanal. Prof. Agamenon Roberto
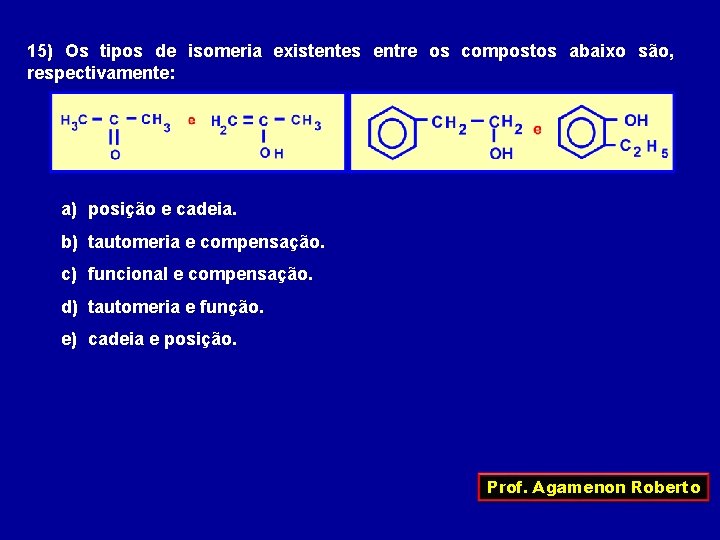
15) Os tipos de isomeria existentes entre os compostos abaixo são, respectivamente: a) posição e cadeia. b) tautomeria e compensação. c) funcional e compensação. d) tautomeria e função. e) cadeia e posição. Prof. Agamenon Roberto
16)(PUC-SP) Sabendo-se que 2, 46 L de um hidrocarboneto gasoso, medidos à pressão de 1 atm e 27°C, têm massa igual a 5, 6 g e que esse hidrocarboneto apresenta isomeria cis - trans, isomeria de cadeia e isomeria de posição, pode-se afirmar que se trata de: a) 1 -buteno. b) 2 -buteno. c) propeno. d) ciclobutano. e) metilciclobutano. Prof. Agamenon Roberto

17)(FGV-SP) São feitas as seguintes afirmações sobre o composto 3, 5 -dimetil-hepta-2 -eno. I. A sua fórmula molecular é C 9 H 18. II. Apresenta um átomo de carbono com arranjo trigonal planar. III. Apresenta dois isômeros ópticos. IV. Apresenta isomeria geométrica. São corretas as afirmações contidas apenas em: a) II e III. b) III e IV. c) I, II e III. d) I, II e IV. e) I, III e IV. Prof. Agamenon Roberto

18)(Ufpr 2010) A asparagina pode ser obtida na forma de dois diferentes isômeros ópticos. Um deles tem sabor doce e é usado como adoçante, enquanto o outro tem sabor azedo. Considere as seguintes afirmativas: 1. O pentan-3 -ol apresenta um carbono assimétrico. 2. O cis-but-2 -eno e o trans-but-2 -eno são isômeros ópticos porque diferem somente na disposição geométrica dos grupos ligados aos carbonos da dupla ligação. Prof. Agamenon Roberto 3. Carbonos aromáticos podem ser assimétricos. 4. Misturas racêmicas são opticamente inativas. Assinale a alternativa correta. a) Somente as afirmativas 2, 3 e 4 são verdadeiras. b) Somente as afirmativas 1 e 2 são verdadeiras. c) Somente a afirmativa 4 é verdadeira. d) As afirmativas 1, 2, 3 e 4 são verdadeiras. e) Somente as afirmativas 2 e 3 são verdadeiras.
- Slides: 66