Ioniske reaksjonsmekanismer Kap 6SolomonFryhle Hele kapitlet viktig i









- Slides: 30

Ioniske reaksjonsmekanismer Kap 6/Solomon/Fryhle Hele kapitlet viktig i farmasien 11/2/2020 1

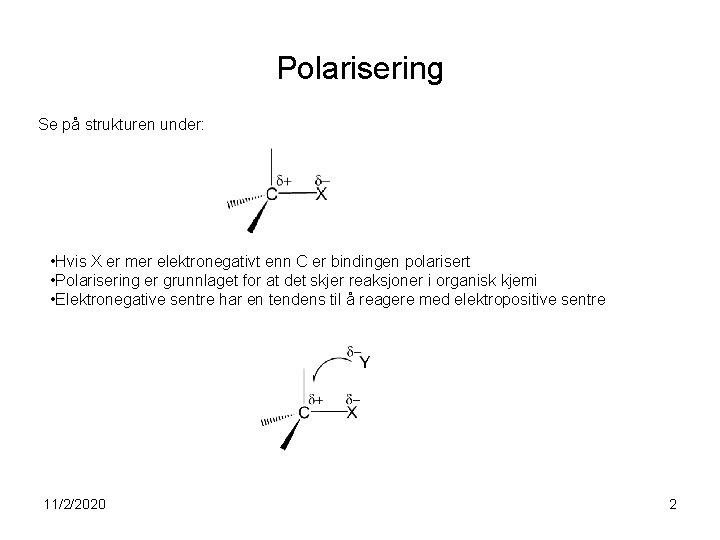
Polarisering Se på strukturen under: • Hvis X er mer elektronegativt enn C er bindingen polarisert • Polarisering er grunnlaget for at det skjer reaksjoner i organisk kjemi • Elektronegative sentre har en tendens til å reagere med elektropositive sentre 11/2/2020 2

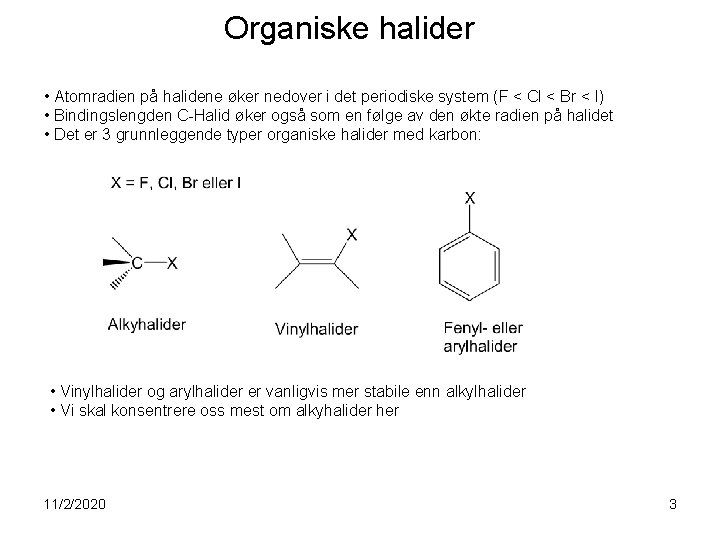
Organiske halider • Atomradien på halidene øker nedover i det periodiske system (F < Cl < Br < I) • Bindingslengden C-Halid øker også som en følge av den økte radien på halidet • Det er 3 grunnleggende typer organiske halider med karbon: • Vinylhalider og arylhalider er vanligvis mer stabile enn alkylhalider • Vi skal konsentrere oss mest om alkyhalider her 11/2/2020 3

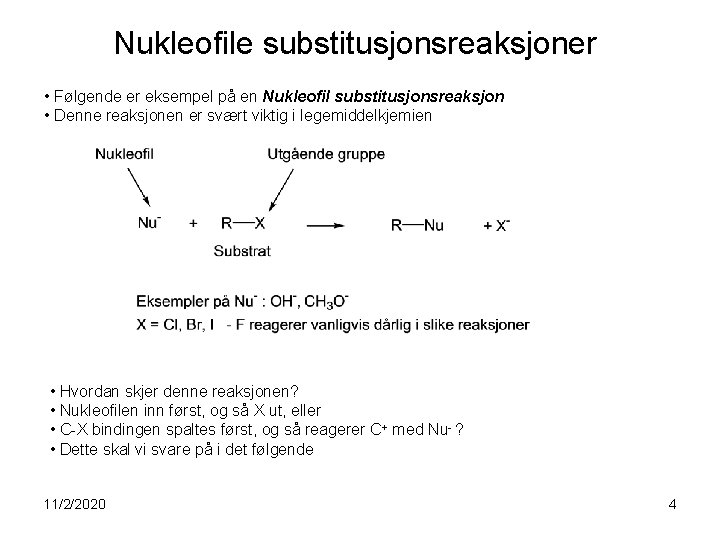
Nukleofile substitusjonsreaksjoner • Følgende er eksempel på en Nukleofil substitusjonsreaksjon • Denne reaksjonen er svært viktig i legemiddelkjemien • Hvordan skjer denne reaksjonen? • Nukleofilen inn først, og så X ut, eller • C-X bindingen spaltes først, og så reagerer C+ med Nu- ? • Dette skal vi svare på i det følgende 11/2/2020 4

Nukleofiler og utgående grupper Nukleofil: • Nukleofil kommer fra Nukleus = kjerne + philos (gresk) = elsker, altså • Nukleofil: elsker kjernen • Nukleofiler er enten et negativt jon, eller en nøytral gruppe med ledig elektronpar • For eksempel kan både H 2 O og OH- være nukleofiler Utgående gruppe: • Gode substrater for substitusjonsreaksjoner må ha en god utgående gruppe • For å kunne fungere som utgående gruppe må den kunne forlate substratet som et stabilt, svakt basisk molekyl eller jon • Halid-joner fyller vanligvis disse kriteriene • Gode utgående grupper er ofte positivt ladet 11/2/2020 5

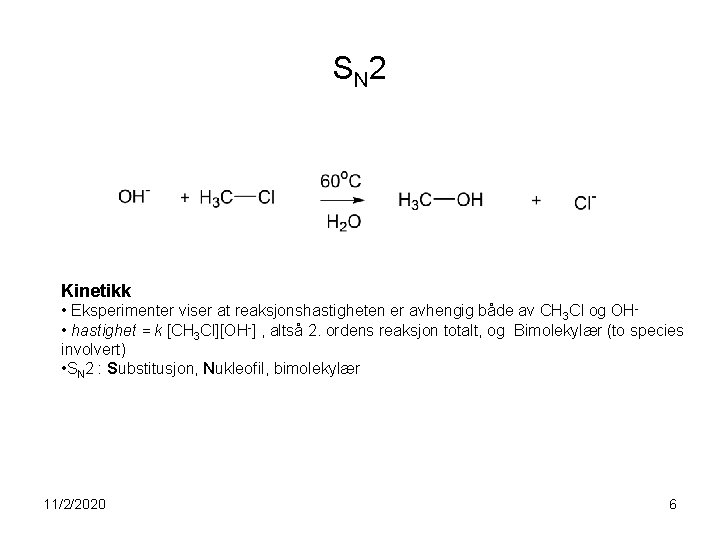
S N 2 Kinetikk • Eksperimenter viser at reaksjonshastigheten er avhengig både av CH 3 Cl og OH • hastighet = k [CH 3 Cl][OH-] , altså 2. ordens reaksjon totalt, og Bimolekylær (to species involvert) • SN 2 : Substitusjon, Nukleofil, bimolekylær 11/2/2020 6

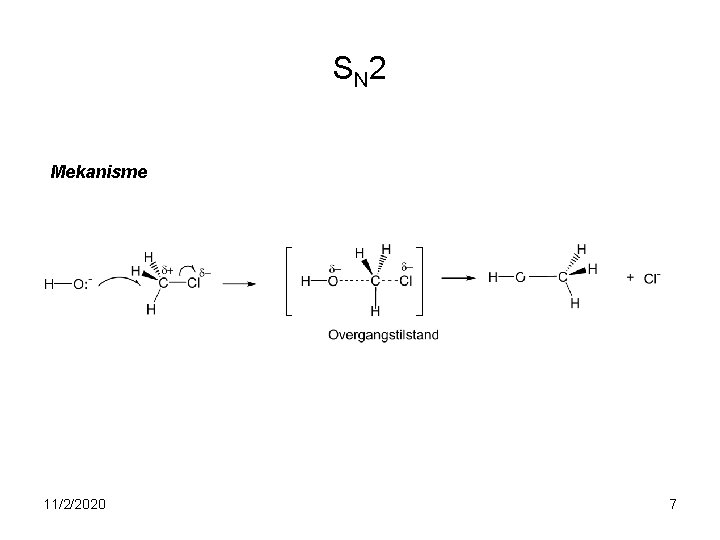
S N 2 Mekanisme 11/2/2020 7

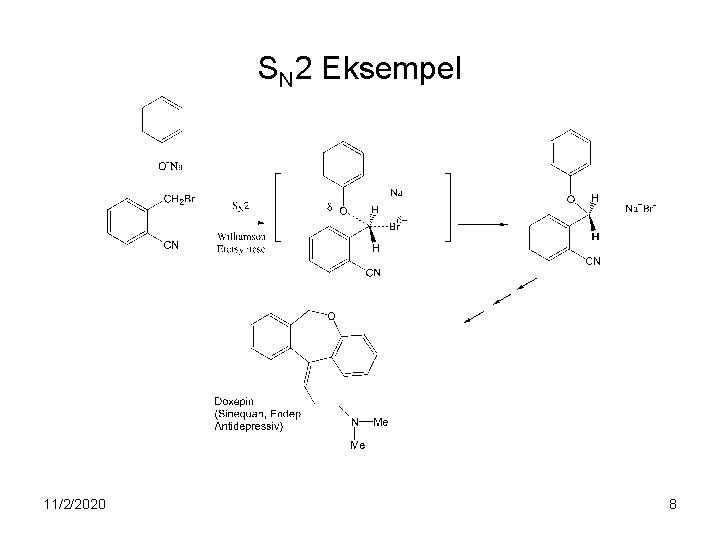
SN 2 Eksempel 11/2/2020 8

Metylklorid reagerer med hydroksyd-jon 11/2/2020 9

Teori overgangstilstander • Reaksjonen på forrige side har en negativ fri energi ΔG 0 = - 100 k. J /mol , eksergonisk reaksjon • log Keq = - ΔG 0/2. 303 RT = 15. 7, Keq = 5. 0 X 1015 • Ekstremt stor likevektskonstant • Negativ ΔG 0 : reaksjonen går nedoverbakke, eksergonisk • Positiv ΔG 0 : reaksjonen går oppoverbakke, endergonisk • Men: hvis kovalente bindinger brytes, går reaksjonene først oppoverbakke • Overgangstilstanden representerer den høyeste energitilstanden: energibarriere Energiforløpet kan sammenliknes med et fjellpass, det kan være høyere eller lavere på den andre siden av passet 11/2/2020 10

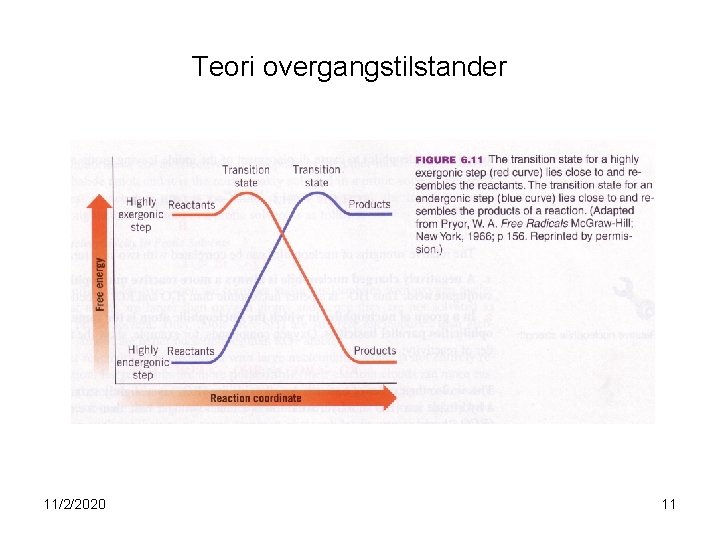
Teori overgangstilstander 11/2/2020 11

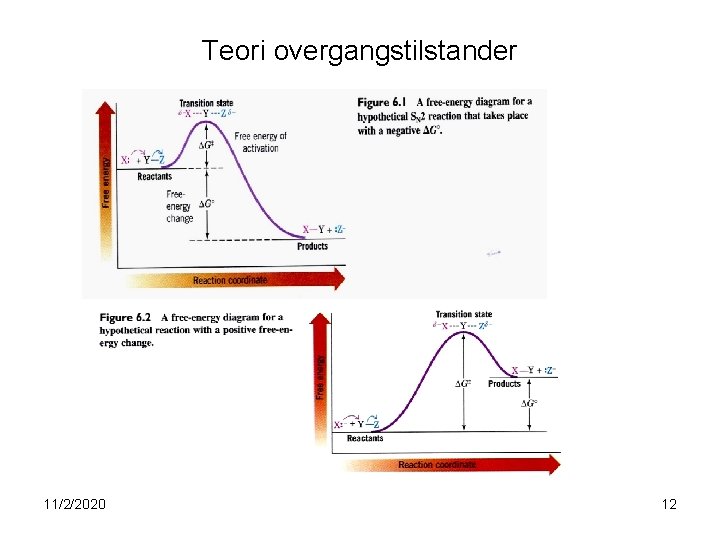
Teori overgangstilstander 11/2/2020 12

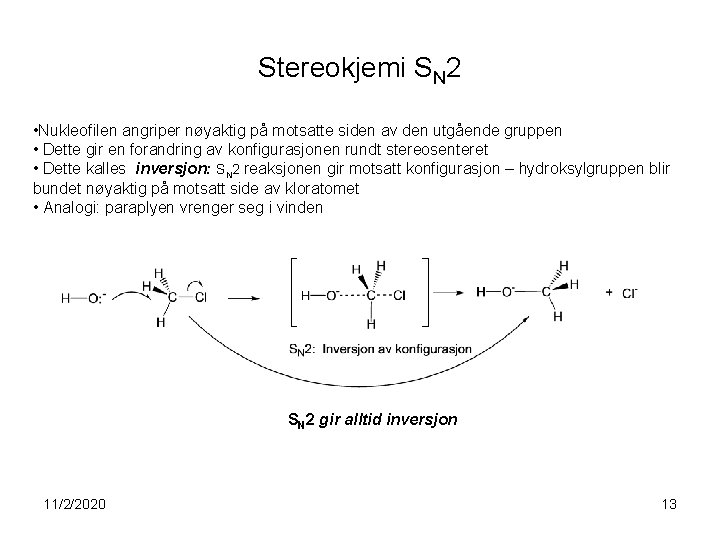
Stereokjemi SN 2 • Nukleofilen angriper nøyaktig på motsatte siden av den utgående gruppen • Dette gir en forandring av konfigurasjonen rundt stereosenteret • Dette kalles inversjon: SN 2 reaksjonen gir motsatt konfigurasjon – hydroksylgruppen blir bundet nøyaktig på motsatt side av kloratomet • Analogi: paraplyen vrenger seg i vinden SN 2 gir alltid inversjon 11/2/2020 13

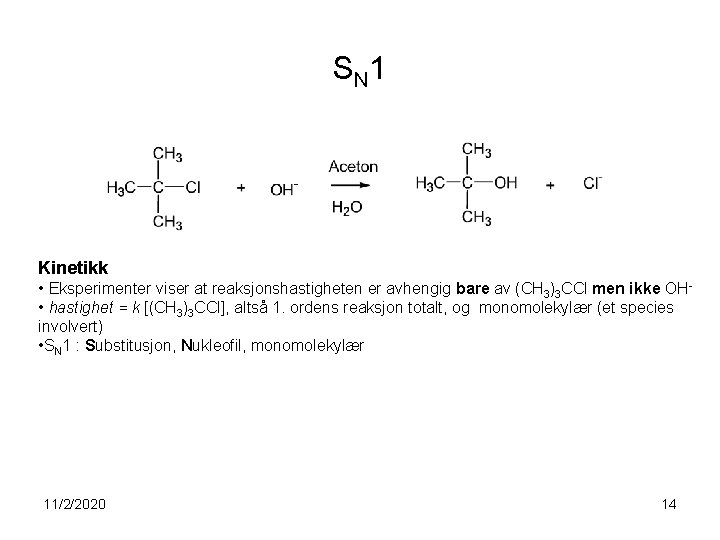
S N 1 Kinetikk • Eksperimenter viser at reaksjonshastigheten er avhengig bare av (CH 3)3 CCl men ikke OH • hastighet = k [(CH 3)3 CCl], altså 1. ordens reaksjon totalt, og monomolekylær (et species involvert) • SN 1 : Substitusjon, Nukleofil, monomolekylær 11/2/2020 14

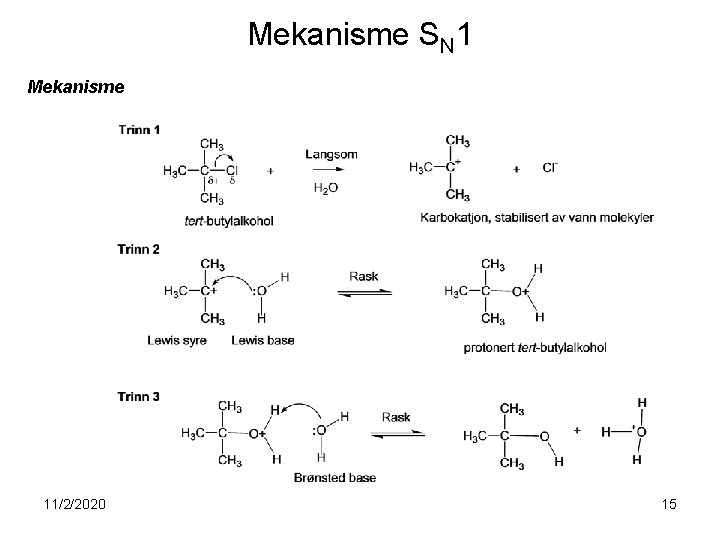
Mekanisme SN 1 Mekanisme 11/2/2020 15

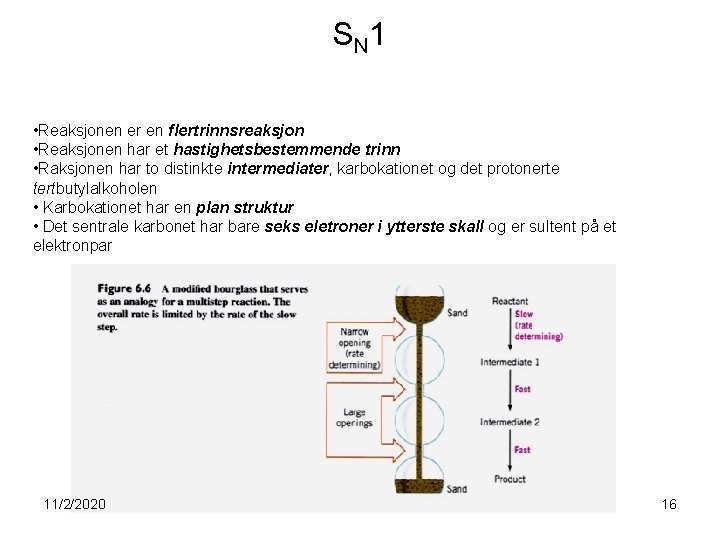
S N 1 • Reaksjonen er en flertrinnsreaksjon • Reaksjonen har et hastighetsbestemmende trinn • Raksjonen har to distinkte intermediater, karbokationet og det protonerte tertbutylalkoholen • Karbokationet har en plan struktur • Det sentrale karbonet har bare seks eletroner i ytterste skall og er sultent på et elektronpar 11/2/2020 16

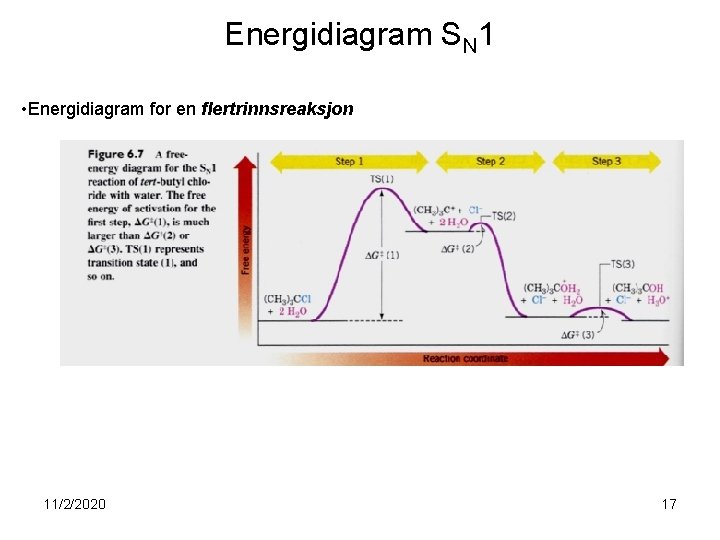
Energidiagram SN 1 • Energidiagram for en flertrinnsreaksjon 11/2/2020 17

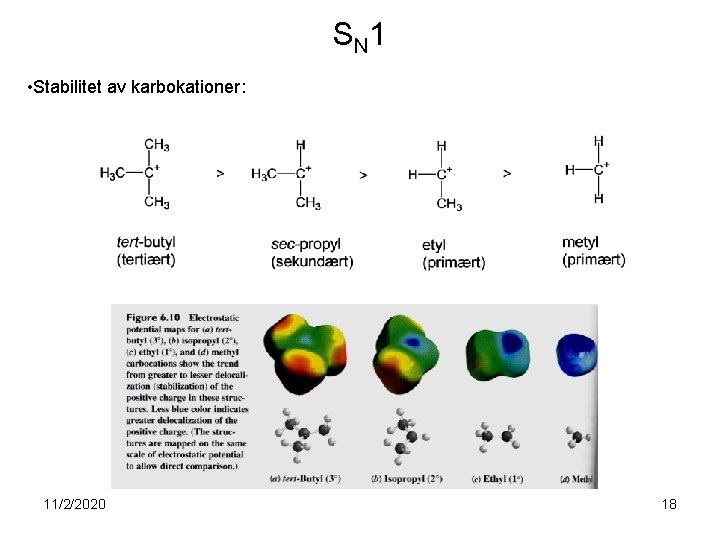
S N 1 • Stabilitet av karbokationer: 11/2/2020 18

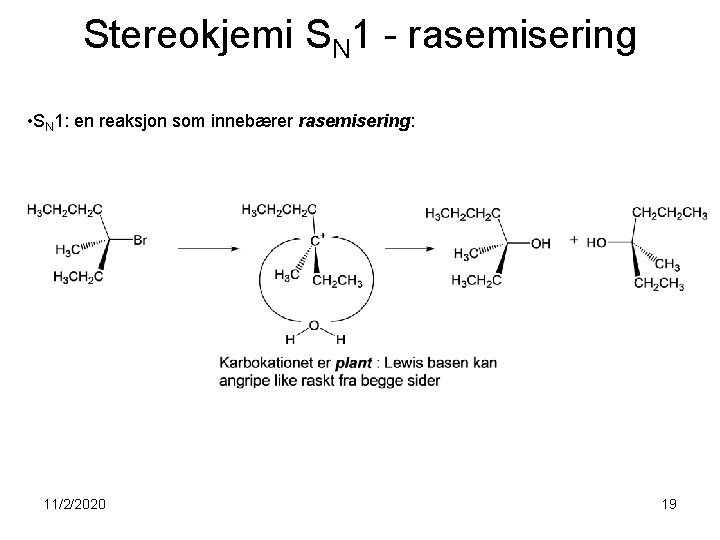
Stereokjemi SN 1 - rasemisering • SN 1: en reaksjon som innebærer rasemisering: 11/2/2020 19

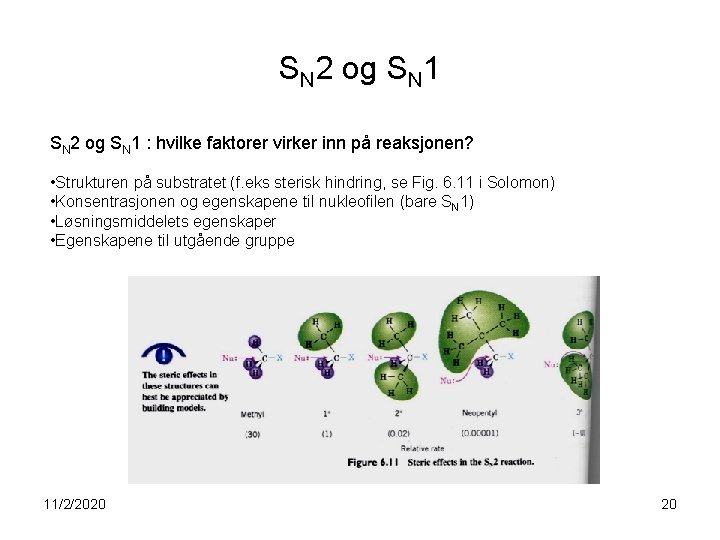
SN 2 og SN 1 : hvilke faktorer virker inn på reaksjonen? • Strukturen på substratet (f. eks sterisk hindring, se Fig. 6. 11 i Solomon) • Konsentrasjonen og egenskapene til nukleofilen (bare SN 1) • Løsningsmiddelets egenskaper • Egenskapene til utgående gruppe 11/2/2020 20

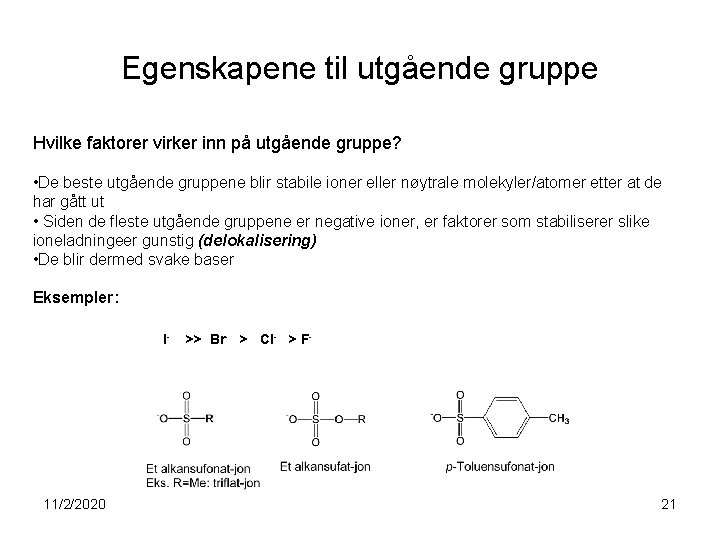
Egenskapene til utgående gruppe Hvilke faktorer virker inn på utgående gruppe? • De beste utgående gruppene blir stabile ioner eller nøytrale molekyler/atomer etter at de har gått ut • Siden de fleste utgående gruppene er negative ioner, er faktorer som stabiliserer slike ioneladningeer gunstig (delokalisering) • De blir dermed svake baser Eksempler: I- 11/2/2020 >> Br- > Cl- > F- 21

SN 2 versus SN 1 Det er et konkurranseforhold mellom SN 2 og SN 1 (se tabell 6. 6 i Solomon) • Forgrening (sekundært/tertiært) favoriserer SN 1 – hvorfor? • Nukleofilen: svake Lewis baser (donerer elektronpar), for eksempel løsningsmiddelmolekyler (solvolyse) favoriserer SN 1, sterke Lewis baser favoriserer SN 2 • Løsningsmiddelet : polare protiske (vann, alkoholer) favoriserer SN 1 polare aprotiske (aceton, DMF, DMSO) favoriserer SN 2 • Utgående gruppe: For både SN 2 og SN 1: jo svakere base jo bedre utgående gruppe Eksempel: studer tabell 6. 6 i Solomon/Fryhle 11/2/2020 22

SN 2 versus SN 1 Tabell 6. 6 i Solomon/Fryhle 11/2/2020 23

Eliminasjonsreaksjoner: en viktig måte å lage olefiner på er dehydrohalogenering • Atomet med halogenet (utgående gruppe) kalles -karbonet • Naboatomet som deltar i reaksjonen kalles -karbonet • Slike reaksjoner kalles 1, 2 -eliminasjoner • Reaksjonen krever vanligvis en sterk base for å plukke protonet på -karbonet 11/2/2020 24

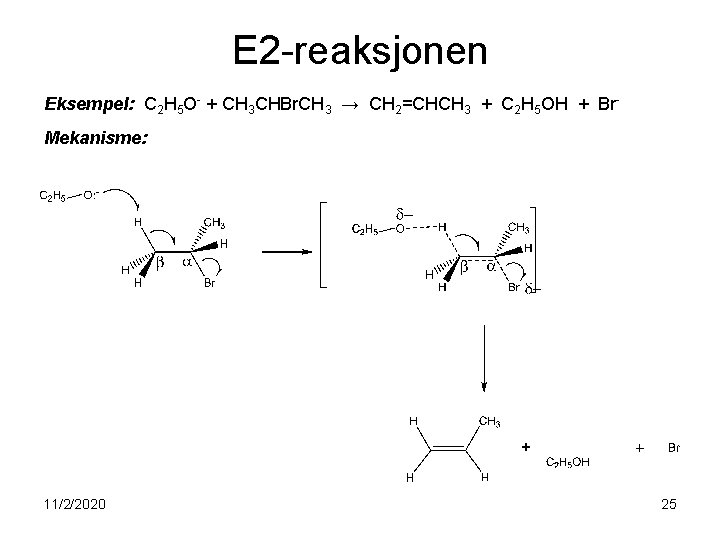
E 2 -reaksjonen Eksempel: C 2 H 5 O- + CH 3 CHBr. CH 3 → CH 2=CHCH 3 + C 2 H 5 OH + Br. Mekanisme: 11/2/2020 25

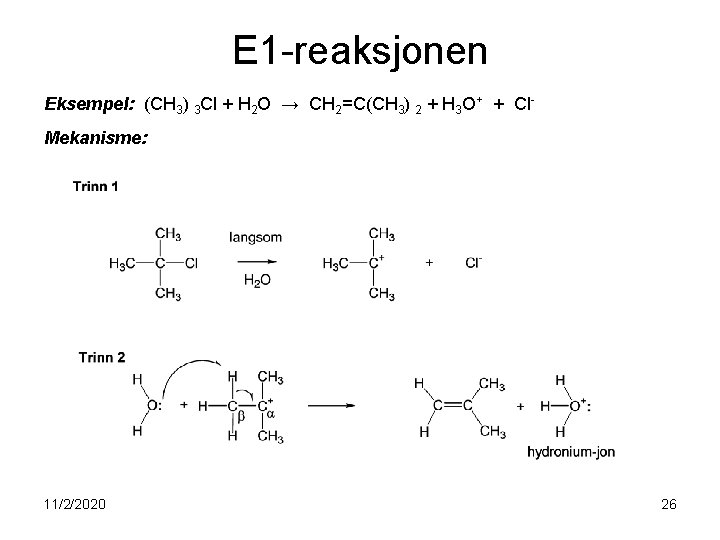
E 1 -reaksjonen Eksempel: (CH 3) 3 Cl + H 2 O → CH 2=C(CH 3) 2 + H 3 O+ + Cl. Mekanisme: 11/2/2020 26

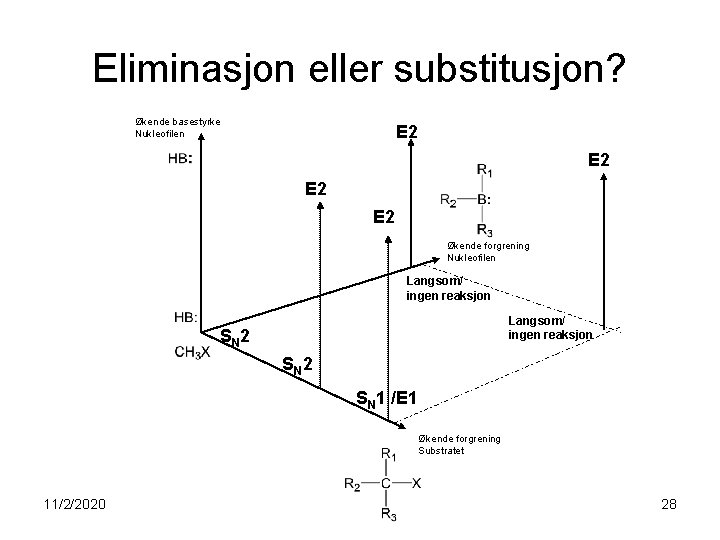
Eliminasjon eller substitusjon? 11/2/2020 27

Eliminasjon eller substitusjon? Økende basestyrke Nukleofilen E 2 E 2 Økende forgrening Nukleofilen Langsom/ ingen reaksjon SN 2 SN 1 /E 1 Økende forgrening Substratet 11/2/2020 28

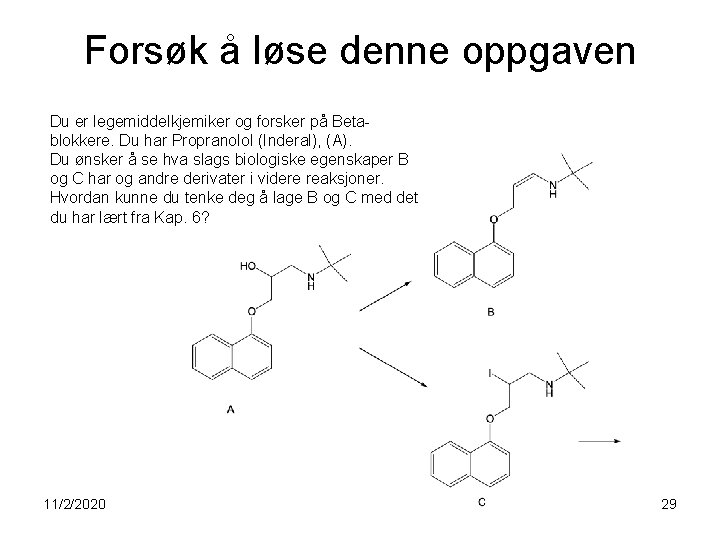
Forsøk å løse denne oppgaven Du er legemiddelkjemiker og forsker på Betablokkere. Du har Propranolol (Inderal), (A). Du ønsker å se hva slags biologiske egenskaper B og C har og andre derivater i videre reaksjoner. Hvordan kunne du tenke deg å lage B og C med det du har lært fra Kap. 6? 11/2/2020 29

Øv på disse oppgavene • 6. 1 • 6. 2 • 6. 13 – 6. 14 • 6. 16 – 6. 18 • 6. 29 • 6. 32 11/2/2020 30