Ionenbindung Ulla Lehmann Natrium ist ein Alkalimetall Es

Ionenbindung - + - + - + - - + - + Ulla Lehmann

Natrium ist ein Alkalimetall. Es gehört zur ersten Gruppe im Periodensystem der Elemente und ist sehr reaktionsfreudig. Natrium wird unter Petroleum aufbewahrt, um einen Kontakt mit Sauerstoff zu vermeiden.
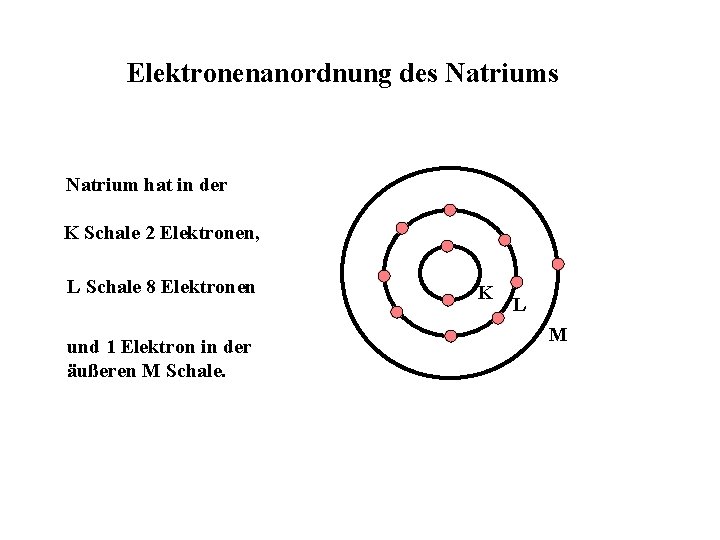
Elektronenanordnung des Natrium hat in der K Schale 2 Elektronen, L Schale 8 Elektronen und 1 Elektron in der äußeren M Schale. K L M

Chlor ist ein Halogen. Es gehört zur siebten Gruppe im Periodensystem der Elemente und ist ebenfalls sehr reaktionsfreudig.
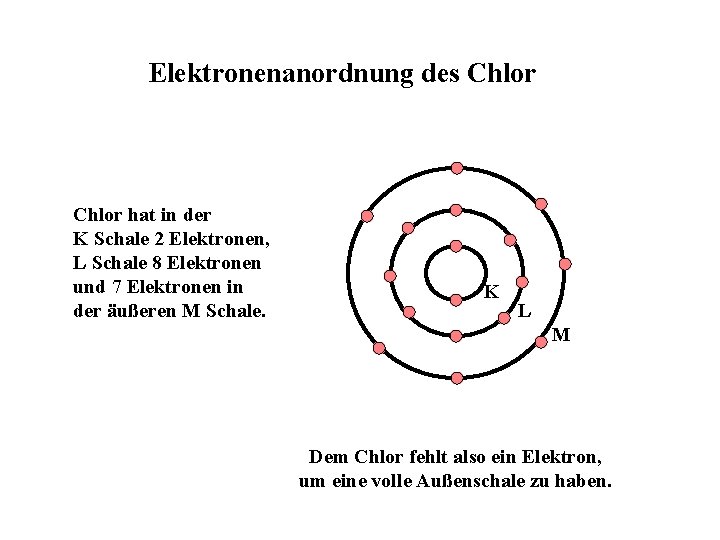
Elektronenanordnung des Chlor hat in der K Schale 2 Elektronen, L Schale 8 Elektronen und 7 Elektronen in der äußeren M Schale. K L M Dem Chlor fehlt also ein Elektron, um eine volle Außenschale zu haben.

Natrium und Chlor reagieren sehr heftig miteinander. Dabei entsteht Natriumchlorid, Kochsalz.

Ionenbindung beim Natriumchlorid Natrium Chlor Das Natrium gibt sein äußeres Elektron an das Chlor ab.
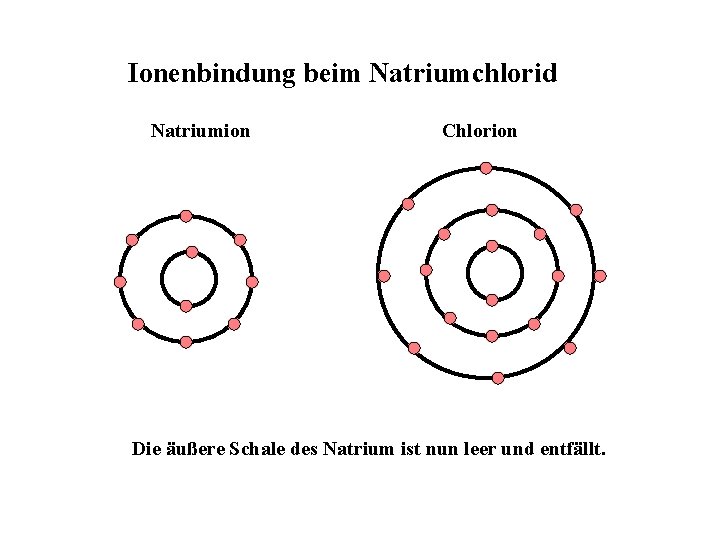
Ionenbindung beim Natriumchlorid Natriumion Chlorion Die äußere Schale des Natrium ist nun leer und entfällt.
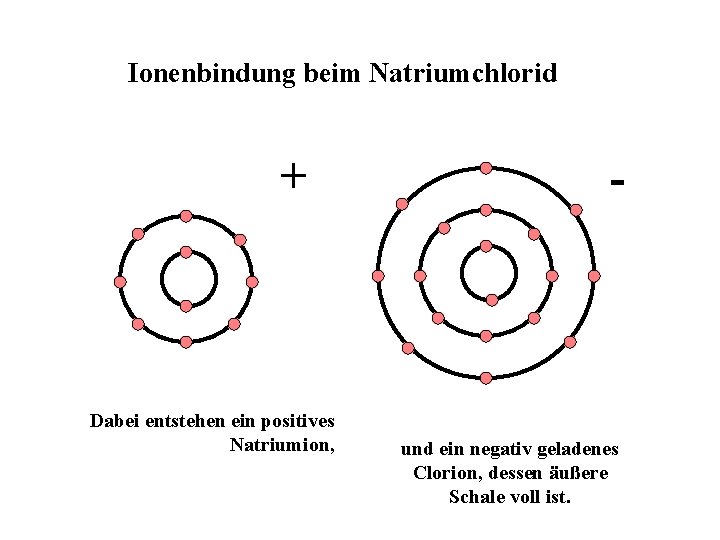
Ionenbindung beim Natriumchlorid + Dabei entstehen ein positives Natriumion, - und ein negativ geladenes Clorion, dessen äußere Schale voll ist.
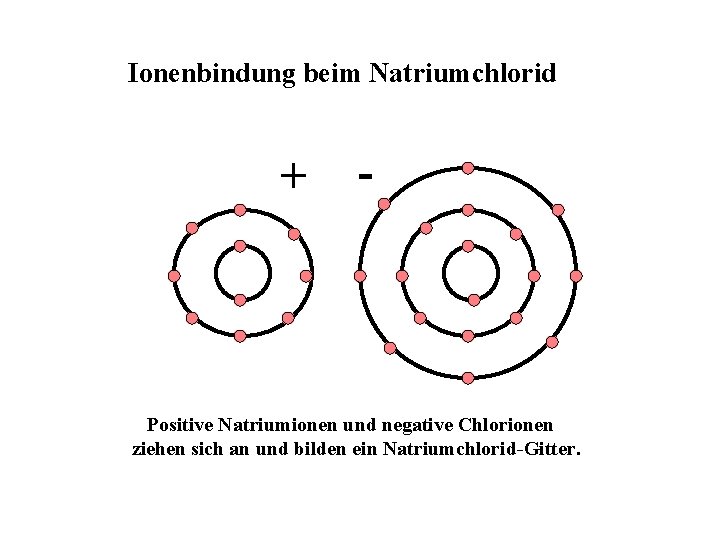
Ionenbindung beim Natriumchlorid + - Positive Natriumionen und negative Chlorionen ziehen sich an und bilden ein Natriumchlorid-Gitter.
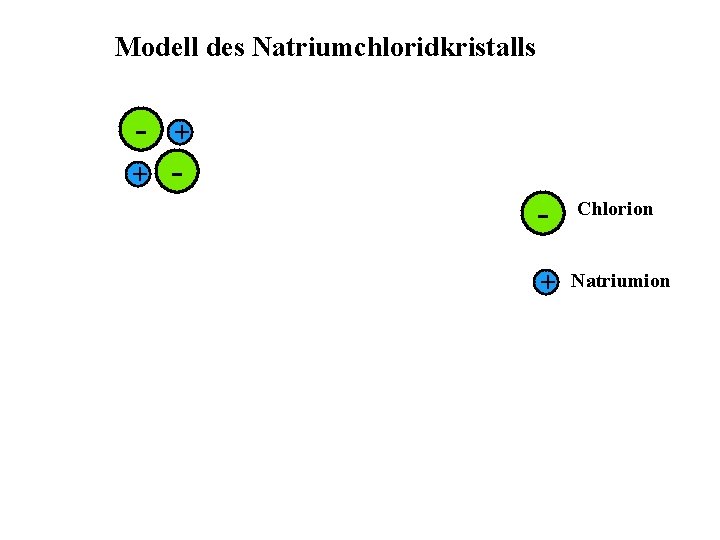
Modell des Natriumchloridkristalls - + + - Chlorion + Natriumion
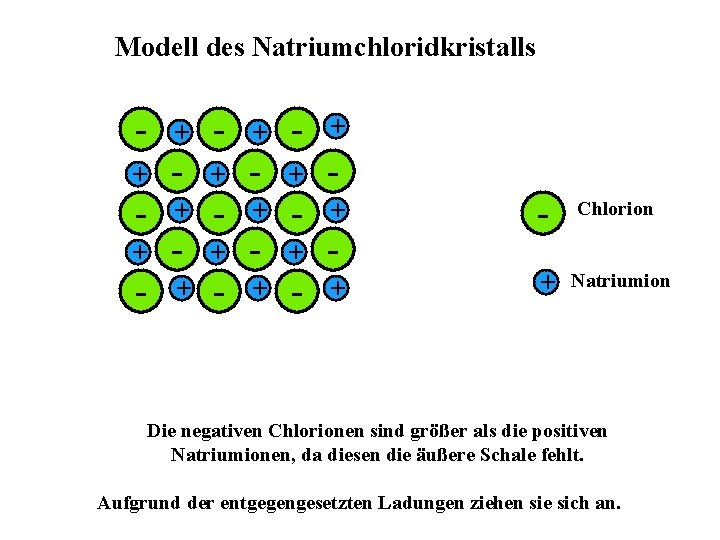
Modell des Natriumchloridkristalls - + - + - + - - + - + - Chlorion + Natriumion Die negativen Chlorionen sind größer als die positiven Natriumionen, da diesen die äußere Schale fehlt. Aufgrund der entgegengesetzten Ladungen ziehen sie sich an.
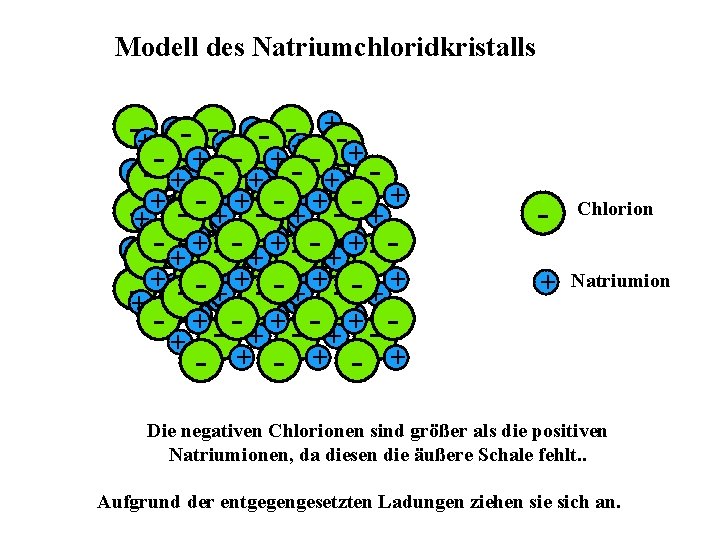
Modell des Natriumchloridkristalls -- + - ++ - -- ++ + -- - + + --- +++ -+ + -- ++ -- + + --- +++ -- ++ - + - + ++ ++ -- + ++ - - ++ -- + - - + + - Chlorion + Natriumion + + -- ++ - + - + + Die negativen Chlorionen sind größer als die positiven Natriumionen, da diesen die äußere Schale fehlt. . Aufgrund der entgegengesetzten Ladungen ziehen sie sich an.
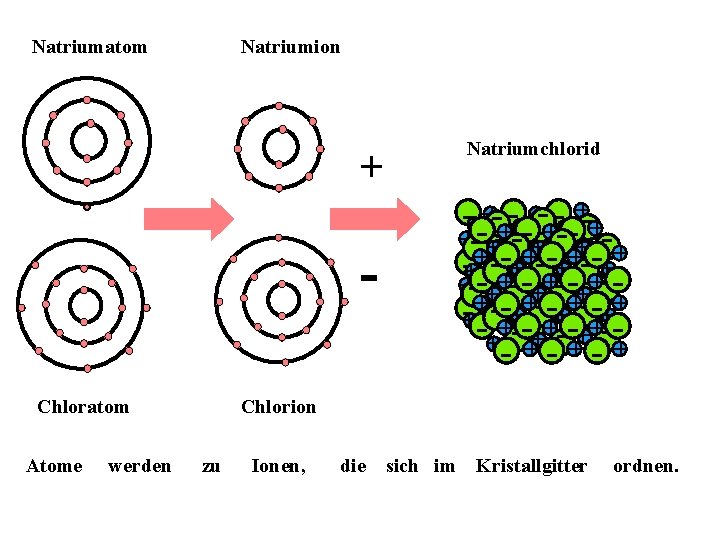
Natriumatom Natriumion Natriumchlorid + - -++- -++ +- +- +-+-+-++-+- +- +- -+-+-++-+-+-++-+- -+ - +- +- + + -- + - ++ + +- + - ++ - +- - + Chloratom Atome werden Chlorion zu Ionen, die sich im Kristallgitter ordnen.

Natriumchlorid Na. Cl Natrium und Chlor haben im Verhältnis 1: 1 zu Kochsalz reagiert. Die Natriumionen sind einfach positiv und die Chlorionen einfach negativ.

Edelgase reagieren praktisch nicht. Ihr atomarer Aufbau ist sehr stabil. Edelgase haben immer eine gefüllte Außenschale und eine besonders hohe Ionisierungsenergie, das heißt man benötigt besonders viel Energie, um ein Elektron aus der äußeren Schale zu entfernen. Diese Energie kann unter normalen Bedingungen von anderen Atomen nicht aufgebracht werden. Eine gefüllte Außenschale mit 8 Außenelektronen (Ausnahme Helium mit 2 Außenelektronen) nennt man Edelgaskonfiguration (edelgasähnlicher Aufbau). Andere Atome streben diesen für sie energiemäßig günstigen Aufbau, nämlich die Edelgaskonfiguration, durch Abgabe (Elemente der 1. , 2. und 3. Gruppen) oder Aufnahme von Elektronen (Elemente der 6. und 7. Gruppen) an. Dabei folgen sie der Oktettregel, 8 Außenelektronen anzustreben. Sie werden dadurch zu Ionen.
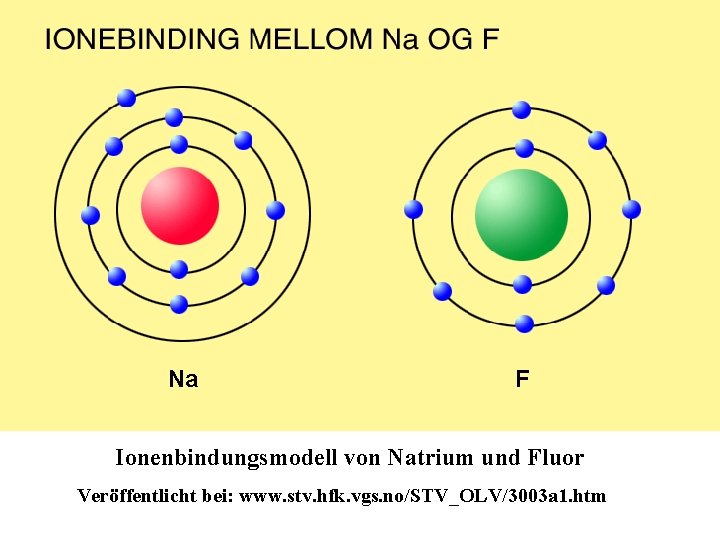
Na F Ionenbindungsmodell von Natrium und Fluor Veröffentlicht bei: www. stv. hfk. vgs. no/STV_OLV/3003 a 1. htm

Ende Teil 1

- Slides: 19