Investigando las bases moleculares de una enfermedad gentica

Investigando las bases moleculares de una enfermedad genética: Síndrome de deleción 22 q 11. 2 Sara R. Heras José Luís García Pérez lab Genyo, Granada
Síndrome de deleción 22 q 11. 2 SD 22 q 11. 2 es la enfermedad genética producida por una microdelección cromosómica MAS FRECUENTE EN HUMANOS PREVALENCIA ESTIMADA: 1 de cada 1000 fetos 1 CADA 4000 NACIMIENTOS Los signos y síntomas del síndrome de deleción 22 q 11. 2 varían de una persona afectada a otra. El síndrome de Di. George El síndrome velocardiofacial (VCFS) El síndrome de Shprintzen CATCH 22 El síndrome de Sedlackova
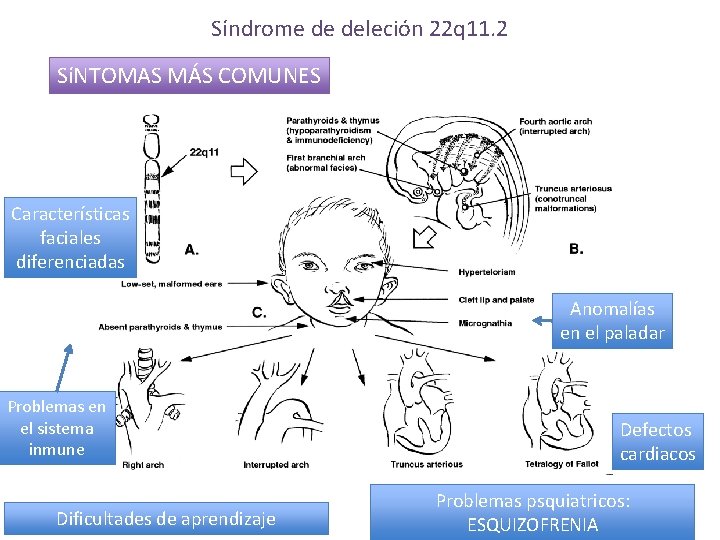
Síndrome de deleción 22 q 11. 2 SíNTOMAS MÁS COMUNES Características faciales diferenciadas Anomalías en el paladar Problemas en el sistema inmune Dificultades de aprendizaje Defectos cardiacos Problemas psquiatricos: ESQUIZOFRENIA
Síndrome de deleción 22 q 11. 2 CAUSA: DESORDEN GENÉTICO
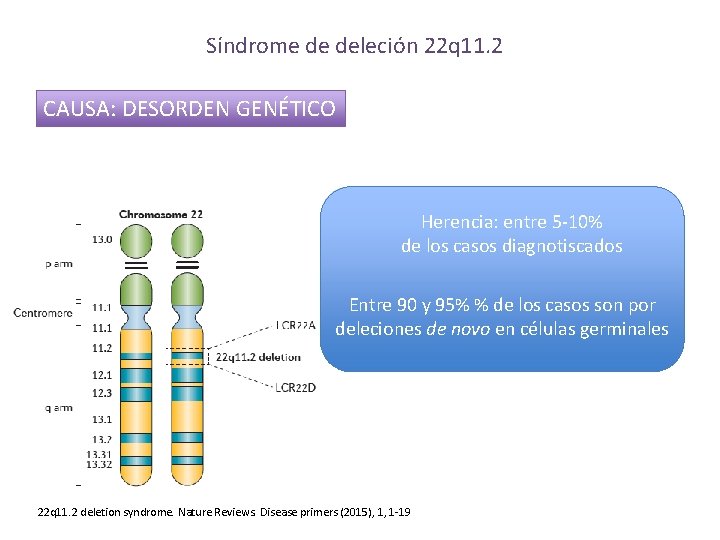
Síndrome de deleción 22 q 11. 2 CAUSA: DESORDEN GENÉTICO Herencia: entre 5 -10% de los casos diagnotiscados Entre 90 y 95% % de los casos son por deleciones de novo en células germinales 22 q 11. 2 deletion syndrome. Nature Reviews. Disease primers (2015), 1, 1 -19
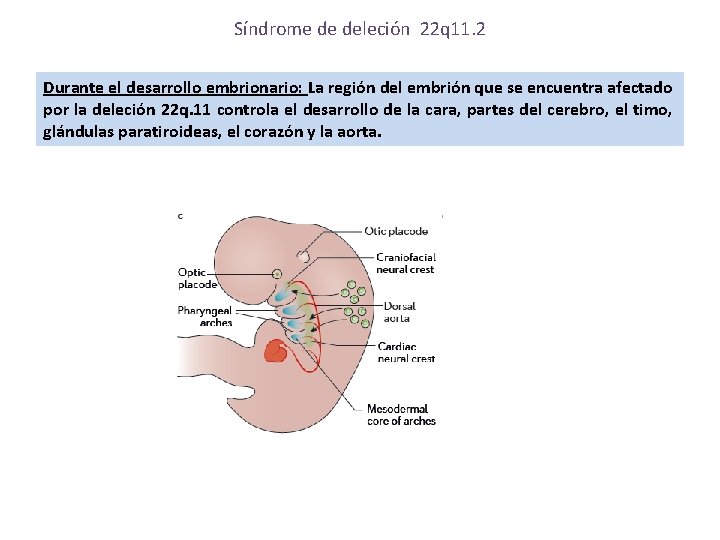
Síndrome de deleción 22 q 11. 2 Durante el desarrollo embrionario: La región del embrión que se encuentra afectado por la deleción 22 q. 11 controla el desarrollo de la cara, partes del cerebro, el timo, glándulas paratiroideas, el corazón y la aorta.
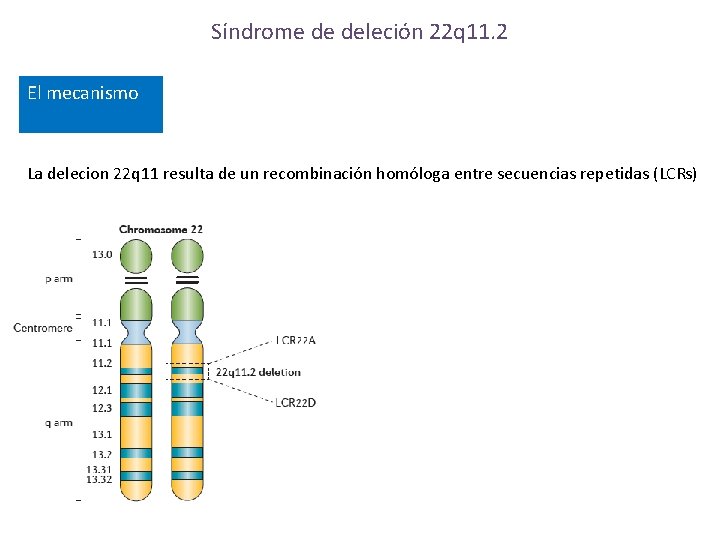
Síndrome de deleción 22 q 11. 2 El mecanismo La delecion 22 q 11 resulta de un recombinación homóloga entre secuencias repetidas (LCRs)
Grandes preguntas sobre la enfermedad quedan por contestar: Por que la region 22 q 11 es particularmente vulnerable a ser delecionada? Por que existe la gran variabilidad clínica? ? -Por las variaciones de los genes en la región 22 q 11. 2 del cromosoma no delecionado --Por genes fuera de la región delecionada.
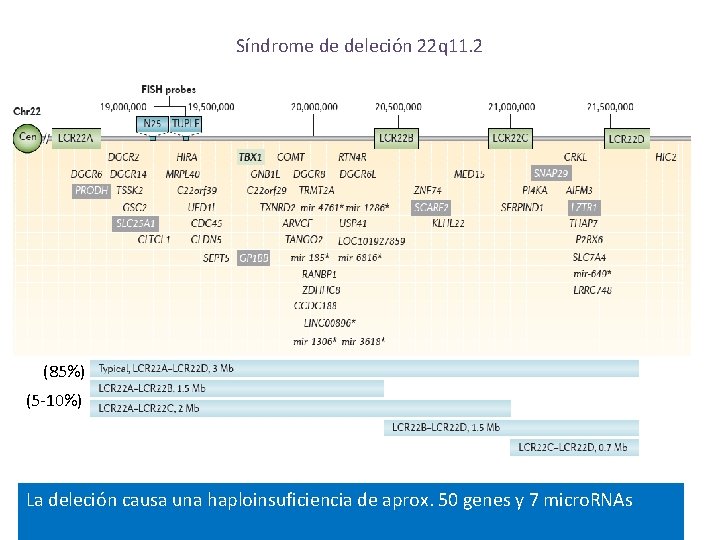
Síndrome de deleción 22 q 11. 2 (85%) (5 -10%) La deleción causa una haploinsuficiencia de aprox. 50 genes y 7 micro. RNAs
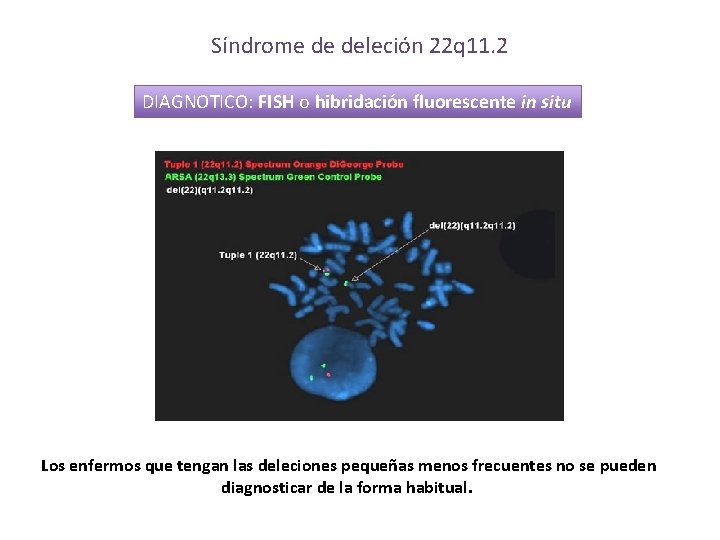
Síndrome de deleción 22 q 11. 2 DIAGNOTICO: FISH o hibridación fluorescente in situ Los enfermos que tengan las deleciones pequeñas menos frecuentes no se pueden diagnosticar de la forma habitual.

CONOCER LAS BASES MOLECULARES DE ESTA ENFERMEDAD ES FUNDAMENTAL PARA ENCONTRAR NUEVOS TRATAMIENTOS

OBJETIVOS DE LOS CIENTÍFICOS DURANTE LA ÚLTIMA DECADA: IDENTIFICAR QUE GEN O GENES SON RESPONSABLES DE CADA SINTOMA MODELOS DE RATÓN
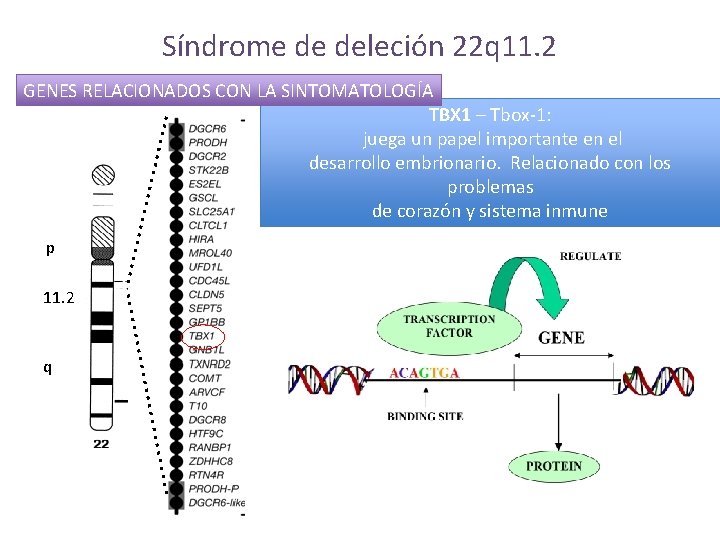
Síndrome de deleción 22 q 11. 2 GENES RELACIONADOS CON LA SINTOMATOLOGÍA TBX 1 – Tbox-1: juega un papel importante en el desarrollo embrionario. Relacionado con los problemas de corazón y sistema inmune p 11. 2 q
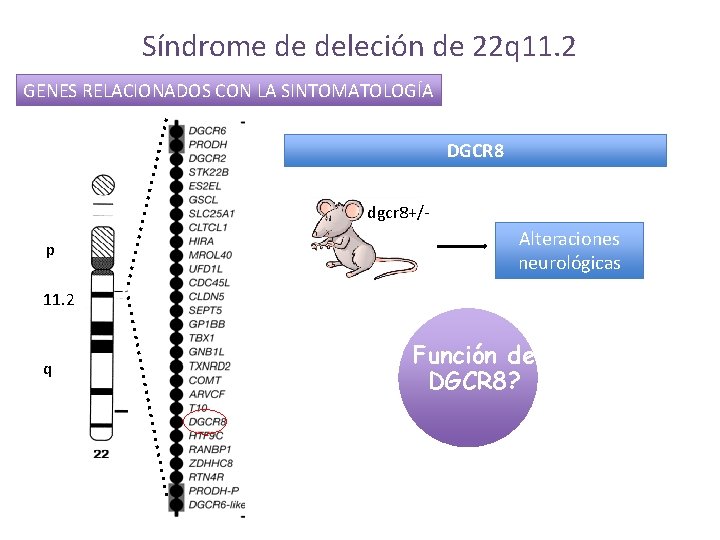
Síndrome de deleción de 22 q 11. 2 GENES RELACIONADOS CON LA SINTOMATOLOGÍA DGCR 8 dgcr 8+/p Alteraciones neurológicas 11. 2 q Función de DGCR 8?
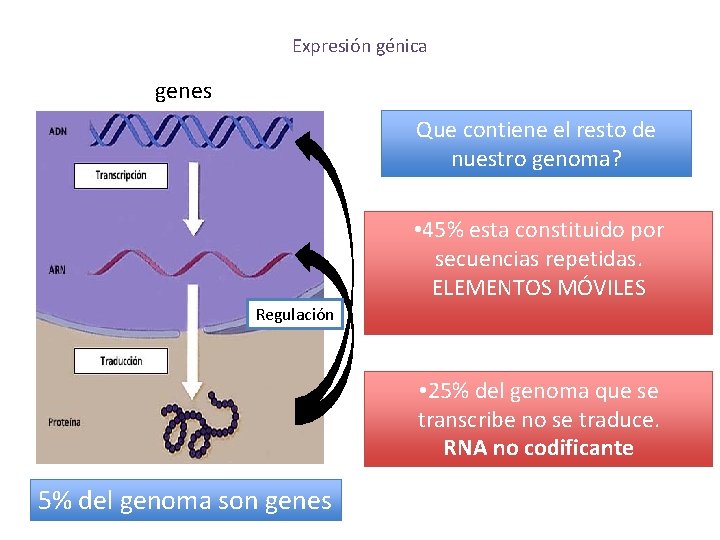
Expresión génica genes Que contiene el resto de nuestro genoma? • 45% esta constituido por secuencias repetidas. ELEMENTOS MÓVILES Regulación • 25% del genoma que se transcribe no se traduce. RNA no codificante 5% del genoma son genes
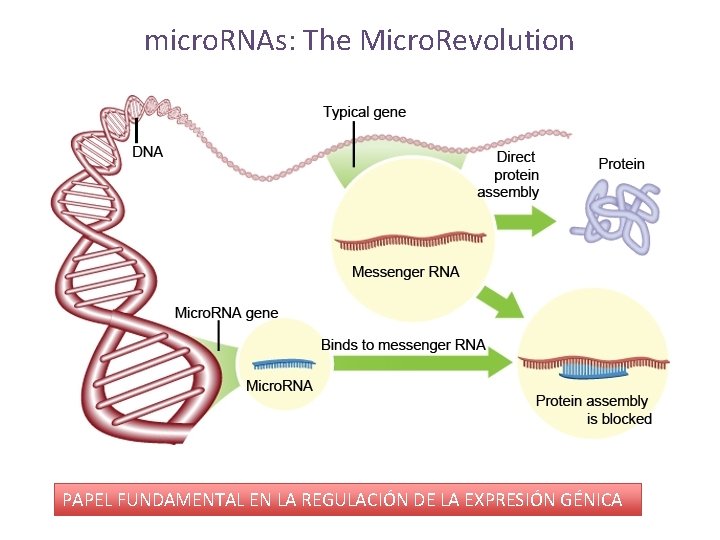
micro. RNAs: The Micro. Revolution PAPEL FUNDAMENTAL EN LA REGULACIÓN DE LA EXPRESIÓN GÉNICA
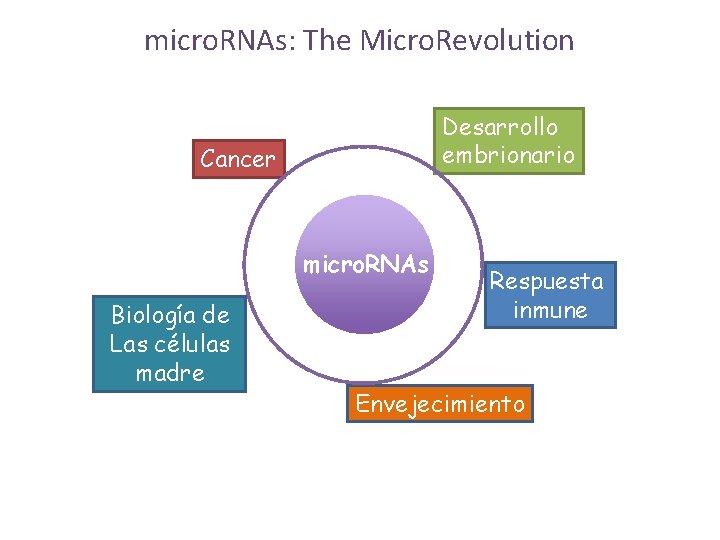
micro. RNAs: The Micro. Revolution Desarrollo embrionario Cancer micro. RNAs Biología de Las células madre Respuesta inmune Envejecimiento

Papel de DGCR 8 en el Síndrome 22 q 11 Ausencia de micro. RNAs puede ser responsible de parte de las alteraciones de pacientes SD 22 q 11 durante el desarrollo embrionario y de los problemas neurológicos en la etapa adulta dgcr 8+/- Alteraciones neurológicas
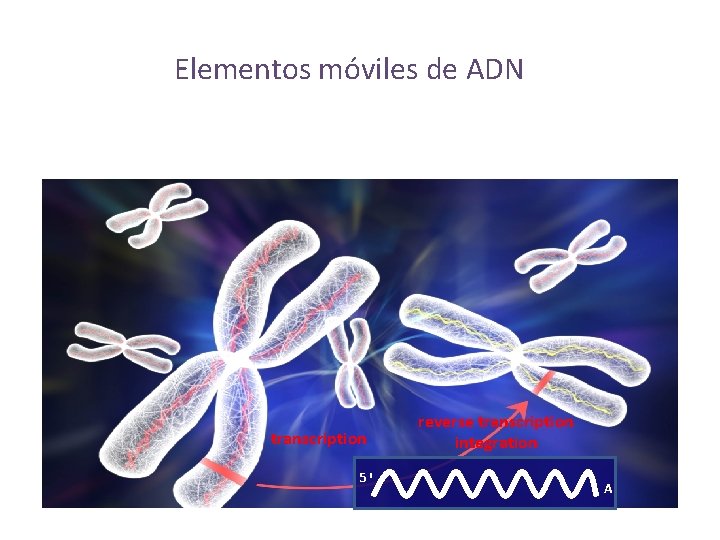
Elementos móviles de ADN transcription 5' reverse transcription integration A
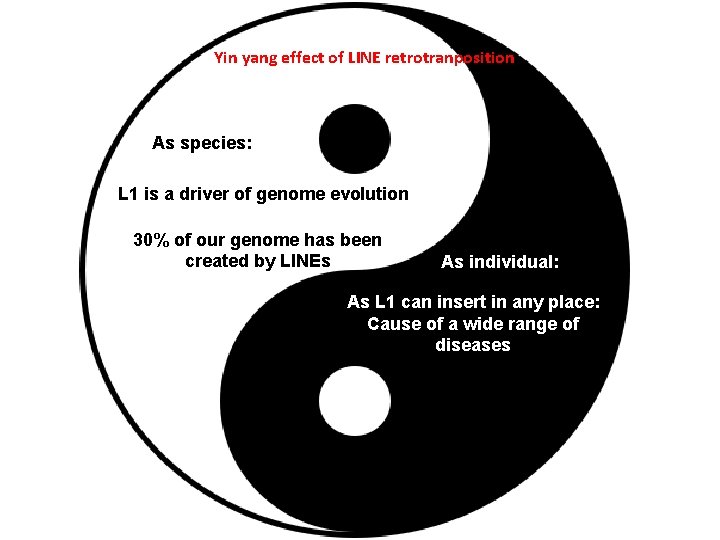
Yin yang effect of LINE retrotranposition As species: L 1 is a driver of genome evolution 30% of our genome has been created by LINEs As individual: As L 1 can insert in any place: Cause of a wide range of diseases
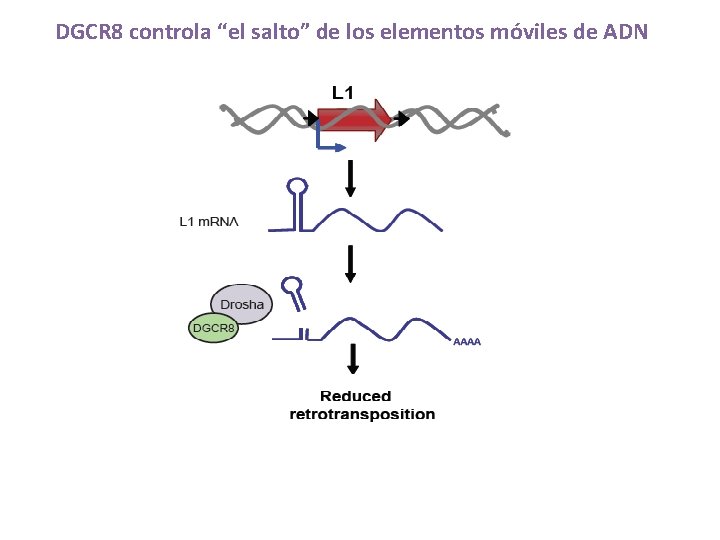
DGCR 8 controla “el salto” de los elementos móviles de ADN
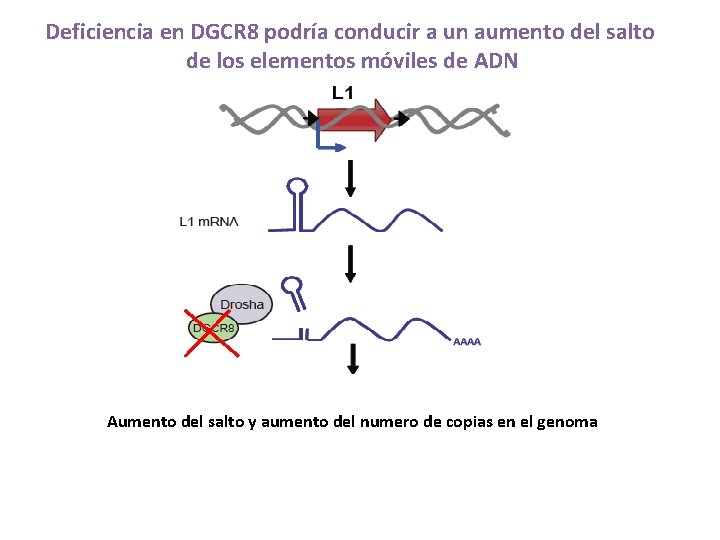
Deficiencia en DGCR 8 podría conducir a un aumento del salto de los elementos móviles de ADN Aumento del salto y aumento del numero de copias en el genoma
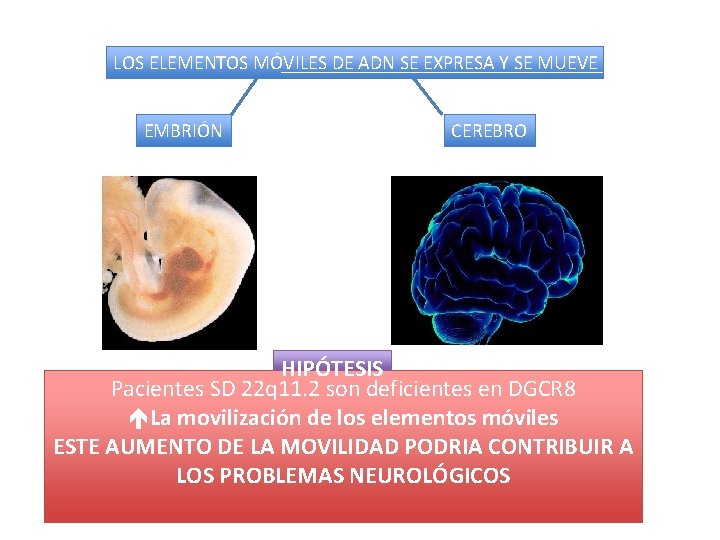
LOS ELEMENTOS MÓVILES DE ADN SE EXPRESA Y SE MUEVE EMBRIÓN CEREBRO HIPÓTESIS Pacientes SD 22 q 11. 2 son deficientes en DGCR 8 éLa movilización de los elementos móviles ESTE AUMENTO DE LA MOVILIDAD PODRIA CONTRIBUIR A LOS PROBLEMAS NEUROLÓGICOS

OBJETIVOS Determinar el impacto de la des-regulación de los ELEMENTOS MÓVILES en SD 22 q 11. 2. Determinar la contribución a la sitomatología de la enfermedad PERSPECTIVAS: TRATAR LA CAUSA Y NO EL SÍNTOMA Mejorar el tratamiento de la enfermedad: -Uso de fármacos inhibidores del “salto” de los elementos móviles.

ACKNOWLEDGEMENTS Jose Luis García-Pérez lab Martín Muñoz Thomas Widmann Marta García Eva Blanco Pablo Tristán David Cano Andrés Pulgarín Valentín Sánchez Meriem Benkaddour César López Ana Ariza Laura Sánchez Raquel Vilar Alejandro Rubio Former Ph. D student: Santiago Morell Angela Maciá Alexandra Helwak (Edinburgh, UK) Pedro Medina lab Marie-Curie CIG-Grant (PCIG-GA-2011 -303812)
- Slides: 25