Introduo s reaes orgnicas e seus mecanismos cidobase

Introdução às reações orgânicas e seus mecanismos (ácido-base) Química Orgânica II Prof. Alonso Goes

Reações � Se enquadram em 4 categorias: ◦ Substituição, Adição, Eliminação, ou rearranjo. � SUBSTITUIÇÃO: ◦ reac o es caracteri sticas de compostos saturados, tais como alcanos, haletos de alquila e compostos aroma ticos (mesmo eles sendo insaturados).
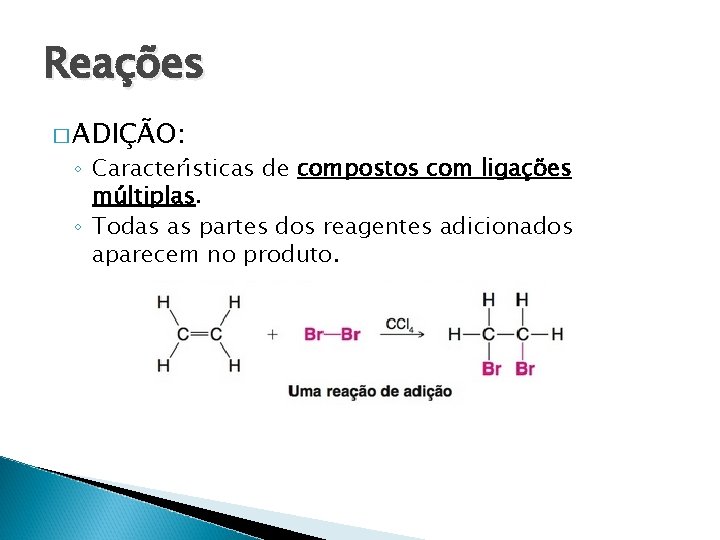
Reações � ADIÇÃO: ◦ Caracteri sticas de compostos com ligac o es mu ltiplas. ◦ Todas as partes dos reagentes adicionados aparecem no produto.

Reações � ELIMINAÇÃO: ◦ É o oposto da adic ão. ◦ Em uma eliminac a o uma mole cula perde os elementos de outra mole cula pequena. ◦ Fornecem um me todo para a preparac a o de compostos com ligac o es duplas e triplas.
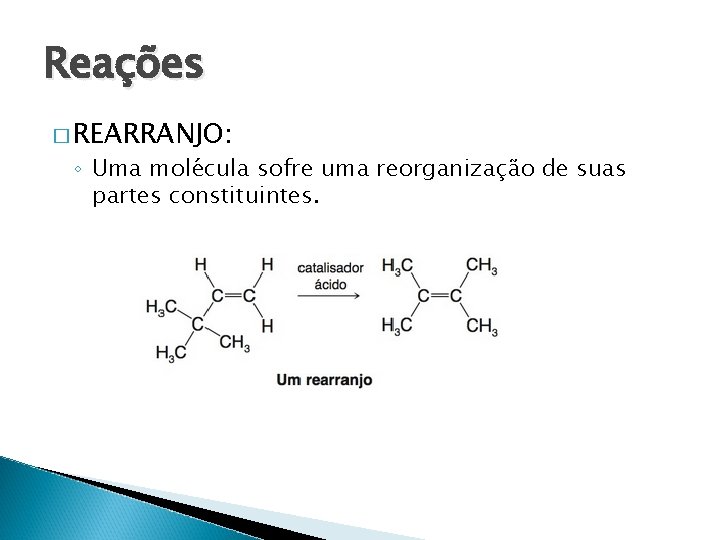
Reações � REARRANJO: ◦ Uma mole cula sofre uma reorganizac a o de suas partes constituintes.

Homo lise e Hetero lise de Ligac o es Covalentes � As reac o es de compostos orga nicos sempre envolvem a formac a o e a quebra de ligac o es covalentes. � Pode quebrar de duas maneiras diferentes.

Hetero lise � Pode quebrar de tal forma que um fragmento retira ambos os ele trons da ligac a o, deixando o outro fragmento com um orbital vazio. � produz fragmentos carregados ou i ons e e denominada reac a o io nica; � No geral, requer que a ligac a o seja polarizada. Apresentam diferentes eletronegatividades.

Homólise �A ligac a o se quebra e cada fragmento retira um dos ele trons da ligac a o; � Produz fragmentos com ele trons desemparelhados chamados de radicais.

Reac o es A cido–Base � Muitas das reac o es que ocorrem na qui mica orga nica sa o reac o es do tipo a cido–base; � Ou envolvem uma reac a o a cido–base em alguma etapa. � Usam-se setas curvas para representar os mecanismos das reações.

A cidos e Bases de Brønsted–Lowry � Envolvem a transfere ncia de pro tons. � Um a cido de Brønsted–Lowry e uma substa ncia que pode doar (ou perder) um pro ton; � Uma base de Brønsted–Lowry e uma substa ncia que pode receber (ou remover) um pro ton.

A cidos e Bases de Lewis � A cidos sa o receptores de pares de ele trons. � Bases sa o doadores de pares de ele trons.
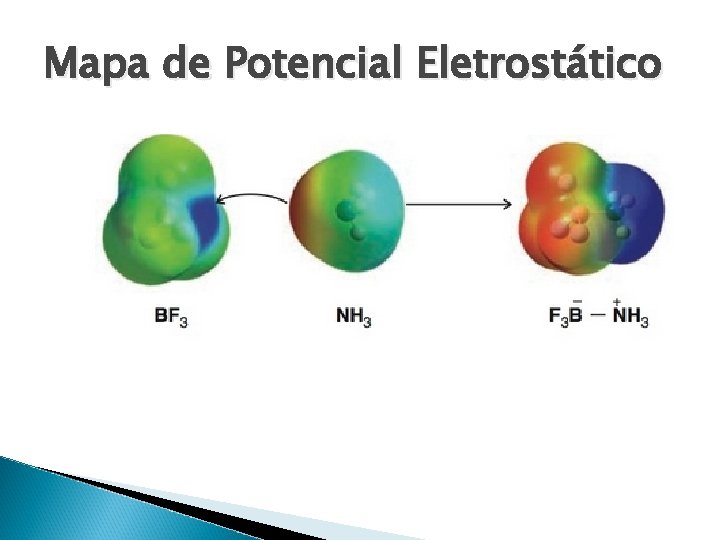
Mapa de Potencial Eletrostático

Hetero lise de Ligac o es com Carbono: Carboca tions e Carba nions � íon com uma carga positiva no a tomo de carbono – carboca tion; � i on com um a tomo de carbono carregado negativamente - carba nion

Carbocátion � Reagem rapidamente com bases de Lewis — mole culas ou i ons que podem doar o par de ele trons que eles precisam para atingir um octeto esta vel de ele trons.
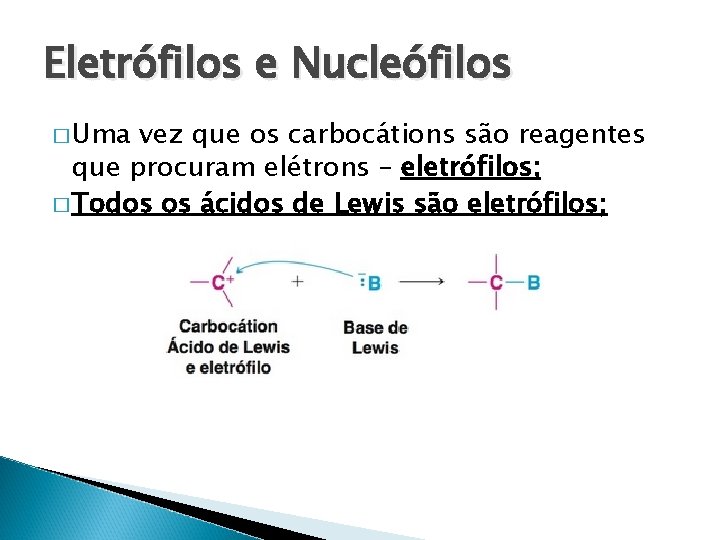
Eletro filos e Nucleo filos � Uma vez que os carboca tions sa o reagentes que procuram ele trons – eletro filos; � Todos os a cidos de Lewis sa o eletro filos;
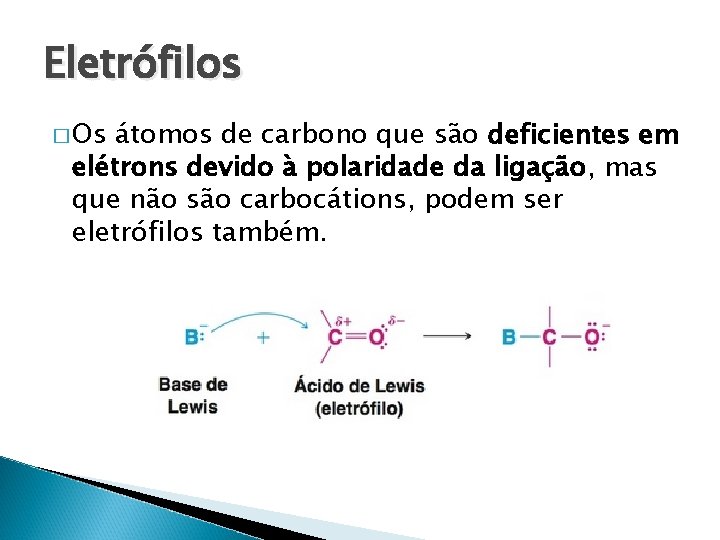
Eletro filos � Os a tomos de carbono que sa o deficientes em ele trons devido a polaridade da ligac a o, mas que na o sa o carboca tions, podem ser eletro filos tambe m.

Nucleófilos � Os carba nions sa o bases de Lewis. � Procuram um pro ton ou algum outro centro positivo para o qual eles possam doar seu par de ele trons e, dessa maneira, neutralizar a sua carga negativa.

Setas Curvas na Representac a o de Reac o es � Mostram a direc a o do fluxo de ele trons em um mecanismo de reac a o. � Dirigem-se da fonte de um par de ele trons para o a tomo que recebe esse par. (Setas curvas tambe m podem mostrar o movimento de um u nico ele tron; � Sempre mostram o fluxo de ele trons de uma regia o de elevada densidade eletro nica para uma regia o de baixa densidade eletro nica.

Uso de setas curvas
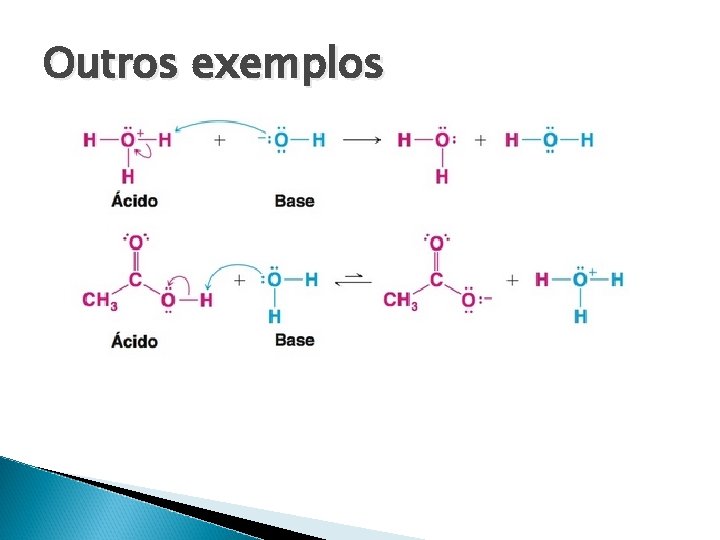
Outros exemplos
- Slides: 20