Introduo a Bioqumica Biomolculas Aula 1 Introduo ao

Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao Curso Representação das Moléculas Aminoácidos Ignez Caracelli Julio Zukerman Schpector Bio. Mat – DF – UNESP/Bauru La. Cr. EMM – DQ – UFSCar Bauru, 17 de agosto de 2009. 1

Avaliação • • 1 seminário em grupo (S) 1 prova (P) atividades (A) média (M) M = 0, 4 S + 0, 6 P + A 2

Avaliação - Conceitos M = 0, 4 S + 0, 6 P + A 6 M 7, 0 7, 1 M 8, 5 conceito C conceito B 8, 6 M 10, 0 conceito A 3

E-mails bit. 603@gmail. com envio e entrega de material e exercícios urgente: ignez@fc. unesp. br julio@power. ufscar. br 4

Sites (disponibilização de material) www. quimica. ufscar. br ou www. ignez. com disciplinas BIT 603 5

Ementa • • • proteínas DNA. lipídeos. açúcares. enzimas. o que está acontecendo… 6
Ementa bioquímica estrutural 7

Ferramentas • • • programas de visualização gráfica bancos de dados conhecimentos de química conhecimentos de bioquímica conhecimentos de interações, ligações 8

Referência Autores: Autores Ignez Caracelli e Julio Zukerman-Schpector Editora: Editora Ed. UFSCar ISBN: 85 -7600 -065 -2 9

Principais Referências • Lehninger • Voet & Voet • Voet, Voet & Pratt 10
Bancos de Dados PDBSum NDB http: //www. rcsb. org/pdb/ http: //www. ebi. ac. uk/thornton-srv/databases/pdbsum/ http: //ndbserver. rutgers. edu/NDB/structurefinder/index. html 11
Estrutura Sistemas Biológicos métodos experimentais espectroscopia UV-visível espectroscopia Raman espectroscopia IV dicroísmo circular ressonância paramagnética eletrônica (EPR) ressonância magnética nuclear (NMR) difração de raios X métodos teóricos modelagem por homologia docking dinâmica molecular alinhamento IC de seqüências 12

Estrutura Ferramentas Computacionais métodos experimentais métodos teóricos difração de raios X modelagem por homologia docking dinâmica molecular alinhamento IC de seqüências 13
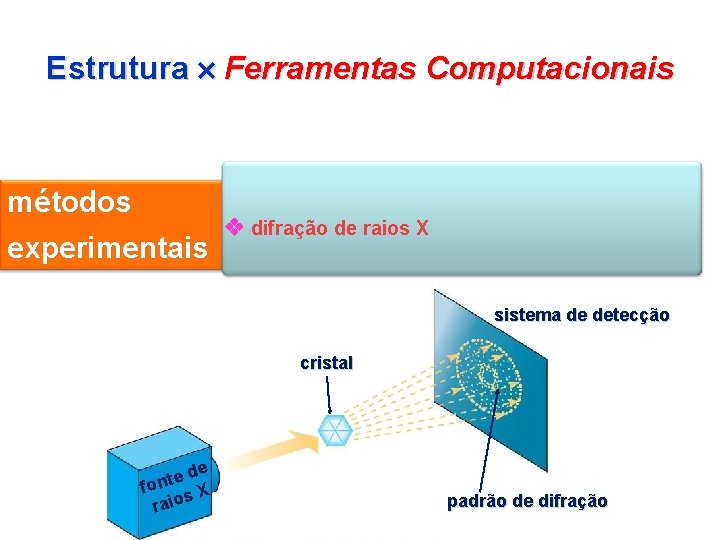
Estrutura Ferramentas Computacionais métodos experimentais difração de raios X sistema de detecção cristal de e t fon s X raio padrão de difração

Estrutura Ferramentas Computacionais métodos teóricos modelagem por homologia docking dinâmica molecular alinhamento IC de seqüências 15

Desafios do século XX problemas dos sistemas “não-vivos”– condutores, supercondutores, novos materiais, energia, radiações, comunicações, . . envolvidos: física, química, matemática, computação, engenharias, . . . IC 16

Desafios do século XXI problemas dos sistemas biológicos envolvidos: física, química, matemática, computação, engenharias, . . . + biologia, bioquímica, genética, fisiologia, . . . IC 17

Desafios dos séculos XX e XXI Genoma: estuda a molécula de DNA e a informação nela armazenada Genoma: sob a forma de genes. Transcriptoma: a transcrição do DNA para o RNA, o primeiro passo Transcriptoma: do fluxo da informação genética, para que seja possivel ter uma idéia da funcionalidade do genoma daquela célula. Proteoma: as proteínas expressas são analisadas e identificadas Proteoma: Metaboloma: visa determinar os metabólitos, os produtos finais dos Metaboloma: diversos processos celulares e que podem englobar, além dos nucleotídeos e aminoácidos, os açúcares, lipídios, esteróides e mais uma infinidade de outras moléculas importantes para a manutenção da atividade biológica. IC 18

Desafios do século XXI 14. 000 genes 20. 000 genes IC 19

Desafios do século XXI Interactoma: estudo das interações proteína- proteína, proteína IC dna, proteína- moléculas pequenas, …. 20
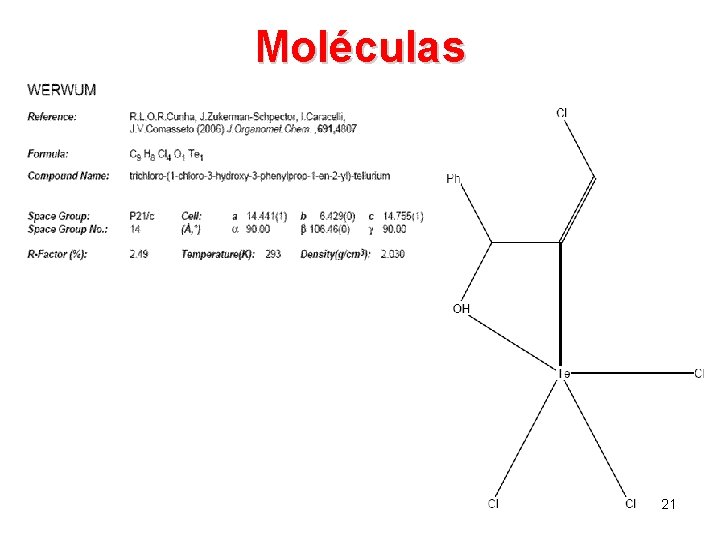
Moléculas 21
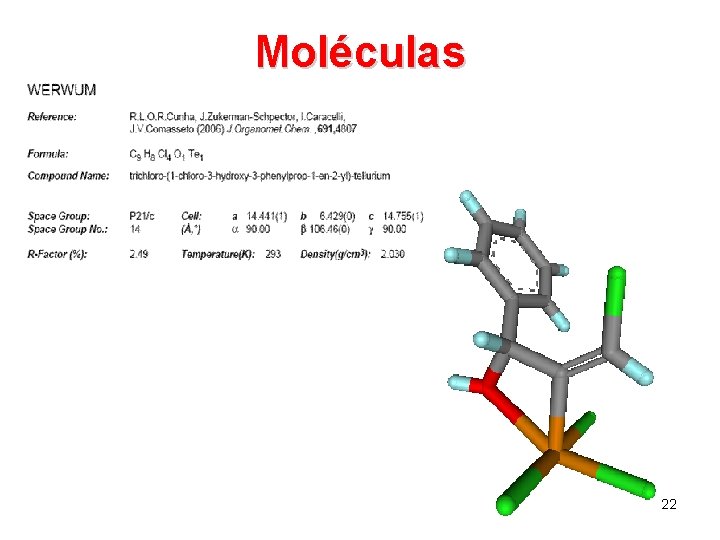
Moléculas 22
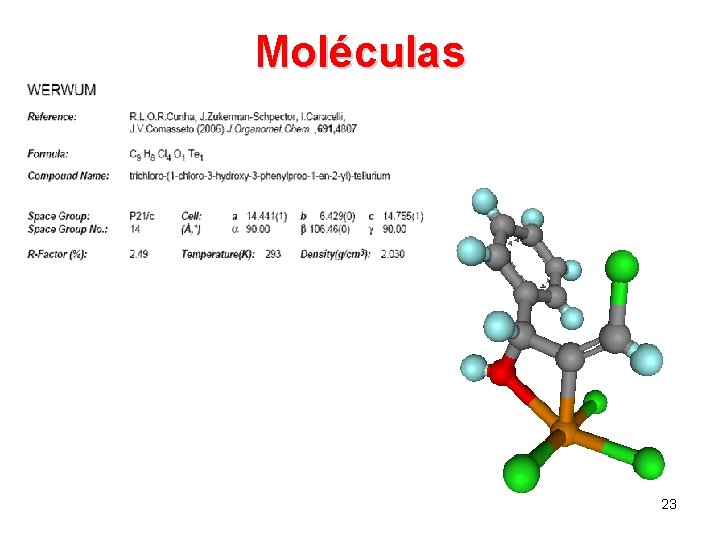
Moléculas 23
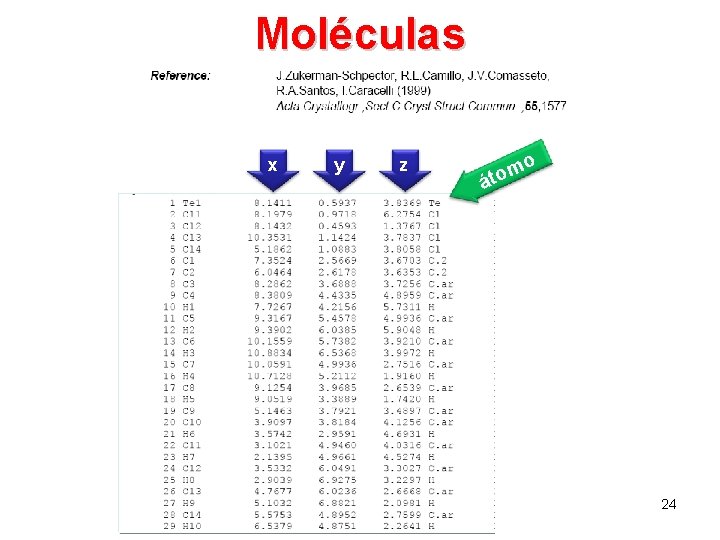
Moléculas x y z o m áto 24

Estrutura tridimensional = conhecer as coordenadas de todos os átomos IC 25
Linguagem x Informação letras aminoácidos frases proteínas 26
Problema Central frases proteínas texto função 27

Estruturas tridimensionais métodos experimentais métodos teóricos 28
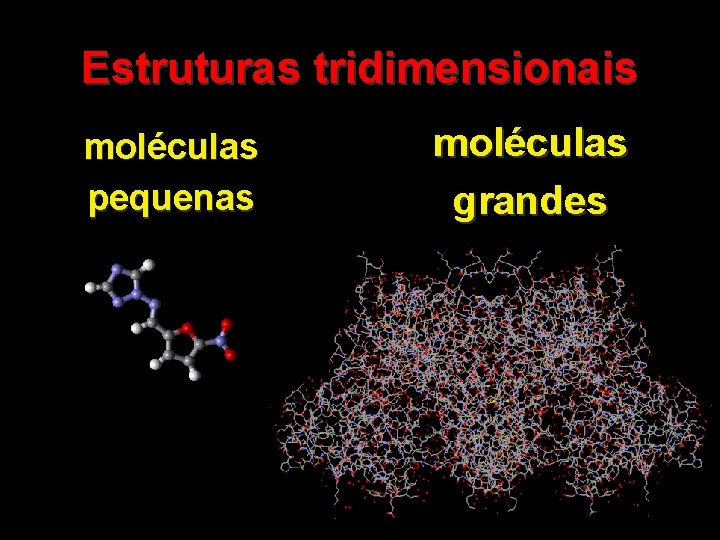
Estruturas tridimensionais moléculas pequenas moléculas grandes 29

Estruturas Tridimensionais métodos experimentais: cristal 30
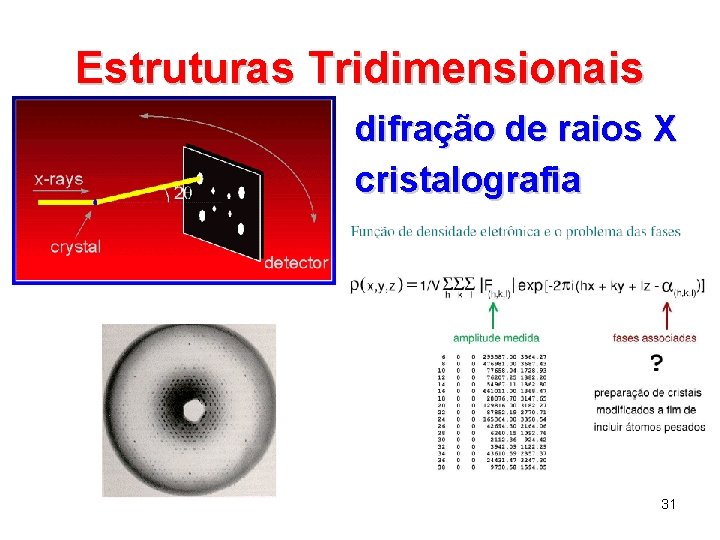
Estruturas Tridimensionais difração de raios X cristalografia 31
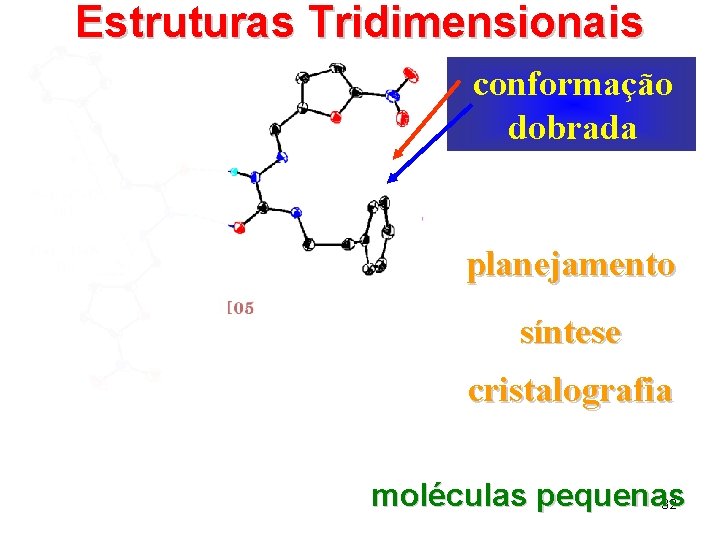
Estruturas Tridimensionais 1 conformação planejada dobrada planejamento síntese cristalografia moléculas pequenas 32
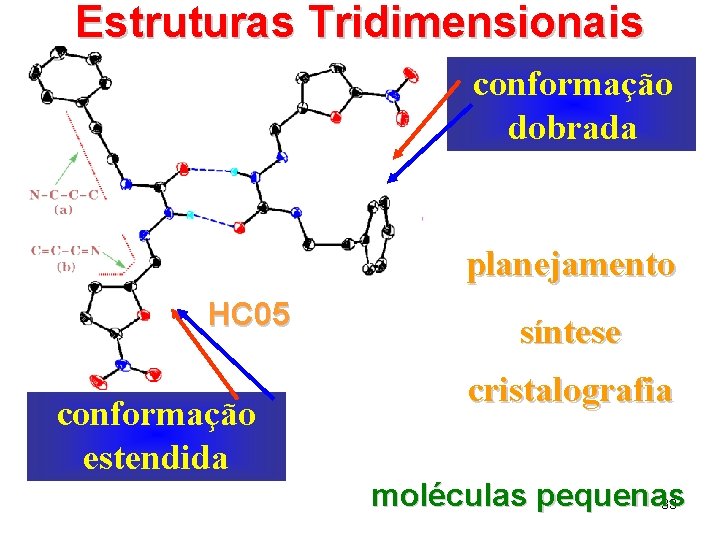
Estruturas Tridimensionais 1 conformação planejada dobrada planejamento HC 05 1 conformação não-planejada estendida síntese cristalografia moléculas pequenas 33
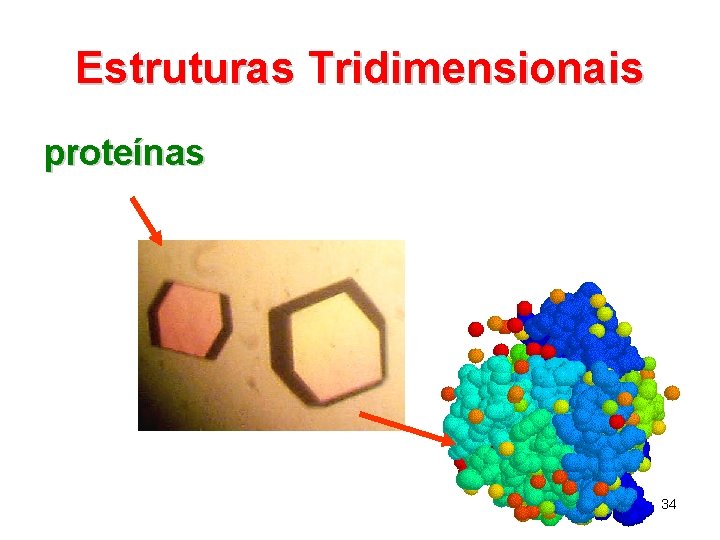
Estruturas Tridimensionais proteínas 34

Estruturas Tridimensionais quem são as proteínas? ? ? como são suas estruturas 3 D? ? como desempenham suas funções? ? ? 35

Estruturas Tridimensionais in silico Modelagem Molecular alinhamento de seqüências predição de estruturas de proteínas modelagem por homologia modelagem de ligantes docking 36

Proteínas 37

Funções biológicas das proteínas • • • Biocatalizadores (enzimas) Receptores de sinais químicos Transportadores Estruturais (citoesqueleto, colágeno) Defesa (sistema imunológico, restrição bacteriana, etc. ) Mobilidade (motores moleculares) Transdução Aderência celular e organização tissular Enovelamento correto de outras proteínas Outras IC 38

Os aminoácidos e proteínas O químico holandês Gerardus Mulder foi o primeiro a dotar o termo proteína em 1838. Do grego proteus: primário, o mais importante. 39

Os aminoácidos e proteínas O primeiro aminoácido descoberto foi a asparagina, asparagina extraída do aspargo, em 1806. O primeiro identificado em uma proteína foi a leucina por Proust em 1819. O último (20 o )a ser descoberto foi a treonina em 1936. (hoje isto nao é mais verdade…) 40

Os aminoácidos e proteínas Os aminoácidos sistemático. não possuem um nome A glicina tem esse nome devido ao gosto doce (glycos = doce). A tirosina foi originalmente isolada do queijo (tyros = queijo). O ácido glutâmico foi encontrado no glúten de trigo. 41

Aspectos Básicos da Estrutura Polipeptídica As proteínas são cadeias (polímeros) constituídos por • 22 L-aminoácidos-padrão unidos por ligações peptídicas • Os aminoácidos reunem-se em combinações praticamente infinitas 42
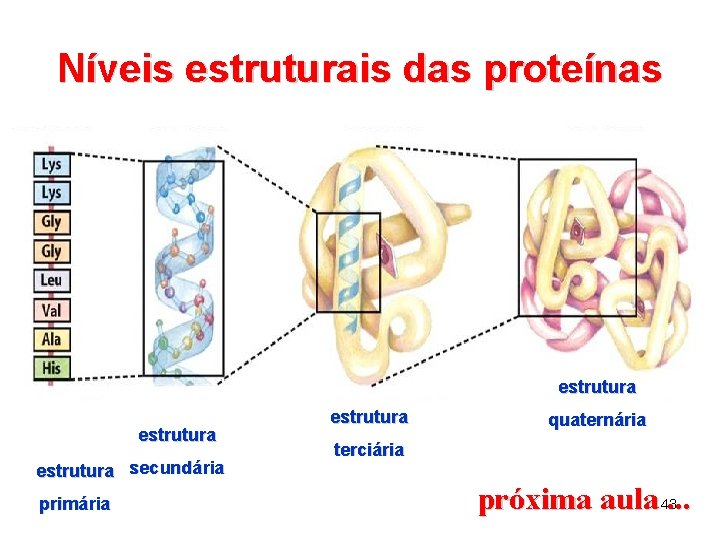
Níveis estruturais das proteínas estrutura secundária primária estrutura quaternária terciária próxima aula 43. . .

Aspectos Básicos da Estrutura Polipeptídica As proteínas são cadeias (polímeros) constituídas por • 22 L-aminoácidos • D-açúcares 44
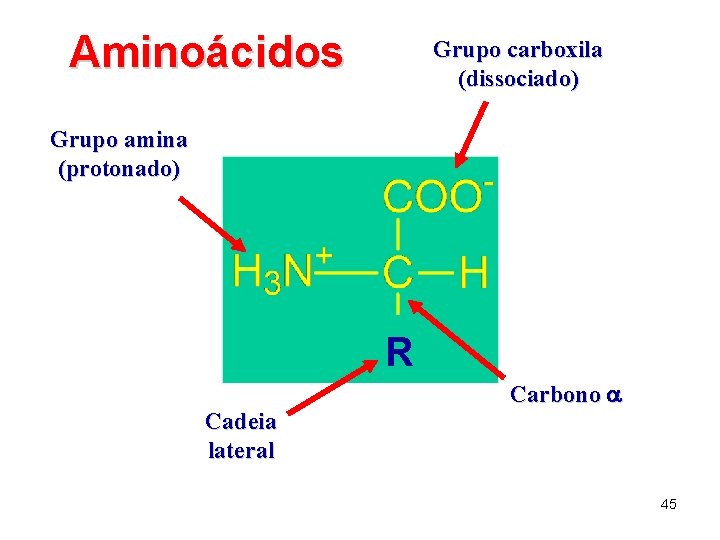
Aminoácidos Grupo carboxila (dissociado) Grupo amina (protonado) R Cadeia lateral Carbono a 45

Ligações nas Proteínas • interações covalentes (fortes) covalentes – ligação peptídica (aa – aa) – ligacao dissulfeto (S —– S; Cys – Cys) • interações não-covalentes (fracas) não-covalentes – interações eletrostáticas – interações de van der Waals – ligações de hidrogênio – interações hidrofóbicas 46

1 o nível estrutural: Estrutura Polipeptídica – seqüência de aminoácidos (formação da cadeia) Proteínas são polipeptídeos constituídos por: polipeptídeos • 22 L-aminoácidos • D-açúcares IC 47

Letras palavras ABCDCDEFGHIJKLMNOPQRSTUVWXYZ ABCORS COBRAS ACDEFGHIKLMNPQRSTVWY IC 48

aminoácidos proteínas K L P A S F D A R E Q W P GLN CYS PRO THR ILE LYS GLU ILE ARG ASP GLN GLY SER CYS TRP ALA PHE GLY ALA VAL GLU ALA ILE SER ASP ARG ILE CYS ILE HIS THR ASN ALA HIS VAL SER VAL GLU VAL SER ALA GLU ASP LEU THR CYS GLY SER MET CYS GLY ASP GLY CYS ASN GLY TYR PRO ALA GLU IC 49 ALA TRP ASN PHE TRP THR ARG LYS

aminoácidos proteínas KRLCGTFLGGPKPPQRVMFTEDLKLPASFDAREQWP QCPTIKEIRDQGSCGSCWAFGAVEAISDRICIHTNA HVSVEVSAEDLLTCCGSMCGDGCNGGYPAEAWNFWT RKGLVSGGLYESHVGCRPYSIPPCEHHVNGSRPPCT GEGDTPKCSKICEPGYSPTYKQDKHYGYNSYSVSNS EKDIMAEIYKNGPVEGAFSVYSDFLLYKSGVYQHVT GEMMGGHAIRILGWGVENGTPYWLVANSWNTDWGDN GFFKILRGQDHCGIESEVVAGIPRTDQYWEKI IC 50
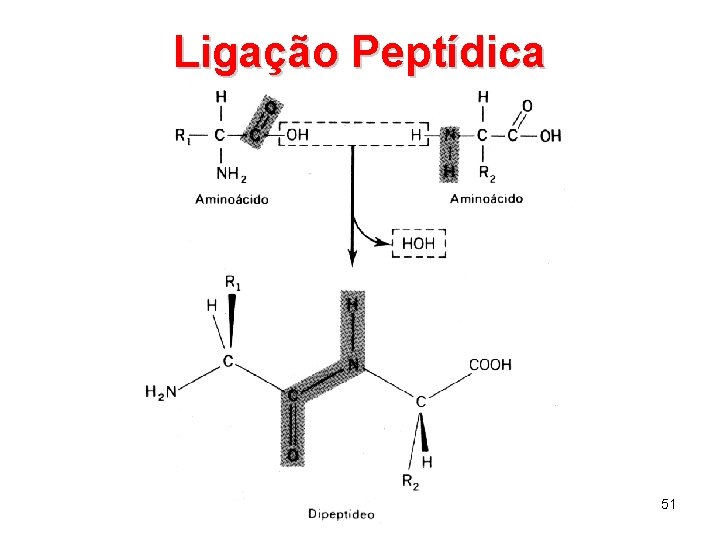
Ligação Peptídica 51
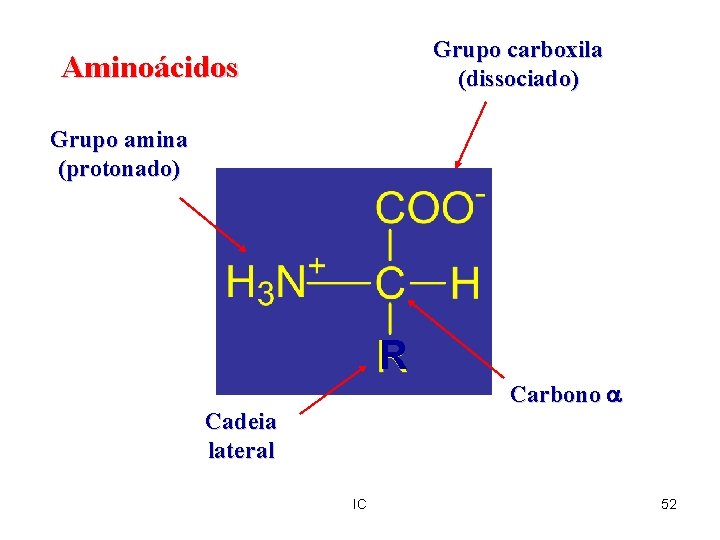
Grupo carboxila (dissociado) Aminoácidos Grupo amina (protonado) R Carbono a Cadeia lateral IC 52
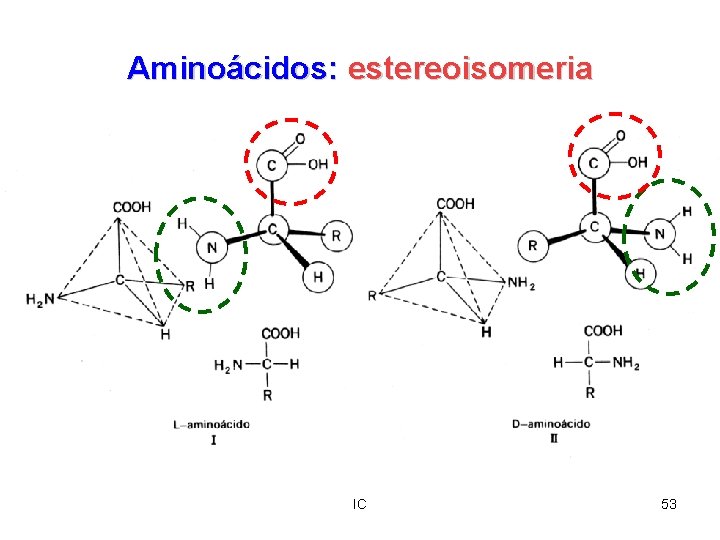
Aminoácidos: estereoisomeria IC 53
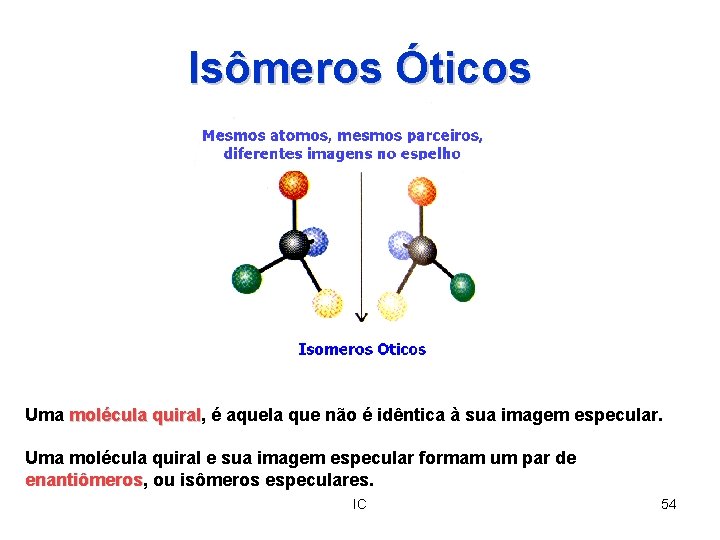
Isômeros Óticos Uma molécula quiral, quiral é aquela que não é idêntica à sua imagem especular. Uma molécula quiral e sua imagem especular formam um par de enantiômeros, enantiômeros ou isômeros especulares. IC 54
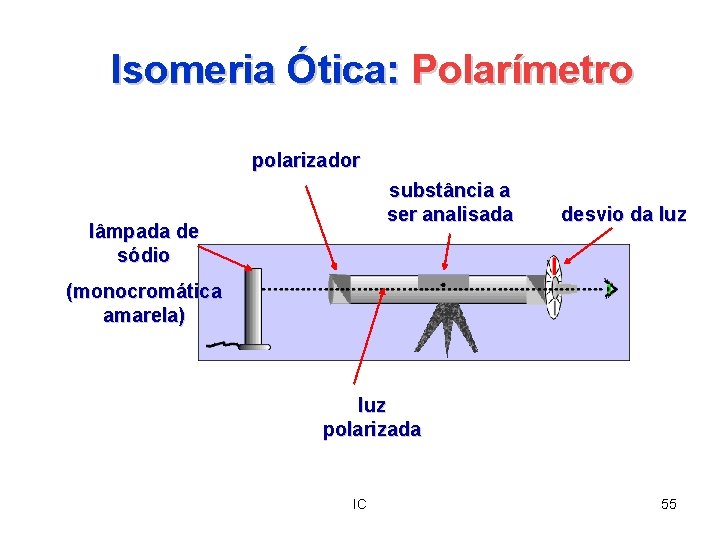
Isomeria Ótica: Polarímetro polarizador substância a ser analisada lâmpada de sódio desvio da luz (monocromática amarela) luz polarizada IC 55

Isomeria Ótica: Polarímetro luz polarizada substância analisada não muda a rotação do disco inativa gira o disco para a direita oticamente ativa: dextrógira ativa D girar o disco para a esquerda oticamente ativa: levógira L ativa IC 56

Isômeros Óticos: exemplo Talidomida 1953 – empresa suíça Ciba 1954 – empresa alemã Chemie Gruenenthal (testes mal conduzidos) prescrito para convulsões epilépticas (inefetivo) IC 57

Isômeros Óticos: exemplo Talidomida ensaios clínicos como um novo antihistamínico como tratamento da alergia (inefetivo) IC 58

Isômeros Óticos: exemplo Talidomida ensaios clínicos como um novo antihistamínico como tratamento da alergia (inefetivo) efetivo como sedante IC 59

Isômeros Óticos: exemplo Talidomida efetivo como sedante o destino definitivo do fármaco foi para tratar náuseas, ansiedade, insônia e vômitos matutinos das grávidas. IC 60

Isômeros Óticos: exemplo Talidomida Três anos más tarde, em 1957, a talidomida se converteu no medicamento para ajudar as grávidas. Seu uso se estendeu rapidamente e em 1958 foi introduzido em vários países da Europa, África, América e também na Austrália. http: //medtempus. com/archives/la-catastrofe-de-la-talidomida/ IC 61

Isômeros Óticos: exemplo Talidomida 1956 IC 62

Isômeros Óticos: exemplo Talidomida obstetra australiano, William Mc. Bride focomielia uma rara enfermidade congênita em que há desenvolvimento incompleto (total ou parcial) de pernas e braços. também apareciam outras anomalias menos raras em outros recém nascidos: surdez, cegueira, má formação de órgãos, . . http: //www. thalidomide. ca/en/information/history_of_thalidomide. html IC 63
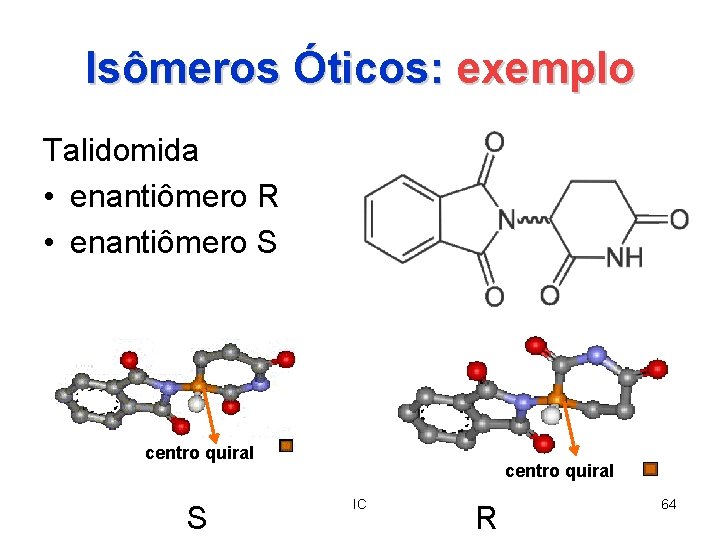
Isômeros Óticos: exemplo Talidomida • enantiômero R • enantiômero S centro quiral IC R 64
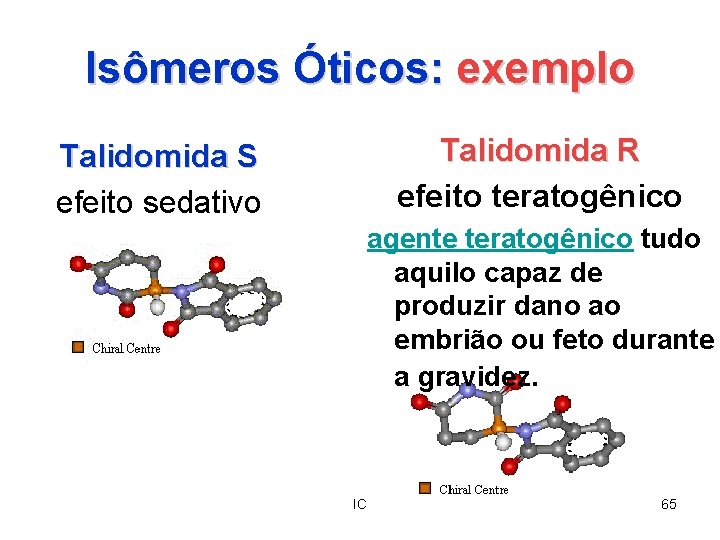
Isômeros Óticos: exemplo Talidomida R efeito teratogênico Talidomida S efeito sedativo agente teratogênico tudo aquilo capaz de produzir dano ao embrião ou feto durante a gravidez. IC 65
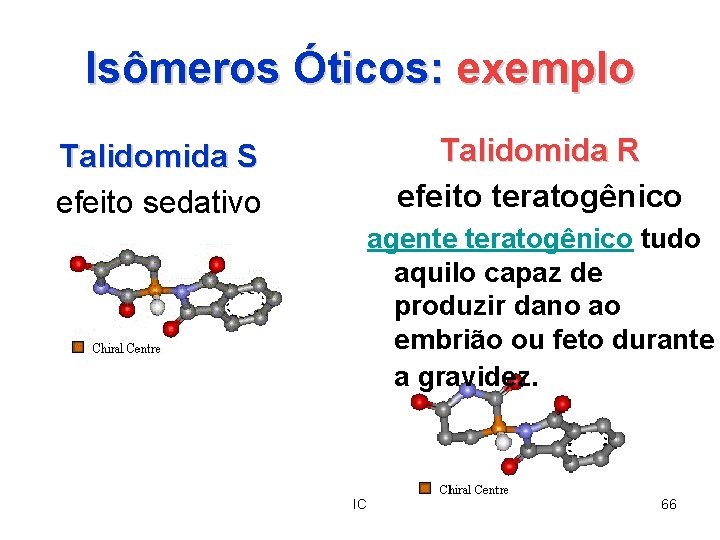
Isômeros Óticos: exemplo Talidomida R efeito teratogênico Talidomida S efeito sedativo agente teratogênico tudo aquilo capaz de produzir dano ao embrião ou feto durante a gravidez. IC 66
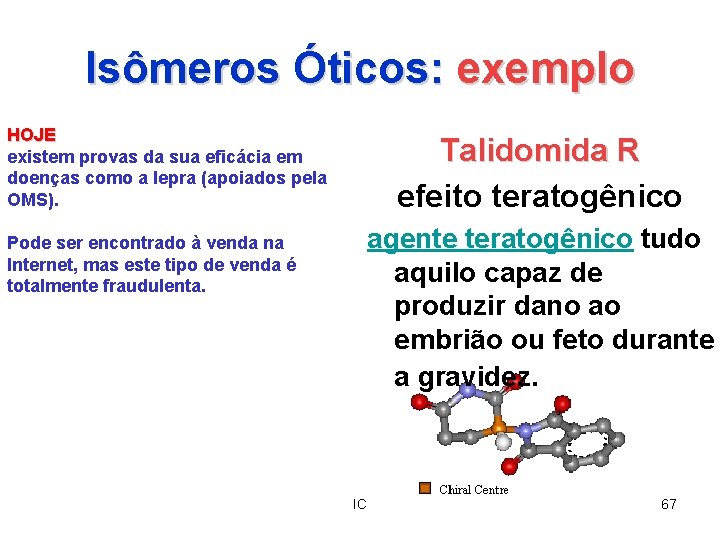
Isômeros Óticos: exemplo HOJE existem provas da sua eficácia em doenças como a lepra (apoiados pela OMS). Pode ser encontrado à venda na Internet, mas este tipo de venda é totalmente fraudulenta. Talidomida R efeito teratogênico agente teratogênico tudo aquilo capaz de produzir dano ao embrião ou feto durante a gravidez. IC 67
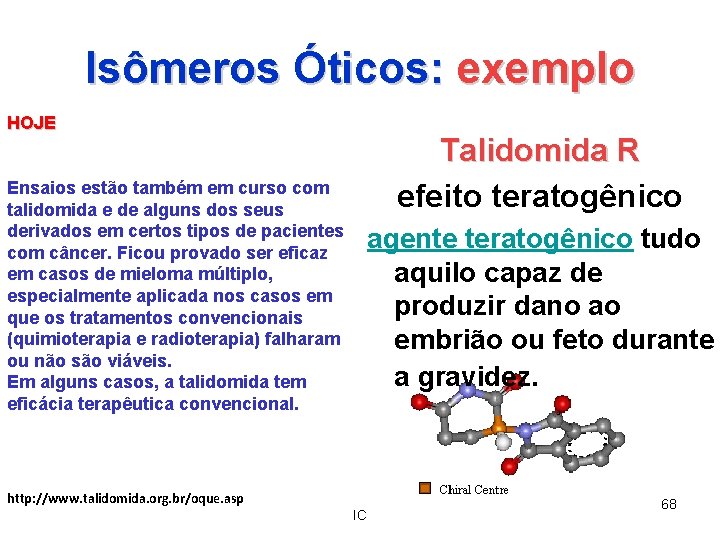
Isômeros Óticos: exemplo HOJE Ensaios estão também em curso com talidomida e de alguns dos seus derivados em certos tipos de pacientes com câncer. Ficou provado ser eficaz em casos de mieloma múltiplo, especialmente aplicada nos casos em que os tratamentos convencionais (quimioterapia e radioterapia) falharam ou não são viáveis. Em alguns casos, a talidomida tem eficácia terapêutica convencional. Talidomida R efeito teratogênico agente teratogênico tudo aquilo capaz de produzir dano ao embrião ou feto durante a gravidez. http: //www. talidomida. org. br/oque. asp IC 68
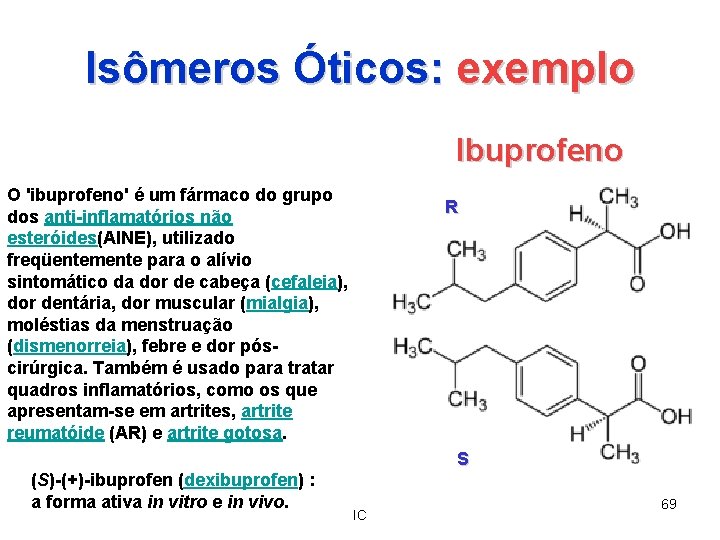
Isômeros Óticos: exemplo Ibuprofeno O 'ibuprofeno' é um fármaco do grupo dos anti-inflamatórios não esteróides(AINE), utilizado freqüentemente para o alívio sintomático da dor de cabeça (cefaleia), dor dentária, dor muscular (mialgia), moléstias da menstruação (dismenorreia), febre e dor póscirúrgica. Também é usado para tratar quadros inflamatórios, como os que apresentam-se em artrites, artrite reumatóide (AR) e artrite gotosa. R S (S)-(+)-ibuprofen (dexibuprofen) : a forma ativa in vitro e in vivo. IC 69
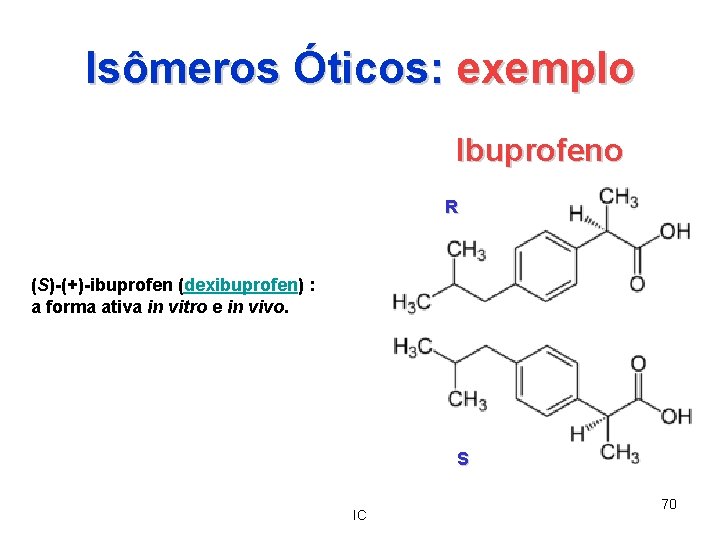
Isômeros Óticos: exemplo Ibuprofeno R (S)-(+)-ibuprofen (dexibuprofen) : a forma ativa in vitro e in vivo. S IC 70

Fármacos vai onde? o que vai fazer? de onde veio?

onde foi parar?

aminoácidos C H O N N P S Se outros. . quais? IC 74

Arquivo texto da proteina PDB – Protein Databank www. rcsb. org/pdb/home. do PDBSum www. ebi. ac. uk/thornton-srv/databases/pdbsum/ IC 75

Arquivo texto da proteina 1 mbn IC 76
- Slides: 76