Introduction Gnrale La biochimie tude des ractions chimiques

Introduction Générale

• La biochimie : étude des réactions chimiques qui se déroulent au sein des êtres vivants, et notamment dans les cellules. • Implique étude des structures, des propriétés chimiques des molécules et les réactions qu’elles subissent. • On peut donc définir la Biochimie comme étant une étude structurale et fonctionnelle des molécules biologies au sein des vivants. • Le principal objectif de la biochimie est de comprendre comment les molécules biochimiques (glucides, lipides, protéines et acides nucléiques essentiellement) se transforment pour fabriquer de nouvelles structures (anabolisme) ou pour produire de l’énergie nécessaire au fonctionnement des cellules (Catabolisme).
• Champ d’application en botanique, médecine, biotechnologique, l’agronomie etc. • La biochimie a un lien étroit avec la génétique et la biologie moléculaire.

• En agronome permet de savoir: • comment les substances chimiques sont synthétisées ou utilisés chez plantes et chez les animaux • comment des problèmes peuvent survenir dans la production, comment les prévenir ou y remédier. • Il est surtout question de connaitre les différentes structures chimiques que l’on retrouve dans le monde vivant et comment globalement ces molécules sont transformé.

Objectif du cours • Objectifs généraux du cours : Décrire les propriétés principales des molécules composant les êtres vivant et les grandes voies de réactions chimiques se déroulant à l'intérieur de la cellule. Objectifs spécifiques du cours : • Exploiter les caractéristiques physicochimiques des solutions aqueuses. • Décrire les propriétés principales des molécules du vivant : glucides, lipides, acides aminés, peptides, protéines, acides nucléiques et leurs comportements en milieu aqueux. • Donner les bases de l'enzymologie classique (cinétique, classification des enzymes, mécanismes réactionnels, . . . ). • Expliquer l'organisation générale des voies cataboliques cellulaires aboutissant à la formation de molécules à liaisons riches en énergie.

Chapitre 1 : Solution aqueuses et solutions tampon

1. 1 Définitions • Solution: mélange homogène d’un soluté dissout dans un solvant, lorsque le solvant est l’eau, on obtient une solution aqueuse, • Une solution solide résulte d’une mélange de plusieurs corps purs • Soluté: molécules (ou les ions) solvatées ou dispersées dans le solvant. • Une solution peut être à l’état solide, liquide ou gazeux • Solution liquides: üun liquide dans un autre : les deux doivent être miscibles; üun solide dans un liquide : le solide doit être soluble dans le solvant. Ce type de solution peut être saturée ; üun gaz dans un liquide

1. 2 Différentes expressions de la concentration •

• Exercice d’application 1. Combien de mole(s) de H 2 SO 4 y a-t-il dans un litre de solution 0, 25 M d'acide sulfurique ? 2. Combien de grammes de Ca(OH)2 y a-t-il dans 0, 25 litre de solution 0, 010 M de ce corps? 3. Quelle la concentration molaire d'une solution renfermant 10 g d'H 2 SO 4 par litre? 4. Combien de mole(s) d'HCl y a-t-il dans 20 ml d'une solution 1, 0 M? 5. Combien de grammes de Na. Cl faut-il dissoudre pour obtenir 100 ml de solution de Na. Cl 0, 10 M?


• Exemple 1 : 5 g de chlorure de sodium Na. Cl (M=58, 44 g mol-1) sont dissous dans 25 g d'eau pure H 2 O (M=18, 02 g mol-1). On calcule la fraction molaire de Na. Cl dans la solution : . n. Na. Cl > (1 mol/58, 44)x 5 = 0, 0855 mol, . n. H 2 O > (1 mol/18, 02)x 25 = 1, 387 mol, XNa. Cl (fraction molaire de Na. Cl) > 0, 0855 / (0, 0855 + 1, 387) = 0, 058.

• C- Molalité (m) : nombre de moles de soluté par kilogramme de solvant. Il se calcule en faisant le rapport du nombre de moles de soluté sur la masse de solvant, en kg. m. A = [ n. A / massesolvant, kg ] • Exemple 4 : Molalité de la solution de Na. Cl de l'exemple 1? . Nombre de moles de Na. Cl (n. Na. Cl) = 0, 0855 mol, . masse de l'eau (solvant, en kg) = 0, 025 kg, et m. Na. Cl (molalité) > (0, 0855/0, 025) = 3, 42 mol kg 1 (3, 42 m).

• Exercice d’application : • Quelle est la normalité d'une solution préparée en dissolvant 8. 370 g du corps composé suivant dans suffisamment d'eau pour obtenir 0. 200 L de solution ? • Un échantillon de 0. 347 L de HNO 2 (aq) (Acide nitreux) 0. 546 N est dilué à 600 m. L. Quelle est la normalité de la solution diluée ? • Une solution aqueuse de H 3 PO 4 contient 12 % en masse de H 3 PO 4. Sa masse volumique est de 1. 06 g/m. L. Calcule la molalité de la solution. • Quel volume d'une solution HCl à 25 % en masse (d=1. 12) doiton utiliser pour préparer 962 m. L de solution 0. 415 N ?

• Pourcentage en masse (%): pourcentage de la masse totale de la solution que représente un des constituants. C'est le rapport de la masse de l'un des constituants sur la masse totale (en respectant les mêmes unités de masse). • pourcent en masse de A = masse. A / [ masse. A + masse. B + masse. C +. . . ] x 100 • Exemple 5 : Pourcentage en masse de Na. Cl dans la solution de l'exemple 1 ? . pourcentage en masse de Na. Cl = masse. Na. Cl / [ masse. Na. Cl + masse. H 2 O ] x 100, soit, ( 5 / [5 + 25] x 100 ) = 16, 7 % Nota : la solution est de 16, 7 % en Na. Cl et 83, 3 % en H 2 O (en masse).

• D- molalité : nombre de moles de soluté contenue dans 1 000 grammes de solvant. S'exprime en mole par kilogramme (mol/kg). • E- La normalité : • La normalité d'une solution acide dans l'eau comme le nombre de mol d'ion H 3 O+ susceptible d'être libérés par un litre de solution. • La normalité oxydo-réductrice d'une solution correspond au nombre de mol d'électrons susceptibles d'être libérés par un litre de solution • la normalité dépend de la nature de espèce chimique avec laquelle on peut faire réagir la solution

1. 3 Dilution des solutions • Diluer une solution permet de diminuer sa concentration. A cet effet on rajoute une quantité précise de solvant à un volume précis de la solution initiale.

• Exemple, Soit une dilution à 50% : cela signifie que la concentration est divisée par 2. On doit donc diviser par 2 le nombre de molécules présentes par litre de solution. Une façon de procéder serait d'ajouter le même volume de solvant que de solution initiale. • calculer le volume d'une solution aqueuse 6 M de H 2 SO 4 , qu'il faut prélever pour obtenir 500 m. L de H 2 SO 4 0, 3 M. • Loi des concentrations: La molarité d'une solution mère (M 1) multipliée par son volume (V 1) est égale à la molarité d'une solution fille (M 2) que multiplie son volume (V 2), avec M, la molarité de la solution exprimée en M/L ou Molaire et V, le volume de la solution exprimé en litre(s).

• 1. Calculer la concentration massique d'une solution de 2 kg de Na. Cl dont le volume atteint 15 L. • 2. Calculer la masse de soluté contenue de 350 m. L de solution à 12 g/L. • 3. Calculer la concentration molaire d'une solution contenant 0, 0115 moles de Na. OH. Le volume total de solution est 11, 5 m. L. • 4. Calculer la concentration molaire d'un vinaigre de massique 7 g/100 m. L. (formule : CH 3 -COOH) • 5. Une solution d'H 2 SO 4 de masse volumique 140 g/L contient 51, 15 % d'acide. Quelle est la molarité de la solution ?

p. H de solutions aqueuses • L’échelle de p. H est comprise entre 0 et 14. • entre 0 et 7: solution acide, • entre 7 et 14: solution basique. • p. H 7 : solution neutre du point de vue acidobasique, ce qu’il ne faut pas confondre avec la neutralité électrique de la solution qui est vérifiée pour n’importe quelle solution. • Le p. H se mesure avec un p. H-mètre, du papier p. H ou s’évalue grossièrement avec des indicateurs colorés comme le bleu de bromothymol.

• a) produit ionique de l'eau • Pour des solutions diluées (dont les concentrations ne dépassent pas 0, 1 mol. L-1), la quantité Ke = [H 3 O+]. [OH-] est constante. Elle est appelée produit ionique de l’eau. • A 25 °C, Ke = 10 -14. • Le fait de connaître la concentration en ions hydronium revient donc à connaître également celle en ions hydroxyde. • b) Définition du p. H • Le p. H est l’opposé du logarithme décimal de la concentration en ions H 3 O+ : p. H) –log[H 3 O+] • Dans le cas de l’eau pure à 25 °C, on retrouve :

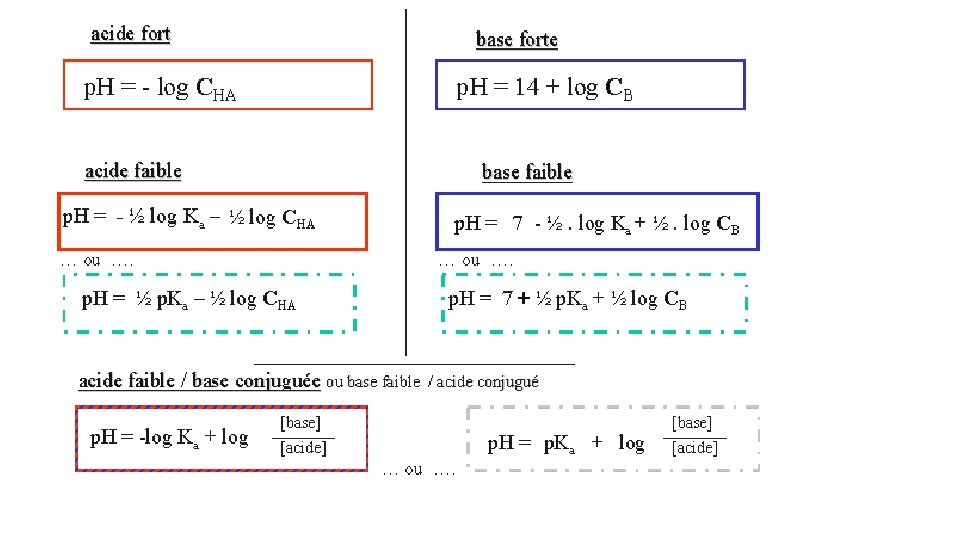
ACIDES FORTS ET FAIBLES • Deux types d’acides: • Si l’acide HA 1 est complètement dissocié, l’acide est dit fort. • HA 1+H 2 O H 3 O++A 1 • Exemple: HCl qui en solution donne H+ et Cl • Si l’acide n’est pas complètement dissocié, il est un acide faible HA 2. • HA 2+H 2 O H 3 O++A 2 • C’est le cas de l’acide éthanoïque (acide acétique)
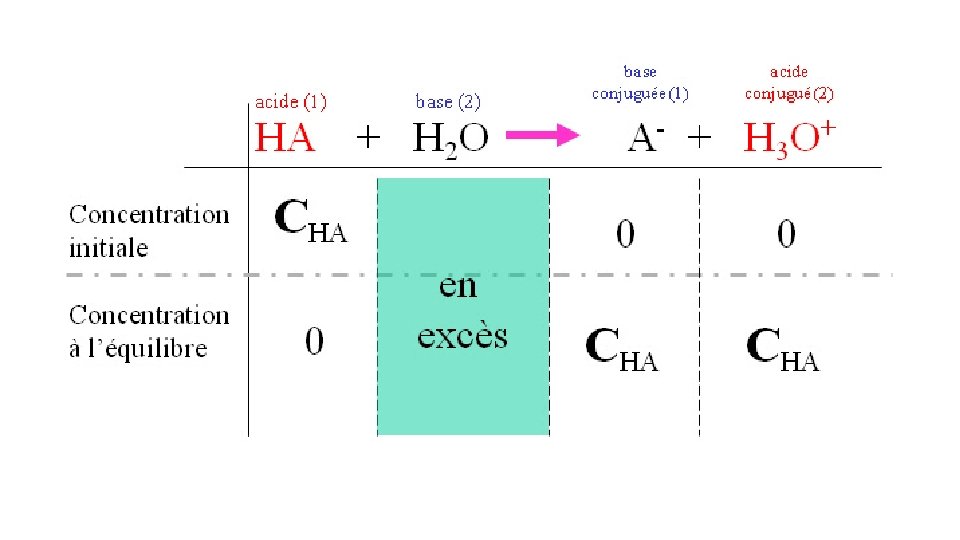

Acides faibles
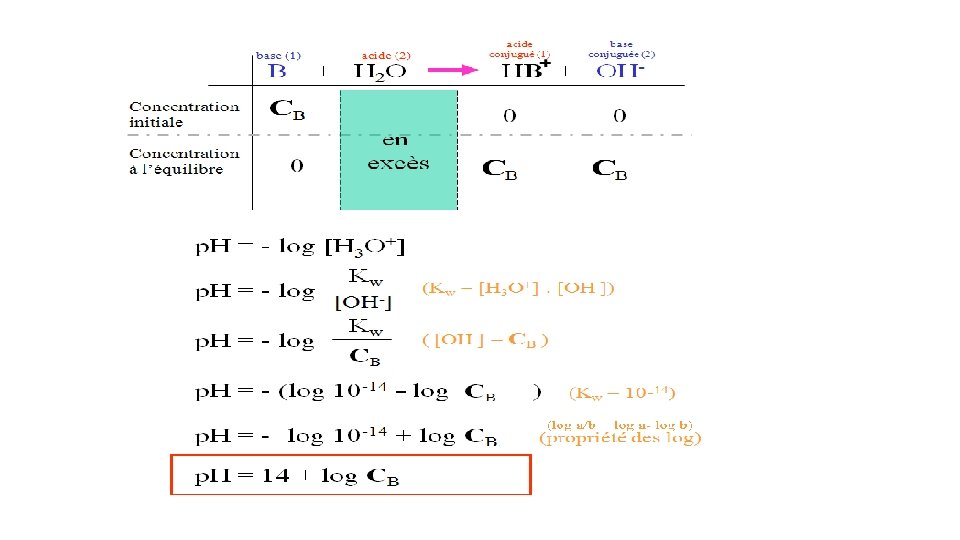

Bases fortes et bases faibles
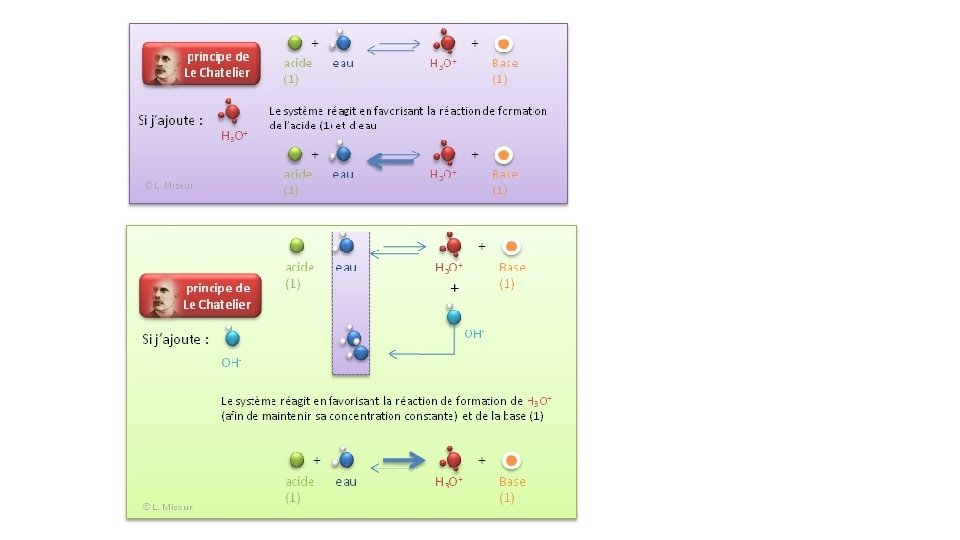

1. 3 Solutions Tampon • Définition • une solution tampon est une solution dont le p. H varie peu ou pas du tout par ajout de petites quantité d’acide ou de base ou par dillution. • C’est donc une solution qui maintient approximativement le même p. H malgré l'addition de petites quantités d'un acide ou d'une base, ou malgré une dilution. • Une telle solution est composée : • soit d'un acide faible HA et de son anion A−. Exemple couple CH 3 COOH/CH 3 COO−, ou du couple NH 4+/NH 3 ; • soit d'une base faible B et de son cation BH+

1. 3. 1 p. H d'une solution tampon •

Préparation d’une solution tampon • Trois possibilités: • par mélange équimolaire d’un acide faible et de sa base conjuguée, • à partir de l’acide faible sur lequel on fait réagir une base forte pour former la forme basique conjuguée de l’acide faible, • à partir de la base faible sur laquelle on fait réagir un acide fort pour former la forme acide conjuguée de la base faible. • Les concentrations en acide faible et base faible doivent être au moins supérieures à 1 mmol. L-1 pour que la solution tampon soit efficace.

1. Préparation d’un mélange équimolaire • solution d’acide faible de concentration CA et d’une solution de sa base conjuguée de concentration CB. • n. A = n. B ou encore CA. VA = CB. VB • VA et VB sont les volumes utilisés d’acide et de base pour préparer la solution tampon. • Exemple d’application: Quel volume d’acide méthanoïque (CA = 100 mmol. L-1) et de méthaoate de sodium (CB = 300 mmol. L-1) pour préparer 1 L de solution tampon à p. H = 3, 8 ? Le p. Ka du couple est de 3, 8.
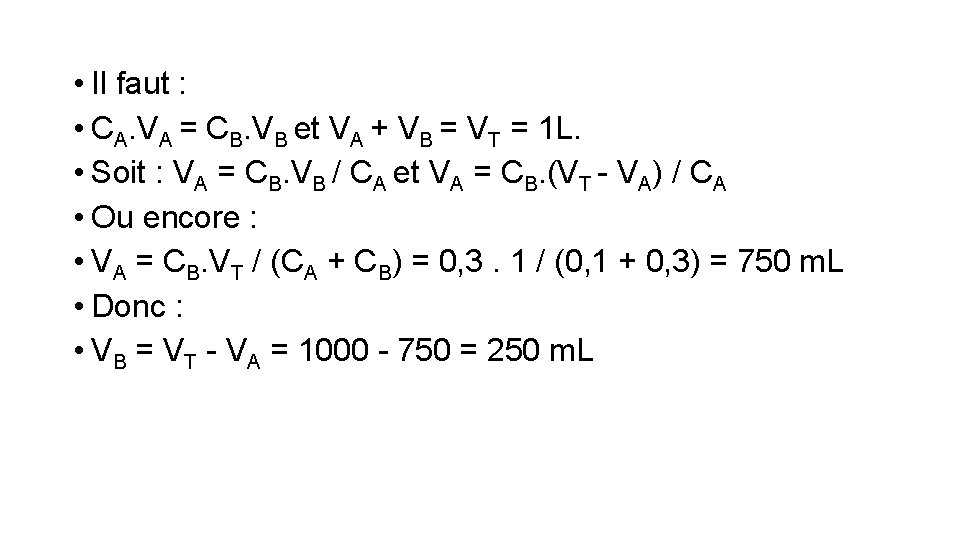
• Il faut : • CA. VA = CB. VB et VA + VB = VT = 1 L. • Soit : VA = CB. VB / CA et VA = CB. (VT - VA) / CA • Ou encore : • VA = CB. VT / (CA + CB) = 0, 3. 1 / (0, 1 + 0, 3) = 750 m. L • Donc : • VB = VT - VA = 1000 - 750 = 250 m. L
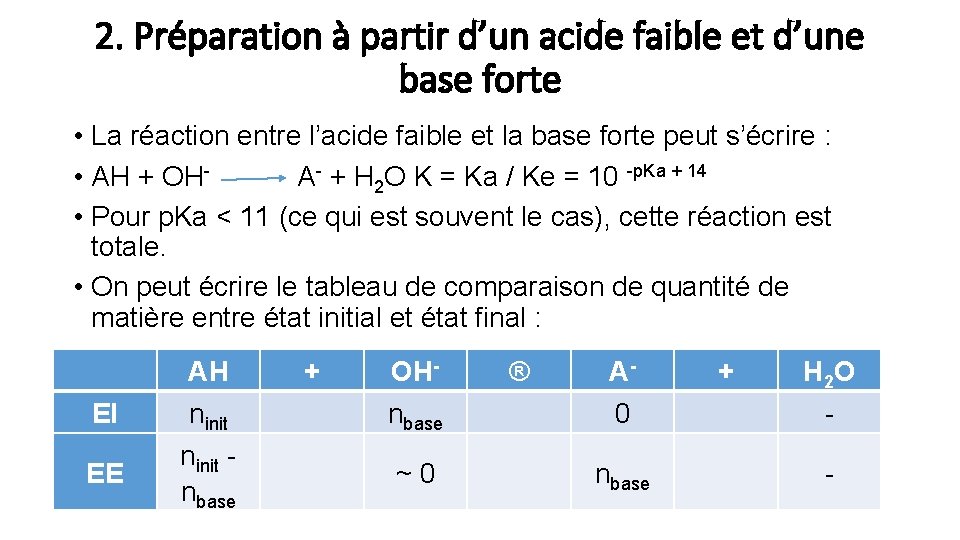
2. Préparation à partir d’un acide faible et d’une base forte • La réaction entre l’acide faible et la base forte peut s’écrire : • AH + OHA- + H 2 O K = Ka / Ke = 10 -p. Ka + 14 • Pour p. Ka < 11 (ce qui est souvent le cas), cette réaction est totale. • On peut écrire le tableau de comparaison de quantité de matière entre état initial et état final : EI EE AH ninit nbase + OHnbase ~0 ® A 0 nbase + H 2 O -

• Pour obtenir une solution tampon à p. H = p. Ka, il faut [AH] = [A-] ce qui est obtenu pour : • ninit - nbase = nbase soit nbase = ½ ninit • La quantité de base forte à ajouter est donc la moitié de la quantité initiale d’acide faible. • Exemple d’application: Quel volume d’hydroxyde de sodium à 100 mmol. L-1 doit-on ajouter à 20 m. L d’une solution d’acide éthanoïque (p. Ka = 4, 8) de concentration 100 mmol. L-1 pour préparer une solution tampon à p. H = 4, 8.

• Pour avoir p. H = 4, 8, il faut : [CH 3 COOH] = [CH 3 COO-]. • La réaction est : • CH 3 COOH + OHCH 3 COO- + H 2 O • Or la réaction est totale : • n(CH 3 COO-) = n(OH-) = ½ ninit (CH 3 COOH) • Or : • ninit (CH 3 COOH) = C. V = 0, 1. 0, 02 = 2 mmol • Il faut donc : • n(OH-) = ½ ninit (CH 3 COOH) = 1 mmol • Soit : • V(Na. OH) = n / [OH-] = 0, 001 / 0, 1 = 10 m. L.

3. Préparation à partir d’une base faible et d’un acide fort • La réaction entre la base faible et l’acide fort peut s’écrire : A- + H 3 O+ AH + H 2 O • Pour p. Ka > 3 (ce qui est souvent le cas), cette réaction est totale. On peut écrire le tableau de comparaison de quantité de matière entre état initial et état final : EI EE Aninit nacide + H 3 O + nacide ~0 ® AH 0 nacide + H 2 O -

• Pour obtenir une solution tampon à p. H = p. Ka, il faut [AH] = [A-] ce qui est obtenu pour : • ninit - nacide = nacide soit nacide = ½ ninit • La quantité d’acide fort à ajouter est donc la moitié de la quantité initiale de base faible. • Exemple d’application: Quel volume d’acide chlorhydrique à 400 mmol. L-1 doit-on ajouter à 40 m. L d’une solution d’ammoniac (p. Ka = 9, 2) de concentration 200 mmol. L-1 pour préparer une solution tampon à p. H = 9, 2. • Pour avoir p. H = 4, 8, il faut : [NH 3] = [NH 4+]. • La réaction est : NH 3 + H 3 O+ ® NH 4+ + H 2 O • Or la réaction est totale : • n(NH 4+) = n(H 3 O+) = ½ ninit (NH 3) • Or : ninit (NH 3) = C. V = 0, 2. 0, 04 = 8 mmol • Il faut donc : n(H 3 O+) = ½ ninit (NH 3) = 4 mmol

Pouvoir tampon • Le pouvoir tampon (β) est le nombre de moles d’acide ou de base forte à ajouter à 1 L de solution tampon pour faire varier le p. H d’une unité, • L’unité du pouvoir tampon est la mol. L-1. • Plus le pouvoir tampon est grand, plus le p. H de la solution tampon varie peu par addition d’un acide ou d’une base. • Evolution du pouvoir tampon • • • La relation est : β = 2, 3. [AH]. [A-] / ([AH] + [A-]) Si : [AH] = [A-] = C b = 2, 3. C² / 2. C = 1, 15. C Si : [AH] =[A-] / 2 = C / 2 b = 2, 3. (C² / 2) / (3/2 C) = 0, 767. C Si : [AH] =[A-] / 4 = C / 4 b = 2, 3. (C² / 4) / (5/4 C) = 0, 460. C Si : [AH] =[A-] / 10 = C / 10 b = 2, 3. (C² / 10) / (11/10 C) = 0, 209. C

Exercice d’application 1. Combien de mole(s) de H 2 SO 4 y a-t-il dans un litre de solution 0, 25 M d'acide sulfurique ? 2. Combien de grammes de Ca(OH)2 y a-t-il dans 0, 25 litre de solution 0, 010 M de ce corps? 3. Quelle la concentration molaire d'une solution renfermant 10 g d'H 2 SO 4 par litre? 4. Combien de mole(s) d'HCl y a-t-il dans 20 ml d'une solution 1, 0 M? 5. Combien de grammes de Na. Cl faut-il dissoudre pour obtenir 100 ml de solution de Na. Cl 0, 10 M?

• Exercice 2: • Le Guronsan® est un médicament indiqué dans le traitement d'appoint de la fatigue alguë. Il se présente sous la forme de comprimés effervescents. Chaque comprimé contient, entre autres, une masse ma = 500 mg d'acide ascorbique (ou vitamine C) et une masse m = 50 mg de caféine. 1. Calculer la concentration massique cm de caféine de la solution obtenue lorsqu'un comprimé est dissous dans un verre contenant un volume V = 200 m. L d'eau. On suppose que la dissolution a lieu sans variation de volume. 2. Comparer cm avec la concentration massique caféine dans un expresso : une portion de volume V′ = 30 m. L contient environ une masse m′ = 40 mg de caféine.

• Exercice 3, 1. Quelle est la normalité d'une solution préparée en dissolvant 8. 370 g du corps composé suivant dans suffisamment d'eau pour obtenir 0. 200 L de solution ? 2. Un échantillon de 0. 347 L de HNO 2 (aq) (Acide nitreux) 0. 546 N est dilué à 600 m. L. Quelle est la normalité de la solution diluée ? 3. Une solution aqueuse de H 3 PO 4 contient 12 % en masse de H 3 PO 4. Sa masse volumique est de 1. 06 g/m. L. Calcule la molalité de la solution. 4. Quel volume d'une solution HCl à 25 % en masse (d=1. 12) doit-on utiliser pour préparer 962 m. L de solution 0. 415 N ?

• Exercice 4, • On mélange 500 m. L d'une solution d'acide sulfurique à la concentration 1 Mol/L et 350 m. L d'une solution d'acide sulfurique à la concentration de 0, 45 Mole/L. Quelle est la concentration de la solution obtenue ?


• Exercice 5 • On ajoute à un litre de cette solution 10 m. L d'acide chlorhydrique concentré, correspondant à 0, 10 mol. En négligeant la variation de volume, calculez le obtenu ; comparez au de la solution obtenue en versant la même quantité d'acide dans un litre d'eau pure.
- Slides: 44